新型冠狀病毒Delta變異株早期病毒載量與臨床特征的關(guān)系
黃春明 胡中偉 黃韞 詹遠(yuǎn)京
廣州醫(yī)科大學(xué)附屬市八醫(yī)院隔離十九區(qū)(廣州510060)
當(dāng)機(jī)體受外來病原體入侵,病毒載量與宿主因素均可能影響病情進(jìn)展及預(yù)后[1-2]。目前臨床研究更多關(guān)注宿主臨床表現(xiàn)及治療,而病毒載量對于疾病的影響關(guān)注較少,本研究根據(jù)RT-PCR 檢測鼻拭子核酸水平,探討新型冠狀病毒(SARS-Cov-2)Delta 變異株早期病毒載量與臨床特征及病毒轉(zhuǎn)陰時(shí)間的關(guān)系。
1 資料與方法
1.1 研究對象及分組 選取2021年5月21日至2021年6月18日廣州醫(yī)科大學(xué)附屬市八醫(yī)院隔離病區(qū)收治的廣州SARS-Cov-2Delta 變異株確診病人,共108 例成年患者納入本研究,所有患者均符合《新型冠狀病毒肺炎診療方案(試行第八版)》診斷標(biāo)準(zhǔn)[3],RT-PCR 檢測結(jié)果表示為周期閾值(Ct),Ct 值越小,病毒復(fù)制拷貝越活躍,病毒載量越高,Ct 值>40,判定為陰性。高拷貝組定義:1 周內(nèi)N 基因和(或)Orf1a/b 基因Ct 值<20,低拷貝組:1 周內(nèi)N 基因和(或)Orf1a/b 基因Ct 值≥20。病毒轉(zhuǎn)陰時(shí)間定義:從第一次鼻咽拭子陽性到兩次連續(xù)(間隔>24 h)陰性試驗(yàn)中的第一次的時(shí)間。本研究所有患者簽署知情同意書,獲得廣州市第八人民醫(yī)院倫理委員會批準(zhǔn)(202007140)。
1.2 臨床資料收集 Delta 變異株感染病人資料收集均來自醫(yī)院電子病歷系統(tǒng),包括性別、年齡、入院基線血常規(guī)、T 淋巴細(xì)胞亞群和第1 周血常規(guī),以及住院期間核酸結(jié)果(每例患者間隔1 d 采集鼻拭子,由醫(yī)院研究所采用RT-PCR 檢測病毒核酸)。全部病例首次SARS-Cov-2 核酸陽性由廣州市疾病預(yù)防控制中心確定,廣東省疾病預(yù)防控制中心確定病毒株基因測序。
1.3 統(tǒng)計(jì)學(xué)方法 采用SPSS 22.0 軟件,正態(tài)分布的計(jì)量資料采用()表示,兩組間比較采用獨(dú)立樣本t檢驗(yàn);非正態(tài)分布的計(jì)量資料,采用M(P25,P75)表達(dá),比較兩組間差異性采用非參數(shù)檢驗(yàn)(Mann-WhitneyU秩和檢驗(yàn))。兩個(gè)率的比較采用χ2檢驗(yàn),P<0.05 為差異有統(tǒng)計(jì)學(xué)意義。
2 結(jié)果
2.1 一般情況 全組患者Ct 值最低值發(fā)生在住院第2(0,3)d,N 基因(20.5 ± 5.7),Orf1a/b 基因(22.1±5.7)。高拷貝組納入59例(其中男38例),平均年齡(54.5±18.2)歲,N 基因(16.6±2.1),Orf1a/b基因(18.2±2.1);低拷貝組納入49例(其中男27例),平均年齡(59.4±16.8)歲,N基因(25.2±5.2),Orf1a/b基因(26.7±5.1),兩組間性別、年齡差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。與低拷貝組比較,高拷貝組合并糖尿病比例更高(P<0.05),但兩組重癥率和其他慢性基礎(chǔ)性疾病差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。高拷貝組患者咽喉不適和腹瀉比例更高(P<0.05),其他癥狀差異均無統(tǒng)計(jì)學(xué)意義(P>0.05,表1)。
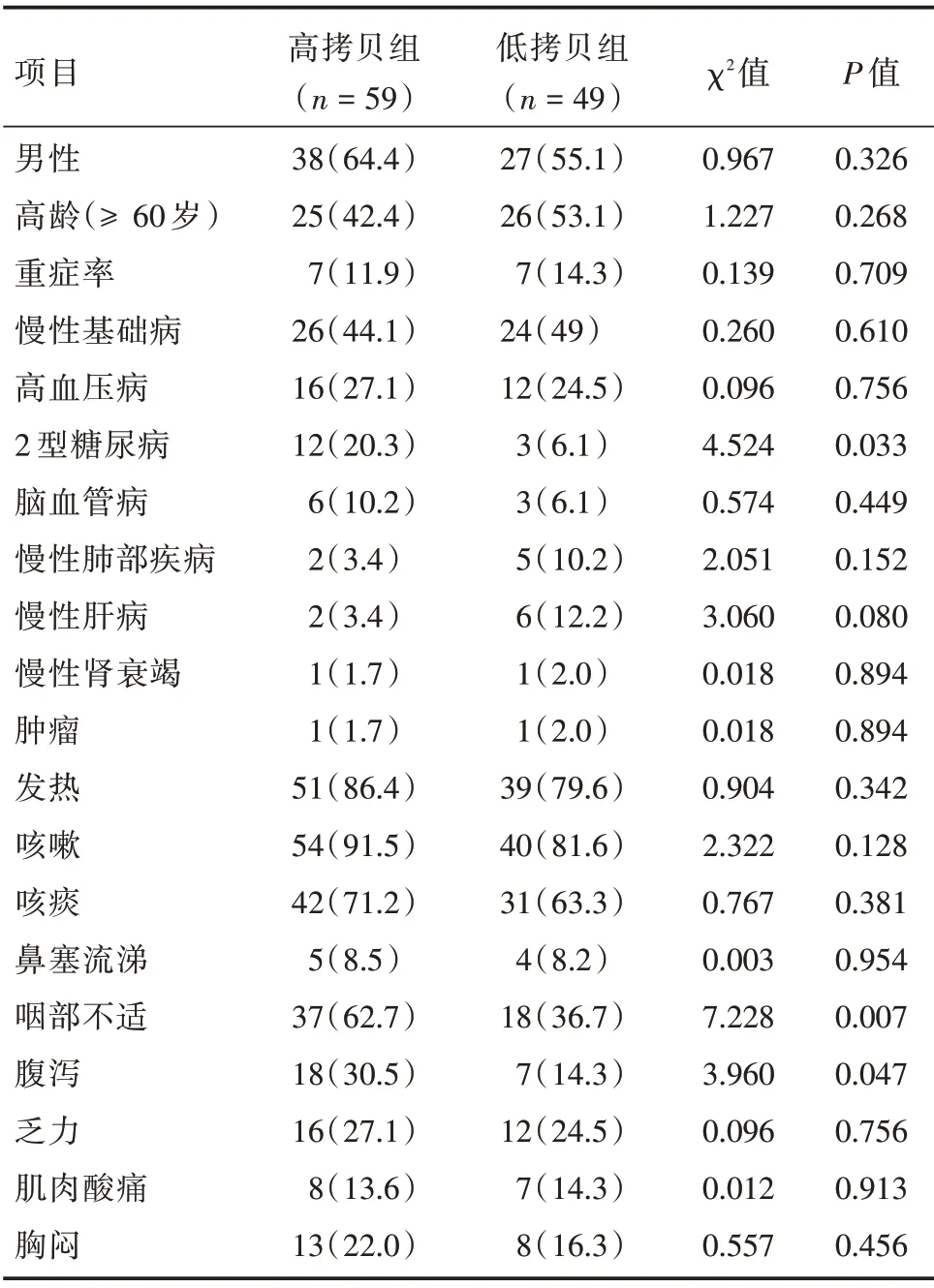
表1 兩組患者基礎(chǔ)病和臨床表現(xiàn)比較Tab.1 Comparison of basic diseases and clinical manifestations between the two groups 例(%)
2.2 兩組患者實(shí)驗(yàn)室結(jié)果分析 與基線低拷貝組比較,高拷貝組基線CD4+T 淋巴細(xì)胞更低(P<0.05),CD3+和CD8+T 淋巴細(xì)胞數(shù)值更低,但差異無統(tǒng)計(jì)學(xué)意義(P>0.05);兩組患者基線時(shí)外周血淋巴細(xì)胞(LYM)和嗜酸性粒細(xì)胞(EOS)差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。與第1周低拷貝組比較,高拷貝組LYM 和EOS 更低(P<0.05,表2)。與高拷貝組基線縱向比較,高拷貝組第1 周LYM 和EOS 差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。與低拷貝組基線比較,低拷貝組第1 周LYM 和EOS 更高(P<0.05,表2)。由于第1 周復(fù)查T 淋巴細(xì)胞亞群例數(shù)很少,因此未做比較。

表2 兩組患者縱向和橫向?qū)嶒?yàn)室結(jié)果比較Tab.2 Comparison of longitudinal and transverse laboratory results between the two groups M(P25,P75)
2.3 兩組患者實(shí)驗(yàn)室檢驗(yàn)異常率比較 兩組患者基線CD3+、CD4+和CD8+T 淋巴細(xì)胞減少很常見,兩組患者基線外周血LYM 和EOS 減少亦很常見。與低拷貝組橫向比較,高拷貝組第1 周LYM 和EOS減少更常見(P<0.05),而兩組患者基線時(shí)各項(xiàng)指標(biāo)異常率差異無統(tǒng)計(jì)學(xué)意義(P>0.05)。
縱向比較,低拷貝組第1 周LYM 和EOS 減少率明顯降低(P<0.05),而高拷貝組基線和第1 周LYM 和EOS 減少率差異無統(tǒng)計(jì)學(xué)意義(P>0.05,表3)。
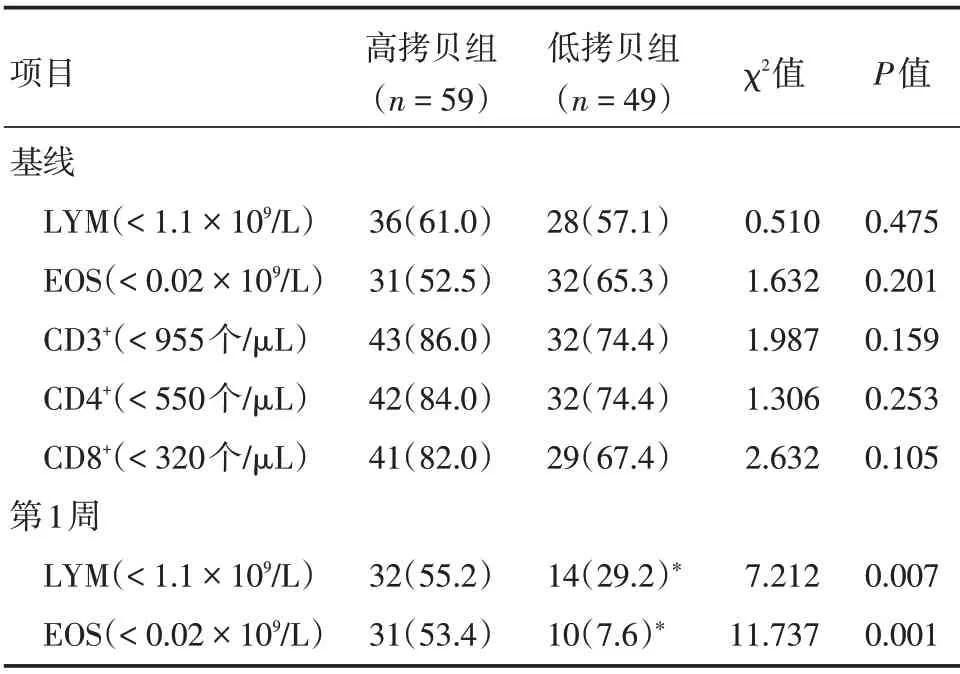
表3 兩組患者生化異常率比較Tab.3 Comparison of biochemical abnormality rates between the two groups 例(%)
2.4 相關(guān)性分析 采用Pearson 相關(guān)分析顯示,Ct 值與第1 周LYM 和EOS 呈正相關(guān)(r= 0.261、0.333,P<0.05);Ct 值與病毒轉(zhuǎn)陰時(shí)間呈負(fù)相關(guān),(r=-0.289,P<0.05)。
2.5 兩組患者治療及臨床轉(zhuǎn)歸 兩組患者均未使用任何抗病毒藥,治療上使用抗生素、激素、高流量濕化氧療和有創(chuàng)通氣差異均無統(tǒng)計(jì)學(xué)意義(P>0.05)。與低拷貝組比較,高拷貝組病毒轉(zhuǎn)陰時(shí)間更長(均P<0.05,表4),兩組患者無一例死亡,總體預(yù)后良好。
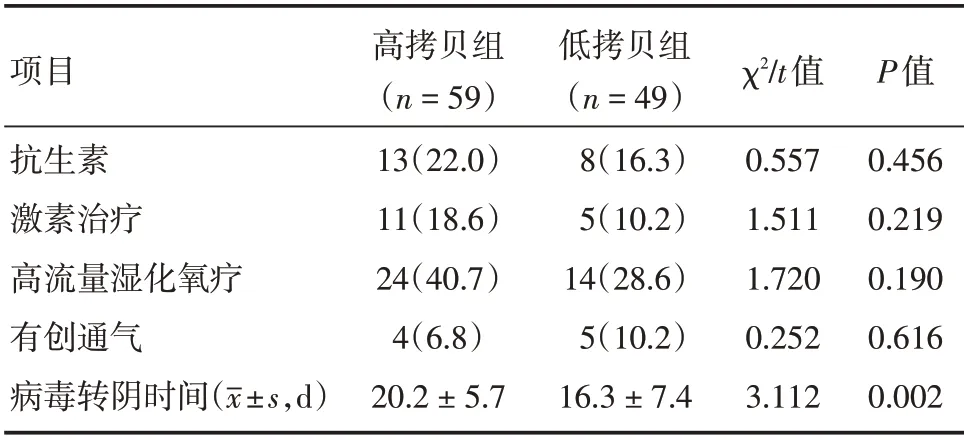
表4 兩組患者治療及臨床轉(zhuǎn)歸比較Tab.4 Comparison of treatment and clinical outcome between the two groups 例(%)
3 討論
SARS-CoV-2 去年席卷全球,成為全球公共衛(wèi)生事件,更讓人擔(dān)憂的是病毒不斷變異[4],今年5月廣州首次報(bào)道本地SARS-CoV-2 Delta 變異株感染者,廣東省疾病預(yù)防控制中心提示廣州本地流行的SARS-CoV-2 Delta 變異株病毒載量是去年野生株的1 260 倍[5],引起廣泛的關(guān)注。目前尚無Delta變異株上呼吸道病毒載量與臨床特征及病毒轉(zhuǎn)陰時(shí)間的報(bào)道,本文將本院收治的Delta 病毒株感染者情況作總結(jié),為疫情防控提供幫助。
本研究共納入108 例成年患者,采用RT-PCR檢測鼻拭子病毒核酸,Ct 值越低,說明病毒載量越高。病人Ct 最低值中位數(shù)為住院第2(0,3)d,N 基因(20.5±5.7),Orf1a/b 基因(22.1±5.7),本次疫情所有患者均為廣州市疾病預(yù)防控制中心確診當(dāng)天,立即送往我院隔離診治,這提示大多數(shù)Delta變異株患者在檢測陽性3 d 內(nèi)病毒復(fù)制最活躍,此時(shí)可能傳染性最強(qiáng)。而野生株研究資料顯示上呼吸道病毒載量峰值大概為1 周,因此,Delta 變異株比野生株病毒載量峰值更早[6]。
本研究以Ct 值20 作截點(diǎn)分為高拷貝組和低拷貝組,結(jié)果顯示高拷貝組和低拷貝組咳嗽和咳痰比例均高,其中咳嗽分別占91.5%和81.6%,兩組患者均有明顯呼吸道癥狀,這說明病毒入侵細(xì)胞途徑及呼吸道損害機(jī)制具有共性,咳嗽、咳痰與早期病毒載量無關(guān);另外,高拷貝組咽喉不適和腹瀉比例更高,而咽喉和腸上皮亦有血管緊張素Ⅱ(ACE-II)表達(dá)[7],這提示高病毒載量可能導(dǎo)致咽部黏膜及腸上皮黏膜損傷加重。
目前糖尿病患者早期病毒載量的報(bào)道少,本研究顯示,高拷貝組患者合并糖尿病的比例更高(20.3%vs.6.1%),這說明糖尿病患者早期體內(nèi)病毒復(fù)制更活躍,將有無合并糖尿病作為因變量,病毒轉(zhuǎn)陰時(shí)間作為變量,合并糖尿病患者病毒轉(zhuǎn)陰時(shí)間更長(20 dvs.17 d,P= 0.041)。糖尿病對病毒復(fù)制及清除的影響機(jī)制尚不明確,ACE-Ⅱ是SARS-CoV-2 進(jìn)入機(jī)體受體,在各種組織中均有表達(dá),包括肺、上呼吸道、心臟、腎小管、小腸黏膜和血管等[7],糖尿病患者多個(gè)組織中ACE-Ⅱ表達(dá)的增加可能增加SARS-CoV-2 感染的風(fēng)險(xiǎn)[8],同時(shí)許多降糖藥物可以增加ACE-Ⅱ的表達(dá)[9],難于控制的高血糖可促進(jìn)肺、鼻氣道、舌頭和口咽的異常ACE-Ⅱ糖基化,可能增加SARS-CoV-2 的結(jié)合位點(diǎn)[10],糖尿病除了影響SARS-Cov-2 進(jìn)入細(xì)胞,還對感染的炎癥反應(yīng)有影響,病毒清除時(shí)間更長[11],這與糖尿病患者易感染因素(中性粒細(xì)胞趨化性和吞噬功能受損)有關(guān)外,還可能與T 淋巴細(xì)胞功能受損和IL-6 等多種因子介導(dǎo)的炎癥因子風(fēng)暴有關(guān)[12]。
SARS-CoV-2 感染可激活先天性和適應(yīng)性免疫反應(yīng),淋巴細(xì)胞和嗜酸性粒細(xì)胞是參與病毒免疫清除的適應(yīng)性免疫細(xì)胞[2,13-14]。本研究高拷貝組基線CD3+、CD4+和CD8+T 淋巴細(xì)胞降低比例超過80%,低拷貝組三者降低比例約70%,其中高拷貝組CD4+T 淋巴細(xì)胞計(jì)數(shù)更低,CD3+和CD8+T 淋巴細(xì)胞計(jì)數(shù)更低趨勢,這說明SARS-Cov-2 Delta 變異株感染早期已普遍存在免疫抑制、免疫消耗,這與去年野生株免疫損傷表現(xiàn)一致[15]。筆者分析基線和第1 周淋巴細(xì)胞計(jì)數(shù)和嗜酸性粒細(xì)胞計(jì)數(shù)動態(tài)變化趨勢,兩組患者基線時(shí)淋巴細(xì)胞和嗜酸性粒細(xì)胞減少均超過50%,隨著病情遷延,1 周后高拷貝組淋巴細(xì)胞和嗜酸性粒細(xì)胞更低,恢復(fù)也更慢,Ct 值與第1 周淋巴細(xì)胞、嗜酸性粒細(xì)胞呈正相關(guān)(即病毒載量與淋巴細(xì)胞、嗜酸性粒細(xì)胞負(fù)相關(guān)),這與以往研究結(jié)論一致[16-19]。上呼吸道病毒載量與免疫細(xì)胞存在關(guān)聯(lián),這種現(xiàn)象已被學(xué)者認(rèn)知,但如何解釋這個(gè)現(xiàn)象,目前其病理生理機(jī)制尚未闡明,一般認(rèn)為機(jī)體感染SARS-CoV-2 后,宿主細(xì)胞釋放的趨化因子刺激不同免疫細(xì)胞(包括淋巴細(xì)胞、嗜酸性粒細(xì)胞等)的募集[20-21],淋巴細(xì)胞在靶器官浸潤被尸檢報(bào)告證實(shí)[22],高病毒載量可導(dǎo)致更嚴(yán)重的炎癥及免疫反應(yīng)[16,18,22],免疫清除和免疫消耗更激烈,導(dǎo)致外周血淋巴細(xì)胞降低;嗜酸性粒細(xì)胞由多能造血干細(xì)胞發(fā)育而來的,尸檢報(bào)告未顯示靶器官嗜酸性粒細(xì)胞浸潤[22],但既往研究提示病毒感染可直接抑制骨髓功能減少嗜酸性粒細(xì)胞生成[23],筆者推測SARS-Cov-2 Delta 變異株可能也具有直接抑制骨髓功能,從而影響其生命周期,具體病理生理機(jī)制需要病毒動力學(xué)研究進(jìn)一步論證。
病毒載量是否影響病毒轉(zhuǎn)陰時(shí)間、臨床診治及預(yù)后亦備受臨床關(guān)注,現(xiàn)有研究存在異質(zhì)性。首先,高病毒載量可能延緩病毒轉(zhuǎn)陰,本研究患者提示高拷貝組患者病毒轉(zhuǎn)陰時(shí)間更長(20 dvs.16 d),Ct 值與病毒轉(zhuǎn)陰時(shí)間呈負(fù)相關(guān)(即病毒載量與病毒轉(zhuǎn)陰時(shí)間呈正相關(guān)),這與LIU 等[24]研究結(jié)果一致,因此病毒載量高是病毒清除延遲的一個(gè)重要因素;然后,高病毒載量是否影響不良預(yù)后(重癥率和死亡率),目前尚無定論[25]。本研究經(jīng)積極搶救治療,無一例死亡,兩組患者重癥率和死亡率差異無統(tǒng)計(jì)學(xué)意義,高病毒載量組采用高流量濕化氧療和糖皮質(zhì)激素治療比例更高趨勢,但尚未達(dá)到統(tǒng)計(jì)學(xué)差異,由于本研究樣本量較少,尤其是重癥患者少,不排除可能造成偏倚。國內(nèi)外有關(guān)病毒載量對臨床分型、預(yù)后的影響已有不少的報(bào)道,YIN 等[19]研究提示輕型、重型和危重型COVID-19 患者的上呼吸道病毒載量相似;SALTOALEJANDRE 等[26]發(fā)現(xiàn)COVID-19 患者的病毒載量在住院期間的不利影響更高,但高病毒載量不是COVID-19 成人患者不良臨床結(jié)局(入住ICU 或死亡)的獨(dú)立危險(xiǎn)因素;MOSTAFA 等[27]采用鼻咽拭子進(jìn)行宏基因組測序表明,病毒載量的增加與早期階段相關(guān),而不是與疾病嚴(yán)重程度相關(guān),上述研究與本研究結(jié)論一致。然而,亦有綜述提示上呼吸道病毒載量與疾病嚴(yán)重程度及不良預(yù)后相關(guān)。現(xiàn)有研究很少關(guān)注疾病發(fā)病時(shí)間、采集核酸時(shí)間及核酸動態(tài)變化,而且不同的病毒株、樣本采集部位、人口學(xué)特征及檢測試劑敏感性等均可能影響病毒核酸水平,從而導(dǎo)致結(jié)果偏倚。從我院收治的Delta 變異株臨床資料分析,疾病的發(fā)生和發(fā)展可能是宿主與病毒共同作用的結(jié)果,病情進(jìn)展可能與病毒載量、宿主人口學(xué)特征、免疫損傷和炎癥風(fēng)暴等多因素有關(guān),單獨(dú)病毒載量預(yù)測不良預(yù)后的價(jià)值有限。
本研究具有一些局限性,(1)本研究病例數(shù)較少,尤其重癥患者少,僅為廣州地區(qū)、單中心病人;(2)本研究采用RT-PCR 檢測病毒核酸,并非病毒培養(yǎng)鑒定。
總之,本研究首次分析了SARS-Cov-2 Delta 變異株早期病毒核酸水平,大多數(shù)患者病毒復(fù)制最活躍是住院前3 d,上呼吸道病毒載量與第1 周淋巴細(xì)胞、嗜酸性粒細(xì)胞呈負(fù)相關(guān),與病毒轉(zhuǎn)陰時(shí)間呈正相關(guān),高病毒臷量是上呼吸道病毒延遲清除的重要因素;糖尿病可能影響上呼吸道病毒載量及病毒清除時(shí)間。另外,筆者未發(fā)現(xiàn)病毒載量與疾疾嚴(yán)重程度的關(guān)聯(lián)性。由于本研究重癥患者少,無死亡病例,病毒載量是否影響治療及預(yù)后需要進(jìn)一步臨床驗(yàn)證。COVID-19 發(fā)生、發(fā)展可能涉及病毒載量、人口學(xué)特征、炎癥風(fēng)暴、免疫抑制、免疫損傷和免疫消耗等多個(gè)因素,下一步研究可探索宿主個(gè)體化炎癥和免疫反應(yīng)對COVID-19 病程和預(yù)后的影響,采用病毒動力學(xué)研究探討病毒載量與機(jī)體免疫的病理生理機(jī)制。

