碳基層狀雙金屬氫氧化物對含氮污染物的除研究進展*
蔣柱武 焦澄遠 余 海 林宏珅 徐 斌,2 裴炎炎#
(1.福建工程學院生態環境與城市建設學院,福建 福州 350118;2.同濟大學環境科學與工程學院,上海 200092)
來源于冶金、農業(化肥農藥)、化工、染料、醫藥廢水的含氮污染物種類繁雜,危害巨大,是亟待解決的環境問題之一。嬰幼兒長期飲用硝酸鹽超標的水會導致藍色嬰兒綜合征、高鐵血紅蛋白癥,成年人暴露在硝酸鹽超標的環境中,將大幅增加罹患腦瘤、白血病、鼻咽腫瘤的風險[1];亞硝態氮作為硝態氮還原過程中的中間產物,易與仲胺反應生成具有致癌作用的亞硝胺[2];富含氨氮污染物的水體,可能引起嚴重的富營養化問題,造成水體代謝功能的喪失[3];有機含氮污染物易形成具有“三致”作用的多環類有機化合物,嚴重危害人體健康[4]。因此,解決水體含氮污染物治理問題刻不容緩。
近年來,國內外在水中含氮污染物去除領域開展了大量的研究,如膜分離法、生物處理法、折點加氯法、吸附法等。膜分離法具有能耗低、安全性高、操作方便等優勢,但受到溶脹現象和化學鍵可逆性的影響,膜的變質問題也難以忽視[5];生物處理法具有效率高、成本低等優勢,但菌種對pH、溫度、溶解氧、碳源和有毒物質濃度等因素具有高度依賴性[6],處理工藝易受環境限制;折點加氯法處理效率高、設備投資少,但易產生氯胺等消毒副產物,且液氯在使用和儲備方面也有較高的要求[7]。在常見的水處理方法中,吸附法具有耗能低、污染少、去除快、可循環等優勢,具有較大的應用前景[8]。其中,層狀雙金屬氫氧化物(LDH)與多孔碳的復合材料(LDH/C)對含氮污染物的吸附,已成為環境功能材料研究的熱點。
LDH是一種陰離子型黏土,二價金屬陽離子(M2+)和三價金屬陽離子(N3+)位于主體層板的八面體孔隙中,客體陰離子和水分子則均勻分布在層間區域。因為LDH具備記憶效應、內部結構可調性、層間陰離子可交換性等特點,所以可作為一種優異的吸附劑用于水污染處理過程中[9]。但LDH致密的堆疊結構限制了自身的吸附容量[10],因此選擇合適的基底材料具有重要的意義。多孔碳是一種以碳為骨架的多孔性材料,包括碳纖維(ACF)、碳納米管(CNT)、石墨烯(GO)等。多孔碳材料由于物化性質穩定、孔隙度高、比表面積大等特點,已廣泛應用于水處理領域[11]。以往LDH復合材料的綜述主要側重于對重金屬、抗生素等污染物的吸附研究,針對碳基LDH去除水中含氮污染物的論述不夠系統,吸附機理的闡述不夠深入,尤其缺少對實際應用過程問題的分析。基于此,本研究根據2015年以來LDH/C研究成果,系統綜述了LDH/C的合成方法;詳細介紹了LDH/C去除含氮污染物的吸附性能;重點闡述了LDH/C去除含氮污染物的吸附機理;最后,指出了LDH/C在研究過程中需要解決的問題。
1 LDH/C的合成方法
LDH/C顯著改善了原材料的表面特性和吸附性能[12],其主要合成方法包括均勻共沉淀法、水熱合成法、結構重建法等。
1.1 均勻共沉淀法
在去離子水中,將超聲處理后的多孔碳材料與含M2+、N3+鹽溶液在受控的堿性條件下混合反應,再將稠密的懸浮液經去離子水沖洗多次后過濾、干燥,得到LDH/C。
DAUD等[13]將超聲處理后的GO溶液與前體鹽溶液按照摩爾比3∶1混合,混合過程中以1 mol/L NaOH溶液維持混合物pH為10.0±0.1,混合攪拌24 h后將黑色稠密懸浮液離心、洗滌、干燥,制備了以GO為碳基骨架的MgAl-LDH復合材料,相較于單一的MgAl-LDH,該復合材料具有較高的熱穩定性、良好的結晶度和較好的催化吸附性能。LINS等[14]將處理后的生物炭(BC)加入Mg、Al鹽溶液中,以NaOH溶液調控混合物pH為10,攪拌4 h后,經離心、洗滌、干燥,制得復合材料MgAl-LDH/BC。
1.2 水熱合成法
水熱合成法是將含M2+、N3+的鹽溶液與多孔碳材料混合后置于特定的密封容器中,在高溫高壓條件下復合的方法。相較于均勻共沉淀法,通過水熱合成法制備的LDH/C的結晶度更高、顆粒更均勻[15]。
WU等[16]將磁性氧化GO超聲處理形成懸浮液,并與前體鹽溶液和六亞甲基四胺(HMT)混合攪拌,再在140 ℃下反應12 h,構筑了磁鐵礦-氧化GO-LDH復合材料(MGL)。與MgAl-LDH相比,MGL的吸附容量更高、比表面積更大、活性位點更多,污染物的去除效果更好。LINGHU等[17]將超聲處理后的GO溶液與MgCl2、AlCl3、HMT溶液均勻混合,再在140 ℃下反應12 h,合成了復合材料MgAl-LDH/GO。
1.3 結構重建法
結構重建法是利用LDH特有的“記憶特性”,制備層間含不同陰離子的LDH復合材料。將LDH/C在一定溫度下煅燒為雙金屬氧化物(LDO)和多孔碳的復合材料,再作為吸附劑加入含陰離子的目標溶液中,得到層間插入特定陰離子的LDH/C[18]。
ZHANG等[19]將單壁碳納米管(SWCNTs)超聲處理后,通過均勻共沉淀法制備了復合材料MgAl-LDH/SWCNTs,再將制備的MgAl-LDH/SWCNTs在N2中500 ℃下煅燒4 h后制得復合材料MgAl-LDO/SWCNTs,并在陰離子溶液中恢復了特定的層板結構。ZHANG等[20]采用均勻共沉淀法制備了復合材料MgAl-LDH/BC,并在馬弗爐中500 ℃下煅燒2 h,制得復合材料MgAl-LDO/BC。該方法有效改善了原材料的孔隙率,增大了表面積,并促進了復合材料表面官能團的形成。
均勻共沉淀法和水熱合成法制備的復合材料一般具有比表面積較大、物化性質穩定、結晶度較高等優點。其中,均勻共沉淀法能效高,反應過程和條件易于控制,方便大規模應用,但是粒徑范圍難以控制;水熱合成法可通過控制反應時間和溫度,較好地控制粒徑、結晶程度[21]。結構重建法有助于改善復合材料的孔隙結構,增加比表面積,從而提高對水中含氮污染物的吸附能力。LDH/C對含氮污染物的吸附親和力,很大程度取決于其理化性質,因此學者們進一步對LDH/C的吸附性能進行了研究。
2 LDH/C的吸附性能
碳元素的軌道雜化方式多樣(sp、sp2、sp3雜化),當碳元素以不同的雜化軌道成鍵時,便形成了物化性能迥異的碳質材料[22-23]。隨著時代的發展和科學的進步,越來越多的多孔碳材料被發現,也就為LDH/C在去除氮污染領域的進一步研究奠定了基礎。目前,LDH/C研究主要針對單一污染源,表1列舉了不同種類的LDH/C的吸附性能。
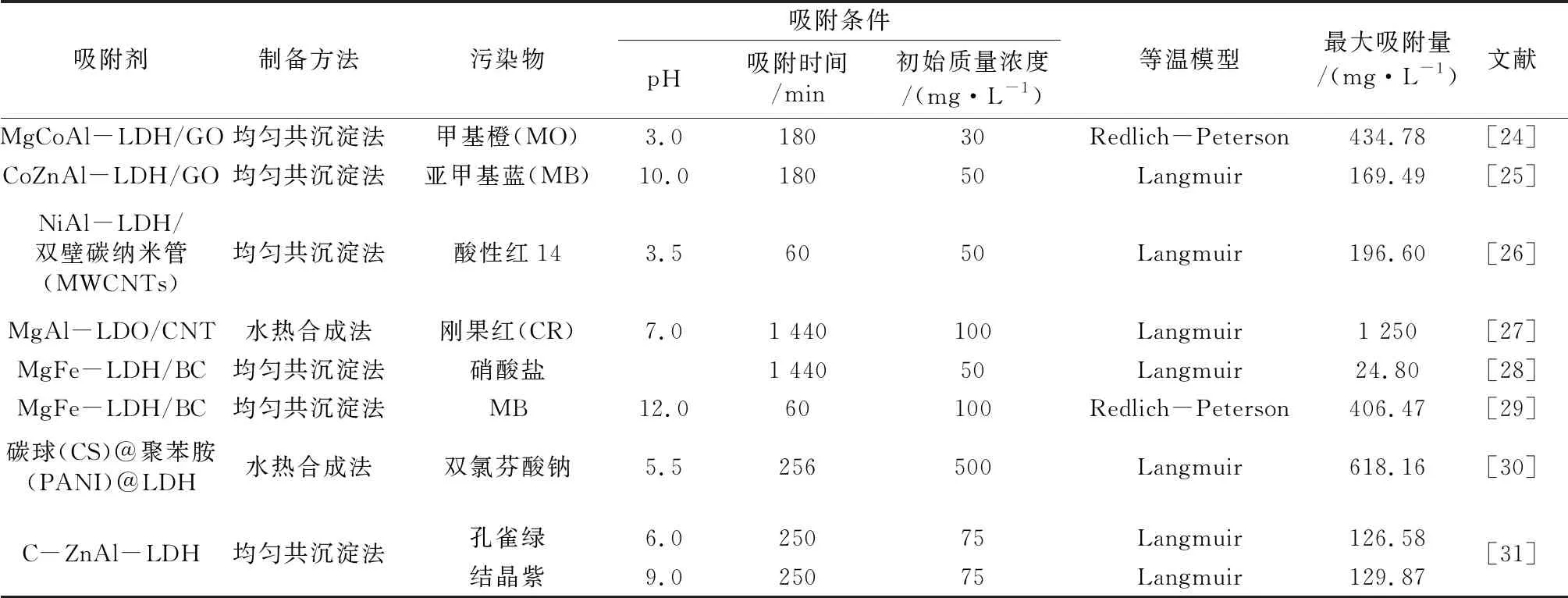
表1 LDH/C的吸附性能Table 1 Adsorption performance of LDH/C
2.1 LDH/GO
GO是一種理化性質出色的二維碳納米材料,被廣泛應用于吸附、離子交換等領域的研究。氧化GO是GO的氧化衍生材料,具有高度發達的孔隙結構、較大的比表面積和極豐富的含氧官能團,因此在凈水領域展現出巨大的應用前景。
KAZEEM等[24]通過均勻共沉淀法制備了三元復合材料MgCoAl-LDH/GO,對MO最大吸附量達434.78 mg/g。MgCoAl-LDH/GO相較于傳統的LDH材料,其比表面積更大、含氧官能團更多,可為MO提供更多的活性位點。SHARIFI BONAB等[25]通過均勻共沉淀法制備了三元復合材料CoZnAl-LDH/GO,該復合材料對MB最大吸附量為169.49 mg/g;該團隊指出,MB上的芳香環可與CoZnAl-LDH/GO形成π-π鍵,進而吸附在CoZnAl-LDH/GO的表面上,提高了CoZnAl-LDH/GO的吸附能力。
2.2 LDH/CNT
CNT是由石墨層卷曲而成的無縫納米管狀材料,根據構成CNT的石墨層數,可分為單壁管、雙壁管、多壁管。CNT具有化學穩定性好、熱穩定性高、機械強度穩定等優勢,且CNT的空心分層結構,使其具有較高的比表面積、較好的吸附性能,在去除含氮污染物研究領域具有極大的應用潛力。
KHODAM等[26]通過均勻共沉淀法將Ni、Al摩爾比為1∶1的NiAl-LDH負載在MWCNTs上得到NiAl-LDH/MWCNTs,用于去除溶液中的酸性紅14。結果表明,溶液初始pH為3.5時,加入0.015 g吸附劑,60 min后可對50 mg/L酸性紅14溶液達到99.04%的吸附效果。相較于傳統的NiAl-LDH,NiAl-LDH/MWCNTs的比表面積更大,且有效減少了LDH材料堆疊現象的出現。YANG等[27]制備的復合材料MgAl-LDO/CNT對CR的最大吸附量為1 250 mg/g。由于LDH材料獨有的“記憶效應”,MgAl-LDO/CNT在CR溶液中重構為表面帶正電性的LDH材料,進而達到對陰離子的吸附效果;CR表面的活性基團(C—OH和COO—)與CNT表面形成的分子間氫鍵進一步提高了對CR的吸附效果。
2.3 LDH/BC
BC具有較好的吸附能力、較高的比表面積、較多的含氧官能團,是LDH可供選擇的載體材料之一。LDH/BC可有效減少LDH團聚現象的出現,并且增大了材料的比表面積,有利于增強材料的吸附性能。
XUE等[28]采用均勻共沉淀法制成復合材料MgFe-LDH/BC,研究其對溶液中的硝酸鹽的吸附性能。結果表明,0.1 g MgFe-LDH/BC可對50 mg/L的硝酸鹽溶液達到30.4%的吸附效果;共存陰離子磷酸鹽和硫酸鹽對吸附效果影響不大,且在50 mg/L的氨根離子干擾下,對硝酸鹽的吸附效果也達到了22.2%。MEILI等[29]采用均勻共沉淀法制成復合材料MgFe-LDH/BC,該復合材料對MB的最大吸附量可達406.47 mg/g。相較于單一的BC材料,MgFe-LDH/BC的孔隙體積減少,表面積增大,證明LDH納米顆粒負載在BC的孔隙中,增大了MgFe-LDH/BC的比表面積,有利于改善MgFe-LDH/BC對MB的吸附效果。
2.4 其他復合材料
XU等[30]合成了復合材料CS@PANI@LDH,測得其對雙氯芬酸鈉的最大吸附量為618.16 mg/g。該團隊提出,CS@PANI@LDH通過靜電引力、氫鍵作用、π-π鍵作用去除溶液中的雙氯芬酸鈉;PANI促使CS和LDH形成良好的結合效果,且含有的胺基和亞胺基有助于氫鍵的生成,提高了對污染物的去除效果;CS@PANI@LDH形成的核殼結構有效防止了LDH聚集現象的出現。GEORGE等[31]將碳包覆在ZnAl-LDH上,制備了復合材料C-ZnAl-LDH,對孔雀綠和結晶紫最大吸附量分別為126.58、129.87 mg/g。該團隊提出,碳涂抹在LDH上有助于C-ZnAl-LDH和染料產生分子間氫鍵,進而達到對染料良好的吸附效果。
3 LDH/C對含氮污染物的吸附機理
LDH/C的吸附機理取決于吸附劑和污染物的種類。通常而言,LDH/C對含氮污染物的吸附機理主要是靜電引力、陰離子交換、化學鍵作用。
3.1 靜電引力
LDH/C對于含氮染料的吸附,主要可歸因于其帶電表面與含氮染料之間的靜電引力[32]。納米碳材料表面存在的含氧官能團充當了染料的活性位點,LDH通過靜電作用吸附去除含氮染料。當pH>等電點(pHpzc)時,LDH表面帶負電荷,有利于吸附陽離子染料;當pH ZHANG等[33]制備了納米碳為碳基骨架的復合材料MgAl-LDH。調節吸附介質的pH時發現,MgAl-LDH在吸附過程存在pH依賴性,即在酸性介質中MgAl-LDH顯正電性,與陰離子染料甲基藍存在靜電引力作用,可顯著提高對甲基藍染料的吸附效果。HU等[34]制備了復合材料NiFe-LDH/ACF,對MO和CR的最大吸附量分別為323.6、448.4 mg/g。該課題組進一步通過Zeta電位對吸附機理進行闡述,在中性條件下NiFe-LDH/ACF的Zeta電位為6 mV,與陰離子染料所帶電荷相反,從而快速去除溶液中的含氮染料。 綜合表1可看出,LDH/C對陰陽離子染料主要表現為單分子層吸附,符合Langmuir模型的擬合結果,即通過改變溶液的pH可提升含氮染料的去除效果。目前,對復合材料的研究主要集中于單一污染源,對多種含氮污染物的競爭吸附性能和機理的研究還不夠深入。 LDH層間陰離子基團可分為4類:無機陰離子、有機陰離子、配合物陰離子、同多和雜多陰離子,可見LDH/C可用作多種陰離子的吸附劑。LDH/C的主體與客體之間超分子作用機理十分復雜,與層間離子的交換能力、層板的溶脹性能、層板的電荷密度、交換過程的pH和LDH材料的組成等因素都有著密切關系。目前,對超分子作用機理的研究仍稍顯薄弱,還需要進一步探索。 LDH/C對于水中含氮污染物的吸附機理,不僅有靜電引力、離子交換,還由于LDH本身富含的大量羥基(—OH)和碳材料表面的含氧原子基團,易與含氮污染物以分子間氫鍵、π-π鍵等化學鍵相連,從而提高了對污染物的去除能力[39]。 LI等[40]制備了復合材料MgAl-LDH/ACF,并以二甲胺四環素(MC)為研究對象,對比分析煅燒前后MgAl-LDH/ACF的吸附能力。根據煅燒后MgAl-LDH/ACF對MC的吸附容量大幅減弱的現象,該團隊提出MC是芳香族化合物,有氫鍵的供體/受體基團,可與ACF表面的含氧或含氮官能團形成氫鍵,提高了MgAl-LDH/ACF的吸附容量,而煅燒后MgAl-LDH/ACF的官能團遭到了破壞,因此吸附容量下降。ZHENG等[41]通過水熱合成法制備了復合材料NiFe-LDH/GO,并測試其對CR、MO等含氮染料的吸附效果。該課題組提出,CR分子中存在—NH2,可與NiFe-LDH/GO中的—OH形成氫鍵改善吸附性能;CR和MO中的苯環可通過π-π鍵與GO相互結合,進一步增強NiFe-LDH/GO對含氮染料的吸附效果。 LDH表面的金屬鍵合羥基和多孔碳材料表面的烷氧基(—CO)、—OH等含氧官能團,易與染料等有機分子表面的官能團形成分子間氫鍵;有機分子表面存在的苯環、碳基鍵團(C—O、C—OH、C—N)等易與多孔碳材料表面的官能團以C=C鍵的形式結合,從而提高了LDH/C對有機分子的吸附能力。 LDH/C可充分發揮各組分材料的協同作用。LDH材料本身可通過靜電引力作用吸附含氮污染物,且由于具有獨特的超分子插層結構,因此更可通過離子交換去除污染物;多孔碳材料為LDH的生長提供了更多的成核位點,有效減少了聚集堆疊現象的出現概率,且由于表面富含大量的含氧官能團,不僅為吸附污染物提供了活性位點,且可通過分子間氫鍵等化學鍵的作用提高對污染物的吸附效果。但目前對LDH/C的研究仍處于起步階段,還不能大規模應用于實際水體,仍需深入探索。 LDH/C吸附含氮污染物已是目前研究的熱點之一,但還缺乏將其投入實際污染水體的長期性研究。今后的研究內容應注重以下4個方面:(1)進一步探究LDH/C對多種含氮污染物的競爭吸附性能和機理;(2)不僅是在去除有機氮領域,更應探究LDH/C對無機氮的去除效果;(3)分子模擬法已被應用到探究超分子作用機理的研究中,但相關的理論闡述仍顯薄弱,需進一步研究;(4)LDH/C吸附含氮污染物的研究大部分停留在實驗階段,缺乏一些實際應用的數據,需進一步解決流程設計、成本估算、循環利用等實際應用難題。3.2 離子交換
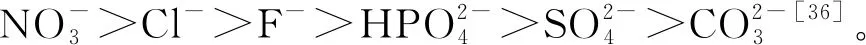
3.3 化學鍵作用
4 結 語

