苯酚與碳酸鈉反應再探究
張立惠 賈衛國 后勇軍 孫影




摘要:針對苯酚和碳酸鈉反應實驗過程中出現的異常現象,通過設計對比實驗,運用紫外分光光度計檢驗反應產物,提供證據支持,詳細分析并闡釋苯酚與碳酸鈉溶液反應過程中產生二氧化碳的原因。
關鍵詞:苯酚;碳酸鈉;數字化實驗;紫外光譜
文章編號:1008-0546(2022)05-0095-03中圖分類號:G632.41文獻標識碼: B
doi:10.3969/j.issn.1008-0546.2022.05.021
一、問題的提出
人教版高中化學教材(2019版)[1]中介紹了苯酚和碳酸鈉溶液反應生成苯酚鈉和碳酸氫鈉,而在實驗過程中,筆者采用CO2傳感器測量密閉體系內碳酸鈉溶液和苯酚溶液混合之后CO2含量的變化,一段時間后發現 CO2的含量增加。為什么會出現“CO2含量增加”的異常現象?已有文獻對該問題的研究較少,多集中在通過平衡常數的計算,從理論上進行分析和討論說明苯酚和碳酸鈉反應只能生成苯酚鈉而不能產生CO2[2-3]。為探究實驗結果與理論相違背的原因,本研究利用數字化實驗與現代儀器分析技術,對實驗現象進行詳細的原理分析及證據推理,以期幫助學生克服認知困難,并對中學化學教學提出建議。
二、實驗過程
1.實驗目的
從理論上分析,苯酚與碳酸鈉溶液反應生成碳酸氫鈉與苯酚鈉,但在實驗過程中,卻檢測出大量的二氧化碳氣體產生。本研究使用Vernier無線 CO2傳感器,對苯酚與碳酸鈉混合溶液中的CO2含量進行測定。
2.實驗儀器與試劑
Vernier無線 CO2傳感器、恒溫油浴鍋(含攪拌功能)、電腦及配套軟件(Vernier Graphical Analysis)、錐形瓶(250 mL)、量筒(50 mL)、磁子、0.5 mol/L碳酸鈉溶液、0.5 mol/L苯酚溶液
3.實驗裝置
見圖1。
4.實驗步驟
(1)檢查裝置氣密性:向錐形瓶中通入適量CO2氣體,將CO2傳感器插入錐形瓶,觀察CO2測定含量示數是否穩定,若不穩定則需要對瓶口磨口部分進行進一步處理,示數穩定后方可進行實驗;
(2)分別取0.5 mol/L碳酸鈉溶液、0.5 mol/L 苯酚溶液各20 mL置于同一錐形瓶(250 mL)中,迅速插入 CO2傳感器,置于30℃油浴鍋中;
(3)啟動磁力攪拌功能,點擊數據采集按鈕,待曲線趨于穩定時停止采集,重復實驗3次,以取得最佳實驗曲線。
(4)以相同實驗步驟測定20 mL 0.5 mol/L碳酸鈉溶液與20 mL水混合時CO2含量。
5.實驗結果與分析
通過圖2可以發現,0.5 mol/L碳酸鈉溶液與0.5 mol/L苯酚溶液反應時,測定體系CO2含量持續緩慢上升;將 20 mL苯酚替換為20 mL水后,測定體系 CO2含量持續下降,且下降速率較快直至趨于穩定。
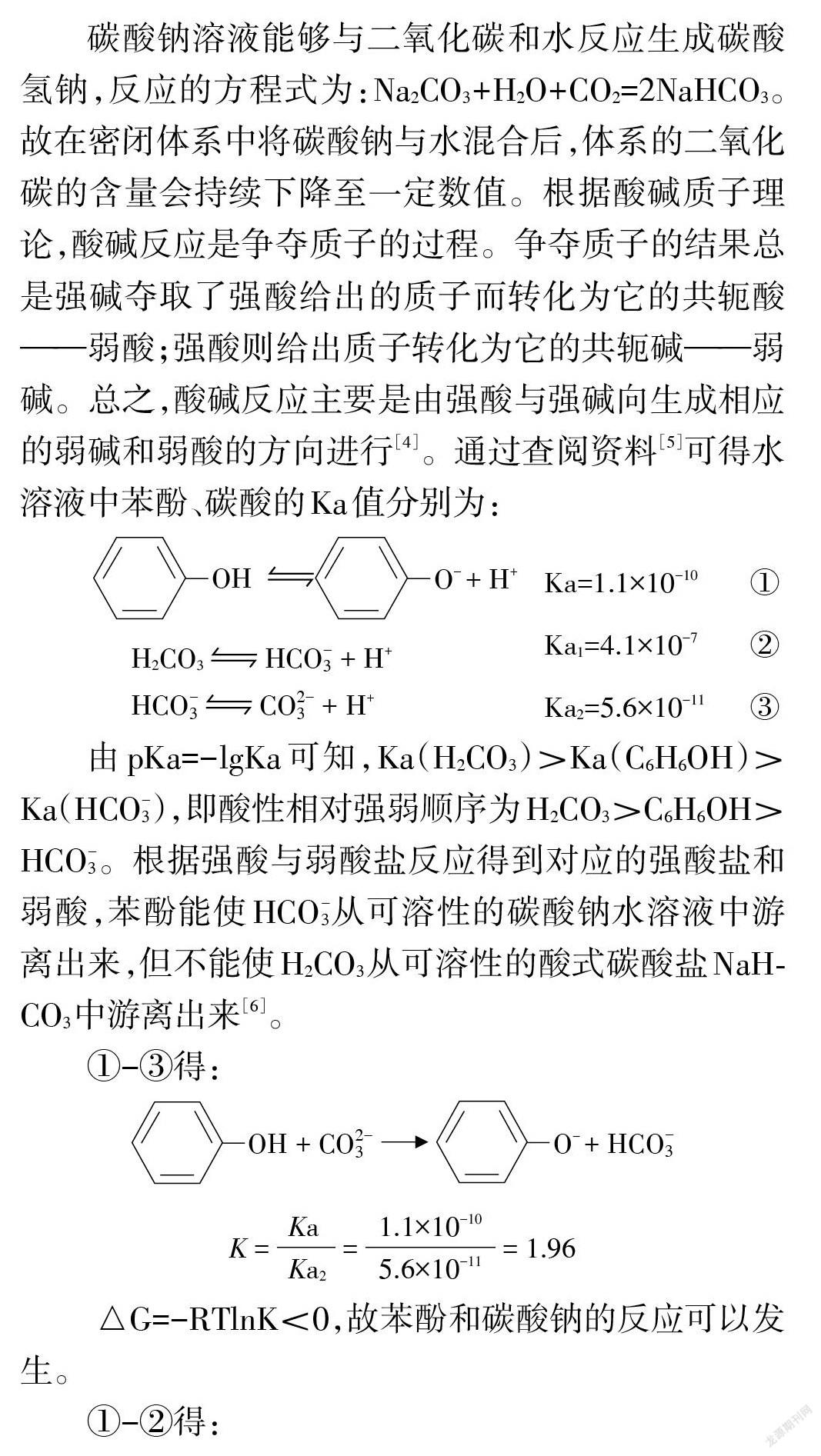
碳酸鈉溶液能夠與二氧化碳和水反應生成碳酸氫鈉,反應的方程式為: Na2CO3+H2O+CO2=2NaHCO3。故在密閉體系中將碳酸鈉與水混合后,體系的二氧化碳的含量會持續下降至一定數值。根據酸堿質子理論,酸堿反應是爭奪質子的過程。爭奪質子的結果總是強堿奪取了強酸給出的質子而轉化為它的共軛酸——弱酸;強酸則給出質子轉化為它的共軛堿——弱堿。總之,酸堿反應主要是由強酸與強堿向生成相應的弱堿和弱酸的方向進行[4]。通過查閱資料[5]可得水溶液中苯酚、碳酸的Ka值分別為:
由pKa=-lgKa 可知,Ka(H2CO3)>Ka(C6H6OH)> Ka(HCO-3),即酸性相對強弱順序為H2CO3>C6H6OH> HCO-3。根據強酸與弱酸鹽反應得到對應的強酸鹽和弱酸,苯酚能使 HCO-3從可溶性的碳酸鈉水溶液中游離出來,但不能使H2CO3從可溶性的酸式碳酸鹽NaH? CO3中游離出來[6]。
①-③得:
△G=-RTlnK<0,故苯酚和碳酸鈉的反應可以發生。
①-②得:
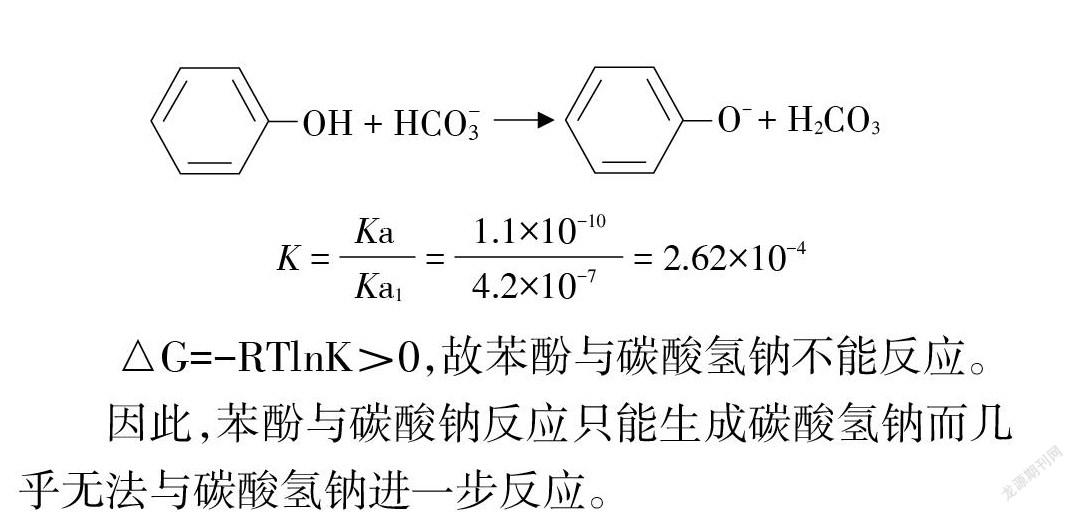
△G=-RTlnK>0,故苯酚與碳酸氫鈉不能反應。
因此,苯酚與碳酸鈉反應只能生成碳酸氫鈉而幾乎無法與碳酸氫鈉進一步反應。
6.對實驗異常現象的解釋探究
通過理論分析可以得出結論,苯酚與碳酸鈉反應產物不可能產生 CO2,而實驗測定碳酸鈉溶液與苯酚溶液反應體系CO2含量確實有所升高,對此提出猜想:是否是碳酸氫鈉的分解導致體系CO2含量的升高?基 于此,利用無線CO2傳感器測定碳酸氫鈉溶液和苯酚共體系及理論計算濃度下碳酸氫鈉溶液單體系的CO2 含量變化,結果如圖3所示:
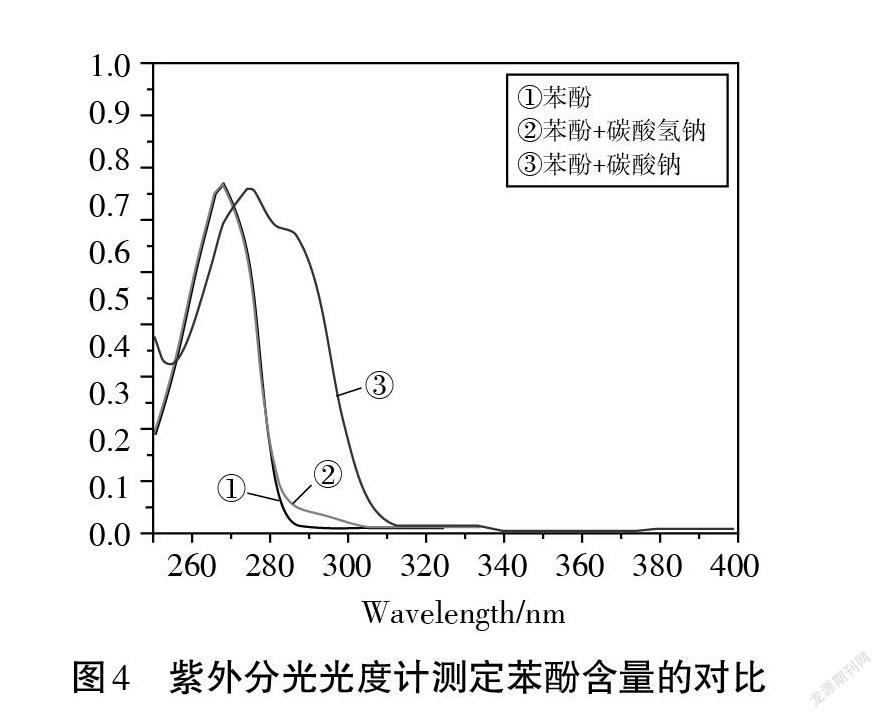
通過圖3可以發現,盡管理論上碳酸氫鈉溶液和苯酚溶液并不會反應,但實驗測得相同溫度下,碳酸氫鈉溶液與苯酚溶液共體系下CO2含量比碳酸氫鈉溶液單體系的CO2含量更高。為了進一步探究苯酚與碳酸氫鈉是否真的發生反應產生少量 CO2。為此,本實驗采用紫外分光光度計來監測苯酚與碳酸氫鈉體系,測定反應前后苯酚含量的變化,并將其與苯酚與碳酸鈉進行對比,結果如圖4所示:
查閱文獻可知,苯酚的最大吸收波長為270 nm[7],由圖4可知,苯酚與碳酸氫鈉混合之后的溶液與苯酚溶液的紫外吸收光譜均在270 nm 出現了峰值且基本重合,苯酚的量幾乎沒有減少,說明苯酚幾乎未與碳酸氫鈉發生反應。而苯酚與碳酸鈉混合之后的溶液紫外吸收光譜發生了紅移,這是由于苯酚與碳酸鈉反應過程中,生成的苯酚負離子,由于其與苯環的共軛增強,使其紫外吸收發生了紅移,由此說明了苯酚和碳酸鈉發生反應生成了苯酚鈉。
Na2CO3溶液與苯酚反應生成 NaHCO3和苯酚鈉, NaHCO3溶液從室溫升高到30℃,有利于反應④、⑤、⑥平衡右移,CO2濃度升高。
在 NaHCO3+ 苯酚的體系中存在可逆反應⑦,由于該反應的平衡常數K=2.62×10-4,宏觀上可以認為苯酚與 NaHCO3不反應,但該反應在實驗條件下可以很快建立平衡,所以,有少量 H2CO3生成,從而有少量 CO2氣體放出,通過傳感器檢出。
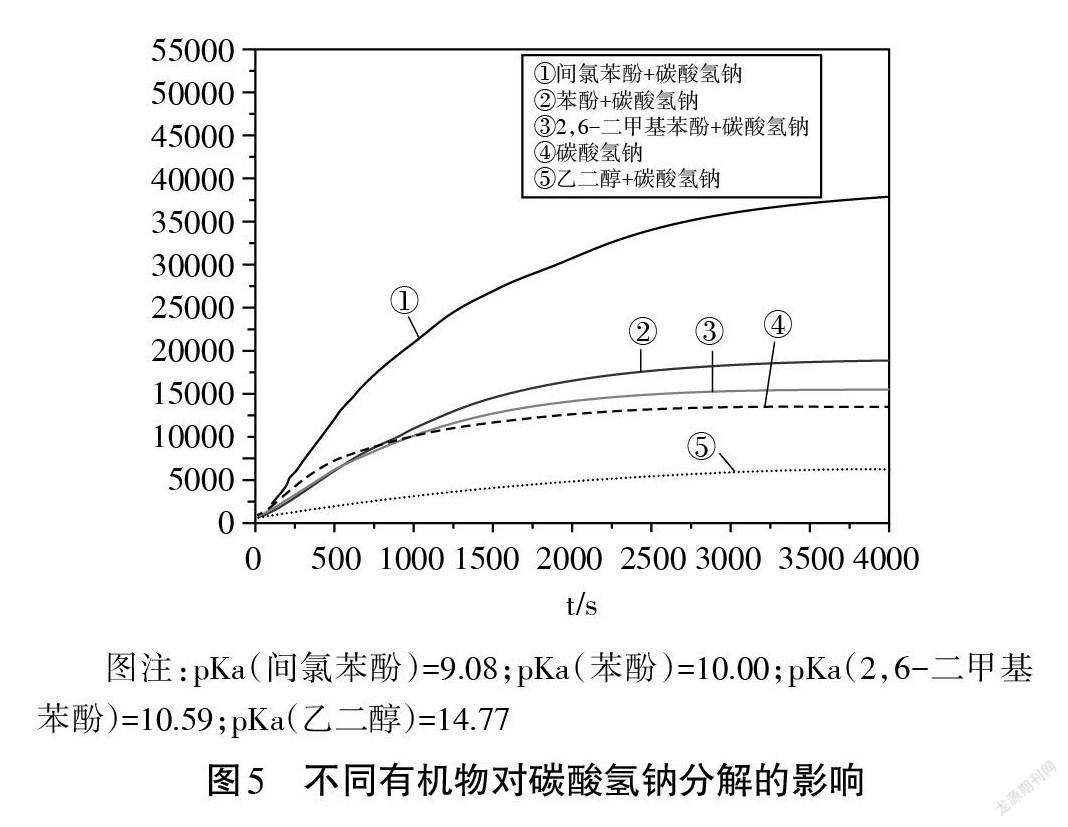
為此,本研究繼續探究了不同pKa 的有機物是否會對碳酸氫鈉的分解產生影響。研究選取幾種均不與碳酸氫鈉反應且 pKa 各不相同的有機物(間氯苯酚、苯酚、2,6-二甲基苯酚、乙二醇),并將上述有機物分別與碳酸氫鈉溶液混合后,測定體系內二氧化碳含量的變化。
由圖5可以看出,在30℃條件下,20 mL 0.5 mol/L 的上述幾種有機物分別與相同體積、相同濃度的碳酸氫鈉溶液混合后,測定體系內CO2含量的變化。結果發現,有機物pKa值越大,碳酸氫鈉分解產生的CO2越少。因此,在相同溫度下碳酸氫鈉溶液與苯酚溶液共體系產生的CO2比單獨碳酸氫鈉溶液產生的CO2含量更高。
三、實驗結論與啟示
1.實驗結論
碳酸鈉溶液與苯酚發生反應,生成了苯酚鈉和碳酸氫鈉。數字化實驗中檢測到的二氧化碳,來源于反應產物碳酸氫鈉的分解,且苯酚體系對碳酸氫鈉分解有促進作用。曲線表征為學生深刻理解苯酚與碳酸鈉溶液的反應提供了強有力的證據支持。同時運用現代技術,如紫外光譜的吸收峰再一次佐證了苯酚與碳酸鈉溶液反應生成了碳酸氫鈉的結論。
2.實驗啟示
本研究利用CO2傳感器多角度逐步探究苯酚與碳酸鈉的反應,以“發現問題-解決問題-發現新問題-解決新問題”的探究進程,促進學生對化學反應異常現象的深度研究。利用現代實驗測試技術為化學反應提供強有力的證據,回應并澄清了學生存在的疑惑,讓學生感受到化學技術進步的同時,引導學生基于證據進行推理,引發學生高階思維。
參考文獻
[1]人民教育出版社,課程教材研究所,化學課程教材研究開發中心.普通高中教科書:化學(選擇性必修3)[M].北 京:人民教育出版社,2019:62.
[2]魏釗,林丹.關于苯酚和碳酸鈉反應的再探討[J].化學教學,2009(8):46-47.
[3]季美娟.關于苯酚和碳酸鈉反應的探討[J].化學教育,2007(3):51.
[4]大連理工大學無機化學教研室.無機化學(第五版)[M].北京:高等教育出版社,2006:112.
[5]武漢大學.分析化學(第五版)[M].北京:高等教育出版社,2006:383-384.
[6]萬新軍,宋明友.苯酚溶于碳酸鈉嗎?[J].化學教育,1994(9):37-38.
[7]麥麥提圖爾蓀·塔伊爾,亞森江·吾甫爾,買買提熱夏提·買買提,等.紫外吸收光譜法測定污染廢水中苯酚含量的研究[J].環境污染與防治,2015,37(2):111.

