運用化學學科解釋促進化學學科理解
王茂力


摘要: 化學教學中開展解釋類活動是提升學生化學學科理解水平的有效手段,也是實現(xiàn)“素養(yǎng)落地”的具體途徑之一。結(jié)合課堂教學案例,提出創(chuàng)設化學學科解釋類活動的兩種方式: 追求本原性方式和促進內(nèi)容結(jié)構(gòu)化方式。
提出對解釋類活動進行評價的三個要素——領(lǐng)域、結(jié)構(gòu)與表征。
關(guān)鍵詞: 化學學科理解; 化學學科解釋; 課堂教學; 解釋類活動
文章編號: 10056629(2022)04005606
中圖分類號: G633.8
文獻標識碼: B
1 問題的提出
在高三后期的多次學情分析中,筆者發(fā)現(xiàn)主觀解釋類題目得分率一直偏低,而且一些本以為“穩(wěn)當”的知識點,卻往往在這類題目面前顯得“搖搖欲墜”。比如對水解本質(zhì)的考查——結(jié)合化學用語解釋氯化鐵對水電離的影響——不少學生回答: 氯化鐵抑制水的電離,原因是水解生成了鹽酸,F(xiàn)eCl3+3H2OFe(OH)3+3HCl,酸抑制水的電離。這才發(fā)現(xiàn)較多學生關(guān)于電離及水解的知識僅停留在對結(jié)論的機械儲存,對水解本質(zhì)還未真正理解。
這不禁引起筆者反思: 如果教學中沒有設計需要學生表達的解釋類問題,學情評估豈不偏差較大?是否平日教學時重結(jié)論而輕過程,導致學生思維流于表面,缺乏歷練,所獲知識孤立、固化而不能有效關(guān)聯(lián)?如果在教學中重視創(chuàng)設解釋類活動并進行有效評價,是否會促進學生化學學科理解水平?
2 相關(guān)概念
2.1 化學學科理解
《辭海》將“理解”定義為“應用已有知識揭露事物之間的聯(lián)系從而認識新事物的過程”[1]。并將理解分為兩類: 一類為“揭露事物間內(nèi)在聯(lián)系的理解”,如對事物因果關(guān)系的確定,另一類為“揭露事物間外部聯(lián)系的理解”。原上海市中學化學課程標準(2004年版)將“理解”作為自然科學學習領(lǐng)域中學生需要達到的“認知水平”要求之一,界定為“把握學習內(nèi)容的由來、意義和主要特征,是對知識的一般認識”[2]。《普通高中化學課程標準(2017年版)》則更具體地提出了“化學學科理解”的概念,將其界定為“對化學學科知識及其思維方式和方法的一種本原性、結(jié)構(gòu)化的認識”[3]。明確了“理解”中所需認識的對象——化學學科知識、思維方式方法,以及能稱得上“理解”層次的認識特點——本原性、結(jié)構(gòu)化。劉英琦[4]進一步對理解的層次進行分類: 經(jīng)驗性理解、本質(zhì)性理解、結(jié)構(gòu)化理解、文化性理解,為知識向素養(yǎng)轉(zhuǎn)化提供了理論指導和實踐方法。
由于“理解”過程為個體的內(nèi)隱心理活動,不可直接觀測評價,故有學者對“化學學科理解”的外在表現(xiàn)予以說明。如“能運用不同的化學方法表征化學學科知識,在學習過程中認同化學學科的育人功能和社會價值,形成化學學科的本質(zhì)認知和具有化學學科特征的科學思維,運用化學知識去認識自然世界,從化學視角去探究、分析和解決與化學相關(guān)的問題或社會議題”[5]。
化學學科理解的形成、發(fā)展或評價一般需要相關(guān)的課堂活動作為載體。通過實踐,筆者認為在化學課堂中創(chuàng)設“解釋類活動”,讓學生深度參與該類活動,是促進其化學學科理解的有效方式。
2.2 化學學科解釋
王后雄[6]等認為,科學哲學家對“科學解釋”的本體討論是從邏輯結(jié)構(gòu)和語用學角度進行的,深入且復雜,而作為教育實踐者則可采取較寬松的哲學立場上對“科學解釋”的定義: 是指在課堂場域之中教學主體的科學解釋行為與能力等。其基本內(nèi)涵是解釋者通過理論或方法來闡述自然現(xiàn)象背后的原因或發(fā)生過程。
由于化學教育屬于科學教育的一部分,因此本文將“化學學科解釋”作為“科學解釋”的一個學科分支,其內(nèi)涵為解釋者基于自身化學學科理解水平,采用化學學科特有的知識、理論、認知方式,通過外顯的行為對現(xiàn)象發(fā)生的原因或者過程用恰當?shù)谋碚鞣绞接枰躁U述。此處“現(xiàn)象”包括兩類: 一類是常見的自然現(xiàn)象或生活現(xiàn)象,一類是需要人為創(chuàng)設或挖掘的“非表層”現(xiàn)象,如實驗現(xiàn)象或數(shù)據(jù)規(guī)律等。
需要注意的是,與一般的化學問題、概念等解釋不同,本文所指化學學科解釋與化學學科理解有一定的對應關(guān)系。筆者借鑒劉英琦對理解的層次分類,認為能起到促進化學學科理解的解釋類活動至少需具備如下條件之一: 能夠觸動學生對之前已有經(jīng)驗產(chǎn)生質(zhì)疑,從而轉(zhuǎn)化、升華為經(jīng)驗性理解,如以“氯水為何呈淺黃綠色”開展解釋活動,從而對“化學反應是單向的不可逆的”前概念形成沖擊;能引導學生深入挖掘從而內(nèi)化為本質(zhì)性理解,如從微觀層面解釋影響物質(zhì)體積的因素,步步深入探究,從而對“宏微觀”形成有一定深度的認識;能帶動學生將已有知識活化、關(guān)聯(lián)而外化成結(jié)構(gòu)性理解,如對硫化氫在生活、生產(chǎn)中的多個“異象”尋求解釋,諸多單一的知識點就可形成有一定功能的結(jié)構(gòu);能與相關(guān)化學史、綠色化學、人本思想關(guān)聯(lián),從而觸動學生心靈生成文化性理解。
3 教學中創(chuàng)設解釋類活動的實踐
3.1 創(chuàng)設解釋類活動的兩種方式
課程標準對化學學科理解內(nèi)涵的界定,為教學中解釋類活動的設計提供了參考。
3.1.1 追求本原性方式: 刨根究底,尋求本原
這種方式一般用于學習新的概念、原理和觀念等,以探尋某表象的合理解釋為活動主線。由表及里的逆向溯源過程,將涉及相關(guān)知識、觀念、方法的系統(tǒng)化建構(gòu),使化學學科理解得到促進。
案例1 氣體摩爾體積教學片斷
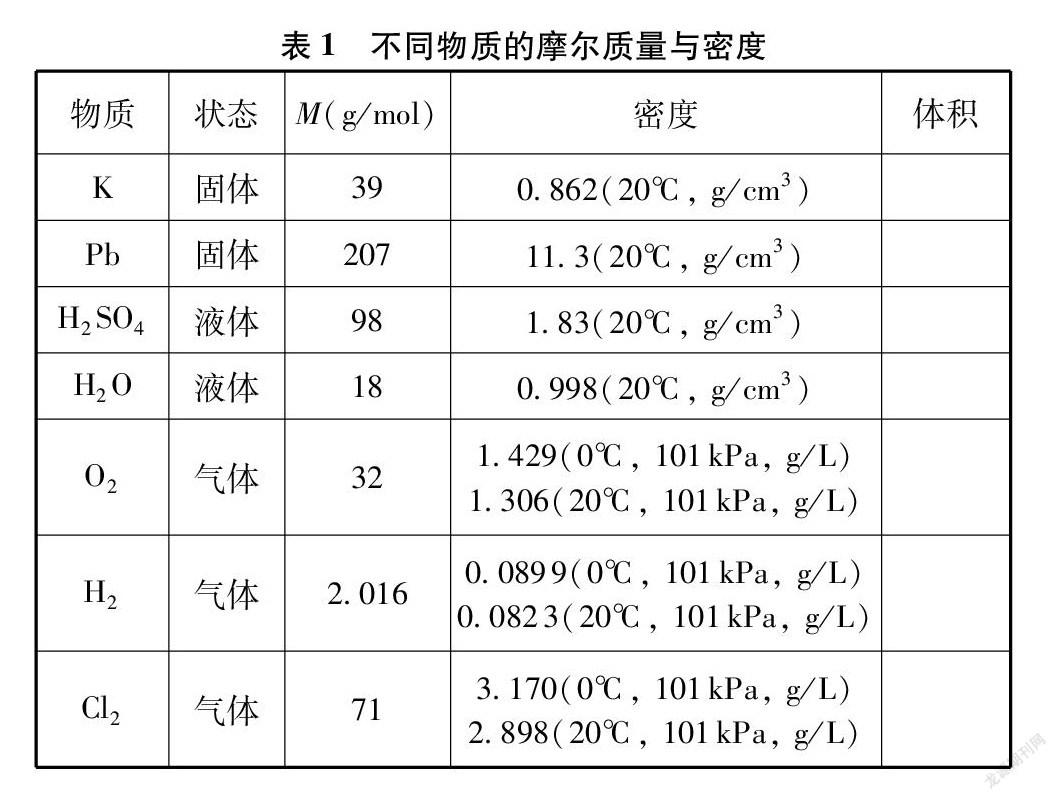
教師: 根據(jù)表1所示數(shù)據(jù),計算每摩爾物質(zhì)在給定條件下的體積,并分析數(shù)據(jù)規(guī)律。
學生1: 每摩爾氣體體積遠大于固體和液體。
學生2: 同溫同壓下,氣體體積幾乎相同;溫度升高,氣體體積增大。
學生3: 固體、液體的體積大小沒有規(guī)律。(其余同學哄笑)
學生3: (辯解)我認為“沒有規(guī)律”在這里也是一種規(guī)律。
教師: 說得很有哲理性呢!大家考慮得很細致,總結(jié)的規(guī)律體現(xiàn)了分類思想,那么如何解釋以上的規(guī)律呢?可以從化學學科的特色思維——“微粒觀”入手。討論一下決定物質(zhì)體積大小的微觀因素有哪些?
(PPT課件給予微觀模型和宏觀事實提示,如圖1所示。)
思考:
(1) 相同條件下,2g的砝碼和200g的砝碼體積誰大?
(2) 4個籃球相互緊靠為一堆與4個乒乓球相互緊靠為一堆,比較兩堆占據(jù)空間體積大小。
(3) 香水一滴,香飄滿屋。
學生4: 體積跟微粒個數(shù)和微粒本身大小有關(guān)。
教師: 能說明一下是正相關(guān)還是負相關(guān)嗎?
學生4: 微粒個數(shù)越多,體積越大,是正相關(guān);微粒本身越大,物質(zhì)體積越大,也是正相關(guān)。
教師: 還有別的影響因素嗎?第三個提示,香水的體積可大致認為從一滴逐漸擴張,過程中微粒有什么變化?
學生5: 我認為體積還和微粒的間距有關(guān),間距越大,物質(zhì)體積越擴張。
教師: 根據(jù)已有經(jīng)驗,你們認為微粒的間距可隨外界條件而改變嗎?探討一下。
學生6: 我認為壓強增大可使微粒間距變小,被壓縮了嘛;還有溫度升高可以使微粒間距變大,有“熱脹冷縮”這個常識。
教師: 我可為學生6的說法提供一個實驗支持。
演示: 用熱手握住試管,片刻后,紅墨水整體往右移動(如圖2所示)。
教師: 把討論中出現(xiàn)的決定物質(zhì)體積的因素,用一個函數(shù)表達式體現(xiàn),即為:
V=f(N, r, d) V: 物質(zhì)的體積 N: 微粒個數(shù) r: 微粒大小 d: 微粒間距
物質(zhì)的量相同,則N相同;對不同氣體而言,只要壓強和溫度相同,則d相同。
接下來我們試試能不能用這個表達式來解釋之前總結(jié)出的數(shù)據(jù)規(guī)律。
教師:“1mol氣體的體積遠大于固體和液體”,如何解釋?
學生7: 都是1mol,所以N相同,而氣體中的微粒間距d遠大于固體和液體中的微粒間距d,所以有此規(guī)律。
教師: 為何不考慮r?
學生7: 我認為氣體微粒間的間距遠比微粒本身大小大,所以微粒本身大小在這里好像不用考慮。
教師: 很好,因素雖多,須分主次。“1mol固體、液體的體積大小沒有明顯規(guī)律”,如何解釋?
學生8: 因為固、液體的d幾乎為零,且都是1mol,即N相同,所以對于1mol固體、液體而言,決定體積的因素就只有r,而不同物質(zhì)的r大小不一,所以有此規(guī)律。
教師: 分析全面!“同溫同壓下,1mol氣體體積幾乎相同”,如何解釋?
學生9: 都是氣體,且同溫同壓,則d相同,都是1mol則N相同,然后氣體分子的r……(發(fā)言同學語塞,片刻寂靜后,全班討論、質(zhì)疑的聲音此起彼伏)
學生9: (有些為難)不同種類的氣體分子r大小不同!好像這樣解釋下去,會把我們之前的客觀規(guī)律都給否定了。
教師: 規(guī)律是對客觀事實的概括,一時解釋不通,不要沮喪,也許是新發(fā)現(xiàn)的開始!回顧一下剛才的困境,為何對于氣體而言,體積大小好像突然就和微粒本身大小不相關(guān)了呢?我們不妨又從微觀粒子中回到宏觀世界來找找靈感,比如你們熟悉的廣播體操。(學生興趣大漲)
設想兩個班,分別為胖子班和瘦子班,人數(shù)一樣,當以集合隊形(大家擠在一起)排隊時,哪個班所占據(jù)地盤大?
全體學生: 胖子班!
教師: 如果以體操隊形(每人站在操場上畫好的長寬等距點上)排隊,哪個班占據(jù)地盤大?
全體學生: (若有所悟)應該是一樣大!
教師: 剛才排隊的例子,能對解決剛才的困難有啟示嗎?
學生9: 現(xiàn)在知道了,當d比r大很多時,r這個因素可以忽略不計。那么1mol氣體的體積就只有和d有關(guān)。而同溫同壓下,氣體的d相同,所以“同溫同壓下,1mol氣體體積幾乎相同”。
(其余同學鼓掌贊同)
……
教師: 請同學們將最初的體積計算數(shù)據(jù)精確到小數(shù)點后三位,再次觀察,1mol不同氣體在標況下的體積是完全相同嗎?對此你如何解釋?
(計算后竊竊私語,有些詫異)
學生10: 應該是實驗誤差引起的,一點誤差沒有是不可能的。
教師:“誤差”是一種合理的解釋,但是科學史上把數(shù)據(jù)差異歸結(jié)為實驗誤差,而與真相失之交臂的情況亦不少。再為大家提示一個方向,可能找到另一種解釋。“什么是理想氣體,它和真實氣體的區(qū)別在哪里?”大家課后查詢資料研究,下次課我們再交流。
該設計避免了直接灌輸定義、公式,力求促進學生對相關(guān)核心知識本質(zhì)性的理解。創(chuàng)設“尋求物質(zhì)體積的規(guī)律解釋”這一情境,在教師溯本求原的指向下,多次利用了化學學科特色思維“宏微觀”,結(jié)合來自于學科域、生活域、跨學科域及同伴域[7]的經(jīng)驗,在尋求解釋方案中建立模型、實施解釋中使用模型、遇到困境時修正模型、再用模、再修模……,有力促進了“宏觀辨識與微觀探析”“證據(jù)推理與模型認知”等素養(yǎng)的提升,達到了促進化學學科理解的目的。
3.1.2 促進內(nèi)容結(jié)構(gòu)化方式: 知識活化、關(guān)聯(lián)及認知模型的建立
習得的知識如果孤立、靜止,那離遺忘也就不遠了。如果能將相關(guān)觀念、知識、方法在真實生活、生產(chǎn)、學科情境中綜合運用,則能使其活化、關(guān)聯(lián)并建構(gòu),這是促進化學學科理解的一種有效方式。而解釋類活動則是進行這類設計的優(yōu)良載體。
某解釋活動如果是“多樣表象同類解釋”類型,學生則可在多樣化情境中歸納此類解釋背后的認知方法,從而主動建構(gòu)有效的認知模型。
該種方式尤適用于小結(jié)拓展或單元復習提升。
案例2 硫化氫性質(zhì)復習
復習課(如表2所示)如果僅采取單維羅列、強化識記的方式,學生容易反感,更不會促進學科理解。從鮮活真實的情境中創(chuàng)設解釋類活動,學生的學習內(nèi)驅(qū)力、已有知識及經(jīng)驗的調(diào)用和重構(gòu)程度則大大提升。為了尋求合理解釋,學生找尋相關(guān)知識,活化、賦能、建構(gòu),表達。諸多學科知識點在解釋活動中具有了學科和人本意義及邏輯,建構(gòu)了有功能的結(jié)構(gòu),自然起到了促進化學學科理解的作用。
案例3 多方因素博弈決定表象的系統(tǒng)化認知模型的建立
解釋性問題設計:
(1) 為何NaHCO3溶液顯堿性,NaHSO3溶液顯酸性?
(2) 稀釋冰醋酸時,為何隨加水量增加,氫離子濃度變化趨勢是先增大后減小?
(3) 足量鎂條和稀硫酸反應時,為何速率先增大后減小?
(4) 推進注射器加水稀釋硫酸(裝置見圖3),為何右側(cè)滴水速率反而加快[9]?
(5) 為何氫氣和氯氣反應是放熱反應(從內(nèi)能或鍵能角度分析)?
(6) 工業(yè)制取硫酸時,接觸室是否需要高壓,為什么?
解釋中涉及到的多個因素:
(1) 多元弱酸根的電離程度、水解程度。
(2) 電離度變化、稀釋效應。
(3) 反應放熱導致溫度升高、酸的濃度隨反應而減小。
(4) 酸濃度減小、注射器加水帶來的體積增量、硫酸稀釋放熱。
(5) 反應物與生成物內(nèi)能比較;氫氣、氯氣和氯化氫的鍵能比較。
(6) 壓強對平衡移動的影響,常壓下生產(chǎn)三氧化硫的轉(zhuǎn)化率、綠色化學。
上述六個問題的表觀事實不同,構(gòu)建合理解釋卻有一個共同的認知方式——考慮多個因素作用時的相對大小。多次強化,遷移應用,“多個因素博弈決定表象”的系統(tǒng)化認知模型得以發(fā)展和充實。
3.2 對解釋活動進行即時評價
內(nèi)隱的學科理解水平可在解釋活動中表征而外顯,因此對解釋活動的評價成為判斷學生學科理解水平的途徑之一。評價解釋活動可通過對三個要素的考查來實施: 領(lǐng)域、結(jié)構(gòu)、表征。
“領(lǐng)域”是指建構(gòu)合理解釋對應的觀念、概念、知識等,可以是單域也可能是多域交互;“結(jié)構(gòu)”是指在對應領(lǐng)域中,諸多因素在關(guān)聯(lián)時要有主次分明、因果一致等嚴謹?shù)倪壿嫿Y(jié)構(gòu);“表征”指通過文字敘述、化學用語、圖示、數(shù)據(jù)等外顯“領(lǐng)域”和“結(jié)構(gòu)”的具體表達。
案例4 工業(yè)生產(chǎn)膽礬
解釋性問題設計:
(1) 工業(yè)生產(chǎn)膽礬一般不選擇銅和熱濃硫酸反應,而更多選擇將銅加入到稀硫酸,維持溫
度80℃,然后不斷鼓入空氣的方法。請作出解釋。
(2) 后者在工業(yè)生產(chǎn)實踐中,發(fā)現(xiàn)最大的問題就是速率較低,提出你的改進措施,并說明理由。
問題(1)的評價要點:
領(lǐng)域: 化工生產(chǎn)的綠色化要求: 從安全、效率、能耗、成本、污染等方面考慮;銅和濃硫酸反應的物料比,以及濃硫酸的利用率;污染物二氧化硫的生成;銅與氧氣反應、氧化銅和稀硫酸反應。
結(jié)構(gòu): 用對比的方式對兩種生產(chǎn)方法進行評價:
硫酸利用率——前者不超過50%,后者理論上可以完全轉(zhuǎn)化;
污染物——前者有二氧化硫生成,后者無污染氣體;
安全性——前者需要溫度高,要用到大量濃硫酸,而后者安全性更具優(yōu)勢。
表征: 需要用對比的方式對兩種工藝進行文字表述,需結(jié)合兩種方法的化學方程式作為二氧化硫的來源說明及硫酸利用率大小比較的依據(jù)。
根據(jù)學生的解釋表達,評價其是否知道一些化學基本知識,同時也考查學生能否活化這些知識并關(guān)聯(lián)綠色化思想為其所用,從而對其化學學科理解水平進行判斷。問題(2)是(1)的升華,從對比、發(fā)現(xiàn)問題上升到解決問題,需要從固體表面積、溫度、濃度對反應速率的影響角度進行合理的解釋。
4 教學中開展解釋類活動的幾點反思
創(chuàng)設規(guī)模可大可小,可以作為單元教學或一整堂課的主線,也可作為生成某重要概念的片段,按需而定。
客觀事實是第一位的,而對該事實的解釋則容易過時[10]。所以在教學中要有避免將解釋絕對化的意識,要為再認識、再發(fā)現(xiàn)預留空間,不要輕易否定學生的“腦洞大開”。
可以將“解釋更新”的科學探究過程作為學生學習的素材,這是讓學生體驗化學學科發(fā)展、深化化學學科理解的優(yōu)質(zhì)渠道。如將制備氫氧化亞鐵實驗中的“灰綠色”成因解釋、“冰為什么很滑”等布置為需要查找文獻的開放式作業(yè),那學生在文獻學習、相互交流中將會受益無窮。
參考文獻:
[1]辭海編輯委員會. 辭海(中)[M]. 上海: 上海辭書出版社, 1999.
[2]上海市教育委員會編制. 上海市中學化學課程標準[S]. 上海: 上海教育出版社, 2004.
[3]中華人民共和國教育部制定. 普通高中化學課程標準(2017年版)[S]. 北京: 人民教育出版社, 2018.
[4]劉英琦. 以深度理解促進學生學科核心素養(yǎng)發(fā)展的教學研究[J]. 中學化學教學參考, 2021, (3): 2.
[5]胡先錦. 為理解而教——化學課堂的應然追求[J]. 化學教學, 2020, (4): 33.
[6]楊季冬, 王后雄. 科學教育中關(guān)注科學解釋的三個視角: 科學發(fā)展、科學學習、國際理念[J]. 化學教學, 2019, (5): 4.
[7]咸于莉. 基于經(jīng)驗立場的“醋和酒香——乙酸”教學[J]. 化學教學, 2020, (3): 50.
[8]德里克·B. 羅威著. 杜凱譯. 化學之書[M]. 重慶: 重慶大學出版社, 2019: 83.
[9]鐘輝生, 謝名軍. 芻議提升教師實驗素養(yǎng)的四種意識[J]. 化學教學, 2019, (12): 28.
[10]北京師范大學等編. 無機化學(上冊·第四版)[M]. 北京: 高等教育出版社, 2002: 3.

