以氣體為載體制備類實驗的基本操作
山東 張市場
《普通高中化學課程標準(2017年版2020年修訂)》對制備類實驗提出以下學業要求:學業質量水平4,質量描述4-2,“能基于‘綠色化學’理念設計無機化合物制備和有機化合物合成的方案,并對方案進行評價和優化”。新高考對制備類實驗提出了更高的要求,要求考查學生運用所學知識分析問題、解決問題的能力,實現知識的遷移和應用,提升學生的化學學科核心素養。制備類實驗是新高考實驗考查的高頻考點,以氣體為載體的制備類實驗的考查尤其多。高考復習教學實踐表明,思維模型的建構能有效地提高高三化學此類實驗復習的質量和效率。
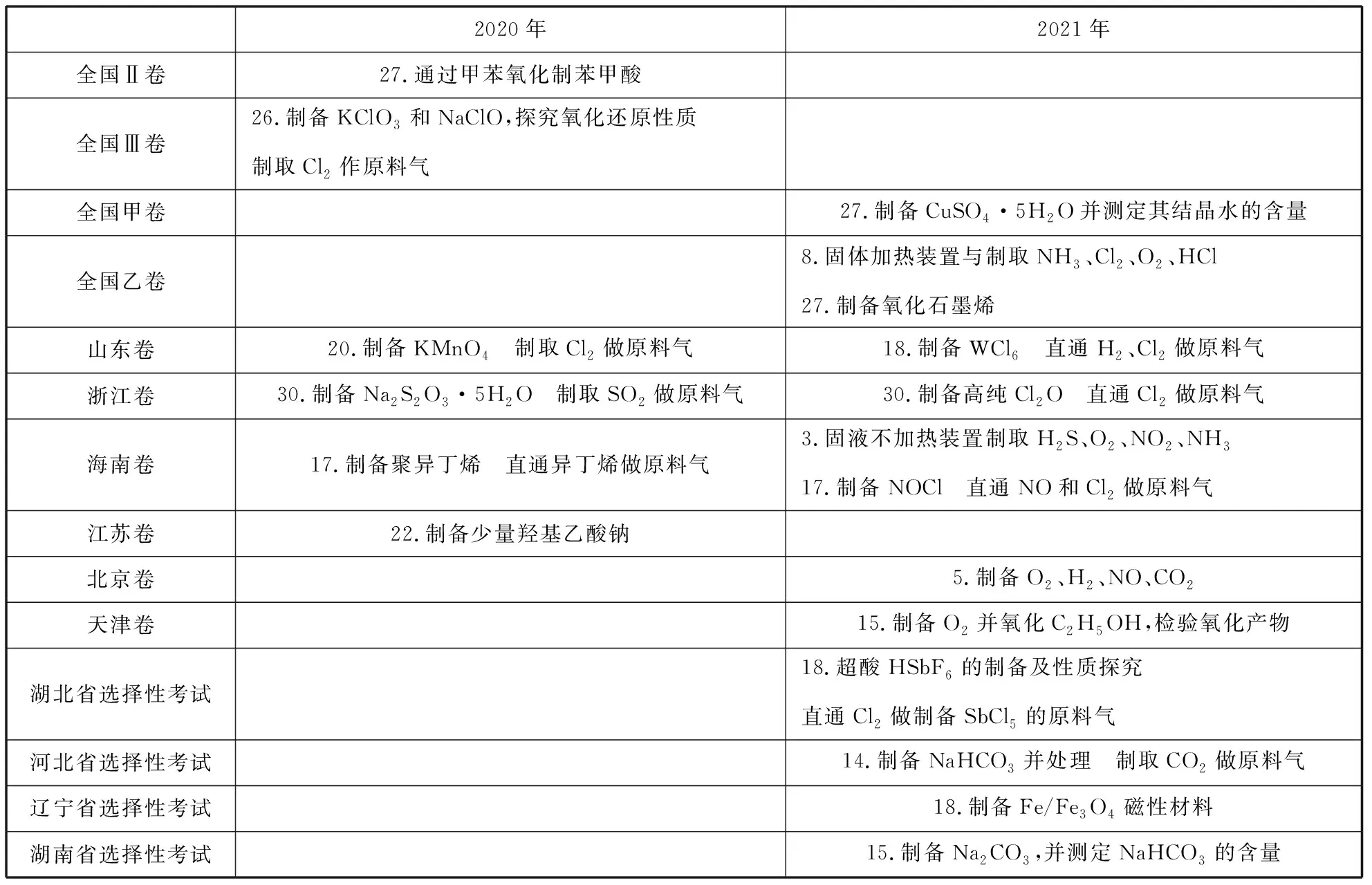
表1 新高考物質制備類綜合實驗兩年考向
此處學情為學生對以氣體為載體的制備類實驗沒有一個清晰、系統的認識,“一看就會,一做就錯”。一知半解,沒有理清邏輯關系,不會規范作答,沒有形成關鍵能力。學生對以氣體為載體的制備類實驗的一些基本的、常見的操作認識似是而非,沒有完全掌握,必備知識不夠。教師通過思維模型的建構,使學生掌握以氣體為載體物質制備類實驗的一般思路和設計方法,提升學生證據推理與模型認知核心素養;掌握以氣體為載體物質制備類實驗的基本操作,規范作答,提升學生科學探究與創新意識核心素養,此過程教師可輔以交互式虛擬實驗室的操作。
一、建構以氣體為載體制備類實驗的解題模型
確定核心制備反應及其反應裝置,以此為中心,結合物質性質確定其他裝置的作用,將復雜裝置分為五部分模型:發生裝置、凈化裝置、制備(收集)裝置、后防裝置、尾氣處理裝置,如圖1。
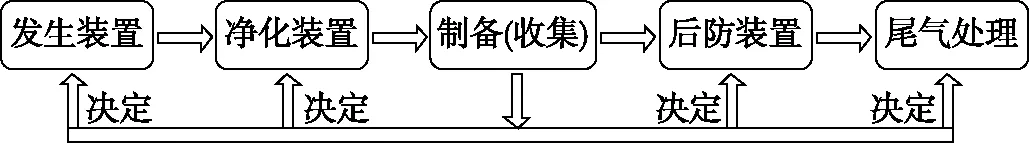
圖1 以氣體為載體制備類實驗的解題模型
例如,“無水四氯化錫(SnCl4)常用作有機合成的氯化催化劑。實驗室可用熔融的錫(熔點232℃)與Cl2反應制備SnCl4(遇水極易水解),裝置如圖所示”。分析其裝置,可建立如下模型,對裝置的劃分如圖2所示。
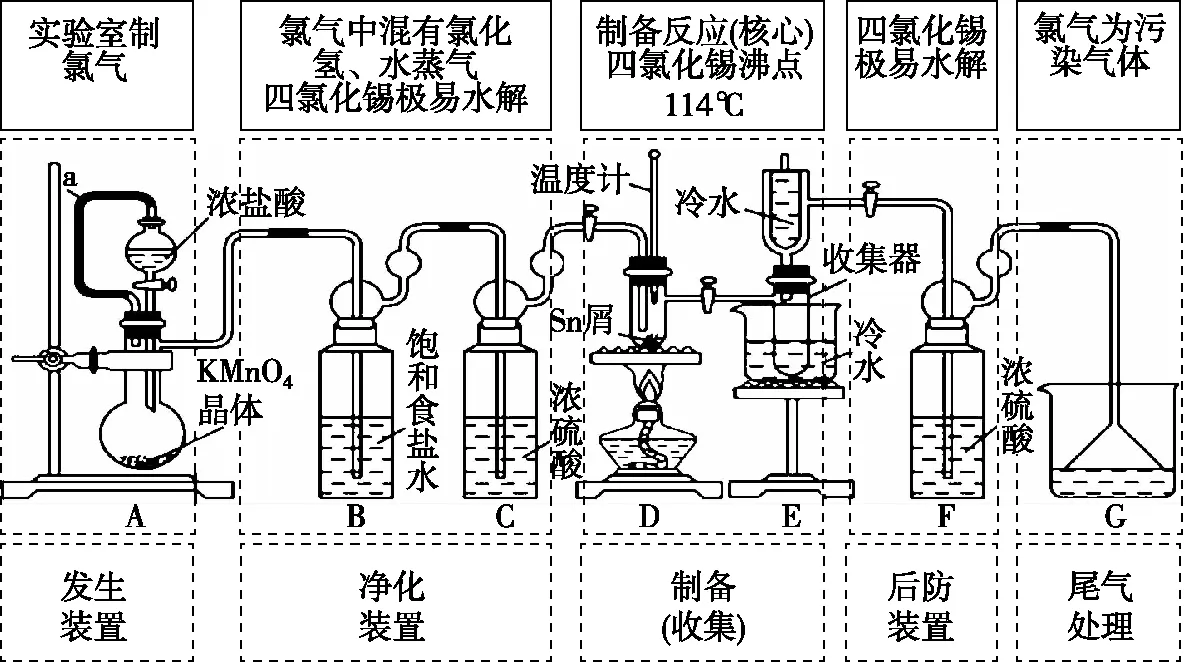
圖2 以氣體為載體制備類實驗的題型建模
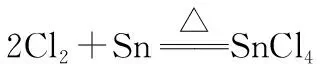
建構模型后將復雜裝置簡單化,明確各分模型的作用后,可以確定分模型的基本操作。將基本操作熟練掌握后,對以氣體為載體的制備類實驗就會駕輕就熟。
二、以氣體為載體制備類實驗的基本操作
1.基本操作——檢查氣密性
有氣體參與反應的裝置都需要檢查氣密性。學生往往不能規范描述。教學中教師可將學生的易錯點用NOBOOK化學虛擬實驗室虛擬實驗,觀察現象,加深印象,得出正確的氣密性檢查方法。檢查氣密性的規范操作為:形成封閉體系→操作形成壓強差→觀察現象→得出結論。
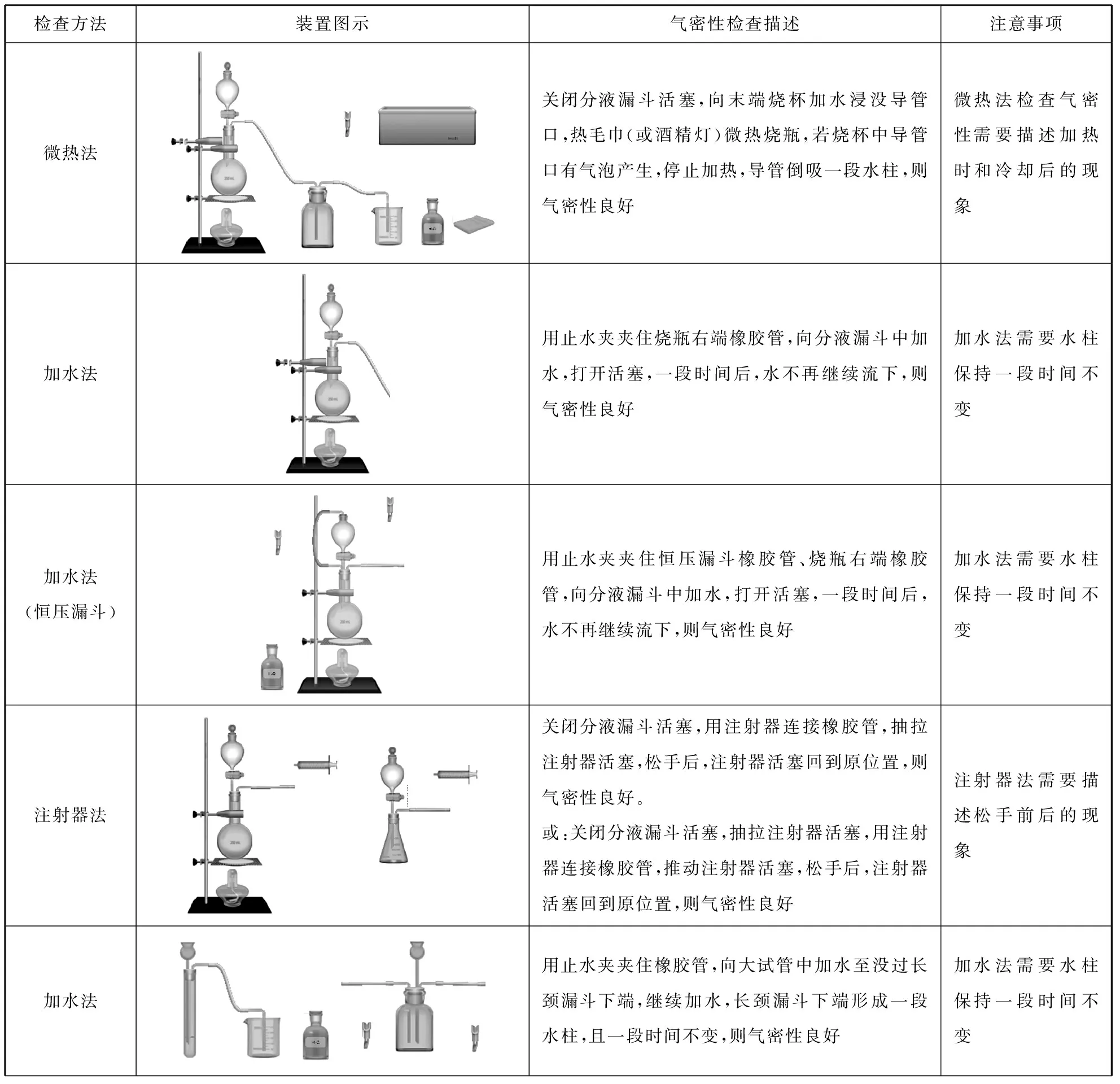
表2 各裝置氣密性的檢查
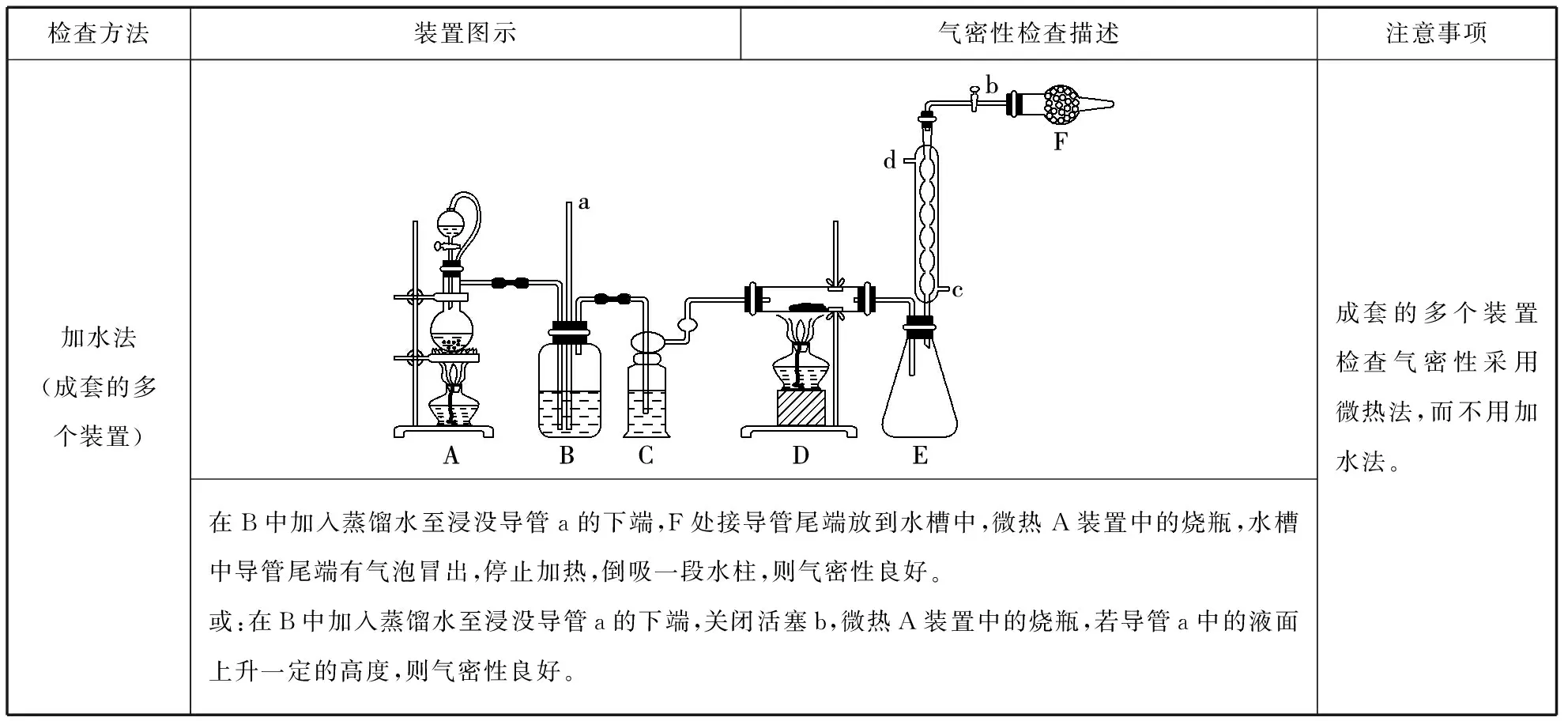
續表
2.基本操作——先通后通
先通:若裝置中空氣干擾實驗,核心制備反應開始前,向裝置中先通入原料氣或無關惰性氣體排除裝置中的空氣,防止其干擾實驗。使用可燃性氣體如:H2、CO、CH4等加熱時,先用原料氣排除裝置中的空氣,再點燃酒精燈,以防止爆炸。對陌生型反應,要注意題目信息,若反應物或生成物易和空氣發生反應,則需先通入原料氣或無關惰性氣體排除裝置中的空氣。先通的目的是排除××裝置中的空氣。實驗中若是其他氣體干擾試驗,則作答為“排除××裝置中的××”。
后通:核心制備反應停止后,若產物與空氣反應,則需要繼續通入原料氣或無關惰性氣體直至產物冷卻,防止其與空氣反應。定量實驗中,需將氣體產物排到后續裝置充分吸收。若原料或產物中有污染性氣體,需將此氣體排到后續吸收裝置,防止污染空氣。規范作答時,后通的目的是“防止產物與空氣反應;或將氣體產物排到××裝置充分吸收;或將污染性氣體排到××裝置充分吸收”。
【例1】(2021·山東省學業水平等級考試·18節選)六氯化鎢(WCl6)可用作有機合成催化劑,熔點為283℃,沸點為340℃,易溶于CS2,極易水解。實驗室中,先將三氧化鎢(WO3)還原為金屬鎢(W)再制備WCl6,裝置如圖3所示(夾持裝置略)。回答下列問題:
(1)檢查裝置氣密性并加入WO3。先通N2,其目的是________;一段時間后,加熱管式爐,改通H2,對B處逸出的H2進行后續處理。
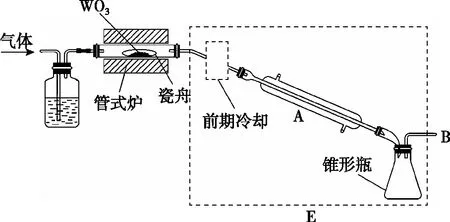
圖3
(2)WO3完全還原后,進行的操作為:①冷卻,停止通H2;②以干燥的接收裝置替換E;③在B處加裝盛有堿石灰的干燥管;④……;⑤加熱,通Cl2;⑥……。
堿石灰的作用是________;操作④是________,目的是________。
【參考答案】(1)排除裝置中的空氣;
(2)吸收多余Cl2,防止污染空氣;防止空氣中的水蒸氣進入E中;再次通入N2;排除裝置中的H2。
【解析】粗寫出核心制備反應:WO3+H2高溫W+H2O,W+Cl2高溫WCl6確定管式爐為制備裝置,E為收集裝置,依據核心制備反應分析前后裝置和操作。H2為可燃性氣體,加熱前應排除裝置中的空氣,H2驗純后方可加熱,需先通;通Cl2反應時,裝置中殘留H2會在加熱時與Cl2反應,應先通N2排除,需先通。據題中信息可知WCl6極易水解,需在制備裝置前后防水,需前防后防:前防為干燥氣體,后防為防止空氣中水蒸氣進入裝置E。Cl2為污染性氣體,需尾氣處理,盛有堿石灰的干燥管可起到后防水蒸氣和尾氣處理的雙重作用。據此對裝置進行模型分析如圖4所示。

圖4
3.基本操作——防倒吸
加熱制取氣體,排水法停止收集時,應先將導管撤出水槽,再撤酒精燈,否則會倒吸。其他裝置,通常為防倒吸,可在兩裝置間加一個安全瓶。教學中教師可通過虛擬實驗演示,明確原理,加深印象。極易溶于水的氣體有HCl、HBr、NH3等,這些氣體必須防倒吸。
【例2】(2020·浙江7月選考·30節選)
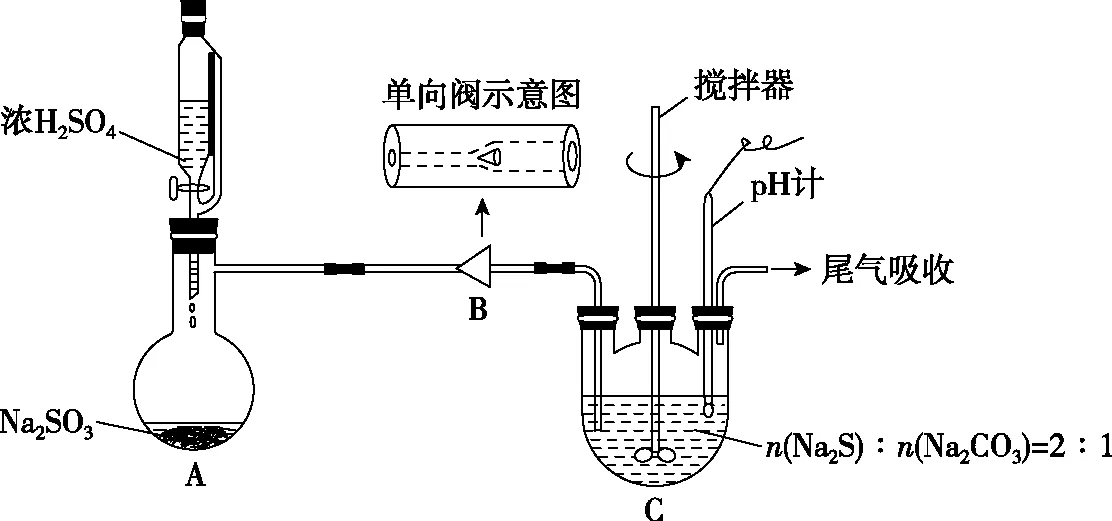
圖5

(1)步驟Ⅰ:單向閥的作用是________。
【答案】防止倒吸
【解析】據題目給出的核心反應,裝置C為制備裝置,裝置A為發生裝置制取反應氣體SO2,SO2會與裝置C中混合溶液發生反應,且導管進入液面以下,需要防倒吸的裝置,單向閥可以防止發生倒吸。
4.基本操作——前防后防

圖6
前防:核心制備反應裝置需要通入氣體加熱的、制備反應物或生成物易水解的、易吸水的,應在核心制備反應裝置之前防水蒸氣,因此,前防的目的是防止水蒸氣進入裝置。
后防:核心制備反應物或生成物易水解的、易吸水的,應在核心制備反應裝置之后防水蒸氣。后防也可能是防空氣中的O2或CO2。回答后防裝置的作用時,應指明所防氣體。因此,后防的目的是“防止××(應指明所防氣體)進入××裝置”。
【例3】(2021·浙江6月選考·30節選)Cl2O是很好的氯化劑,實驗室用如圖7裝置(夾持儀器已省略)制備高純Cl2O。已知:

②常壓下,Cl2沸點-34.0℃,熔點-101.0℃;Cl2O沸點2.0℃,熔點-120.6℃。

請回答:
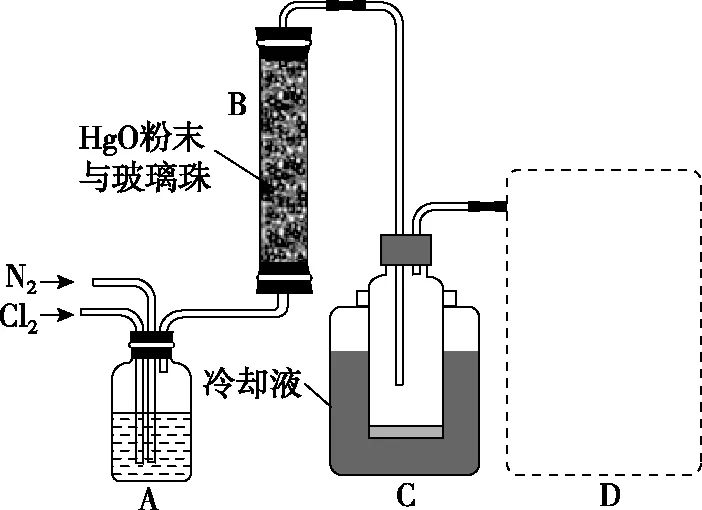
圖7
(1)①裝置A的作用是去除原料氣中的少量水分,可用的試劑是________。
②將上圖中裝置組裝完整,虛框D中應選用________。
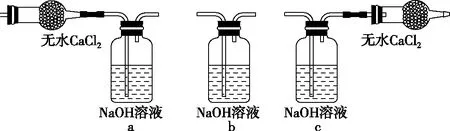
【參考答案】(1)①濃硫酸;②a

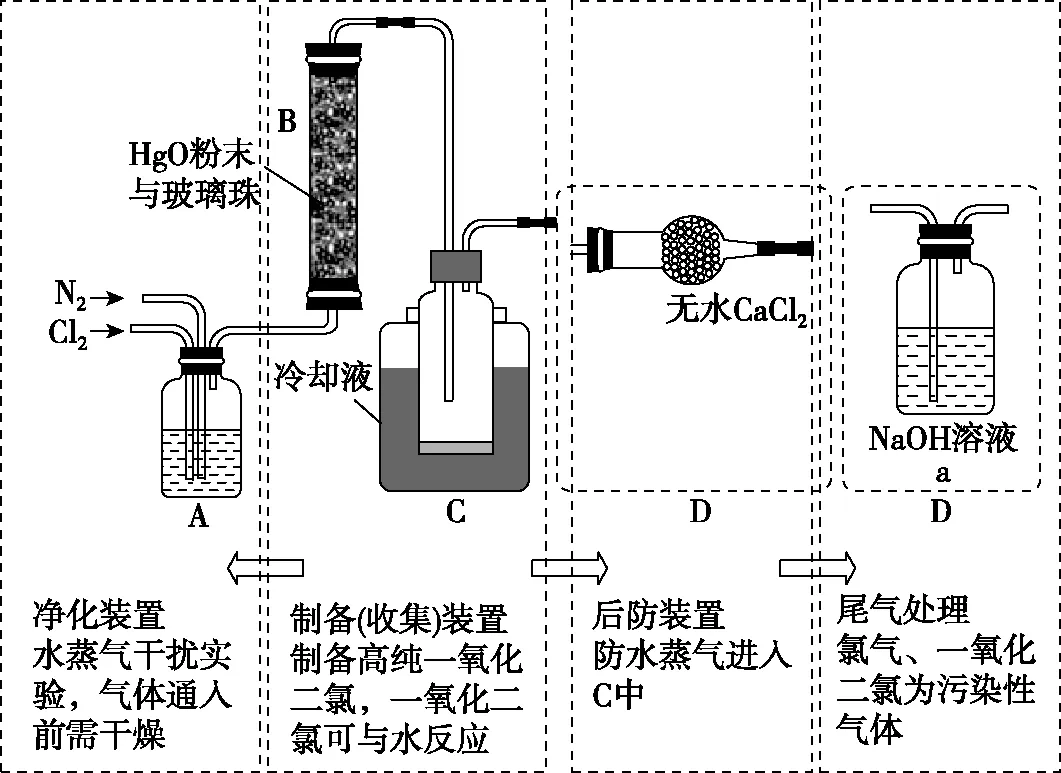
圖8
5.綜合應用裝置連接
思維模型建構后,通過各模型基本操作的訓練,學生對以氣體為載體制備類實驗有了更深的認識,更深的理解,可以遷移應用,完成制備類綜合實驗解題。
【例4】(2021·河北省選擇性考試·14節選)化工專家侯德榜發明的侯氏制堿法為我國純堿工業和國民經濟發展做出了重要貢獻,某化學興趣小組在實驗室中模擬并改進侯氏制堿法制備NaHCO3,進一步處理得到產品Na2CO3和NH4Cl,實驗流程如圖9:
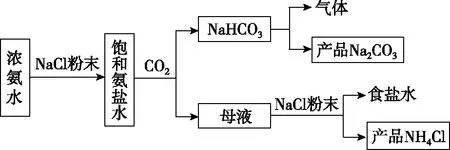
圖9
回答下列問題:
(1)從A~E中選擇合適的儀器制備NaHCO3,正確的連接順序是________(按氣流方向,用小寫字母表示)。
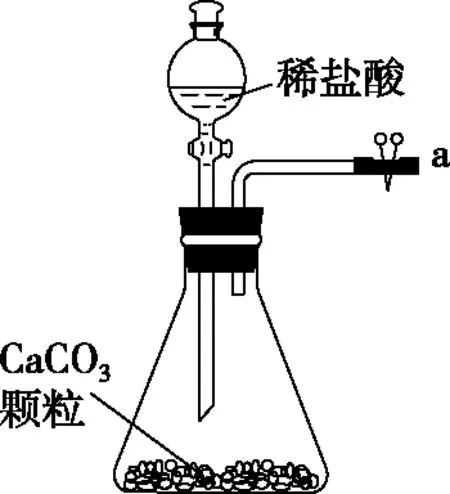
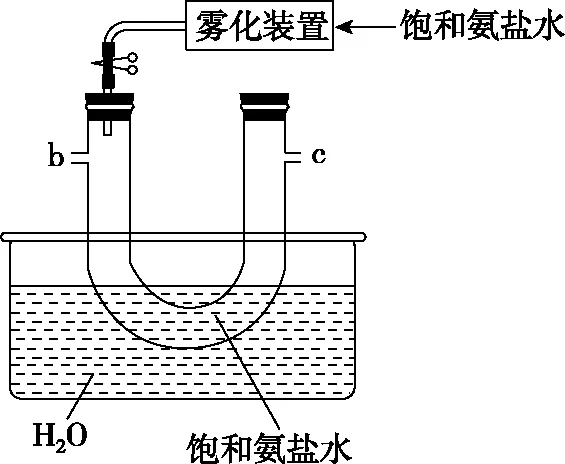
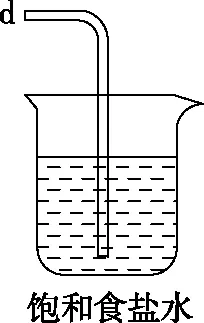
(3)生成NaHCO3的總反應的化學方程式為________。


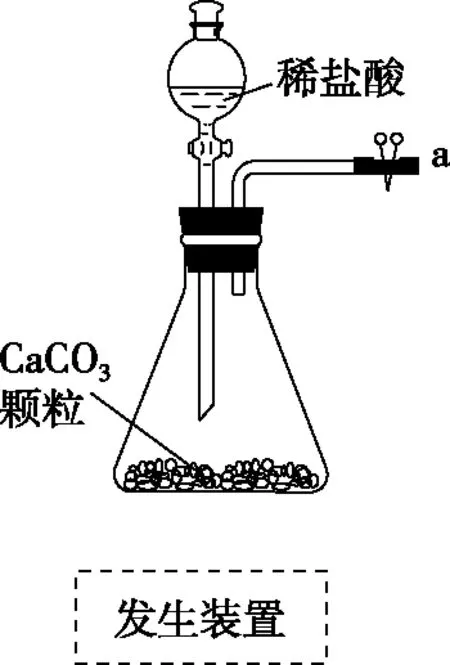
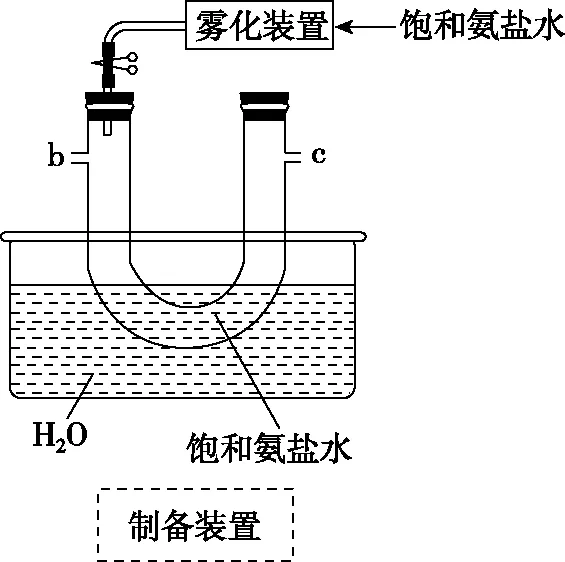
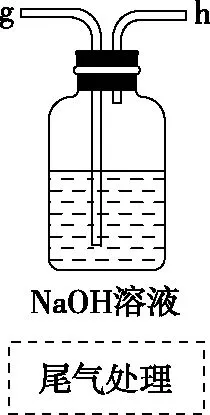
圖10
按解題模型五個部分順序排序:發生裝置、凈化裝置、制備(收集)裝置、后防裝置、尾氣處理,得出裝置連接順序。
三、總結


