MAGiC序列在乳腺腫瘤良惡性鑒別診斷中的應用
柴青煥,胡曉欣,肖 勤,楊 孟,岳 磊,顧雅佳
復旦大學附屬腫瘤醫院放射診斷科,復旦大學上海醫學院腫瘤學系,上海 200032
乳腺疾病是女性常見疾病,而乳腺癌是嚴重威脅女性健康的主要乳腺疾病之一。近年來,乳腺癌發病率逐年升高,根據世界衛生組織(World Health Organization,WHO)最新癌癥統計報告,乳腺癌已經取代肺癌,成為全球第一大癌癥[1]。早發現、早治療是提高患者生存率的有效途徑。因此,乳腺病變的早期發現及準確鑒別對患者治療方案的選擇和預后情況的評估均有重要意義[2]。目前,乳腺疾病的常規影像學檢查方法主要包括超聲檢查、乳腺X線攝影和磁共振成像(magnetic resonance imaging,MRI)[3]。相較于超聲檢查和乳腺X線攝影,MRI具有軟組織對比度良好、可多方位及多序列成像、無電離輻射、病灶檢出率高和定量信息豐富等優勢,可以對疾病進行定量、定性分析,提供更加精準的診斷信息以評估治療效果及提示預后[4]。定量MRI(quantitative MRI,QMRI)技術是通過某些特殊的序列,如定量圖譜MRI(MRI compilation,MAGiC)序列,測量或者反映組織的某些特性值的技術。QMRI不僅能提供組織器官的基本結構信息,也能提供病變發生、發展過程中豐富的生物學和病理生理學信息,是目前國際上MRI研究的前沿技術[5]。QMRI技術通過研究疾病對單一組織參數的改變,提高對疾病的靈敏度[6];可測量的定量參數包括Tl、T2、質子密度(proton density,PD)、彌散常數、磁化轉移(magnetic transfer,MT)及磁共振波譜的膽堿CHO值等[7]。近年來的研究[8-9]表明,QMRI有助于乳腺病變程度的診斷。
美國GE醫療研發了多對比度QMRI序列MAGiC,該序列一次掃描可得到多種不同對比度的圖像,包括T1、T2、T1液體抑制反轉恢復( fluid-attenuated inversion recovery,FLAIR)、T2 FLAIR、短反轉時間反轉恢復(short inversion time inversion recovery,STIR)、雙反轉恢復(dual inversion recovery,DIR)和PD加權圖像,提供了更多的對比度圖像信息[10]。MAGiC序列首次實現了MRI圖像從常規灰階圖像到組織定量圖譜的轉變,得到定量化數據,可以更加靈活且回溯性地對圖像進行各種調節,獲取更多有價值的定量圖像數據,幫助醫師進行更優的臨床決策。此外,MAGiC在定量測量組織的弛豫時間T1、T2和PD值時,無需增強掃描,避免了動態增強MRI檢查造影劑造成的不可逆性腎損傷[11]。因此,本研究擬通過采用MAGiC掃描序列對乳腺病灶的T1、T2、PD值進行比較,探討MAGiC序列在乳腺腫瘤惡性程度診斷中的應用價值。
1 資料和方法
1.1 資料
收集2020年1—8月在復旦大學附屬腫瘤醫院初次行MRI檢查(包括MAGiC序列掃描),有乳腺腫物且此后繼續在院治療的女性乳腺疾病患者42例。年齡25~72歲,平均年齡47歲。納入標準:女性,25~75歲,乳房腫塊可觸及,乳腺影像報告和數據系統(Breast Imaging and Reporting Data System,BI-RADS)分級4A以上[14],MRI檢查后在本院有穿刺、活檢或手術后病理學檢查報告。排除標準:處于妊娠或哺乳期;MRI檢查前有抗腫瘤治療史,既往有乳腺癌或其他惡性腫瘤化療史。本研究符合《赫爾辛基宣言》的要求,并獲得患者知情同意。
1.2 方法
1.2.1 MAGiC序列的定量及多對比圖像的生成
多動態多回波使用相同的梯度反轉過程的重復形式,用于產生單個梯度回波,該梯度回波在單個射頻脈沖后又產生額外的梯度回波[12]。多重(或雙重)回波梯度回波,當橫向磁化完全消失時T2弛緩尚未發生。基于多動態多回波的MAGiC序列是一個定量序列,能對組織的物理性質如縱向弛豫時間T1、橫向弛豫時間T2、PD、縱向弛豫率R1(縱向弛豫時間T1的倒數)、橫向弛豫率R2(橫向弛豫時間T2的倒數)等進行絕對定量,而不依賴于MRI掃描儀設置。
MAGiC成像利用對多種物理性質的定量探測,僅通過1次掃描合成與常規T1、T2、T1 FLAIR、T2 FLAIR、PD和STIR等常規MRI圖像相似的MRI圖像[13];從1次掃描中重建多重對比,如重復時間(repetition time,TR)、回波時間(echo time,TE)和反轉時間(inversion time,TI)等參數可通過數學推理進行修改,而非預先確定。因此,MAGiC序列中R1、R2和PD值的定量通過設置回波時間TE和重復時間TR的任意組合,生成T1加權圖像(T1-weighted imaging,T1WI)、T2加權圖像(T2-weighted imaging,T2WI)或PD加權圖像(PD-weighted imaging,PDWI)來測量。反轉恢復圖像,如FLAIR圖像和STIR圖像也可通過添加TI得到;此外,利用2個反轉延遲時間(TI1和TI2)可合成DIR圖像。
1.2.2 圖像采集
采用美國GE公司的Signa Pionner 3.0 T MRI掃描儀,使用8通道乳腺專用相控陣表面線圈。患者俯臥于專用的乳腺相控陣表面線圈上,使雙側乳房自然懸垂于線圈孔洞內[15]。在常規的臨床乳腺MRI檢查中增加MAGiC序列。在注射造影劑前行MAGiC序列掃描,掃描參數:8個自動計算的反轉恢復時間,TR=4 128 ms,層厚=4.5 mm,層間隔=0.5 mm,視野=30 cm,圖像矩陣=224×224,帶寬=31.25 kHz。
1.2.3 圖像處理
掃描所得的MAGiC圖像使用MAGiC viewer后處理軟件打開并處理。獲得T1WI、T2WI、PDWI、FLAIR、STIR、DIR等各種對比度圖像;同時也得到T1map、T2map以及PDmap等定量圖譜。參照常規乳腺MRI增強圖像,在MAGiC序列掃描獲得的各種對比度圖像中,選取病灶的最大直徑層面勾畫感興趣區(region of interest,ROI)。每個受試者圖像所勾畫的ROI中所有體素的平均T1、T2和PD值將由MAGiC viewer自動計算得出(圖1)。良性與惡性分別有不同的定量值,乳腺良惡性T1、T2、PD值的對比實例如圖2所示。
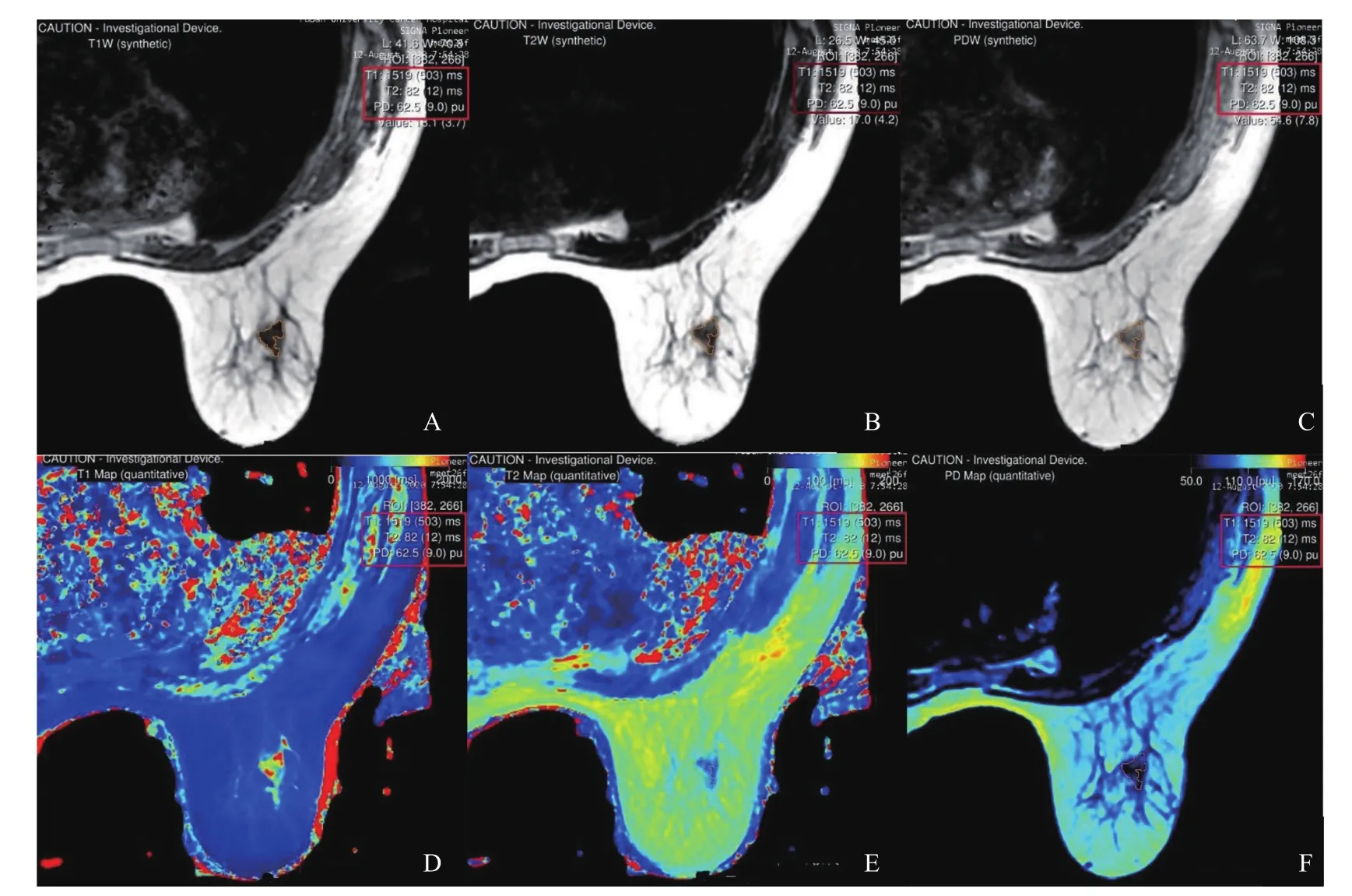
圖1 MAGiC viewer自動計算定量值示例
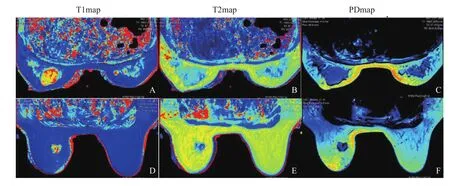
圖2 乳腺良惡性病變T1、T2、PD定量圖譜的比較
1.3 統計學處理
本研究根據病理學檢查結果將受試者分為良性和惡性兩類。基于SPSS 24.0軟件對良性組和惡性組對應的定量指標(T1、T2、PD值)及年齡進行統計學分析。首先,對T1、T2、PD及年齡差異進行顯著性檢驗,采用Shapiro-Wilk檢驗進行正態性檢驗、Levene檢驗判斷兩組數據觀測變量是否方差齊(方差相等),在經檢驗滿足獨立樣本t檢驗假設條件的前提下,進行獨立樣本t檢驗;然后,基于t檢驗結果,將差異有統計學意義(P<0.05)的變量,在經檢驗滿足logistic回歸假設條件前提下,納入logistic回歸模型進行分析;最后,采用支持向量機(support vector machine,SVM)分類算法訓練分類器對數據進行分類實驗,分別使用徑向基函數(radial basis function,RBF)及多項式等方式作為執行SVM處理的內核函數,調整訓練模型至有比較好的預測質量。
2 結 果
2.1 臨床資料
選取42例年齡為25~72歲、明確有乳腺腫塊的患者行MAGiC序列掃描。良惡性患者情況:良性共18例,纖維腺瘤5例,導管不典型增生3例,囊腫1例,炎性改變9例;惡性共24例,浸潤性導管癌20例,導管原位癌4例。
2.2 獨立樣本t檢驗
經統計學分析得到良惡性乳腺腫瘤的T1、T2、PD、年齡箱式圖(圖3)。可以看出,本研究的各組數據中沒有顯著異常值,滿足獨立樣本t檢驗的假設條件。
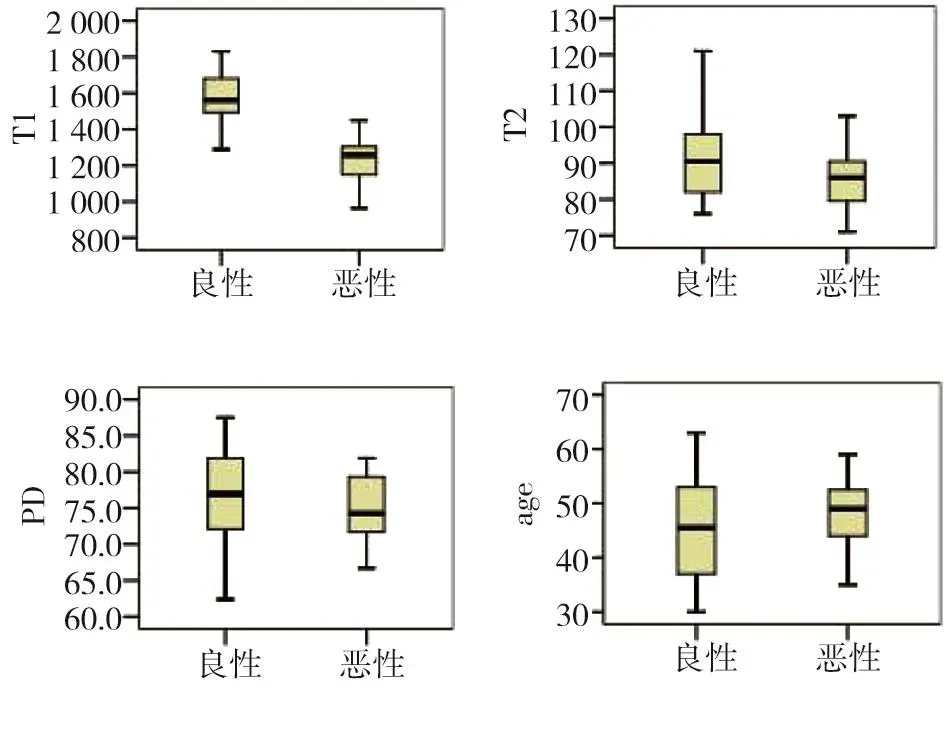
圖3 良性組和惡性組的T1、T2、PD、年齡箱式圖
本研究采用獨立樣本t檢驗,判斷良惡性乳腺腫瘤在T1、T2、PD及年齡上的差異。研究數據不存在顯著異常值,且在各組內接近正態分布,同時方差齊。其獨立樣本t檢驗結果如表1所示。
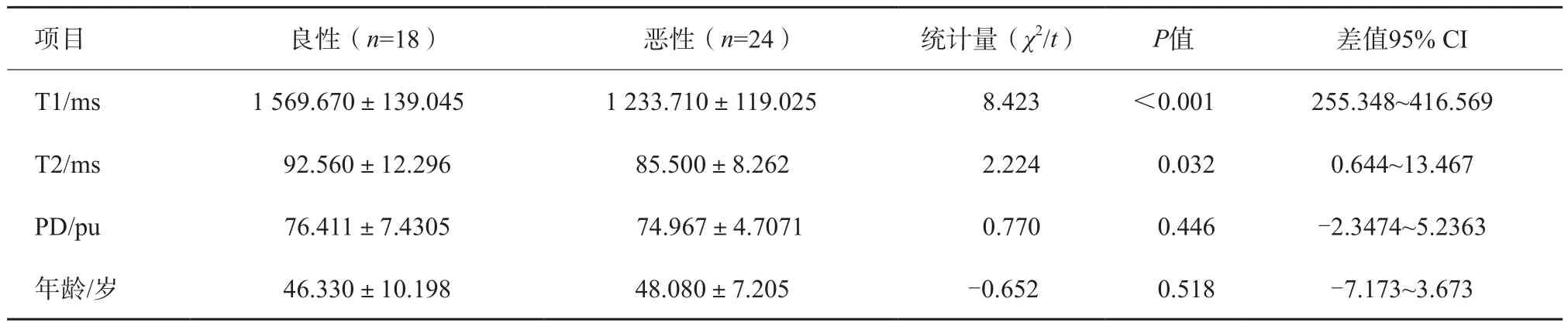
表1 良性組和惡性組T1、T2、PD、年齡的獨立樣本t檢驗分析結果
結果表明,良性組平均T1值高于惡性組,差異有統計學意義(t=8.423,P<0.001);良性組平均T2值高于惡性組,差異有統計學意義(t=2.224,P=0.032);PD差異無統計學意義(t=0.770,P=0.446);年齡差異無統計學意義(t=-0.652,P=0.518)。綜上所述,T1,T2值可選取作為判斷良惡性乳腺腫瘤的特征。
2.3 Logistic回歸分析
本研究采用二分類logistic回歸評估T1、T2和年齡對研究對象良惡性乳腺腫瘤的影響。使用Box-Tidwell方法檢驗連續自變量T1、T2和年齡與其logit轉換值間是否為線性時模型共納入6項,Bonferroni校正后顯著性水平為0.008 33(0.05/6)。線性檢驗結果得到所有連續自變量與其logit轉換值間存在線性關系。最終,得到的logistic模型具有統計學意義(χ2=40.277,P<0.001,表2)。該模型能夠正確分類90.5%的研究對象。模型的靈敏度為91.7%,特異度為88.9%。模型納入的3個自變量中,T1表現出顯著的統計學意義。
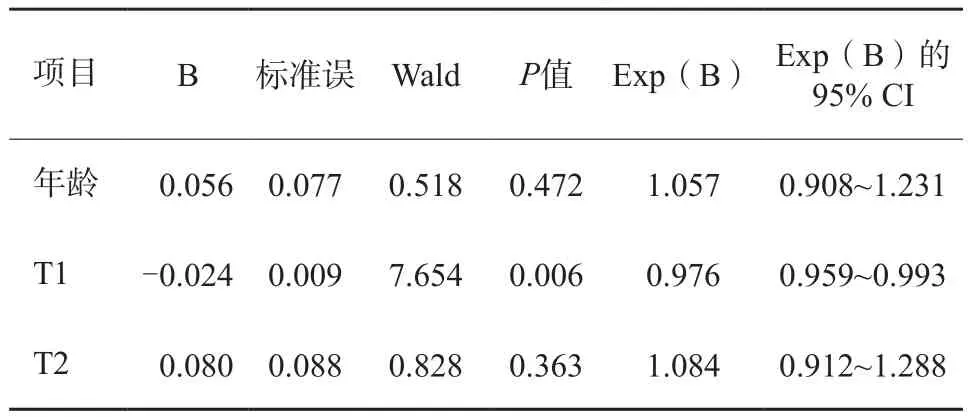
表2 logistic回歸分析結果
2.4 基于SVM分類器檢測
采用SVM分類算法和留一交叉驗證的方法訓練分類器進行分類實驗,根據準確度、靈敏度、特異度和曲線下面積(area under curve,AUC)這4個指標來評判分類結果的質量,具體結果見表3,其中采用多項式作為內核函數訓練分類器能夠得到較好的準確度和靈敏度(分別為0.929和1.000)。
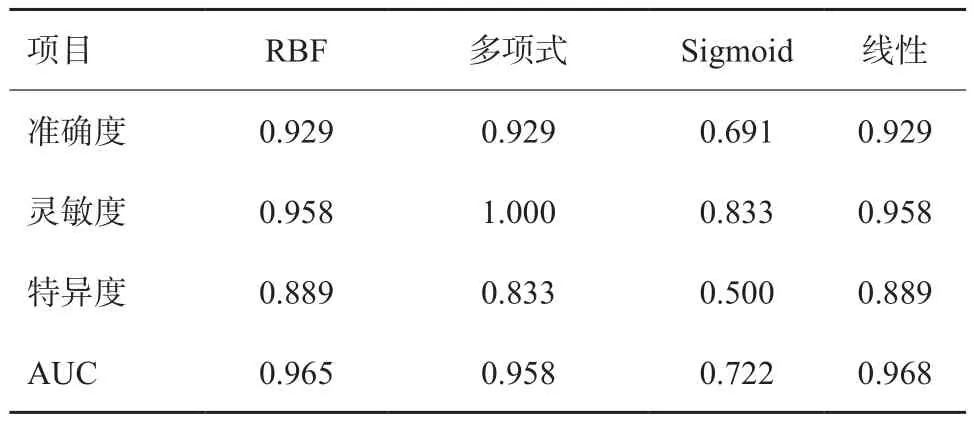
表3 基于SVM分類的結果
3 討 論
MAGiC序列在1次掃描中提供多種不同對比度的圖像和多種定量圖譜,包括T1WI、T2WI和PDWI圖等。MAGiC序列的應用可獲得常規對比圖像無法獲得的定量值,為疾病診斷、療效評價和預后研究等提供一個強大的定量工具,同時也可減少MRI掃描和閱片的時間。本研究中我們利用MAGiC序列掃描得到的圖像,對乳腺良惡性病變進行T1、T2、PD值的差異分析,以期對乳腺病變提供更全面的功能表征。在本研究中,我們發現乳腺惡性病變的平均T1、T2值均顯著高于良性病變,而PD值差異無統計學意義。
在T1、T2兩種定量指標中,定量T1值顯示出較高的鑒別診斷效率,兩種指標相結合能進一步提高乳腺癌良惡性的診斷準確度,為改善患者治療和預后提供了重要信息。MRI是多參數成像,T1和T2值取決于組織成分,如大分子濃度、水化狀態和組織含水量[12]。腫塊的成分受到病理、生理條件的影響,定量的T1和T2值可以根據組織成分的變化,反映可能的病理學性質。
本實驗中乳腺腫塊良性病變與惡性病變的T1值存在顯著差異,良性組T1(1 569.67±139.045)高于惡性組(1 233.71±119.025),差值為335.958(95% CI 255.348~416.569),這個結果與Meng等[16]和與Chen等[17]研究的結果不同。縱向弛豫時間T1是組織的固有屬性之一。在相同場強的磁場環境下,不同的組織具有不同的T1;同一組織在不同場強的磁場中亦表現出不同的T1;更為重要的是,同一組織生理狀態下的T1和病理狀態下的T1同樣表現不同。Chen等[17]在場強為3 T的磁場下對比了志愿者的纖維腺瘤組織T1值[(1 256±171)ms]和浸潤性導管癌的T1值[(1 183±256)ms]差異無統計學意義。本研究和Meng等[16]及Chen等[17]研究結果產生差異的原因可能與所使用的磁場環境、序列參數及患者選擇的不同有關。本研究所選取的是MRI報告為BI-RADS 4A以上有明確腫塊的患者,良惡性以病理學檢查結果為金標準;良性患者不局限于纖維腺瘤,這也可能是導致研究結果不同的原因。同時在Chen等[17]的研究中,計算了年輕健康志愿者正常實質的T1值,證實了年輕女性的實質受到激素水平的顯著影響,T1值在月經周期波動。健康志愿者的ROI中分布的脂肪組織比有乳腺病變的女性多。這種差異可能導致健康志愿者的T1值超過乳腺病變患者的T1值。進一步大樣本量的研究將有助于獲得更準確的T1定量結果。
弛豫過程是一個能量轉變的過程,需要一定的時間,組織的T1和T2弛豫時間是同時發生的。本研究中乳腺良性腫塊組T2值[(92.56±12.296)ms]高于惡性腫塊組T2值[(85.50±8.262)ms],差值為7.056(95% CI 0.644~13.467);與既往研究[16,18]一致。影響乳腺T2值的因素很多,包括水分含量、纖維組織含量、乳腺組織細胞密度等。人體內的水可分為自由水和結合水,其中自由水由于分子較小,橫向弛豫時間較長。而生物大分子與水的結合顯著縮短了T2。因此,自由水的量決定了橫向弛豫時間T2[19];在乳腺癌中,具有豐富細胞質的大的乳腺癌細胞快速生長,導致惡性腫瘤中的組織細胞密度高于良性病變。腫瘤組織常伴有細胞壞死,大分子物質釋放到細胞周圍的空間,使細胞外空間進一步縮小;特別是浸潤性癌癥,淋巴細胞和漿細胞浸潤間質,導致游離水減少,縮短了橫向弛豫時間。同時,在良性病變中,如纖維腺瘤中的黏液樣變性和乳腺疾病中慢性炎癥引起的間質水腫延長了橫向弛豫時間。因此,T2值的差異對于鑒別乳腺良惡性病變具有參考價值。如Liu等[20]利用常規T2 mapping技術,發現乳腺良惡性病變的T2均值分別為94.48和82.69 ms。Jung等[18]也通過SyMRI得到乳腺癌T2均值為84.75 ms。證實了乳腺良性病變的T2值高于惡性病變這一結論。未來我們將進一步探索MAGiC序列在健康受試者和乳腺病變患者中測量的定量值,以及MAGiC序列在乳腺MRI增強掃描前和增強掃描后測量的定量值的不同,來準確地對乳腺良惡性病變的T1、T2值界定一個標準。
本研究存在局限性。首先,我們沒有將MAGiC序列所測得的T1、T2值與常規序列所測得的T1、T2值進行比較。其次,我們測量的是每個病變最大直徑所在圖像層面的T1、T2值,而不是整個病變,可能丟失了其余病變的細節。第三,ROI的測量為手動測量,可能存在測量誤差。第四,本研究所獲得的樣本量尚小,需要增加樣本量來確定乳腺癌和良性病變的T1和T2值的范圍。
本研究表明基于MAGiC序列獲得的定量T1和T2值可以有效地區分乳腺良惡性病變,T1弛豫時間表現出較高的診斷效率。T2弛豫時間雖然在t檢驗過程中差異有統計學意義,但在邏輯回歸分析時沒有表現出顯著差異,這可能與T2弛豫時間自身時間短、變化不明顯有關。總之,在MRI中,基于MAGiC序列的定量MRI技術能夠提高乳腺良惡性病變的診斷價值;在常規乳腺MRI的基礎上可提供更多的鑒別診斷依據,值得臨床應用和推廣。

