Cu(II)聯咪唑硝基衍生物配合物的合成表征及其與CT-DNA相互作用研究*
王航天,范倩倩,李 焱,楊莉寧
(西安醫學院藥學院,陜西 西安 710021)
人類在長期與惡性腫瘤斗爭過程中,持續不斷地進行高效低毒的抗癌藥物的研發。咪唑類生物配體能與生物酶和受體等形成氫鍵、發生疏水作用和π-π相互作用,且具有抗癌、抗微生物和抗氧化的藥用特性,因而被人們廣泛關注[1]。作為人體的內源性金屬,銅的有機配體配合物能夠與DNA相互作用,它們具有較好的生物氧化還原活性和較強的核堿親和力[2-3]。探究金屬配合物與DNA之間的相互作用方式,對識別DNA特異結構、設計和篩選抗癌金屬藥物,以及研究DNA的水解斷裂等都有著重要意義[4-6]。我們設計合成了聯咪唑硝基衍生物—N,N’-二甲基-5-硝基-2,2’-聯咪唑(NO2Me2biim, L) (圖1),并以它為配體,得到了其過渡金屬銅(Ⅱ)配合物,采用紫外-可見光譜(Uv-vis)、熒光光譜、相對黏度等分析方法初步研究了配體及其配合物與小牛胸腺DNA(CT-DNA)的相互作用。
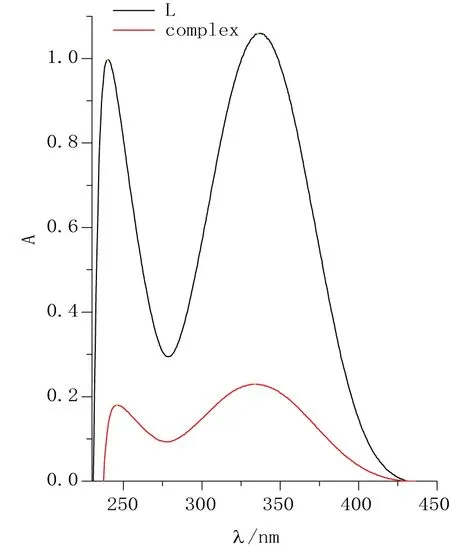
圖1 —N,N’-二甲基-5-硝基-2,2’-聯咪唑結構式
1 材料與方法
1.1 儀器試劑
德國EA 元素分析系統公司VARI-EL型元素分析儀,上海大譜儀器有限公司DDS-307型電導儀,德國 Brucker 公司EQUINOX55 型紅外光譜儀,日本島津公司UV-1800紫外分光光度計,日本日立公司F-4500熒光分光光光度計,上海申玻玻璃儀器廠烏氏黏度計。
小牛胸腺DNA(CT-DNA),三羥甲基氨基甲烷(Tris)均購自美國Sigma公司,Cu(ClO4)2結晶水合物自制,按文獻方法合成配體NO2Me2biim[7],其余試劑均為國產分析純試劑,蒸餾水為二次蒸餾水。
1.2 配合物的合成
稱取 0.5 mmol 自制的Cu(ClO4)2結晶水合物溶于甲醇中,加入 15 mL 0.5 mmol 配體NO2Me2biim的甲醇溶液,室溫下攪拌反應 1 h,過濾,濾液靜置 14 d,析出綠色球狀晶體。
1.3 配體及配合物與CT-DNA相互作用實驗
配體及配合物與CT-DNA相互作用的紫外光譜、熒光光譜及黏度法實驗均采用文獻已報道的經典方法進行[8]。
2 結果與討論
2.1 配合物的組成與結構表征
配合物的化學式、元素分析及摩爾電導率(Λm)列于表1。

表1 配合物的元素分析及摩爾電導率
室溫條件下,配合物乙醇溶液的摩爾電導率值表明配合物在乙醇中是非電解質[9],即銅離子與配體和高氯酸根離子配位形成中性配合物。


表2 配體及配合物的主要紅外吸收頻率(cm-1)及歸屬
由圖2紫外-可見吸收光譜可見,配體中咪唑環共軛體系的π→π*躍遷使其在 240 nm 和 336 nm 處表現出兩個主要吸收峰。配體與金屬離子發生配位形成配合物后,相應的紫外吸收峰的強度發生了明顯變化。
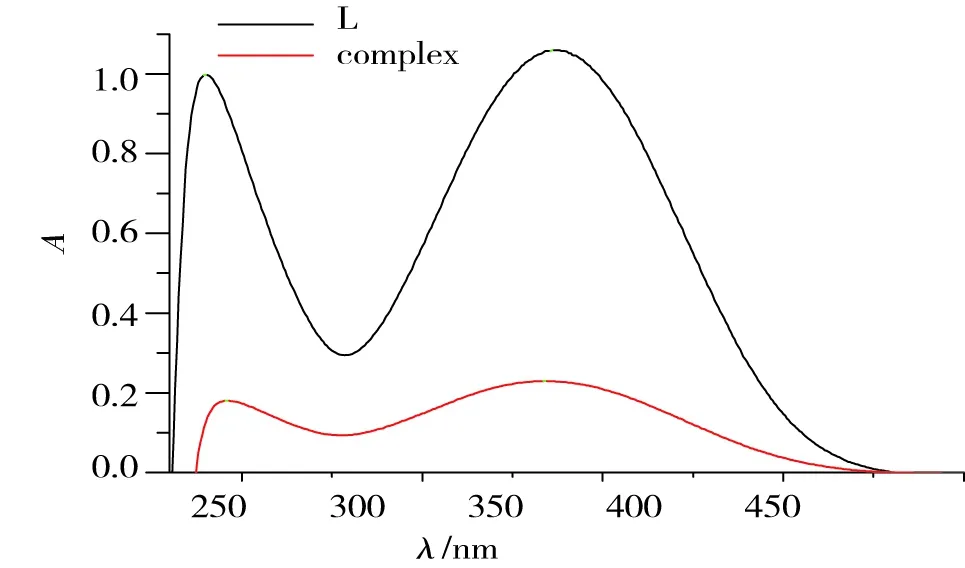
圖2 配體和配合物的紫外吸收光譜
綜合上述IR、摩爾電導率、UV-Vis和元素分析結果,推測配合物組成為[Cu(NO2Me2biim)2(ClO4)2],高氯酸根和配體都與金屬進行單齒配位形成四配位的銅配合物[12],結構如圖3所示。
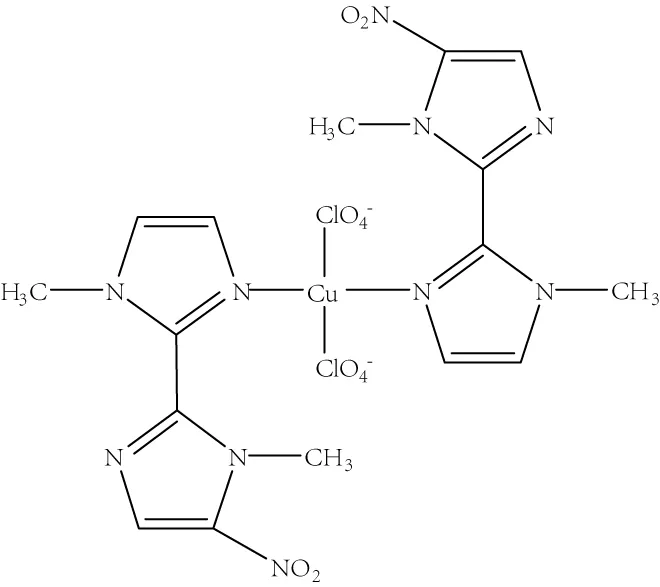
圖3 [Cu(NO2Me2biim)2(ClO4)2]結構式
2.2 配體及Cu(Ⅱ)配合物與DNA相互作用紫外吸收光譜
圖4表明,當配體和配合物溶液的濃度一定時,二者的最大紫外特征吸收峰隨著CT-DNA加入量的增加均表現為減色效應,而Cu(Ⅱ)配合物在 240 nm 附近的吸收峰卻又表現為增色效應,與配體不同的是位移和強度都發生了一定的變化。此現象發生的原因可能是當配合物與DNA相互作用時,破壞了配合物聚集體及配合物分子之間的氫鍵[13-14],同時配合物的紫外吸收還出現1個等吸收點,等吸收點的產生代表了配合物與DNA形成了復合物[15]。吸收減弱及出現等吸收點是靜電作用或嵌插作用的特征。
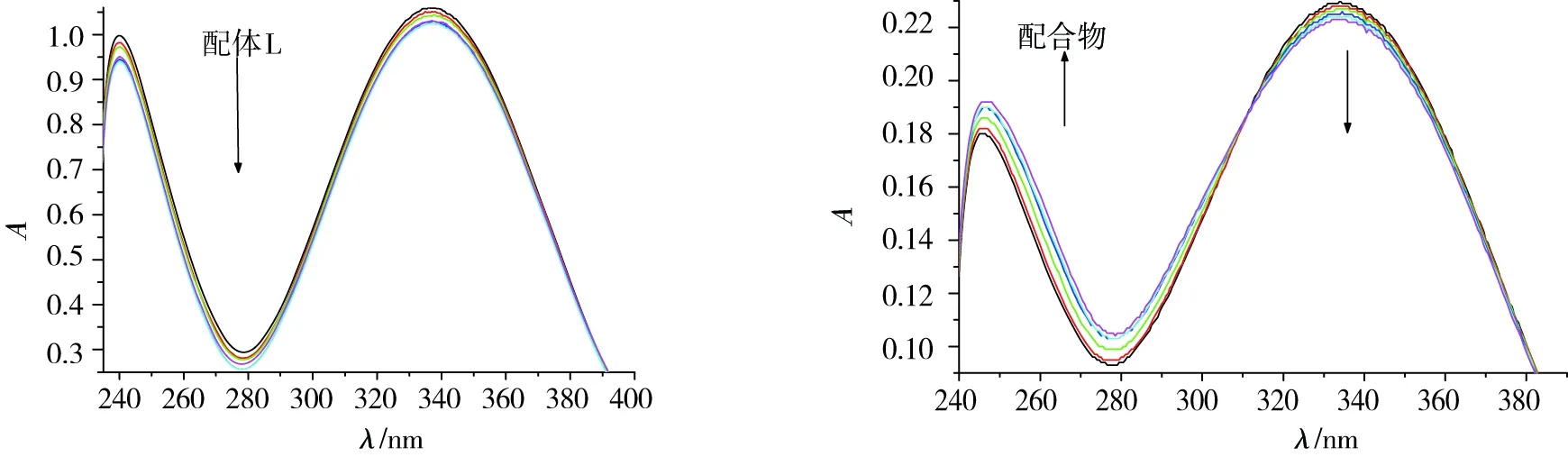
圖4 配體L及Cu(Ⅱ)配合物與DNA作用的紫外吸收光譜
2.3 配體及Cu(Ⅱ)配合物與DNA相互作用的熒光光譜
配體的熒光強度隨著DNA濃度的增大而減小,熒光發射峰發生了較大的紅移,而Cu(Ⅱ)配合物的熒光光譜強度則增大,如圖5所示。研究表明,當小分子與DNA相互作用,其熒光光譜減弱甚至發生猝滅,可能是二者在水溶液中互相碰撞發生能量交換所致。
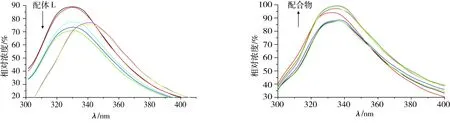
圖5 配體L及Cu(Ⅱ)配合物與DNA作用的熒光發射光譜
2.4 配體及其配合物與 DNA 相互作用的黏度
DNA相對黏度隨配合物濃度的增加而逐漸減小,隨配體濃度的增加而逐漸增大,如圖6所示。小分子以插入模式與DNA作用,使DNA雙螺旋鏈增長,黏度增大;以部分插入方式與DNA作用,DNA雙螺旋發生扭曲,黏度減小[16]。
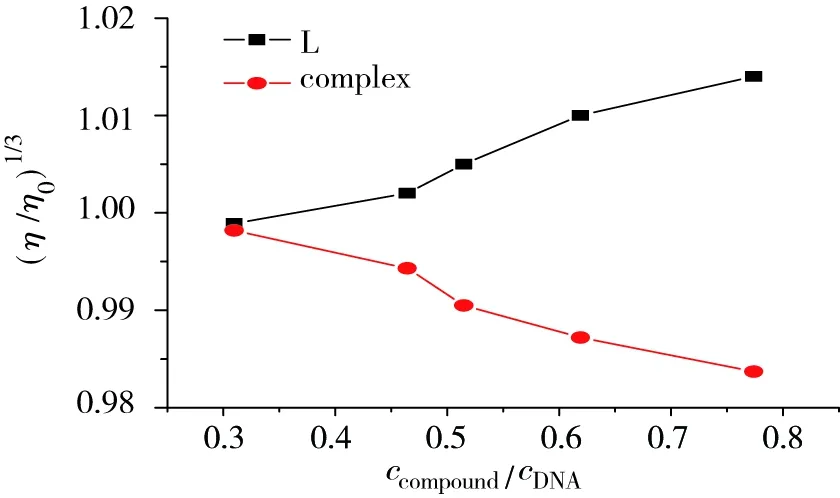
圖6 DNA的相對黏度隨配體及Cu(Ⅱ)配合物加入量的變化
3 結論
合成了N,N’-二甲基-5-硝基-2,2’-聯咪唑的銅(Ⅱ)配合物并對其進行了性質表征,確定了配合物的可能結構。與DNA相互作用的研究結果表明,配體及其Cu(Ⅱ)配合物與DNA相互作用模式分別為典型插入和部分插入模式,配體結構的平面性比配合物更好,所以其與DNA的相互作用力較強。

