鹽酸與碳酸鈉分步反應探究實驗裝置的改進
郭雨琦 孟慶華 劉翠 邢蓓蓓
摘要: 在評析相關文獻工作的基礎上,根據鹽酸與碳酸鈉分步反應的原理,探析鹽酸與碳酸鈉反應過程中模擬的pH、 CO2濃度變化的雙縱坐標曲線應具有的特征。為獲得接近該模擬曲線的實驗數據,采用蠕動泵、真空循環泵對實驗裝置進行改進,優化實驗條件。實驗結果表明,鹽酸溶液與碳酸鈉溶液均為0.01mol/L、滴定速度約為5mL/min、空氣循環流速度為第三檔的條件下,較準確地反映了反應物之間的量比關系,改善了CO2濃度測定數據滯后等問題,獲得的pH、 CO2濃度變化的雙縱坐標曲線與模擬曲線基本一致。
關鍵詞: 碳酸鈉溶液; 鹽酸溶液; 反應機理; 實驗裝置改進
文章編號: 1005-6629(2022)11-0070-05
中圖分類號: G633.8
文獻標識碼: B
1 問題提出
碳酸鈉、碳酸氫鈉與酸的反應是蘇教版高中化學教材(必修)第一冊中“碳酸鈉、碳酸氫鈉”一節的教學內容,其中“學以致用”欄目中“表3-6碳酸鈉與碳酸氫鈉的性質比較”中描述:“碳酸鈉、碳酸氫鈉與酸反應都放出CO2氣體,但NaHCO3與酸反應比Na2CO3更劇烈”,這種
宏觀的實驗現象隱含的微觀原因是什么?一般學生根據實驗現象均認為是NaHCO3與酸的反應比Na2CO3與酸的反應速率快,而真正的微觀原因是Na2CO3與酸的反應是分步進行的:Na2CO3與酸反應先生成NaHCO3,過量的酸繼續與NaHCO3反應生成CO2氣體。如何讓學生更容易理解掌握碳酸鈉與鹽酸反應是分步進行的,進而建構多元弱酸鹽與較強酸反應的認知模型?教育學理論認為,形象思維可以降低抽象內容的學習困難,有助于學生更好地理解抽象的概念和理論[1,2]。所謂形象思維就是利用感官直接接受具體形象的信息,在頭腦中形成表象,再利用這些表象進行類比、概括、聯想、想象等思維加工直至形成認識。中學化學中的數字化實驗就是將抽象知識可視化進而充分發揮學生的形象思維作用的重要手段。獲得的數據和圖像將直觀有效地呈現Na2CO3與酸分步反應的機理和反應的微觀本質。
2 相關文獻簡評
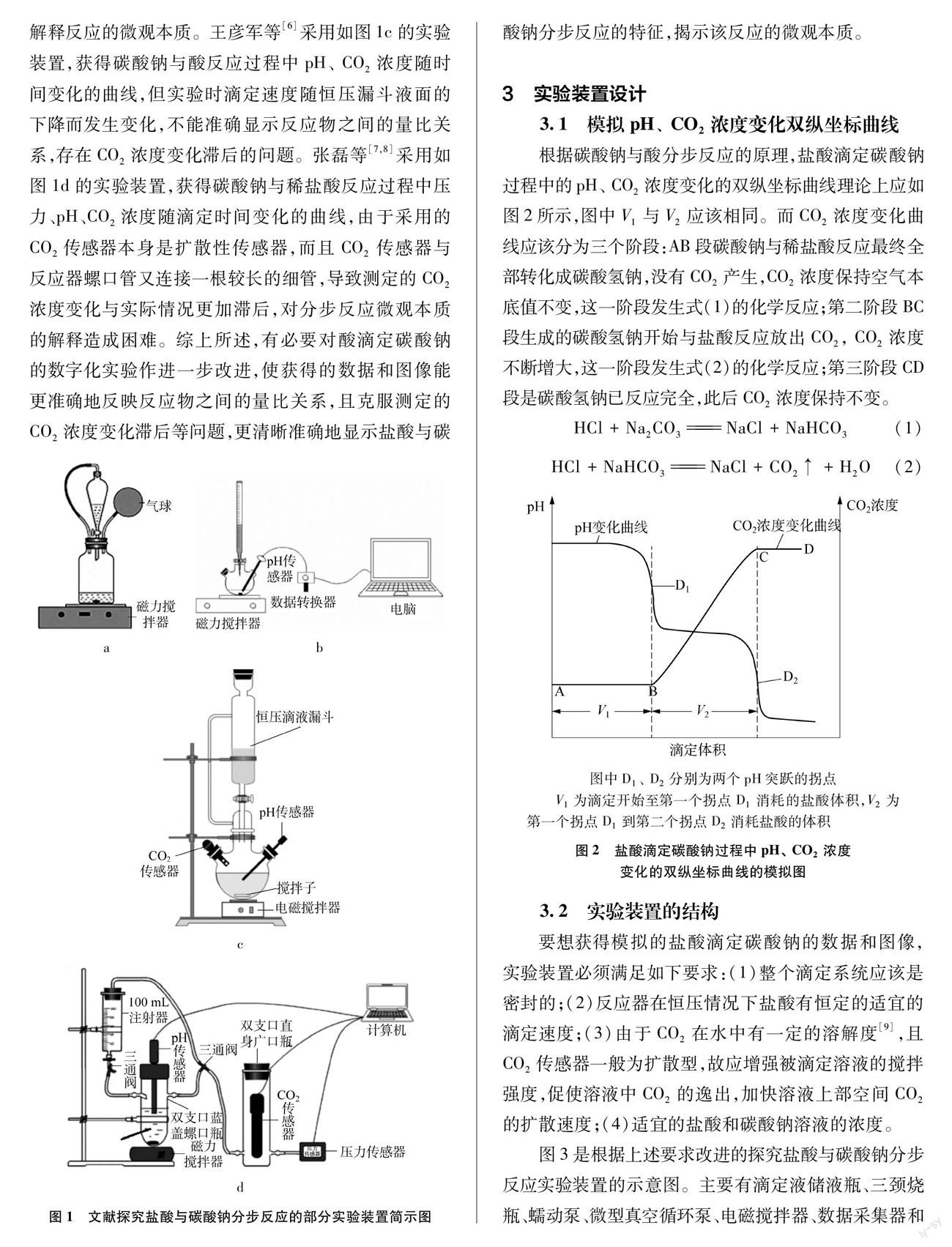
有關Na2CO3與酸的分步反應許多研究者已做了大量的探究工作,早期的文獻報道主要集中在對傳統實驗裝置的改進以及對實驗條件的探尋,使分步反應的實驗現象更明顯、易于觀測等[3]。隨著數字化技術的發展,將壓強傳感器、pH傳感器、CO2傳感器與數據采集器和計算機依次相連,采集實驗過程中多種物理量(如壓強、pH、 CO2濃度)的變化數據并以圖像形式呈現,可視化地顯示了分步反應的特征,經過軟件對數據進行分析,學生通過形象思維就比較容易獲得實驗結論。伍強等[4]采用了如圖1a所示的恒壓式實驗裝置來探究Na2CO3溶液與酸的互滴反應,但實驗結果對現象背后反應的本質仍難以解釋清楚,用該裝置進行實驗時,要求鹽酸與碳酸鈉溶液的濃度要嚴格一致,否則對實驗現象尤其是顏色的觀察會有影響。符吉霞等[5]采用如圖1b的裝置記錄碳酸鈉與酸反應過程中pH隨時間的變化曲線,只能說明反應是分步進行的,但不能解釋反應的微觀本質。王彥軍等[6]采用如圖1c的實驗裝置,獲得碳酸鈉與酸反應過程中pH、 CO2濃度隨時間變化的曲線,但實驗時滴定速度隨恒壓漏斗液面的下降而發生變化,不能準確顯示反應物之間的量比關系,存在CO2濃度變化滯后的問題。張磊等[7,8]采用如圖1d的實驗裝置,獲得碳酸鈉與稀鹽酸反應過程中壓力、pH、CO2濃度隨滴定時間變化的曲線,由于采用的CO2傳感器本身是擴散性傳感器,而且CO2傳感器與反應器螺口管又連接一根較長的細管,導致測定的CO2濃度變化與實際情況更加滯后,對分步反應微觀本質的解釋造成困難。綜上所述,有必要對酸滴定碳酸鈉的數字化實驗作進一步改進,使獲得的數據和圖像能更準確地反映反應物之間的量比關系,且克服測定的CO2濃度變化滯后等問題,更清晰準確地顯示鹽酸與碳酸鈉分步反應的特征,揭示該反應的微觀本質。
3 實驗裝置設計
3.1 模擬pH、 CO2濃度變化雙縱坐標曲線
根據碳酸鈉與酸分步反應的原理,鹽酸滴定碳酸鈉過程中的pH、 CO2濃度變化的雙縱坐標曲線理論上應如圖2所示,圖中V1與V2應該相同。而CO2濃度變化曲線應該分為三個階段:AB段碳酸鈉與稀鹽酸反應最終全部轉化成碳酸氫鈉,沒有CO2產生,CO2濃度保持空氣本底值不變,這一階段發生式(1)的化學反應;第二階段BC段生成的碳酸氫鈉開始與鹽酸反應放出CO2, CO2濃度不斷增大,這一階段發生式(2)的化學反應;第三階段CD段是碳酸氫鈉已反應完全,此后CO2濃度保持不變。
HCl+Na2CO3NaCl+NaHCO3(1)
HCl+NaHCO3NaCl+CO2↑+H2O(2)
圖中D1、 D2分別為兩個pH突躍的拐點
V1為滴定開始至第一個拐點D1消耗的鹽酸體積,
V2為第一個拐點D1到第二個拐點D2消耗鹽酸的體積
3.2 實驗裝置的結構
要想獲得模擬的鹽酸滴定碳酸鈉的數據和圖像,實驗裝置必須滿足如下要求:(1)整個滴定系統應該是密封的;(2)反應器在恒壓情況下鹽酸有恒定的適宜的滴定速度;(3)由于CO2在水中有一定的溶解度[9],且CO2傳感器一般為擴散型,故應增強被滴定溶液的攪拌強度,促使溶液中CO2的逸出,加快溶液上部空間CO2的擴散速度;(4)適宜的鹽酸和碳酸鈉溶液的濃度。
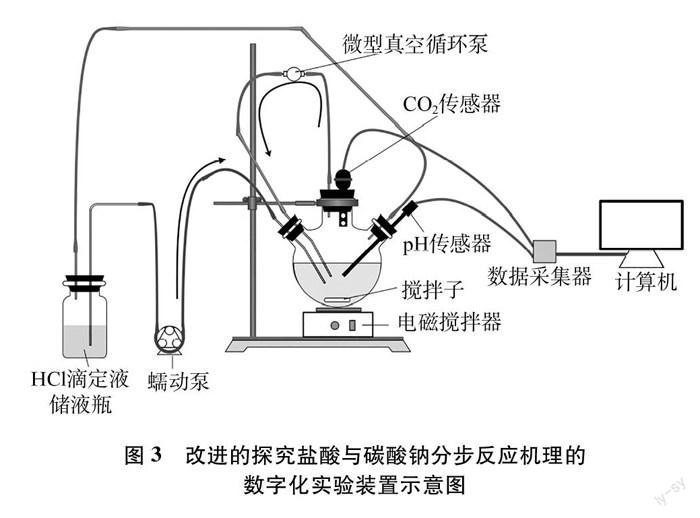
圖3是根據上述要求改進的探究鹽酸與碳酸鈉分步反應實驗裝置的示意圖。主要有滴定液儲液瓶、三頸燒瓶、蠕動泵、微型真空循環泵、電磁攪拌器、數據采集器和計算機(包括相關數據采集、處理軟件)等組成。儲液瓶、三頸燒瓶各開口用直徑不同、帶孔的橡膠塞密封。蠕動泵可使滴定液的滴加速度恒定不變,并可方便調節滴定速度。儲液瓶與三頸燒瓶用橡膠管連通,可使滴定系統氣壓保持平衡。滴定過程中使用電磁攪拌器
攪動三頸燒瓶中的溶液。微型真空循環泵驅動空氣通入溶液中加強溶液攪動強度,使溶解其中的CO2逸出,加快系統內CO2的擴散,克服CO2傳感器檢測的滯后問題。利用數據采集器的兩個通道同時采集滴定過程中的pH、 CO2濃度的數據,為方便比較采用雙縱坐標曲線直觀顯示二者的變化。
4 儀器和藥品試劑
4.1 儀器
威尼爾(Vernier)CO2-BAT型CO2傳感器、威尼爾(Vernier)PH-BAT型pH傳感器、威尼爾(Vernier)LabQuest Mini型數據收集器、數據采集軟件(Logger Pro3.14.1)、威尼爾(Vernier)STIR電磁攪拌器、HY-V1微型真空循環泵(科斯達機電)、(為微型真空循環泵供電)24V可變直流電源、BT100-2J蠕動泵(220V交流供電,保定蘭格恒流泵有限公司)、外徑5mm壁厚1mm硅膠軟管、500mL三頸燒瓶(定制)、500mL廣口試劑瓶
4.2 藥品試劑
碳酸鈉(分析純,西隴科學股份有限公司)、碳酸氫鈉(分析純,國藥集團化學試劑有限公司)、濃鹽酸(分析純,西隴科學股份有限公司)、純凈水
溶液的配制:1.0mol/L HCl溶液儲備液;1.0mol/L Na2CO3溶液儲備液;1.0mol/L NaHCO3溶液儲備液;不同濃度的上述各種溶液可分別取上述儲備液用純凈水稀釋獲得。
5 實驗部分
5.1 空氣循環泵的使用方法
改進的實驗裝置采用微型真空循環泵的型號是HY-V1,直流電壓供電,最大工作電壓為24V。泵頭有一個進氣口和一個出氣口,最大空氣流速為12L/min,根據提供給真空循環泵電壓大小(0V、 8V、 16V、 24V)分別將空氣循環流速定義為0檔、1檔、2檔和3檔。
設置不同的工作電壓可改變空氣循環流速,0V即空氣不循環,電壓越大空氣循環流速越快。
5.2 蠕動泵的使用方法
蠕動泵又叫恒流泵或軟管泵,由驅動器、泵頭和軟管三部分組成;蠕動泵通過泵頭上的滾輪對泵軟管進行交替擠壓,在管內形成負壓,液體從泵軟管進口端吸入,從出口端流出,就像用手指擠壓一根充滿液體的軟管,隨著手指向前滑動管內的液體便向前移動。實驗中采用外徑5mm壁厚1mm硅膠軟管,設置蠕動泵驅動器不同的轉速,使滴定速度分別為5mL/min、 7.5mL/min、 10mL/min和15mL/min。
5.3 實驗步驟
按圖3所示組裝實驗裝置,實驗操作步驟如下:
(1)將滴定液裝入干燥潔凈的滴定液儲液瓶中;
(2)打開蠕動泵、微型真空循環泵、電磁攪拌器、計算機電源(并啟動數據采集處理軟件),設置各儀器的工作參數;
(3)(滴定液首次使用時)啟動蠕動泵工作一段時間,用滴定液沖洗管道并使管內充滿滴定液;
(4)清洗三頸燒瓶,并將適量體積的碳酸鈉溶液(被滴定液)定量移入潔凈的三頸燒瓶中,檢查確認滴定系統處于密封狀態;
(5)先啟動微型真空循環泵、電磁攪拌器工作,然后啟動蠕動泵,同時開始數據采集,進行滴定分析;
(6)需結束滴定分析時,先停止數據采集(并保存數據),然后依次停止蠕動泵、電磁攪拌器以及微型真空循環泵的工作。
6 實驗結果與討論
6.1 濃度對pH、 CO2濃度雙縱坐標曲線形狀的影響
在探究鹽酸與碳酸鈉分步反應的文獻中,鹽酸溶液與碳酸鈉溶液濃度一般均采用相同的濃度值,但不同文獻中溶液的濃度是不同的,濃度范圍一般在0.1~1.0mol/L之間。
本文最終所采用碳酸鈉、碳酸氫鈉以及鹽酸溶液的濃度均為0.01mol/L。
實驗發現,若按文獻采用的最小濃度0.1mol/L,將20.00mL Na2CO3溶液定量轉移至500mL三頸燒瓶中進行滴定分析時,滴定曲線在第二個拐點D2后CO2濃度已超出CO2傳感器的檢測上限。于是便不斷降低濃度進行實驗,當濃度為0.01mol/L時,在較優的真空循環泵空氣循環流速和滴定速度下,pH、 CO2濃度的變化曲線比較接近模擬曲線。若濃度低于0.01mol/L后,則pH變化曲線的第一突躍就不太明顯,CO2濃度的變化也因生成量太少而有滯后現象,因此確定溶液的濃度均為0.01mol/L較為適宜。
6.2 空氣循環流速對pH、 CO2濃度雙縱坐標曲線形狀的影響
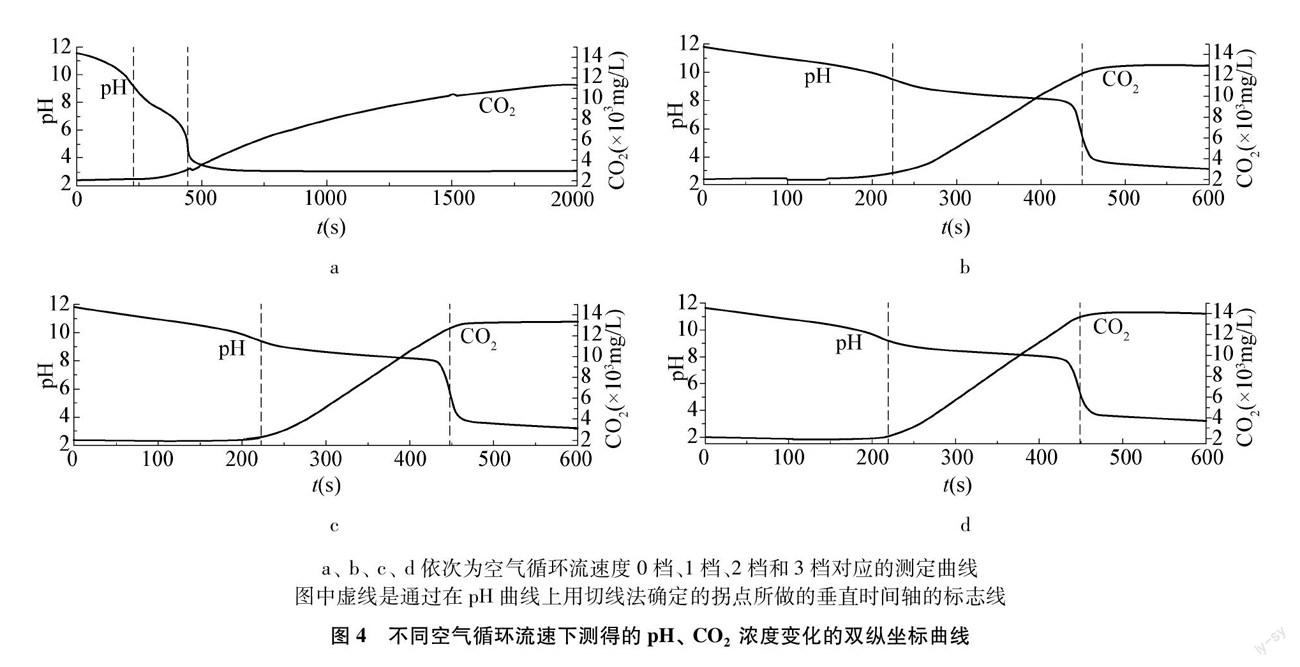
真空循環泵在最大工作電壓24V下(第三檔)工作,基本可消除CO2滯后現象。圖4是溶液濃度值采用0.01mol/L,滴定速度采用5mL/min時不同的空氣循環流速下,測得的pH、 CO2濃度雙縱坐標曲線。從圖4a可以看出空氣不循環時,測定的CO2濃度變化遠遠滯后于化學反應;圖4b、 4c、 4d顯示,隨空氣循環流速增大,CO2滯后程度不斷減小,因此確定真空循環泵在最大工作電壓24V下(第三檔)工作較為適宜。
6.3 滴定速度對pH、 CO2濃度雙縱坐標曲線形狀的影響
在其他條件較優的條件下,滴定速度為5mL/min比較適宜。圖5是溶液濃度采用0.01mol/L,空氣循環流速為第三檔時滴定速度分別為5mL/min、7.5mL/min、 10mL/min和15mL/min測得的pH、 CO2濃度變化的雙縱坐標曲線,依次對應的是圖5a、 5b、 5c、 5d。從圖中可以看出隨滴定速度的增加,CO2滯后現象越嚴重,原因是在第一拐點后隨著滴定速度的增加,單位時間內產生的CO2總量增加,CO2不能及時擴散到傳感器造成的。但若滴定速度太小,實驗時間又會拖得太長,綜合考慮后確定滴定速度為5mL/min。
表1是對圖5a、 5b、 5c、 5d中pH變化曲線采用切線法確定的化學計量點計算的V1和V2值,表中數據表明V1基本與V2相同。
根據上述實驗結果確定較優實驗條件為:溶液濃度宜采用0.01mol/L、空氣循環流速為第三檔、滴定速度為5mL/min。圖6是在較優條件下獲得的鹽酸與碳酸鈉反應的pH、 CO2濃度變化的雙縱坐標曲線,與圖2的理想曲線基本一致。為便于分析對比,還在較優條件下測定了鹽酸與碳酸氫鈉反應的pH、 CO2濃度變化的雙坐標曲線如圖7所示。比較圖6和圖7就能解釋碳酸鈉、碳酸氫鈉分別與酸反應時,宏觀上為什么NaHCO3與酸反應比Na2CO3與酸反應更快更劇烈。
7 結語
在利用數字化實驗探索某些知識可視化實驗時,要充分考慮實驗裝置結構、實驗條件等因素對獲得的圖像
的直觀性影響,通過對實驗裝置結構和實驗條件的優化,讓知識點的特征和規律在圖像中充分呈現,
展示和發揮學生的形象思維的作用,有助于學生更好地理解抽象概念及理論,提高教學效果。
盡管本次改進的實驗裝置在較優條件下基本上能得到與理想曲線一致的pH、 CO2濃度變化的雙坐標曲線,但畢竟溶液濃度(0.01mol/L)太小,致使鹽酸與碳酸鈉反應的pH曲線第一突躍不太明顯,若要增大濃度,有必要從三頸燒瓶的體積和形狀上作進一步的改進,后續相關工作將另文報道。
致謝:感謝江蘇省徐州市第二中學孟彥老師對本論文研究過程中實驗裝置應用方面的支持。
參考文獻:
[1] 陳屹, 吳俊明. 化學的形象思維訓練及能力培養[J]. 化學教學, 2021, (3): 8~12.
[2] 江家發. 化學教學論[M]. 蕪湖: 安徽師范大學出版社, 2014: 147~150.
[3] [4] 伍強, 方瑞光. 碳酸鈉和碳酸氫鈉與稀鹽酸反應實驗的創新設計[J]. 化學教學, 2016, (8): 63~65.
[5] 符吉霞, 丁偉. 碳酸鈉和碳酸氫鈉與稀鹽酸反應的創新實驗設計及教學應用[J]. 教育與裝備研究, 2020, (2): 28~32.
[6] 王彥軍, 施彩娟. 基于化學學科素養培育的創新實驗研究[J]. 新課程導學, 2019, (25): 25~26, 28.
[7] 張磊, 王璇, 孫美華. 基于傳感器檢測探究鹽酸與碳酸鈉溶液的反應[J]. 化學教學. 2021, (6): 74~77.
[8] 張磊, 王璇, 董金水. 碳酸鈉溶液與鹽酸反應原理探究的裝置改進[J]. 化學教學, 2022, (1): 64~68.
[9] 徐環. 電解質溶液中CO2的鹽效應和沉積物-海水界面CO2擴散通量的研究[D]. 青島: 中國海洋大學碩士學位論文, 2003: 31~45.

