MPP+對N2a細胞中CDR1as基因表達的影響
張小琴 王友翠 謝俊霞

[摘要]目的 探討1-甲基-4-苯基吡啶離子(MPP+)對N2a細胞中環狀RNA小腦變性相關蛋白1反義轉錄物(CDR1as)基因表達的影響。方法 常規培養N2a神經母細胞瘤細胞,給予100 μmol/L的MPP+分別處理3、6、9和12 h。采用實時熒光定量PCR檢測 CDR1as基因的表達。結果 與用基礎培養液處理的對照組相比,經MPP+處理3、6、9和12 h的N2a細胞CDR1as基因表達明顯降低(F=10.010,q=7.003~8.609,P<0.05)。結論 MPP+能誘導N2a細胞中 CDR1as基因的表達顯著降低,提示 CDR1as基因可能參與帕金森病的發病。
[關鍵詞]RNA,環狀;CDR1as;1-甲基-4-苯基吡啶;N2a細胞;帕金森病
[中圖分類號]R338.2[文獻標志碼]A[文章編號]2096-5532(2022)03-0333-04
doi:10.11712/jms.2096-5532.2022.58.121
EFFECT OF 1-METHYL-4-PHENYLPYRIDINIUM ON EXPRESSION OF THE CEREBELLAR DEGENERATION-RELATED PROTEIN 1 ANTISENSE TRANSCRIPT GENE IN N2A CELLS
ZHANG Xiaoqin, WANG Youcui, XIE Junxia
(Department of Physiology and Pathophysiology, School of Basic Medicine, Qingdao University, Qingdao 266071, China)
[ABSTRACT] Objective To investigate the effect of 1-methyl-4-phenylpyridinium (MPP+) on the expression of the cerebellar degeneration-related protein 1 antisense transcript (CDR1as) gene in N2a cells.Methods Neuroblastoma N2a cells were cultured with conventional methods and then treated with 100 μmol/L MPP+for 3, 6, 9, and 12 h. Quantitative real-time PCR was used to measure the mRNA expression of CDR1as.Results Compared with the control group treated with the basal medium, the N2a cells treated with MPP+for 3, 6, 9, and 12 h had a significant reduction in the mRNA expression of CDR1as (F=10.010,q=7.003-8.609,P<0.05).Conclusion MPP+induces a significant reduction in the expression of the CDR1as gene in N2a cells, suggesting that the CDR1as gene may be involved in the pathogenesis of Parkinsons disease.
[KEY WORDS] RNA, circular; CDR1as; 1-methyl-4-phenylpyridinium; N2a cells; Parkinson disease
帕金森病(PD)是僅次于阿爾茨海默病的第二大神經退行性疾病[1-9]。PD主要的病理特征是中腦黑質多巴胺(DA)能神經元大量變性丟失,導致紋狀體內DA含量減少,而變性丟失的 DA能神經元內均出現α-突觸核蛋白積聚[10-13]。環狀RNA是一類不具有5′末端帽子和3′末端 poly(A)尾巴、以共價鍵形成環形結構的RNA分子。由于呈閉合環狀結構,對核酸外切酶不敏感,因此環狀RNA比線性RNA更為穩定,且具有物種保守性、組織時序性及疾病表達特異性[14-20]。有文獻報道,環狀RNA小腦變性相關蛋白1反義轉錄物(CDR1as)可作為miR-7海綿調控miR-7靶基因的表達[21-22]。已有研究表明,α-突觸核蛋白基因的拷貝增加或點突變均可導致α-突觸核蛋白積聚,從而引發PD[23-24]。而miR-7可以與α-突觸核蛋白基因編碼 mRNA的3′UTR 區相互作用,從而抑制其翻譯[25-26]。這提示作為miR-7海綿的CDR1as基因可能參與了DA能神經元的變性丟失。因此,闡明CDR1as基因在PD中發揮的作用至關重要。本研究旨在探討經1-甲基-4-苯基吡啶離子(MPP+)處理的PD細胞模型中CDR1as基因的表達變化。
1材料與方法
1.1主要試劑及其來源
MPP+(M0896)由美國Sigma公司提供,用雙蒸水稀釋至10 mmol/L,分裝,-20 ℃避光保存;DMEM高糖基礎培養液(01-052-1ACS)購自BI公司;TRIzol購自ambion公司;PCR逆轉錄試劑盒(AG11711)和SYBR Green(AG11702)購自艾科瑞生物公司;胎牛血清(澳洲源,FND500)購自依科賽公司;青霉素和鏈霉素混合雙抗液(F1400)購自索萊寶公司。
1.2細胞培養
小鼠神經母細胞瘤N2a細胞培養于含體積分數0.05胎牛血清、100 kU/L青霉素和100 mg/L鏈霉素混合雙抗的DMEM高糖培養液中,在37 ℃、體積分數0.05 CO2條件下培養。
1.3四甲基偶氮唑鹽(MTT)法檢測細胞活力
將N2a細胞接種于96孔板中,每孔細胞懸液200 μL(細胞數為8×104個),培養24 h后,棄上清,對照組直接加入新鮮基礎培養液,MPP+組加入終濃度為100 μmol/L的MPP+,分別處理3、6、9和12 h。細胞處理結束后,每孔加入5 g/L的MTT 20 μL,培養4 h后取出培養板,棄上清,每孔加入100 μL的二甲基亞砜(DMSO),振蕩10 min。用酶標儀檢測波長570 nm處的吸光度(A)值,計算細胞存活率。
1.4實時熒光定量PCR(RT-PCR)檢測CDR1as基因表達
將傳代N2a細胞接種于12孔板,分為對照組(A組)和100 μmol/L MPP+處理3、6、9、12 h組(B、C、D、E組)。采用TRIzol法冰上裂解各組細胞5 min。按照PCR逆轉錄試劑說明書操作,提取細胞總RNA。取1 μg的總RNA,加入1 μL gDNA Clean Reagent、2 μL 5×gDNA Clean Buffer,用RNA free water補至10 μL,42 ℃變性2 min;隨后向上述反應體系中加入Evo M-MLV RTase Enzyme Mix 1 μL、RT Primer Mix 1 μL、5×RTase Reaction Buffer Mix Ⅰ 4 μL、RNA free water 4 μL,37 ℃作用15 min,繼以85 ℃、5 s逆轉錄合成cDNA。采用SYBR Green染料法相對定量測定CDR1as基因的表達。RT-PCR 檢測所用引物及其序列見表1。應用2-ΔΔCt方法計算目的基因相對表達量。
1.5統計學處理
應用Graph Pad Prism 6軟件進行統計學處理。實驗所得計量資料結果以x±s形式表示,兩組均數比較采用t檢驗;多組均數比較采用單因素方差分析(One-Way ANOVA檢驗),繼以Tukey法進行進一步組間兩兩比較。P<0.05表示差異有統計學意義。
2結果
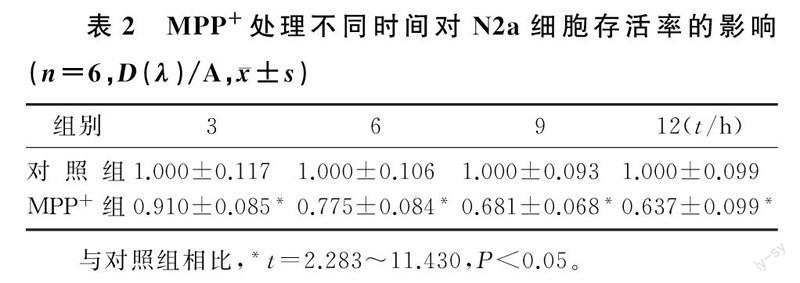
2.1MPP+作用不同時間對N2a細胞存活率影響
與對照組相比較,經100 μmol/L MPP+作用3、6、9和12 h的N2a細胞存活率均有明顯下降,差異具有統計學意義(t=2.283~11.430,P<0.05)。見表2。
2.2MPP+作用不同時間后N2a細胞中CDR1as基因的表達變化
RT-PCR檢測結果顯示,A、B、C、D、E組N2a細胞中CDR1as基因的表達水平分別為1.070±0.338、0.207±0.034、0.290±0.039、0.354±0.121和0.368±0.137(n=6)。與對照組比,經100 μmol/L MPP+作用3、6、9和12 h的N2a細胞CDR1as基因表達水平明顯降低,差異均具有顯著意義(F=10.010,q=7.003~8.609,P<0.05)。
3討論
PD是世界上第二大常見的神經退行性疾病,隨著人口老齡化加劇,發病人數逐年增加[1-9]。PD主要病理學特征是黑質區DA能神經元進行性丟失,紋狀體DA含量降低。臨床上主要表現為肌僵直、靜止性震顫、姿勢不穩、運動遲緩,影響了病人的生活質量[27]。左旋多巴是治療PD的常用藥物,但大多數病人長期服用左旋多巴后出現不自主運動、認知障礙、癡呆等副作用[28]。因此,尋找新的治療靶點具有重要的意義。近期研究發現,CDR1as參與PD的發病進程,但其確切的機制尚未闡明。
研究表明,CDR1as基因在人和小鼠腦組織中可有效地環化,而檢測不到線性CDR1as[29]。人源CDR1as基因序列含有74個miR-7結合位點,小鼠CDR1as基因序列含有130個miR-7結合位點,且在不同物種間高度保守[21-22,29]。CDR1as與miR-7共同高表達于腦組織神經元的胞體和突起,在小腦、中腦、海馬、嗅球神經元中均能檢測到CDR1as基因的表達[29-30]。研究發現,CDR1as基因在興奮性
神經元中表達水平較高,CDR1as基因敲除小鼠表現出興奮性突觸誘發電位功能障礙[29]。在斑馬魚胚胎中過表達人源CDR1as會導致中腦體積縮小,其表型與miR-7缺失相似,且通過補充miR-7前體可部分恢復中腦體積,提示CDR1as可能是通過與miR-7相互作用,即作為miR-7海綿吸附miR-7而發揮作用[19]。有文獻報道,在PD病人和1-甲基-4-苯基-1,2,3,6-四氫吡啶誘導的PD小鼠的中腦黑質區,miR-7的表達均顯著降低,在小鼠中腦黑質區敲低miR-7,則會導致α-突觸核蛋白積聚并伴有DA能神經元的變性丟失,同時紋狀體內DA含量顯著下降,提示miR-7可能在α-突觸核蛋白的轉錄后調節中發揮重要作用[31-32]。此外,miR-7在調節PD發病進程中的神經炎癥和DA能神經元死亡中具有重要作用[33-36]。因此,CDR1as可能通過調節miR-7-α-突觸核蛋白軸調控PD的發展。本研究應用濃度為100 μmol/L的MPP+處理N2a細胞構建PD細胞模型,并檢測了CDR1as在不同時間點的變化,結果顯示,N2a細胞經過MPP+處理3、6、9和12 h后CDR1as表達顯著降低,提示CDR1as基因可能間接參與了PD的發病。
有研究顯示,在CDR1as基因敲除小鼠大腦中,miR-7的表達減少而不是增加,這表明還有其他機制參與了miR-7表達的調節[29]。采用CLIP-Seq技術對miR-7-target RNA-Ago2嵌合體中的靶序列進行分析和排序發現,無論是在人類還是小鼠大腦中,排在第1位的都是CDR1as基因,排在第2位的是長鏈非編碼RNA Cyrano,提示Cyrano在中樞神經系統中對miR-7具有重要的調控作用[29]。Cyrano高表達于腦神經元的胞體和突起,含有1個與miR-7幾乎完全配對(除第9/10位外)的結合位點,且該位點高度保守[37]。然而,Cyrano是否通過miR-7在PD發病中發揮作用還需進一步探究。
研究表明,在人類和小鼠腦中,CDR1as基因也存在miR-671的結合位點,miR-671可以近乎完全與CDR1as基因互補配對,隨后與Ago2蛋白結合,最終實現對CDR1as基因的有效降解,且此相互作用在物種間高度保守,提示這種特異性的相互作用可能具有重要生物學功能[29,38]。本研究中,N2a細胞經過MPP+處理3、6、9和12 h后CDR1as基因表達顯著降低,這一現象是否與miR-671有關還需進一步研究。
綜上所述,N2a細胞經過MPP+處理3、6、9和12 h后CDR1as基因表達水平顯著降低,本文結果為研究CDR1as基因在PD發病中的作用提供了實驗依據。
[參考文獻]
[1]PRINGSHEIM T, JETTE N, FROLKIS A, et al. The prevalence of Parkinsons disease: a systematic review and meta-analysis[J].? Movement Disorders, 2014,29(13):1583-1590.
[2]QI S G, YIN P, WANG L H, et al. Prevalence of Parkin-sons disease: a community-based study in China[J].? Movement Disorders: Official Journal of the Movement Disorder Society, 2021,36(12):2940-2944.
[3]YUAN X, TIAN Y, LIU C Y, et al. Environmental factors in Parkinsons disease: new insights into the molecular mechanisms[J].? Toxicology Letters, 2022,356:1-10.
[4]ROCCA W A. The burden of Parkinsons disease: a worldwide perspective[J].? The Lancet Neurology, 2018,17(11):928-929.
[5]MARRAS C, BECK J C, BOWER J H, et al. Prevalence of Parkin-sons disease across North America[J].? Npj Parkinsons Disease, 2018,4:21.
[6]JANKOVIC J, TAN E K. Parkinsons disease: etiopathoge-nesis and treatment[J].? Journal of Neurology, Neurosurgery, and Psychiatry, 2020,91(8):795-808.
[7]VEYS L, VANDENABEELE M, ORTUO-LIZARN I, et al. Retinal α-synuclein deposits in Parkinsons disease patients and animal models[J].? Acta Neuropathologica, 2019,137(3):379-395.
[8]SUNG V W, NICHOLAS A P. Nonmotor symptoms in Parkinsons disease: expanding the view of Parkinsons disease beyond a pure motor, pure dopaminergic problem[J].? Neurologic Clinics, 2013,31(3 Suppl):S1-S16.
[9]DICKSON D W. Neuropathology of parkinson disease[J].? Parkinsonism & Related Disorders, 2018,46:S30-S33.
[10]DEL TREDICI K, BRAAK H. Review: sporadic Parkinsons disease: development and distribution of α-synuclein pathology[J].? Neuropathology and Applied Neurobiology, 2016,42(1):33-50.
[11]DECRESSAC M, MATTSSON B, LUNDBLAD M, et al. Progressive neurodegenerative and behavioural changes induced by AAV-mediated overexpression of α-synuclein in midbrain dopamine neurons[J].? Neurobiology of Disease, 2012,45(3):939-953.
[12]JUNN E, MOURADIAN M M. Human alpha-synuclein over-expression increases intracellular reactive oxygen species levels and susceptibility to dopamine[J].? Neuroscience Letters, 2002,320(3):146-150.
[13]MASLIAH E, ROCKENSTEIN E, VEINBERGS I, et al. Dopaminergic loss and inclusion body formation in alpha-synu-
clein mice: implications for neurodegenerative disorders[J].? Science (New York, N Y), 2000,287(5456):1265-1269.
[14]VO J N, CIESLIK M, ZHANG Y J, et al. The landscape ofcircular RNA in cancer[J].? Cell, 2019,176(4):869-881.e13.
[15]LI J W, SHI Q Q, WANG Q, et al. Profiling circular RNA in methamphetamine-treated primary cortical neurons identified novel circRNAs related to methamphetamine addiction[J].? Neuroscience Letters, 2019,701:146-153.
[16]CHEN S J, HUANG V, XU X, et al. Widespread and functional RNA circularization in localized prostate cancer[J].? Cell, 2019,176(4):831-843.e22.
[17]VEN? M T, HANSEN T B, VEN? S T, et al. Spatio-temporal regulation of circular RNA expression during porcine embryonic brain development[J].? Genome Biology, 2015,16:245.
[18]RYBAK-WOLF A, STOTTMEISTER C, GLAZAR P, et al. Circular RNAs in the mammalian brain are highly abundant, conserved, and dynamically expressed[J].? Molecular Cell, 2015,58(5):870-885.
[19]SALZMAN J, CHEN R E, OLSEN M N, et al. Cell-type specific features of circular RNA expression[J].? PLoS Genetics, 2013,9(9):e1003777.
[20]JECK W R, SORRENTINO J A, WANG K, et al. Circular RNAs are abundant, conserved, and associated with ALU repeats[J].? RNA (New York, N Y), 2013,19(2):141-157.
[21]MEMCZAK S, JENS M, ELEFSINIOTI A, et al. Circular RNAs are a large class of animal RNAs with regulatory potency[J].? Nature, 2013,495(7441):333-338.
[22]HANSEN T B, JENSEN T I, CLAUSEN B H, et al. Natural RNA circles function as efficient microRNA sponges[J].? Nature, 2013,495(7441):384-388.
[23]ROCHA E M, DE MIRANDA B, SANDERS L H. Alpha-synuclein: pathology, mitochondrial dysfunction and neuro-inflammation in Parkinsons disease[J].? Neurobiology ofDisease, 2018,109:249-257.
[24]SINGLETON A B, FARRER M, JOHNSON J, et al. Alpha-Synuclein locus triplication causes Parkinsons disease[J].? Science (New York, N Y), 2003,302(5646):841.
[25]DOXAKIS E. Post-transcriptional regulation of alpha-synu-clein expression by mir-7 and mir-153[J].? The Journal of Biological Chemistry, 2010,285(17):12726-12734.
[26]JUNN E, LEE K W, JEONG B S, et al. Repression of alpha-synuclein expression and toxicity by microRNA-7[J].? Procee-dings of the National Academy of Sciences of the United States of America, 2009,106(31):13052-13057.
[27]OKEEFFE G W, SULLIVAN A M. Evidence for dopaminergic axonal degeneration as an early pathological process in Parkinsons disease[J].? Parkinsonism & Related Disorders, 2018,56:9-15.
[28]NUTT J G. Motor fluctuations and dyskinesia in Parkinsons disease[J].? Parkinsonism & Related Disorders, 2001,8(2):101-108.
[29]PIWECKA M, GLAZAR P, HERNANDEZ-MIRANDA L R, et al. Loss of a mammalian circular RNA locus causes miRNA deregulation and affects brain function[J].? Science (New York, N Y), 2017,357(6357):eaam8526.
[30]BAK M, SILAHTAROGLU A, M?LLER M, et al. micro-RNA expression in the adult mouse central nervous system[J].? RNA (New York, N Y), 2008,14(3):432-444.
[31]MCMILLAN K J, MURRAY T K, BENGOA-VERGNIORY N, et al. Loss of microRNA-7 regulation leads to α-synuclein accumulation and dopaminergic neuronal loss in vivo[J].? Molecular Therapy: the Journal of the American Society of Gene Therapy, 2017,25(10):2404-2414.
[32]ZHAO J J, ZHOU Y, GUO M M, et al. microRNA-7: expression and function in brain physiological and pathological processes[J].? Cell & Bioscience, 2020,10:77.
[33]ZHOU Y, LU M, DU R H, et al. microRNA-7 targets Nod-like receptor protein 3 inflammasome to modulate neuroinflammation in the pathogenesis of Parkinsons disease[J].? Molecular Neurodegeneration, 2016,11:28.
[34]CHOI D C, CHAE Y J, KABARIA S, et al. microRNA-7 protects against 1-methyl-4-phenylpyridinium-induced cell death by targeting RelA[J].? The Journal of Neuroscience: the Official Journal of the Society for Neuroscience, 2014,34(38):12725-12737.
[35]KONG B, WU P C, CHEN L, et al. microRNA-7 protects against 1-methyl-4-phenylpyridinium iodide-induced cell apoptosis in SH-SY5Y cells by directly targeting Krüpple-like factor 4[J].? DNA and Cell Biology, 2016,35(5):217-225.
[36]LI S Z, LV X C, ZHAI K H, et al. microRNA-7 inhibits neuronal apoptosis in a cellular Parkinsons disease model by targeting Bax and Sirt2[J].? American Journal of Translational Research, 2016,8(2):993-1004.
[37]ULITSKY I, SHKUMATAVA A, JAN C H, et al. Conserved function of lincRNAs in vertebrate embryonic development despite rapid sequence evolution[J].? Cell, 2011,147(7):1537-1550.
[38]HANSEN T B, WIKLUND E D, BRAMSEN J B, et al. miRNA-dependent gene silencing involving Ago2-mediated cleavage of a circular antisense RNA[J].? The EMBO Journal, 2011,30(21):4414-4422.
(本文編輯馬偉平)

