秋水仙堿與克拉霉素相互作用致不良反應20例文獻分析*
朱玲娜,程軍,汪龍
(安徽省蚌埠市第三人民醫院藥學部,蚌埠 233099)
秋水仙堿是一種從秋番紅花中提取的生物堿,根據歷史記載,4000年前就作為痛風的一種特殊治療藥物[1]。現今,秋水仙堿在痛風和家族性地中海熱(familial mediterranean fever,FMF)中已被廣泛使用[2]。除此之外,它也用于治療其他疾病,如白塞病(behcet disease,BD)、心包炎、冠狀動脈疾病以及纖維化疾病等[3]。秋水仙堿是一種CYP3A4和(或)P-糖蛋白的底物,當與CYP3A4和(或)P-糖蛋白抑制劑聯合使用時,會延遲血液中秋水仙堿的排泄,從而增加秋水仙堿的潛在毒性[4]。據報道[5],同時使用強CYP3A4和P-糖蛋白抑制劑(如克拉霉素、伊曲康唑、酮康唑和一些蛋白酶抑制劑)會造成嚴重后果。近年來,國外陸續有秋水仙堿與其他藥物相互作用致不良反應(adverse drug reaction,ADRs)報道,且發現許多病例報道涉及克拉霉素[6-8],克拉霉素是一種用于治療呼吸道感染、幽門螺桿菌(HelicobacterPylori,Hp)感染和分枝桿菌感染等的抗菌藥物。筆者在本研究以秋水仙堿與克拉霉素相互作用致ADRs的個案報道為基礎,分析其發生特點,為臨床安全用藥提供參考。
1 資料與方法
1.1資料來源 以“秋水仙堿”“克拉霉素”及“藥物相互作用”為中文關鍵詞,檢索中國知網(CNKI)、維普數據庫(VIP)和萬方數據庫;以“colchicine”“ clarithromycin”和“drug interaction”為英文關鍵詞檢索PubMed、Medline、Elsevier數據庫,時間為2005年1月—2021 年2月,檢索發表的秋水仙堿與克拉霉素相互作用致ADRs的個案報道。
納入標準:國內外公開發表的個案報道;文獻記載相關信息完整;明確病例發生ADRs與秋水仙堿和克拉霉素聯合使用相關。
1.2方法 詳細閱讀納入文獻,提取患者的性別、年齡、使用秋水仙堿和克拉霉素的相關診斷以及使用劑量、藥物聯合使用后出現癥狀的時間、臨床表現、腎功能不全史、肌酸激酶(creatine kinase,CK)值、治療、轉歸以及藥物相互作用概率量表評定結果等有效信息,應用Excel軟件進行統計分析。
2 結果
2.1一般情況 檢索到符合納入標準的文獻12 篇,全部為國外病例報道,共20例患者。其中,男11例,女9例;年齡23~78歲,平均(54.9±16.0)歲。使用秋水仙堿的相關診斷包括:FMF 12例,痛風 6例,高尿酸血癥(hyperuricemia,HUA)1例,BD 1例;使用克拉霉素的相關診斷包括:Hp感染 9例,社區獲得性肺炎(community acquired pneumonia,CAP)5例,急性上呼吸道感染(acute upper respiratory infection,AURI)2例,慢性鼻竇炎(chronic nasosinusitis,CN) 2例,牙周炎(periodontal disease,PD)1例,睪丸炎(orchitis,OCS)1例。秋水仙堿使用劑量0.5~4 mg·d-1,克拉霉素的使用劑量為0.5~1.0 g·d-1。具體見表1。
2.2藥物聯合使用后發生ADRs的時間及臨床表現 病例中藥物聯合使用后發生ADRs時間為1 ~14 d,其中1~7 d有13例(65.0%),8~14 d有3例(15.0%),另有4例信息不詳。20例病例報道對秋水仙堿和克拉霉素聯合使用致ADRs的臨床表現均作了描述,主要為腹痛、腹瀉、嘔吐、肌痛和肌無力等,少數表現為發熱、全血細胞減少及多臟器功能衰竭等。具體見表1。
2.3腎功能不全史及CK值情況 10例患者腎功能正常,8例患者有腎功能不全史,2例不詳。CK值有13例均表現為不同程度的升高,其中最高值達31 000 U·L-1,7例不詳。具體見表1。
2.4治療、轉歸結果 患者出現ADRs后,均暫停使用秋水仙堿和克拉霉素,多數患者接受水化、補充電解質治療,部分患者接受廣譜抗菌藥物、粒細胞集落刺激因子等治療,并有少數患者在以上治療的基礎上增加物理療法。20例患者經治療后,12例患者癥狀消退,4例死亡,4例不詳。具體見表1。
3 討論
目前,秋水仙堿被批準用于治療FMF和痛風等疾病。克拉霉素是一種CYP3A4和P-糖蛋白的強抑制劑,可顯著延長秋水仙堿的半衰期,當2種藥物聯用時,會增加嚴重ADRs的發生風險。本研究調查結果顯示,秋水仙堿與克拉霉素相互作用致ADRs的公開發表的個案病例報道有20例,國內尚未見報道。ADRs患者中,男性占55%,性別差異不明顯。以>50歲患者居多,VILLA等[19]通過檢索美國FDA不良事件報告系統(FAERS)數據庫發現,因秋水仙堿和克拉霉素聯用而發生ADRs的患者,53%在65~85歲,提示老年患者可能有更高的發生風險。
本調查收集的20例秋水仙堿和克拉霉素相互作用致ADRs的病例報告中,秋水仙堿的平均劑量為1.4 mg·d-1(0.5~4.0 mg·d-1),其中有7例 ≤1.0 mg·d-1。因此,正常劑量的秋水仙堿也可能與克拉霉素發生相互作用并致嚴重的ADRs。另外,OZEN等[2]提示,FMF患者在接受更高劑量的秋水仙堿后,可能會有更大的中毒風險。一份已發表的長期小劑量克拉霉素(0.2 g·d-1)治療腸道BD的病例報告顯示[20],小劑量克拉霉素和秋水仙堿聯合使用并未引起ADRs。因此,小劑量克拉霉素可能對秋水仙堿的代謝及排泄影響較小。20例病例報告中,有15例患者克拉霉素使用劑量為1.0 g·d-1,該劑量是否會影響秋水仙堿的代謝及排泄,筆者尚未見相關報道研究。因此,克拉霉素的使用劑量與ADRs的發生關系尚不清楚。
一項關于秋水仙堿和克拉霉素在腎功能不全患者中相互作用的回顧性研究結果顯示[21],腎功能不全可能會增加這2種藥物相互作用發生致死性ADRs的風險。本調查的20例病例報告顯示,4例死亡患者中,有2例存在腎功能不全。但目前尚不清楚腎功能損害程度對這種相互作用的影響。一項針對腎小球濾過率與秋水仙堿血藥濃度關系的小樣本的研究提示[22],相較于腎功能正常的患者,腎小球濾過率較低患者秋水仙堿藥物濃度-時間曲線下面積(AUC)會增加。因此,腎功能不全可能會增加秋水仙堿和克拉霉素相互作用發生ADRs的風險,臨床使用應予以關注。
HUNG等[21]開展的一項回顧性病例對照研究提示,88例聯用秋水仙堿和克拉霉素治療的腎功能不全患者中,嚴重ADRs的致死率為10%。其中在聯用藥物1~2 d患者中,致死率為3%;在聯用藥物>2 d的患者中,致死率達18%。本調查的20例病例中,65%的ADRs發生在藥物聯合使用后7 d內;4例(20.0%)患者死亡,均發生在2種藥物聯用后的2 周內。本調查與上述研究均提示,秋水仙堿和克拉霉素相互作用致ADRs潛伏時間較短,且死亡率較高,醫務人員務必重視。
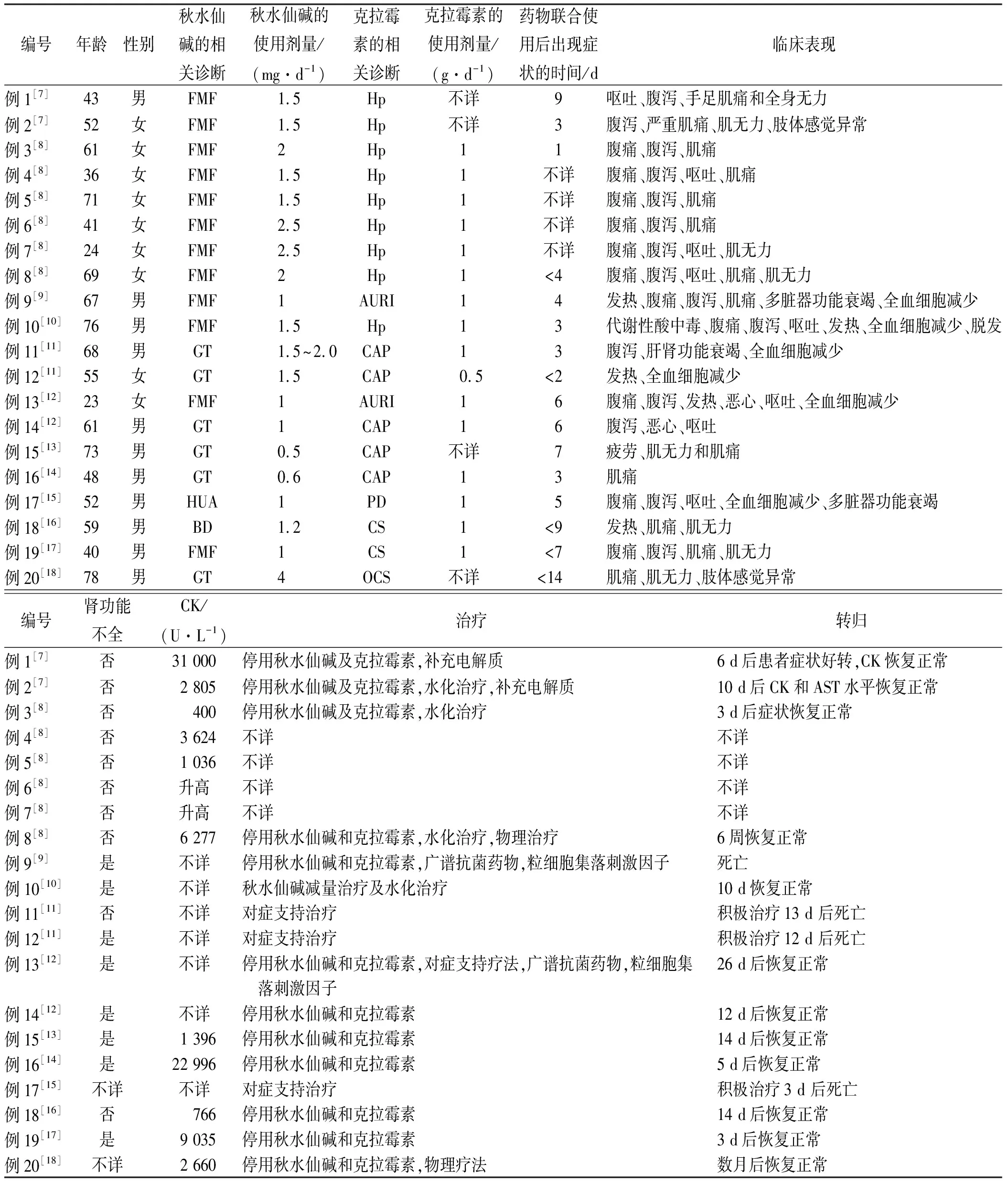
表1 秋水仙堿與克拉霉素相互作用致不良反應
秋水仙堿與克拉霉素相互作用致ADRs的機制尚不完全清楚,可能與秋水仙堿和克拉霉素聯合使用導致血清和組織中秋水仙堿濃度升高有關。關于秋水仙堿的代謝和沉積已被廣泛研究[23-25],秋水仙堿在小腸被吸收后,經歷大量的系統前代謝,導致生物利用度僅為25%~50%。30%被吸收的秋水仙堿被分配到胃腸道、肌肉、心臟、脾臟和白細胞[26]。秋水仙堿在白細胞中濃度很高,藥物過量可能導致嚴重骨髓抑制的發生。20%的秋水仙堿以藥物原型從尿中排泄,而其余50%則主要通過肝臟的CYP3A4代謝(去乙酰化、去甲基化和葡萄糖醛酸化等)[27]。克拉霉素能夠通過抑制腸上皮P-糖蛋白而增加秋水仙堿的吸收和系統前代謝,進而提高其口服給藥的生物利用度。此外,克拉霉素還可以通過干擾P-糖蛋白而影響秋水仙堿的肝代謝和腎排泄。TERKELTAUB等[28]研究表明,克拉霉素能夠使秋水仙堿的血藥濃度提高230%,使其半衰期從9 h延長至30 h。
秋水仙堿與克拉霉素相互作用引起的ADRs通常可分為3個連續階段。第一階段發生在24 h內,主要以胃腸道癥狀為主。第二階段發生在24 h后,癥狀涉及多器官功能衰竭,伴有以下癥狀的患者死亡的風險更高:骨髓增生異常(例如全血細胞減少)引起的骨髓抑制;腎功能不全;心律失常;彌散性血管內凝血以及神經肌肉疾病。如果患者在第二階段幸存下來,最后階段,即恢復期,則以血惡液質和脫發為特征[29]。在秋水仙堿與克拉霉素致ADRs治療方面,建議首先暫停使用這2種藥物,采用對癥支持治療為主。對于存在嚴重白細胞減少患者給予每日皮下注射粒細胞集落刺激因子。也有關于使用秋水仙素特異性Fab片段治療嚴重秋水仙堿中毒的報道,但這些抗體并不容易獲得[30]。此外,可以輔助給予物理和康復治療。
綜上所述,克拉霉素和秋水仙堿相互作用可能引起致命的后果,與秋水仙堿的使用劑量、2種藥物聯用持續時間、腎功能不全等因素相關。由于秋水仙堿的替代品很少,并考慮到克拉霉素的使用常與感染性急癥有關,因此,建議在服用克拉霉素時,暫停使用秋水仙堿。臨床醫生也可以考慮更換克拉霉素為其他抗菌藥物,但不推薦更換為紅霉素。因紅霉素也可引起嚴重的秋水仙堿中毒[31]。阿奇霉素不抑制CYP3A4,一項針對21例聯用秋水仙堿和阿奇霉素的藥動學研究表明[28],阿奇霉素僅可導致秋水仙堿AUC小幅度升高(57%)。因此,在接受秋水仙堿治療的患者中,阿奇霉素可能比克拉霉素更安全。

