蔗汁中淀粉含量快速檢測方法應用研究
張家智,溫惠宇,勞權惠,楊 釗1,,3,于福才*,蒙 軍,董榮富,3,王 寶
(1中糧營養健康研究院有限公司/老年營養食品研究北京市工程實驗室/營養健康與食品安全北京市重點實驗室,北京 102209;2中糧崇左糖業有限公司/廣西壯族自治區甘蔗產業鏈延伸工程研究中心,廣西崇左 532200;3中糧糖業控股股份有限公司/農業部糖料與番茄質量安全控制重點實驗室/國家糖料加工技術研發專業中心/中糧糖業控股股份有限公司博士后科研工作站,新疆昌吉 831100)
0 前言
在制糖生產過程中,蔗汁中非糖成分對其澄清工藝指標的確定具有很大影響[1]。其中,甘蔗中淀粉顆粒受壓榨滲透熱水作用分散于蔗汁,經受熱糊化溶解為可溶性黏稠糊狀物,并難以凝聚或沉淀,進而增加蔗汁黏度、降低沉降效率,增大糖膏黏度、阻礙蔗糖結晶,明顯提高澄清環節過濾難度,嚴重影響煮糖環節成糖品質與糖蜜提取率[1-2]。若成品糖中淀粉含量過高,會出現白砂糖混濁、酸性絮凝物偏高等問題,影響成品質量[2-3]。有研究報告指出,原糖中淀粉含量高是煉糖廠精制澄清階段過濾性能低下的主要因素[4-5],且碳酸法澄清工藝比亞硫酸法具有更佳的清凈效果[5-6]。所以測定中間蔗汁中淀粉含量對于監控白砂糖質量與提升澄清過濾性能具有重要意義。
目前蔗汁中淀粉含量的常用測定方法為酶解法和碘顯色法。酶解法通過淀粉酶和鹽酸將淀粉逐步分解為葡萄糖,通過測定其中還原糖含量以換算淀粉含量,但是反應慢、歷時長、重現性差[7];碘顯色法利用淀粉與碘間的顯色反應通過比色分析來測定淀粉含量,可用酒精將淀粉沉淀后離心分離,或將蔗汁煮沸過濾后直接測定,但是誤差較大,結果可信度低[8-10]。陳駿佳[11]等結合酶解法與碘顯色法各自優點建立了一種蔗汁與糖漿中淀粉含量測定新方法,但由于國內現有糖漿淀粉含量的分析數據較少,其中多選擇白砂糖進行測定,而少有針對中間蔗汁與糖漿開展,對實際生產指導意義有限[4-7,10-12]。故本實驗在此基礎上選取崇左某糖廠原糖生產過程中的初壓汁、末壓汁、混合汁與澄清汁作為研究對象,進一步對中間蔗汁淀粉含量快速測定方法展開研究。
1 試驗與方法
1.1 試驗設計原理
將蔗汁煮沸以液化淀粉顆粒,添加適量醋酸鉛以澄清除雜,靜置一段時間后經壓濾得到蔗汁清液;而后取定量清液加入過量淀粉酶,將其中淀粉完全分解后再升溫使酶失活,從而得到無淀粉的蔗汁清液。以無淀粉蔗汁清液為空白對照,利用碘顯色法測量其中淀粉含量。
1.2 主要儀器與試劑
60目標準篩;數顯恒溫水浴鍋,江蘇科析儀器有限公司;ZD-5L型正壓過濾器,海寧市正大過濾設備有限公司;微孔過濾膜(孔徑為0.45 μm),海寧市正大過濾設備有限公司;手動微量移液器,艾本德(上海)國際貿易有限公司;721-100型可見分光光度計,上海菁華科技儀器有限公司。
堿式醋酸鉛(糖用),高溫淀粉酶2.0P(液)(無錫怡竹生物科技有限公司,8萬u/g),1 mol/L鹽酸,稀碘液(15 mmol/L KI,5 mmol/L I2)。
淀粉標準溶液:稱取約1.50 g可溶性淀粉并平鋪于直徑為10 cm的稱量皿中,在120℃的烘箱中烘干約2 h,取出后放入干燥器冷卻至室溫,準確稱取0.25 g烘干淀粉于150 mL燒杯內,用少量水調和后緩慢倒入約l00 mL的沸水中,煮至透明后繼續煮沸l0 min,冷卻至室溫后加水定容至500 mL,制得500 mg/L的淀粉標準溶液,即配即用。
1.3 實驗方法
1.3.1 經澄清除雜制備蔗汁清液
經60目標準篩過濾后取500 mL中間蔗汁加入到1000 mL燒杯中,加熱煮沸15 min,煮沸過程中適當加水補足。加入適量醋酸鉛后攪拌,靜置待絮凝物沉淀完全,取上層清液,經孔徑為0.45 μm的微孔過濾膜趁熱壓濾后,得到不少于150 mL的澄清濾液備用。
1.3.2 酶解法制備空白蔗汁清液
量取100 mL蔗汁清液于150 mL燒杯中,加入50 μL高溫淀粉酶,在70~80℃下反應30 min以上,以確保淀粉酶能完全去除清液中原有的淀粉,再立即煮沸20 min使淀粉酶失活,煮沸過程小火加熱,并補水至100 mL,取出后冷卻至室溫。
1.3.3 碘顯色法確定淀粉在蔗汁清液中的反應曲線
采用不同規格的微量移液槍于7個10 mL比色管中各加入1 mL無淀粉蔗汁清液及1 mL 1 mol/L鹽酸;依次加入500 mg/L可溶性淀粉標準溶液0、50、100、200、300、400、500 μL,加入5 mL稀碘液后加水補足至10 mL定容;搖勻并放置5 min備用。上述各比色管中蔗汁淀粉濃度分別為0、25、50、100、150、200、250 mg/L。以空白對照組調零,于580 nm波長下測定蔗汁吸光度,并以吸光度為橫坐標,相應淀粉含量為縱坐標作圖,繪制蔗汁中淀粉含量的標準工作曲線并建立回歸方程。
1.3.4 樣品淀粉含量測定
于1個10 mL比色管中加入1 mL蔗汁清液,依次加入1 mL稀鹽酸、3 mL蒸餾水、5 mL稀碘液,充分搖勻并放置5 min。以空白對照組調零測定蔗汁樣液吸光度,再由標準工作曲線計算其淀粉含量。
2 結果與討論
2.1 方法可行性分析
根據相關文獻報道,蔗汁中淀粉與碘作用生成的絡合物顯青藍色,并在560~600 nm處出現吸收波峰,且在580 nm處有最大吸收,故以蔗汁清液為空白對照于室溫下直接測定淀粉理論可行[4]。同時,已知樣品濁度與色值均對其吸光度測定有所影響,醋酸鉛作為澄清劑,一方面不與糊化淀粉反應,對測量結果無影響,另一方面可去除蔗汁中的非糖分與雜質,有利于后續吸光度測量。同時以無淀粉的蔗汁清液作為空白對照組,也能排除蔗汁中色素等干擾物質的影響,取得準確可靠的測定結果。
2.2 不同醋酸鉛添加量對蔗汁清液濁度及其標準工作曲線測定的影響
隨著澄清處理過程中醋酸鉛添加量逐漸增加,中間蔗汁經壓濾后其相應清液濁度的變化趨勢各不相同,如圖1所示。其中,初壓汁、末壓汁與混合汁相對應的蔗汁清液濁度均呈先降低后增加的趨勢,其中末壓汁受醋酸鉛添加量影響程度大于初壓汁和混合汁,且需要更多量醋酸鉛才能達到較好的澄清效果;清汁因其自身濁度較低,添加醋酸鉛后反而因返濁造成其清液濁度上升。
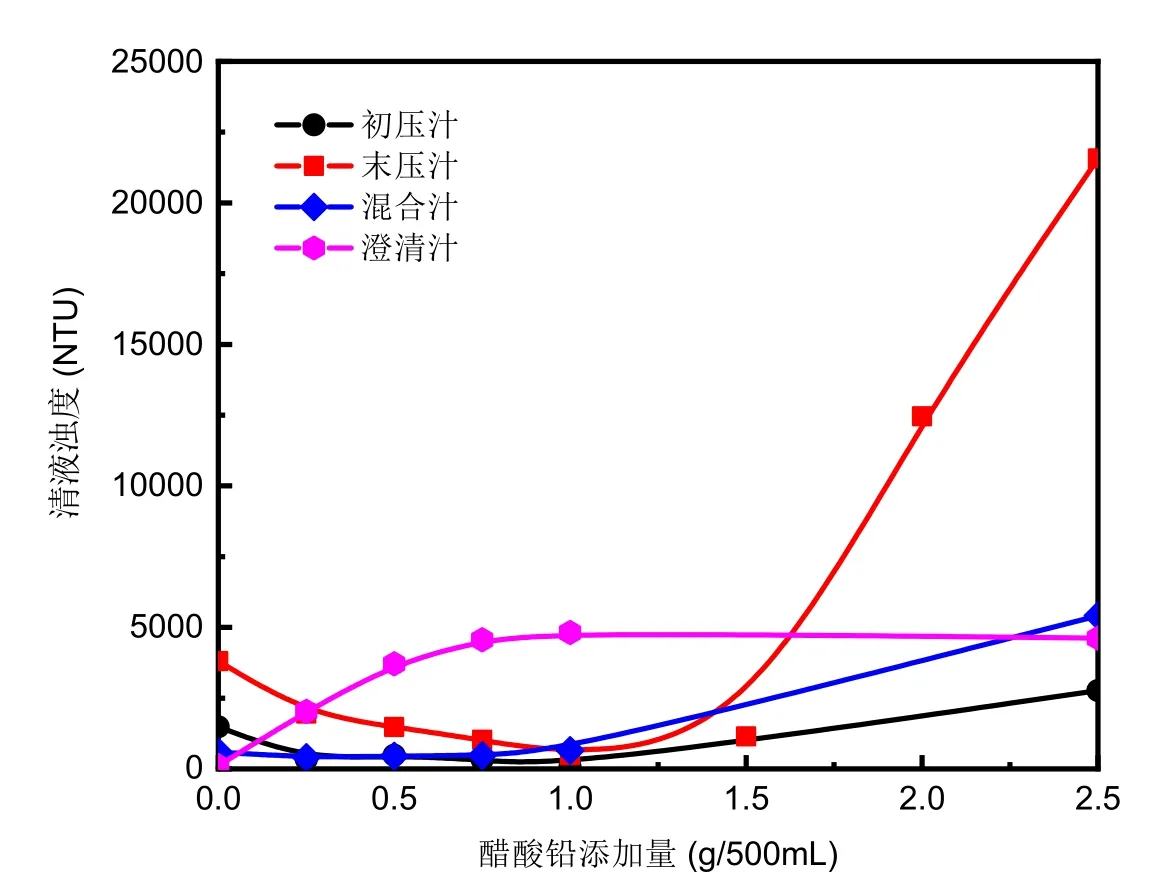
圖1 不同醋酸鉛添加量下中間蔗汁清液濁度變化曲線
以500 mL混合汁為例,不同醋酸鉛添加量所得到的標準工作曲線有著如圖2所示的變化趨勢,結合其清液濁度變化趨勢來看,當醋酸鉛添加量為0.0和2.5 g時其濁度較大,分別對應591和5412 NTU,其標準工作曲線斜率分別為590.83和578.53,而當醋酸鉛添加量為0.25和0.75 g時其濁度較小,分別為402和472 NTU,其標準工作曲線斜率均在560上下,較為穩定。這一方面是少量的醋酸鉛所起到的澄清作用有限,另一方面是過量的醋酸鉛殘留于蔗汁清液內會造成一定程度的返濁,同時也可能會對淀粉酶活性造成影響。
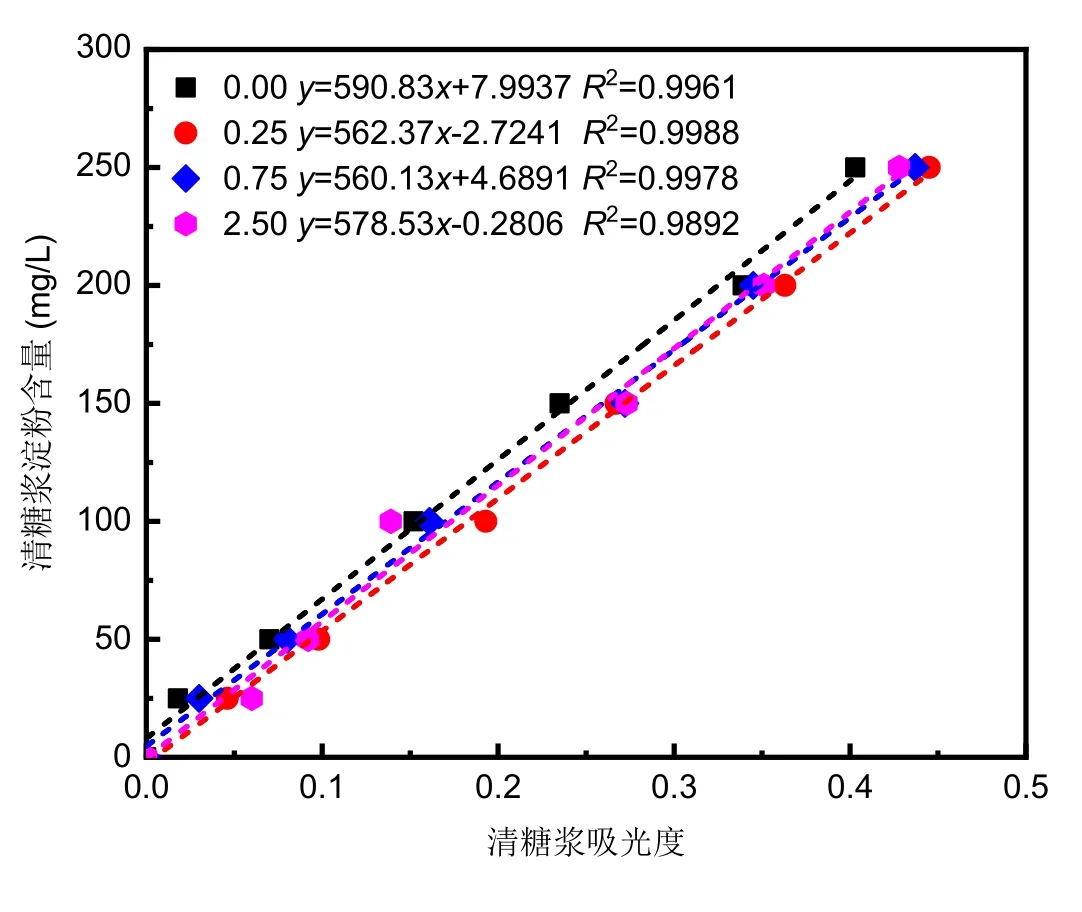
圖2 不同醋酸鉛添加量下混合汁淀粉含量測定標準工作曲線
綜上所述,選擇適宜的醋酸鉛添加量至關重要,需確保經過煮沸澄清過濾后的蔗汁清液能夠達到較好的澄清度,也需保證經過淀粉酶降解淀粉后能夠獲得穩定有效的空白對照組。在本次研究中,針對多批次中間蔗汁樣品進行試驗得到,當醋酸鉛添加量分別為0.25 g(初壓汁)、1.0 g(末壓汁)、0.25 g(混合汁)和0.0 g(清汁)時,其蔗汁清液的濁度均低于500 NTU,并且醋酸鉛添加量需隨著甘蔗原料的改變而重新測定調整,從整體上看均在0.25 g/500 mL左右。
2.3 中間蔗汁淀粉含量測定對應的標準工作曲線結果與分析
將4種中間蔗汁所對應的標準工作曲線繪制如圖3所示后發現,其標準曲線整體上均處于相近狀態,斜率均在565上下,擬合相關系數R2均在0.99以上。通過添加醋酸鉛可控制蔗汁清液濁度在相近且較低水平,從而標準工作曲線斜率也具有相近性或統一性。
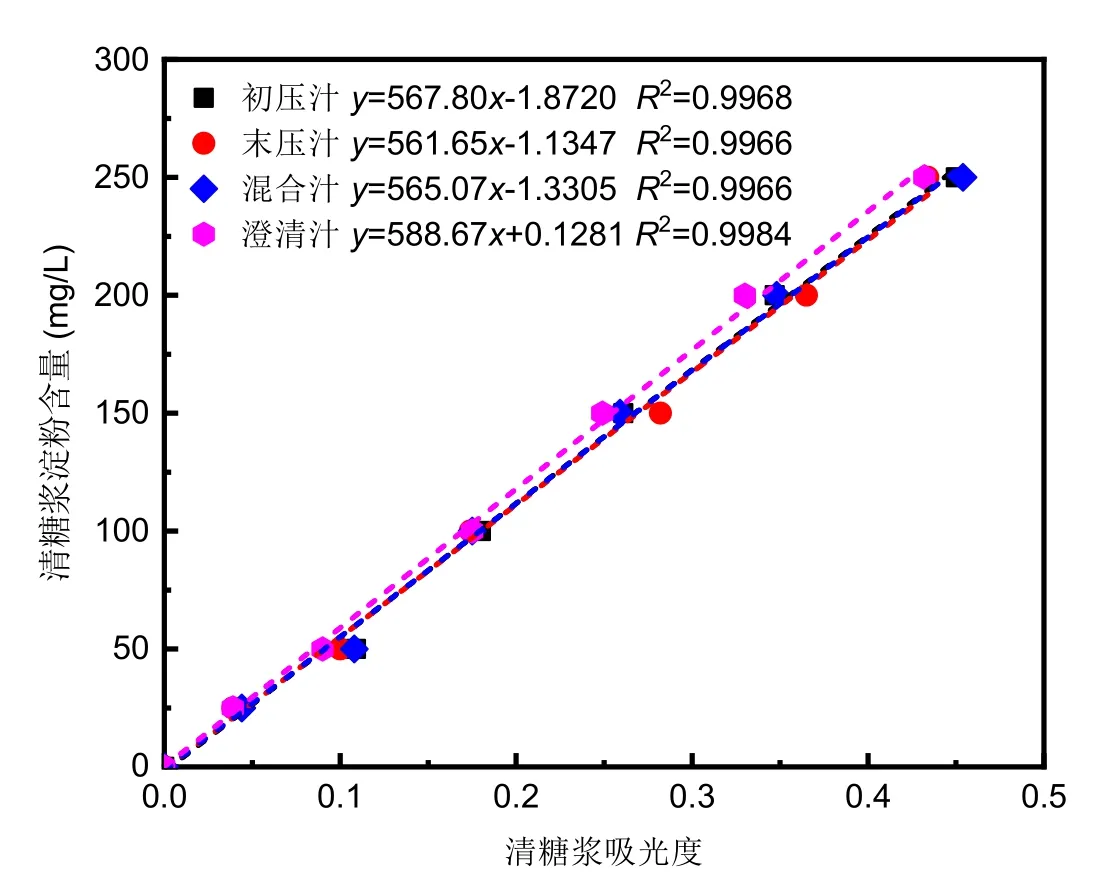
圖3 中間蔗汁的淀粉含量測定標準工作曲線匯總圖
針對混合汁平行測定3次所得標準工作曲線的 斜率分別為565.07、566.23、562.37,其標準差為1.62%,表明此方法精度較高,重現性較好,符合分析要求。
2.4 中間蔗汁淀粉含量測定加標測試結果與分析
針對混合汁測得的淀粉含量及其標準工作曲線進行加標測試,即在檢測得到混合汁淀粉含量后,人為定量添加淀粉后再進行淀粉含量檢測,如表1所示。結果顯示,加標測試回收率在99%~102%之間,表明該方法檢測結果較為準確,其標準工作曲線均穩定可靠。
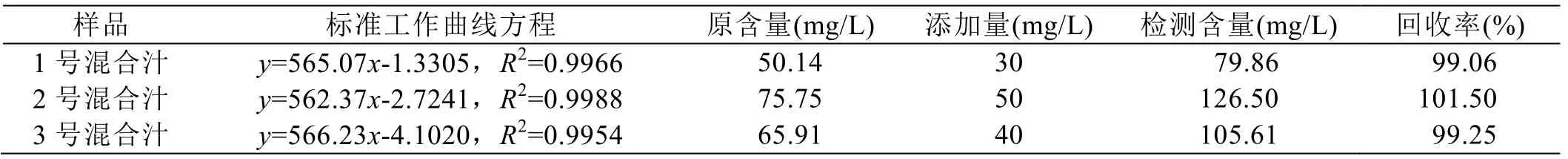
表1 混合汁淀粉含量檢測加標測試回收率
3 總結
本方法基于酶解法和碘顯色法采用醋酸鉛進行澄清除雜,方法可行,加快測定分析速度。實驗表明:當醋酸鉛添加量約為0.50 g/L時,即可將中間蔗汁澄清處理到較低濁度,且不同工段處的中間蔗汁均具有相近的標準工作曲線。這為制糖廠中間蔗汁的淀粉含量實時監測提供了一個快速簡便的方法。

