高溫脅迫下蘿卜苗期的轉錄組分析
周娜 鄭陽 陸景偉 胡燕 陶偉林 雷開榮 潘曉雪


摘要:【目的】對高溫脅迫下蘿卜幼苗進行轉錄組測序分析,篩選不同耐熱性蘿卜品種間的差異表達基因,為闡明蘿卜幼苗響應高溫脅迫的分子機制提供理論參考。【方法】以耐熱蘿卜品種1116T和熱敏感蘿卜品種Wr129為對象,對其進行高溫(40 ℃)脅迫處理0(常溫,對照)和24 h,提取各時間點樣品總RNA進行轉錄組測序,以|log2Fold Change|≥1,P<0.05且TPM≥10為標準,篩選出差異表達基因(DEGs),并進行GO功能注釋和KEGG代謝通路富集分析。【結果】隨著高溫脅迫時間的增加,Wr129和1116T幼苗莖葉逐漸發生萎蔫,脅迫24 h后Wr129葉片萎蔫下垂且干枯變黃,而1116T葉片輕度萎蔫下垂,仍保持綠色。12個文庫共獲得81.45 Gb Clean data,平均有62.30%的reads比對到蘿卜參考基因組的一個位置。從2個不同耐熱性品種中共鑒定到2701個差異表達基因。GO功能注釋結果顯示,2629個差異表達基因在GO數據庫中得到注釋,其中,有559個差異表達基因被注釋為細胞組分類別中的葉綠體被膜、葉綠體基質和葉綠體類囊體3個條目,470個差異表達基因被注釋為與脅迫響應相關的生物學過程。KEGG代謝通路富集結果顯示,1166個差異表達基因富集到124條代謝通路,其中,有74個差異表達基因富集到光合作用和光合作用-天線蛋白代謝通路,23個基因富集到卟啉和葉綠素代謝通路,大部分基因在高溫脅迫下被誘導;35個差異表達基因富集到谷胱甘肽代謝途徑,其中14個谷胱甘肽-S-轉移酶基因(GSTs)在高溫脅迫下上調表達。高溫脅迫24 h,Wr129和1116T幼苗葉片PSII的最大光化學效率(Fv/Fm)和總葉綠素含量均下降,但1116T的下降幅度較小。【結論】Wr129和1116T的耐熱性存在明顯差異,其原因是1116T植株可通過調控光合作用和抗氧化系統相關基因的表達,減緩Fv/Fm和葉綠素含量下降速率,從而提高植株對高溫脅迫的耐受能力。
關鍵詞: 蘿卜;高溫脅迫;轉錄組;耐熱性;光合作用;谷胱甘肽代謝
中圖分類號: S631.103.6? ? ? ? ? ? ? ? ? ? ? ? ? ? ? 文獻標志碼: A 文章編號:2095-1191(2022)03-0665-11
Transcriptome analysis of Raphanus sativus seedlings in response to high temperature stress
ZHOU Na ZHENG Yang LU Jing-wei HU Yan TAO Wei-lin LEI Kai-rong PAN Xiao-xue
(1Vegetable and Flower Research Institute,Chongqing Academy of Agricultural Sciences,Chongqing? 401329, China;
2Biotechnology Research Institute, Chongqing Academy of Agricultural Sciences/Municipal-level Key
Laboratory of Adversity Agriculture in Chongqing, Chongqing? 401329, China)
Abstract:【Objective】To investigate the difference of gene expression in Raphanus sativus seedlings responding to the high temperature through transcriptome sequencing analysis,so as to provide theoretical basis for the molecular mechanism of tolerance to heat stress in R. sativus. 【Method】The heat-resistant radish variety 1116T and heat-sensitive radish variety Wr129 were treated with high temperature (40 ℃) stress for 0 (room temperature, control) and 24 h. The total RNA of samples at each time point was extracted for transcriptome sequencing. Taking | log2 Fold Change |≥1, P<0.05 and TPM≥10 as the standard, the differentially expressed genes (DEGs) were screened, and GO function and KEGG metabolic pathway enrichment analysis were performed. 【Result】With the increase of heat stress time,the stems and leaves of Wr129 and 1116T seedlings gradually wilted. After 24 h of stress,the leaves of Wr129 wilted, drooped and became dry and yellow,while the leaves of 1116T were slightly wilted, drooped and remained green. A total of 81.45 Gb clean data were obtained from 12 libraries,and on average of 62.30% of the reads were mapped to the reference genome. In total,2701 DEGs were screened. Through GO functional annotation analysis,2629 DEGs were annotated in the GO database,of which 559 DEGs were enriched to three items of chloroplast envelope,chloroplast stroma and chloroplast thylakoid in cellular component categories,and 470 DEGs were annotated as related to stress response in biological process. KEGG metabolic pathway enrichment showed that 1166 DEGs were annotated into 124 metabolic pathways,of which 74 DEGs were enriched in photosynthetic pathway and the photosynthesis-antenna protein pathway,23 DEGs were enriched in the porphyrin and chlorophyll metabolic pathway,and most genes were induced under heat stress. While 35 DEGs involved in the glutathione metabolism pathway,and 14 glutathione-S-transferase genes(GSTs) up-regulated in this pathway. The maximum photochemical efficiency (Fv/Fm) and total chlorophyll content of PSII in leaves of Wr129 and 1116T seedlings decreased under high temperature stress for 24 h, but the decrease of 1116T was small. 【Conclusion】The heat tolerance of Wr129 and 1116T is obviously different,because 1116T can improve its heat resistance by the regulation of metabolic process relating to antioxidant and photosynthetic systems and slow the Fv/Fmvalue and chlorophyll content rate.0C38D6C5-CCD8-4036-9CA4-D1323DE818F9
Key words: Raphanus sativus; heat stress; transcriptome; heat tolerance; photosynthesis; glutathione metabolism
Foundation items: Special Fund Project for Construction of National Modern Agricultural Industry Technology System(CARS-25); Technology Innovation and Application Development Program of Chongqing(cstc2019jscx-gksbX0143)
0 引言
【研究意義】隨著全球氣候變暖,夏季極端高溫天氣的出現頻率和持續時間增加,高溫已成為制約作物生長和造成蔬菜生產減產的最主要因素之一(郭仰東等,2018)。蘿卜(Raphanus sativus L.)為十字花科蘿卜屬一、二年生根菜類蔬菜,因具有高產穩產、適應性強、營養豐富等特點,在我國廣泛種植(Kitashiba et al.,2014)。但蘿卜喜冷涼氣候,最適生長溫度為5~25 ℃,當溫度超過30 ℃時,會減緩蘿卜幼苗的生長速度,甚至死苗,嚴重制約了蘿卜的優質生產與均衡供應(初敏等,2014)。因此,研究蘿卜幼苗在高溫脅迫下的分子機制,對蘿卜優良基因資源的挖掘及耐熱的蘿卜新品種培育具有重要意義。【前人研究進展】高溫不僅對植物造成明顯的外部損傷,還會損害葉綠體結構、破壞光合系統、誘導細胞內活性氧(Reactive oxygen species,ROS)積累、損傷細胞膜系統、引起代謝功能和生理過程發生紊亂等,從而影響植物的生長和產量形成,甚至造成植株死亡(Higashi et al.,2015;Li et al.,2018;Zhao et al.,2020)。為適應高溫脅迫,植物則通過一系列被動的改變來緩解高溫熱害,如降低葉綠素總含量(Mathur et al.,2014)、積累滲透調節物質(Wang et al.,2018)、產生抗氧化酶和抗氧化劑來清除 ROS對細胞的傷害(梁國旺等,2020)。Sheng等(2006)研究發現,高溫脅迫下草坪草中的抗壞血酸(Ascorbate,AsA)和谷胱甘肽(Glutathione,GSH)含量顯著高于對照(未高溫處理),表明高溫脅迫下草坪草可通過調控抗氧化劑的含量從而維持細胞內氧代謝平衡。蘇小雨等(2021)研究發現,與熱敏性芝麻品種SP19相比,耐熱芝麻品種鄭太芝3號可通過提高抗氧化酶活性、保持光系統Ⅱ(PSII)活性及降低葉綠素降解速率來提高植株對高溫脅迫的耐受能力。除此之外,植物還可通過激活一系列脅迫響應基因如轉錄因子、蛋白激酶、熱激蛋白等基因的表達來應對高溫脅迫(Goloubinoff,2012)。轉錄組測序技術(RNA-Seq)由于其精確的數字化信號、較高的檢測通量和低成本的特點,已被廣泛應用于解析植物對高溫脅迫的響應機制。Lu等(2017)通過小麥(Triticum aestivum L.)轉錄組測序分析發現,高溫脅迫處理后谷胱甘肽-S-轉移酶(Glutathione-S-transferase,GST)基因可能在細胞抵抗氧化脅迫中發揮重要作用。Wang等(2019)通過辣椒(Capsicum annuum L.)轉錄組測序分析發現,谷胱甘肽代謝途徑在耐熱品種幼苗響應高溫脅迫中發揮關鍵作用,推測其相關基因表達和代謝物積累是辣椒耐熱品種具有較高耐熱性的主要原因之一。Ma等(2020)通過半夏(Pinellia ternate L.)轉錄組測序分析發現,高溫脅迫處理后差異表達基因主要涉及鈣離子信號、植物激素信號轉導和光合作用代謝等通路。Zhang等(2020)通過茄子(Solanum melongena L.)轉錄組測序分析發現,高溫脅迫下大量與抗氧化酶系統、植物激素和轉錄因子相關的基因差異表達。Yang等(2021)通過棗(Ziziphus jujuba Mill.)轉錄組測序分析發現,高溫脅迫處理后葉片中的差異表達基因富集到與光合作用相關及葉綠體組織相關的條目。【本研究切入點】近年來,對蘿卜耐熱性研究主要集中在耐熱品種和生理指標的篩選等方面(初敏等,2014)。利用轉錄組測序技術研究蘿卜幼苗耐熱方面的報道極少,僅有研究比較單一基因型在常溫和高溫脅迫下基因的差異表達(Wang et al.,2018;Yang et al.,2019),而未比較耐熱基因型與熱敏感基因型在高溫脅迫下基因的表達差異。【擬解決的關鍵問題】以耐熱蘿卜品種1116T和熱敏感蘿卜品種Wr129為試驗材料,通過分析其葉片在常溫和高溫下轉錄水平上的差異,以期為蘿卜耐熱機制解析提供依據,也為蘿卜優良基因資源的挖掘及利用提供理論支持。
1 材料與方法
1. 1 試驗材料
供試蘿卜品種Wr129A2A1(簡稱Wr129)和11162-3-1T-1(簡稱1116T)由重慶市農業科學院蔬菜花卉研究所提供。TRIzol? 試劑購自美國Invitrogen公司;Reverse Transcription System反轉錄試劑盒購自美國Promega公司;SYBR Green PCR Master Mix定量試劑盒購自TaKaRa公司。主要儀器設備:Climacell222人工氣候箱(MMM,德國)、Applied Biosystems 7500定量PCR儀(ABI,美國)。
1. 2 試驗方法
1. 2. 1 蘿卜幼苗高溫脅迫處理 將飽滿干凈大小一致的種子放入55~58 ℃熱水中浸泡30 min,然后置于有兩層濾紙的培養皿中發芽,種子萌發后點播于裝有育苗基質的營養缽中,每盆定苗6株,放入馴化室培養(晝夜溫度25 ℃,12 h光照/12 h黑暗,相對濕度60%~70%)。待苗生長至五葉一心期后在人工氣候箱中進行高溫(40 ℃)脅迫處理24 h,0 h作為對照(常溫),取相同部位的葉片進行液氮速凍,于-80 ℃保存備用,所有處理均設3個重復。0C38D6C5-CCD8-4036-9CA4-D1323DE818F9
1. 2. 2 Fv/Fm值和葉綠素含量測定 參照吳思佳等(2021)的方法測定PSII最大光化學效率(Fv/Fm),設10次重復。參照王紅娟(2020)的方法測定葉綠素含量。
1. 2. 3 轉錄組測序分析 利用TRIzol?試劑提取各時間點樣品總RNA,將其送至杭州聯川生物技術股份有限公司,并委托其完成質控、建庫及Illumina NovaseqTM 6000雙末端測序(測序讀長為PE150)工作。原始數據(Raw reads)在NCBI數據庫的登錄號為SUB11454056。首先,利用FastQC Version 0.11.5(Bolger et al.,2014)對原始測序數據進行過濾處理得到Clean reads,利用HISAT2 Version hisat2-2.0.4 (Kim et al.,2019)將得到的Clean reads比對到蘿卜品種象牙白參考基因組(http://Brassica_Genome_data/ Rapsa_Xiang_V1.0)得到bam文件。然后,利用StringTie Version? stringtie-1.3.4d.Linux_x86_64將所有樣本的初組裝結果進行合并,再使用gffcompare Version? gffcompare-0.9.8.Linux_x86_64檢測轉錄本與參考注釋,比較得到最終的組裝注釋結果。最后,使用R包Rsubread Version 1.22.2(Liao et al.,2019)計算每個基因的TPM(Transcripts per million),使用R包edgeR(Robinson et al.,2010)對樣本之間進行顯著差異分析,以|log2 Fold Change|≥1,P<0.05且TPM≥10為標準篩選差異表達基因(Differentially expressed genes,DEGs)。利用ClusterProfiler對差異表達基因進行GO(Gene ontology)功能注釋分類和KEGG (Kyoto encyclopedia of genes and genomes)代謝通路富集分析,矯正后P<0.05。
1. 2. 4 qRT-PCR檢測 為驗證轉錄組測序得到差異表達基因的正確性,利用Trizol試劑參照說明書提取各時間點樣品總RNA并按照Reverse Transcription System反轉錄試劑盒進行cDNA的第一鏈合成。以cDNA為模板、RsActin為內參(Xu et al.,2012),利用SYBR Green PCR Master Mix定量試劑盒檢測差異表達基因的相對表達量。qRT-PCR反應體系20 μL為:反應液中含2×SYBR Green PCR Master Mix 10 μL,cDNA模板2 μL,10 μmol/L上、下游引物各1 μL,ddH2O 補充至20 μL。擴增程序:95 ℃ 3 min;95 ℃ 5 s,58 ℃ 30 s,72 ℃ 10 s,進行40個循環;60 ℃收集熒光。每個反應均設置3次生物學重復和3次技術重復,基因相對表達量采用2-ΔΔCt法計算。所有基因特異引物(表1)由生工生物工程(上海)股份有限公司合成。
1. 3 統計分析
利用SPSS 20.0的雙尾檢驗法進行顯著性分析,使用Origin 2019b繪圖。
2 結果與分析
2. 1 高溫脅迫下植株形態觀察結果
由圖1可知,Wr129和1116T的五葉一心幼苗未受高溫脅迫(0 h)時植株形態正常,隨著高溫脅迫時間的增加,蘿卜幼苗莖葉逐漸發生萎蔫,脅迫24 h 后Wr129葉片全部萎蔫下垂,干枯變黃,而1116T葉片輕度萎蔫下垂,仍然保持綠色,說明Wr129和1116T的耐熱性存在明顯差異。將高溫脅迫24 h后的植株放在室溫恢復7 d,結果發現Wr129全部死亡,而1116T老葉全部枯死,新葉恢復生機。根據上述幼苗形態變化,選擇高溫脅迫24 h的植株進行后續高溫響應基因鑒定。
2. 2 蘿卜轉錄組測序分析結果
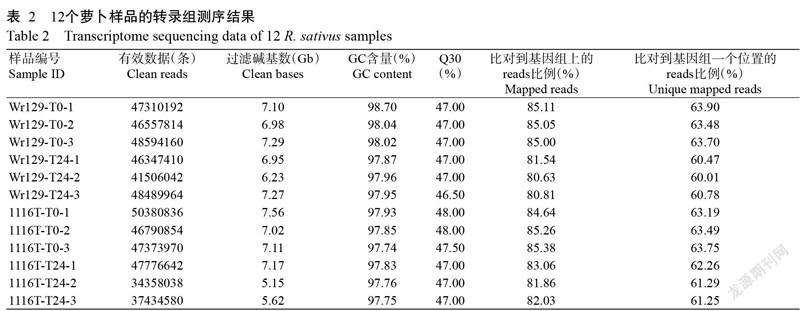
對Wr129和1116T高溫脅迫處理0和24 h兩個時間點的12個樣品 RNA 進行測序,去掉接頭、低質量的reads后,12個文庫共獲得81.45 Gb Clean data,每個文庫的測序超過34358038條,Q30值在97.74%及以上。利用Hisat 對各樣品Clean reads進行組裝及拼接后,能比對到參考基因組上的reads比對效率為80.63%~85.38%,平均有62.30%的reads能比對到基因組的一個位置(表2)。12個樣品的整體質量滿足后續分析要求。
2. 3 高溫脅迫下差異表達基因篩選
以|log2 Fold Change|≥1,P<0.05且TPM≥10為標準篩選差異表達基因, 結果(表3)發現1116T-T0/Wr129-T0組合中有669個差異表達基因,其中,上調基因259個,下調基因410個;1116T-T24/Wr129-T24組合中有2263個差異表達基因,其中,上調基因1337個,下調基因926個。由于有231個差異表達基因在兩個組合中均差異表達,最終在這兩個不同耐熱性的品種中共篩選到2701個差異表達基因。表明在高溫脅迫下不同耐熱性蘿卜的部分基因在轉錄水平上存在明顯差異。
2. 4 差異表達基因的GO功能注釋分析結果
對上述篩選獲得的2701個差異表達基因進行GO功能注釋,結果發現2629個差異表達基因在 GO 數據庫中得到注釋,主要涉及細胞組分(Cellular component)、分子功能(Molecular function)和生物過程(Biological process)三個大類。在前20個條目中,細胞組分和生物過程分別占60%和35%,其中,559個差異表達基因被注釋為細胞組分類別中的葉綠體被膜、葉綠體基質和葉綠體類囊體3個條目,470個差異表達基因被注釋為與脅迫響應相關的生物學過程(圖2)。0C38D6C5-CCD8-4036-9CA4-D1323DE818F9
2. 5 差異表達基因的KEGG代謝通路富集結果
利用KEGG數據庫對所有差異表達基因的代謝通路進行富集分析,結果發現有1166個差異表達基因富集到124條代謝通路,其中顯著富集的KEGG(P<0.05)通路有16條,包括光合作用(Photosynthesis)(57個)、光合作用-天線蛋白(Photosynthesis-antenna proteins)(17個)、光合生物碳固定(Carbon fixation in photosynthetic organisms)(36個)、卟啉和葉綠素代謝(Porphyrin and chlorophyll metabolism)(23個)、谷胱甘肽代謝(Glutathione metabolism)(35個)和內質網蛋白質加工(Protein processing in endoplasmic reticulum)(68個)等信號通路(圖3)。
2. 6 高溫脅迫響應相關差異表達基因在代謝通路中的功能分析結果
2. 6. 1 光合作用代謝通路 KEGG富集分析結果表明,高溫脅迫導致與光合作用相關的能量代謝和對植物代謝至關重要的基本生理過程發生明顯變化(圖3)。74個差異表達基因富集到光合作用和光合作用-天線蛋白2條通路。與熱敏感品種Wr129相比,高溫脅迫24 h后大多數與PSI亞基(PsaD、PsaE、PsaF、PsaG、PsaH、PsaK、PsaL和PsaO)、PSII亞基(Psb27、PsbA、PsbO、PsbQ、PsbS和PsbW)、細胞色素b6f復合體(Cytb6f)(PetA)、電子傳遞(PetF和PetH)、ATP合酶(ATPF0B、 ATPF1D和ATPF1G)和捕光葉綠素a/b結合蛋白(LCHA1、LCHA3、LCHA4、LCHA5、LCHB1、LCHB2、LCHB3、LCHB5和LCHB6)等相關基因在耐熱品種1116T幼苗葉片中上調表達(圖4-A~圖4-F),其中,1116T中的捕光葉綠素a/b結合蛋白家族基因LHCB2的表達量是Wr129的4.48倍。在與光合作用暗反應相關的差異表達基因中,32個(91.43%)相關基因包括核酮糖-1,5-二磷酸羧化/加氧酶小亞基(RBCS)、磷酸核糖激酶(PRK)、磷酸甘油酸激酶(PGK)、甘油醛3-磷酸脫氫酶(GAPA)和蘋果酸脫氫酶(MDH)在耐熱材料1116T幼苗葉片中上調表達(圖4-G),表明耐熱材料1116T在高溫脅迫下能維持較高的光合能力,植株才得以緩慢生長,因此其耐熱性更強。
2. 6. 2 卟啉和葉綠素代謝通路 PSII的最大光化學效率(Fv/Fm)用于反映植物在逆境脅迫下的光抑制程度。高溫脅迫24 h后,Wr129和1116T幼苗葉片Fv/Fm均呈下降趨勢,分別降低79.20%和23.28%,二者存在極顯著差異(P<0.01,下同),室溫恢復生長7 d后,1116T的Fv/Fm為0.703,幾乎能恢復到正常水平,而Wr129僅為0.254,二者仍存在極顯著差異(圖5-A)。同樣,高溫處理24 h后Wr129和1116T葉片總葉綠素含量也減少,Wr129和1116T分別降低72.80%和38.53%(圖5-B)。且與Wr129相比,高溫脅迫24 h后大多數參與葉綠素合成途徑的谷氨酰-tRNA還原酶(hemA)、Mg2+螯合酶(CHLD、CHLH和CHLP)、谷氨酸-1-半醛轉氨酶(hemL)、尿卟啉原脫羧酶(hemE)、二乙烯還原酶(DVR)、原卟啉原Ⅸ氧化酶(PPOX)和葉綠素合酶(CHLG)基因在1116T幼苗葉片中上調表達,而與葉綠素降解相關的持綠基因(SGR)則下調表達(圖5-C)。
2. 6. 3 谷胱甘肽代謝通路 植物在受到非生物脅迫時,細胞內會產生多余的活性氧,從而造成氧化脅迫。谷胱甘肽作為一種在植物中普遍存在的抗氧化劑,能夠清除多余的活性氧,使細胞處于氧化還原反應的穩態。本研究中35個差異表達基因富集在谷胱甘肽代謝通路上,其中有22個基因持續上調表達,包括1個谷胱甘肽合成酶(Glutathione synthetase,GSS)基因和14個谷胱甘肽-S-轉移酶(Glutathione S-transferase, GST)基因(圖6-A)。隨機選取8個GSTs基因進行qRT-PCR檢測,結果如圖6-B~圖6-I所示。與Wr129相比,1116T中除Rsa10032310(GST)在高溫脅迫0和24 h顯著上調表達外,其余GSTs基因僅在高溫脅迫24 h顯著上調,表明耐熱品種1116T通過調控谷胱甘肽代謝通路相關GSTs基因的表達,減少細胞內脂類物質的過氧化反應,從而提高對高溫脅迫的耐受能力。
3 討論
高溫是制約蘿卜的優質生產與均衡供應的主要限制因素(初敏等,2014)。為了了解蘿卜幼苗對高溫脅迫響應的分子機制,本研究以耐熱品種1116T和熱敏感品種Wr129為研究對象,通過轉錄組測序數據比較分析兩者在高溫脅迫24 h后在轉錄水平上響應高溫脅迫的基因差異,共鑒定了2701個差異表達基因),表明高溫脅迫下不同耐熱性蘿卜品種在差異表達基因轉錄水平上存在明顯差異,且GO功能注釋分析結果顯示,1029個差異表達基因被富集到細胞組分類別中的葉綠體被膜、葉綠體基質和葉綠體類囊體及與脅迫響應相關的生物學過程;KEGG 代謝通路富集分析結果顯示,144個差異表達基因富集到光合作用和谷胱甘肽代謝通路,說明光合作用和谷胱甘肽代謝途徑相關基因在蘿卜幼苗響應高溫脅迫中發揮重要的調控作用。
光合作用是植物對溫度變化最敏感的代謝反應,高溫脅迫主要影響葉綠體光系統 I(PSI)和光系統 II(PSII)中的光反應及基質中的碳同化反應(Zhao et al.,2020)。葉綠素含量和Fv/Fm通常被作為判斷植物耐受逆境脅迫的重要指標(吳思佳等,2021)。研究表明,耐熱型水稻可在高溫條件下通過維持較高的葉綠素含量從而提高對高溫的耐受能力(Sailaja et al.,2015),轉基因擬南芥過表達BrHSF16基因會導致Fv/Fm顯著增加,并在高溫條件下表現出明顯的生長優勢(張慧敏等,2021)。本研究結果顯示,高溫處理24 h后,雖然1116T和Wr129的葉綠素含量和Fv/Fm值均下降,但1116T的下降幅度明顯小于Wr129,且與Wr129相比,1116T中大多數葉綠素合成相關基因的轉錄水平顯著上調,表明1116T在高溫脅迫下可通過減緩Fv/Fm和葉綠素含量下降速率來維持較高的光合能力,導致其耐熱性更強。此外,KEGG代謝通路富集分析結果顯示,109個差異表達基因富集到光合作用的光反應、暗反應和光合作用-天線蛋白通路;與Wr129相比,1116T中大多數基因在高溫脅迫后迅速上調表達,表明耐熱品種1116T可通過調控光合作用相關基因的表達,以此減少高溫脅迫對植株的生理傷害和對光合作用的抑制。0C38D6C5-CCD8-4036-9CA4-D1323DE818F9
作物受高溫等逆境脅迫時,細胞內氧代謝平衡失調,ROS含量升高,促進多聚不飽和脂肪酸降解并產生丙二醛,進而對植物組織和細胞進一步損傷。谷胱甘肽是一種在植物體內普遍存在的非酶系統抗氧化劑,在調節細胞內氧化還原信號轉導中發揮重要作用(Zagorchev et al.,2013)。研究發現,高溫顯著影響辣椒的抗氧化酶系統,谷胱甘肽代謝途徑相關基因可在短期內迅速響應高溫脅迫并參與辣椒的耐熱調控(Wang et al.,2019)。本研究KEGG代謝通路富集分析結果顯示,35個差異表達基因富集在谷胱甘肽代謝途徑上,與Wr129相比,25個基因在高溫脅迫24 h后上調表達,說明其在蘿卜響應高溫脅迫的過程中發揮作用。谷胱甘肽轉移酶是具有多種功能的蛋白超家族,能以GSH為底物催化過氧化氫的轉化,保護細胞免受氧化所導致的損傷,在植物抵御外源物質毒害和非生物脅迫中發揮重要作用(Chi et al.,2011)。本研究發現,與Wr129相比,1116T中14個GSTs基因在高溫脅迫后上調表達,說明在高溫脅迫下耐熱品種1116T也與水稻(Lee et al.,2007)、小麥(Lu et al.,2017)、辣椒(Wang et al.,2019)一樣通過積累GST來提高自身對高溫脅迫的耐受能力,但是具體調控機制有待進一步探究。
4 結論
Wr129和1116T的耐熱性存在明顯差異,其原因是1116T可通過調控光合作用和抗氧化系統相關基因的表達,并減緩Fv/Fm和葉綠素含量下降速率提高植株對高溫脅迫的耐受能力。
參考文獻:
初敏,莊志群,王秀峰,王淑芬,楊鳳娟,魏珉,史慶華. 2014. 不同耐熱性蘿卜幼苗對高溫脅迫的生理響應[J]. 山東農業大學學報(自然科學版),45(3):334-339. [Chu M,Zhuang Z Q,Wang X F,Wang S F,Yang F J,Wei M,Shi Q H. 2014. Study on physiological response to high temperature stress in different heat tolerance radish seedlings[J]. Journal of Shandong Agricultural University (Na-tural Science Edition),45(3):334-339.] doi:10.3969/j.issn. 1000-2324.2014.03.003.
郭仰東,張磊,李雙桃,曹蕓運,齊傳東,王晉芳. 2018. 蔬菜作物應答非生物逆境脅迫的分子生物學研究進展[J]. 中國農業科學,51(6):1167-1181. [Guo Y D,Zhang L,Li S T,Cao Y Y,Qi C D,Wang J F. 2018. Progresses in research on molecular biology of abiotic stress responses in vegetable crops[J]. Scientia Agricultura Sinica,51(6):1167-1181.] doi:10.3864/j.issn.0578-1752.2018.06.015.
梁國旺,李增強,周步進,常蒙蒙,陳濤,陳鵬. 2020. 紅麻谷胱甘肽還原酶基因(HcGR)的克隆及鹽脅迫下表達分析[J]. 南方農業學報,51(10):2412-2419. [Liang G W,Li Z Q,Zhou B J,Chang M M,Chen T,Chen P. 2020. Clo-ning of glutathione reductase gene(HcGR)and its expression in response to salt stress of kenaf(Hibiscus cannabinus)[J]. Journal of Southern Agriculture,51 (10):2412-2419.] doi:10.3969/j.issn.2095-1191.2020.10.012.
蘇小雨,高桐梅,李豐,魏利斌,田媛,王東勇,朱松濤,衛雙玲. 2021. 不同耐熱基因型芝麻苗期對高溫脅迫的生理響應機制[J]. 華北農學報,36(6):96-105. [Su X Y,Gao T M,Li F,Wei L B,Tian Y,Wang D Y,Zhu S T,Wei S L. 2021. Physiological response mechanism to high temperature stress in different heat-tolerant genotypes of sesame seedlings[J]. Acta Agriculturae Boreali-Sinica,36(6):96-105.] doi:10.7668/hbnxb.20192 390.
王紅娟,於春,路獻勇,江本利,胡積送,余黎明,朱加保,閆曉明. 2020. 不同氮濃度對薏苡幼苗生長和光合特性的影響[J]. 南方農業學報,51(8):1925-1931. [Wang H J,Yu C,Lu X Y,Jiang B L,Hu J S,Yu L M,Zhu J B,Yan X M. 2020. Effects of different nitrogen concentrations on seedling growth and photosynthetic characteristics of coix[J]. Journal of Southern Agriculture,51(8):1925-1931.] doi:10.3969/j.issn.2095-1191.2020.08.017.0C38D6C5-CCD8-4036-9CA4-D1323DE818F9
吳思佳,李仁英,謝曉金,張婍,陳佳林,徐向華,胡宗薈,盧炳浩,張娜. 2021. 抽穗期高溫對水稻葉片光合特性、葉綠素熒光特性和產量構成因素的影響[J]. 南方農業學報,52(1):20-27. [Wu S J,Li R Y,Xie X J,Zhang Q,Chen J L,Xu X H,Hu Z H,Lu B H,Zhang N. 2021. Effects of high temperature on characteristics of photosynthesis and chlorophyll fluorescence and yield components of rice at heading stage[J]. Journal of Southern Agriculture,52(1):20-27.] doi:10.3969/j.issn.2095-1191.2021.01.003.
張慧敏,趙乾宇,李紅穎,盧玲,張一卉,邱念偉,王鳳德,高建偉. 2021. 過量表達大白菜BrHSF16基因提高轉基因擬南芥耐熱性[J]. 植物生理學報,57(10):1915-1925. [Zhang H M,Zhao Q Y,Li H Y,Lu L,Zhang Y H,Qiu N W,Wang F D,Gao J W. 2021. Overexpression of BrHSF16 gene in Chinese cabbage improves heat tole-rance of transgenic Arabidopsis[J]. Plant Physiology Journal,57(10):1915-192.] doi:10.13592/j.cnki.ppj.2021. 0206.
Bolger A M,Lohse M,Usadel B. 2014. Trimmomatic:A flexible trimmer for Illumina sequence data[J]. Bioinforma-tics,30(15):2114-2120. doi:10.1093/bioinformatics/btu 170.
Chi Y H,Cheng Y S,Vanitha J,Kumar N,Ramamoorthy R,Ramachandran S,Jiang S Y. 2011. Expansion mechanisms and functional divergence of the glutathione S-transferase family in sorghum and other higher plants[J]. DNA Research,18(1):1-16. doi:10.1093/dnares/dsq031.
Goloubinoff F P. 2012. How do plants feel the heat ? [J]. Trends in Biochemical Sciences,37(3):118-125. doi:10.1016/j.tibs.2011.11.007.
Higashi Y,Okazaki Y,Myouga F,Shinozaki K,Saito K. 2015. Landscape of the lipidome and transcriptome under heat stress in Arabidopsis thaliana[J]. Scientific Reports,27(5):10533. doi:10.1038/srep10533.
Kim D,Paggi J M,Park C,Bennett C,Salzberg S L. 2019. Graph-based genome alignment and genotyping with HISAT2 and HISAT-genotype[J]. Nature Biotechnology,37(8):907-915. doi:10.1038/s41587-019-0201-4.
Kitashiba H,Li F,Hirakawa H,Kawanabe T,Zou Z,Hasegawa Y,Tonosaki K,Shirasawa S,Fukushima A,Yokoi S,Takahata Y,Kakizaki T,Ishida M,Okamoto S,Sakamoto K,Shirasawa K,Tabata S,Nishio T. 2014. Draft sequen-ces of the radish(Raphanus sativus L.) genome[J]. DNA Research,21(5):481-490. doi:10.1093/dnares/dsu014.
Lee D G,Ahsan N,Lee S H,Kang K Y,Bahk J D,Lee I J,Lee B H. 2007. A proteomic approach in analyzing heat-responsive proteins in rice leaves [J]. Proteomics,7(18):3369-3383. doi:10.1002/pmic.200700266.
Li B J,Gao K,Ren H M,Tang W Q. 2018. Molecular mechanisms governing plant responses to high temperatures[J]. Journal of Integrative Plant Biology,60(9):757-779. doi:10.1111/jipb.12701.
Liao Y,Smyth G K,Shi W. 2019. The R package Rsubread is easier,faster,cheaper and better for alignment and quantification of RNA sequencing reads[J]. Nucleic Acids Research,47(8):e47. doi:10.1093/nar/gkz114.0C38D6C5-CCD8-4036-9CA4-D1323DE818F9
Lu Y Z,Li R Q,Wang R C,Wang X M,Zheng W J,Sun Q X,Tong S M,Dai S J,Xu S B. 2017. Comparative proteomic analysis of flag leaves reveals new insight into wheat heat adaptation[J]. Frontiers in Plant Science,8:1086. doi:10.3389/fpls.2017.01086.
Ma G J,Zhang M D,Xu J L,Zhou W X,Cao L W. 2020. Transcriptomic analysis of short-term heat stress response in Pinellia ternata provided novel insights into the improved thermotolerance by spermidine and melatonin[J]. Ecotoxicology and Environmental Safety,202:110877. doi:10.1016/j.ecoenv.2020.110877.
Mathur S,Agrawal D,Jajoo A. 2014. Photosynthesis:Response to high temperature stress[J]. Journal of Photochemistry & Photobiology.,B Biology,137:116-126. doi:10.1016/j.jphotobiol.2014.01.010.
Robinson M D,McCarthy D J,Smyth G K. 2010. edgeR:A bioconductor package for differential expression analysis of digital gene expression data[J]. Bioinformatics,26(1):139-140. doi:10.1093/bioinformatics/btp616.
Sailaja B,Subrahmanyam D,Neelamraju S,Vishnukiran T,Rao Y V,Vijayalakshmi P,Voleti S R,Bhadana V P,Mangrauthia S K. 2015. Integrated physiological,biochemical,and molecular analysis identifies important traits and mechanisms associated with differential response of rice genotypes to elevated temperature[J]. Frontiers in Plant Science,6:1044. doi:10.3389/fpls.2015.01044.
Sheng X,Li J L,Zhang X Q,Wei H,Cui L J. 2006. Effects of heat acclimation pretreatment on changes of membrane lipid peroxidation,antioxidant metabolites,and ultrastructure of chloroplasts in two cool-season turfgrass species under heat stress[J]. Environmental & Experimental Botany,56(3):274-285. doi:10.1016/j.envexpbot.2005.03.002.
Tang R M,Gupta S K,Niu S Y,Li X Q,Yang Q,Chen G S,Zhu W J,Haroon M. 2020. Transcriptome analysis of heat stress response genes in potato leaves[J]. Molecular Biology Reports,47(6):4311-4321. doi:10.1007/s11033-020-05485-5.
Wang J,Lv J H,Liu Z B,Liu Y H,Song J H,Ma Y Q,Ou L J,Zhang X L,Liang C L,Wang F,Juntawong N,Jiao C H,Chen W C,Zou X X. 2019. Integration of transcriptomics and metabolomics for pepper(Capsicum annuum L.) in response to heat stress[J]. International Journal of Molecular Sciences,20(20):5042. doi:10.3390/ijms2020 5042.
Wang L,Liu L,Ma Y,Li S,Dong S,Zu W. 2018. Transcriptome profilling analysis characterized the gene expression patterns responded to combined drought and heat stresses in soybean[J]. Computational Biology and Che-mistry,77:413-429. doi:10.1016/j.compbiolchem.2018.09. 012.0C38D6C5-CCD8-4036-9CA4-D1323DE818F9
Wang R H,Mei Y,Xu L,Zhu X W,Wang Y,Guo J,Liu L W. 2018. Genome-wide characterization of differentially expressed genes provides insights into regulatory network of heat stress response in radish(Raphanus sativus L.) [J]. Functional & Integrative Genomics,18(2):225-239. doi:10.1007/s10142-017-0587-3.
Xu Y Y,Zhu X W,Gong Y Q,Xu L,Wang Y,Liu L W. 2012. Evaluation of reference genes for gene expression studies in radish(Raphanus sativus L.) using quantitative real-time PCR[J]. Biochemical and Biophysical Research Communications,424(3):398-403. doi:10.1016/j.bbrc. 2012.06.119.
Yang L,Jin J,Fan D Y,Hao Q,Niu J X. 2021. Transcriptome analysis of jujube(Ziziphus jujuba Mill.) response to heat stress[J]. International Journal Genomics,2021:3442277. doi:10.1155/2021/3442277.
Yang Z,Li W,Su X,Ge P F,Zhou Y,Hao Y Y,Shu H Y,Gao C L,Cheng S H,Zhu G P,Wang Z W. 2019. Early response of radish to heat stress by strand-specific transcriptome and miRNA analysis[J]. Internation Journal Molecular Sciences,20(13):3321. doi:10.3390/ijms2013 3321.
Zagorchev L,Seal C E,Kranner I,Odjakova M. 2013. A central role for thiols in plant tolerance to abiotic stress[J]. Internation Journal Molecular Sciences,14(4):7405-7432. doi:10.3390/ijms14047405.
Zhang A D,Zhu Z W,Shang J,Zhang S M,Shen H B,Wu X X,Zha D S. 2020. Transcriptome profiling and gene expression analyses of eggplant(Solanum melongena L.) under heat stress[J]. PLoS One,15(8):e0236980. doi:10. 1371/journal.pone.0236980.
Zhao J G,Lu Z G,Wang L,Jin B. 2020. Plant responses to heat stress:Physiology,transcription,noncoding RNAs,and epigenetics[J]. Internation Journal Molecular Scien-ces,22(1):117. doi:10.3390/ijms22010117.
(責任編輯 陳 燕)0C38D6C5-CCD8-4036-9CA4-D1323DE818F9

