超高效液相色譜-四極桿/靜電場軌道阱高分辨質譜法非靶向篩查蘋果中苯脲類農藥
岳 寧,李曉慧,李敏潔,王 琦,邵 華,鄭鷺飛,王 靜,金 芬
(中國農業科學院農業質量標準與檢測技術研究所,北京 100081)
我國是苯脲類農藥的生產和使用大國,苯脲類農藥主要用作除草劑和殺蟲劑,其中苯脲類除草劑(Phenylurea herbicides,PUHs)作為光合系統電子傳遞抑制劑,在世界范圍內廣泛使用,主要用于防治果園及大田作物中的禾本科雜草和闊葉雜草[1];而苯甲酰脲類殺蟲劑(Benzoylurea insecticides,BPUs)主要是在PUHs 的結構骨架上引入苯甲酰基和鹵素取代基[2],可干擾目標害蟲的幾丁質合成[3],是防治農產品抗性害蟲的主要農藥品種之一。然而,苯脲類農藥的水溶性高,多具有內吸性,在土壤中殘留的半衰期長,對農產品和地下水可能造成污染[4-8]。美國環境保護總局(EPA)將敵草隆和殺鈴脲等苯脲類農藥定為Ⅲ類毒性或Ⅳ類毒性[9],歐盟也將其列入優先控制污染物清單[10-11]。近年來,苯甲酰脲類殺蟲劑作為第三代殺蟲劑,以獨特的作用機制和高效的殺蟲活性,成為新型農藥創制活躍領域之一[12]。為應對新型化合物的發現和預警需求,有必要建立農產品中苯脲類農藥的非靶向快速篩查方法。
現有關于農產品以及水體中苯脲類農藥的殘留分析方法均為靶向分析技術[13-14],無法實現對新型苯脲類農藥的快速非靶向篩查。近年來,超高效液相色譜-四極桿/靜電場軌道阱高分辨質譜(UPLCQ/Orbitrap HRMS)由于具有分析時間短、選擇性高及分辨率高等特點[15],在新型危害物和天然產物質譜裂解規律研究中的應用日益增多。目前,該技術已成功用于農產品中有機磷類等農藥殘留、蘇丹紅等食品添加劑及大環內酯類等獸藥殘留的快速非靶向篩查[16-18]。然而,目前尚無基于質譜特征碎裂規律的苯脲類農藥殘留高分辨質譜快速篩查方法的報道。
本研究采用UPLC-Q/Orbitrap HRMS 技術解析了13 種PUHs 和9 種BPUs 共22 種苯脲類農藥的特征離子碎片和特征中性丟失。將22 種苯脲類農藥按取代基的不同分為4 類,并分析了其主要裂解途徑、特征碎片離子和規律,并將基于該特征裂解規律的篩查方法應用于北京市售蘋果中苯脲類農藥的非靶向篩查,為苯脲類農藥殘留的快速篩查提供參考。
1 實驗部分
1.1 儀器與試劑
超高效液相色譜儀(Vanquish Flex UHPLC Systems,美國Thermo Fisher 公司);四極桿/靜電場軌道阱高分辨質譜儀(Q Exactive HF-HRMS 質譜儀,美國Thermo Fisher 公司);Milli-Q 超純水器(美國Millipore公司)。
乙腈、甲醇、甲酸均為色譜純,購自美國Fisher 公司。N-丙基乙二胺(PSA,50 μm)、十八烷基鍵合硅膠(C18,50 μm)分散固相萃取吸附劑,購自美國Sigma-Aldrich 公司;13 種苯脲類除草劑標準品,純度>98.7%,購自德國Dr.Ehrenstorfer 公司;9 種苯甲酰脲類殺蟲劑標準品,質量濃度均為100 μg/mL,購自農業部環境保護科研監測所。12 批紅富士蘋果樣品分別于2021 年10 月購自北京地區的3 個超市。
1.2 標準溶液配制
分別稱取13 種苯脲類除草劑標準品,用甲醇溶解并定容配成100 μg/mL 的標準儲備液;準確量取13種苯脲類除草劑和9種苯甲酰脲類殺蟲劑的儲備液(100 μg/mL),用甲醇稀釋定容配制成200 μg/L 的混合標準溶液,待分析。
1.3 儀器條件
色譜條件:色譜柱:Acquity BEH C18色譜柱(100 mm×2.1 mm,1.7 μm,美國Waters公司)。柱溫:40 ℃;流動相:A 相為0.1%的甲酸水溶液,B 相為甲醇;流速0.4 mL/min;進樣量5 μL。流動相梯度洗脫程序:0~1.0 min,90%A;1.0~2.0 min,90%~70%A;2.0~4.0 min,70%~40%A;4.0~5.0 min,40%~0%A;5.0~9.0 min,0%A;9.0~9.1 min,0%~90%A;10.0 min,90%A。
質譜條件:離子源:熱電噴霧離子源(HESI);離子模式:正離子;歸一化碰撞能(NCE):20%、40%、60%;鞘氣流速:40 Arb;輔助氣流速:10 Arb;噴霧電壓:3.50 kV;毛細管溫度:320 ℃;輔助氣加熱溫度:300 ℃;脫溶劑氣和錐孔氣:氮氣。標準品掃描模式:平行反應監測模式(PRM):通過Xcalibur Instrument Setup 軟件界面Global lists 中Iclusion List 輸入22 種苯脲類化合物的分子式;分辨率:90 000;S-lens電壓:55 V;隔離窗口:2.0 u;樣品掃描模式:數據采集使用一級母離子全掃描和數據依賴的二級子離子掃描模式(Full MS/dd-MS2),質量掃描范圍m/z100 ~1 500。一級分辨率:70 000,二級分辨率:17 500。自動增益控制進入軌道阱中的離子數(AGC target)為1e6,最大注入時間為100 ms。
1.4 樣品前處理
參照國家標準GB 20769-2008[19]進行樣品前處理。準確稱取10.00 g(精確至0.01 g)樣品勻漿于50 mL塑料離心管中,加入10 mL乙腈混合,渦旋(轉速為2 000 r/min)提取5 min,放冷,在室溫條件下以6 000 r/min離心5 min。取1 mL上清液加入裝有30 mg PSA和25 mg C18凈化劑混合物的2 mL塑料離心管中,渦旋5 min 后,在室溫條件下以6 000 r/min 離心5 min,取上清液經0.22 μm 微孔濾膜過濾,供進樣分析。
2 結果與討論
2.1 正離子模式下苯脲類農藥的質譜分析
根據基本結構骨架,苯脲類農藥可分為苯脲類除草劑(PUHs)和苯甲酰脲類殺蟲劑(BPUs)兩大類。其中PUHs 的基本結構骨架由脲基和苯環兩部分構成(圖1A);而BPUs 是在PUHs 的結構骨架基礎上引入苯甲酰基活性亞結構和鹵素取代基,其基本結構骨架包括苯甲酰基、脲橋和苯胺三部分。不同的BPUs結構差異主要體現在酰胺、苯甲酰基和苯胺上取代基的不同。因此根據苯甲酰基上鹵素取代基的不同,可將BPUs 分為氟原子取代的BPUs(圖1B)和氯原子取代的BPUs(圖1C)。典型PUHs 和BPUs 中不同取代基的具體信息見表1。
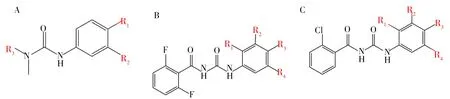
圖1 苯脲類農藥的一般結構通式Fig.1 General structural formulas of phenylurea pesticides

表1 苯脲類農藥結構通式中R取代基的詳細信息Table 1 The substituents of general structural formula of phenylurea pesticides
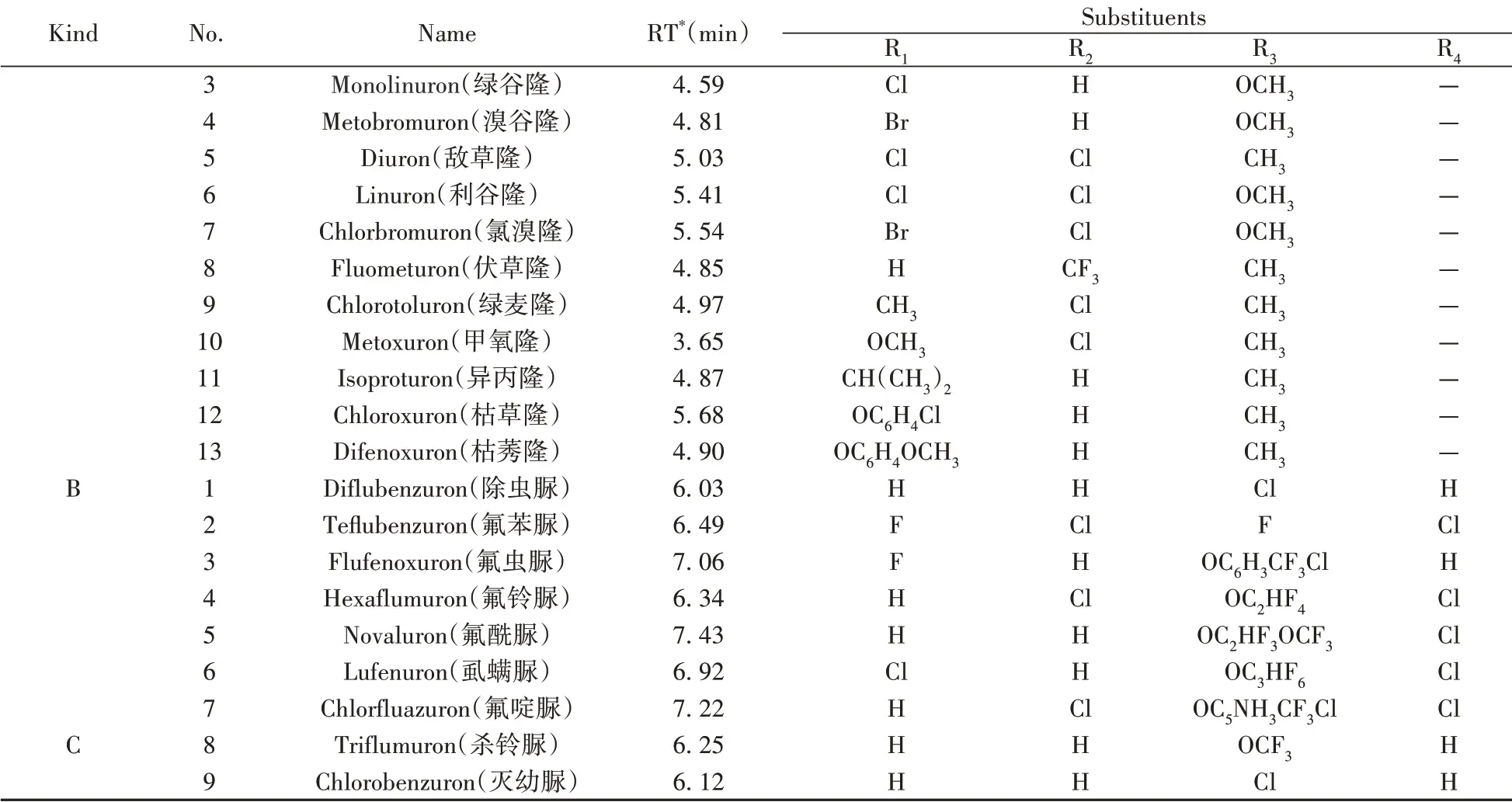
(續表1)
本研究22 種苯脲類農藥的分子離子精確質量數和主要特征離子碎片的信息見表2。在正離子模式下,13 種PUHs 和9 種BPUs 均可產生特征明顯的準分子離子峰[M+H]+,其準分子離子峰的精確質量數與理論值的偏差小于5×10-6(表2),可作為定性依據。4 類典型PUHs 和BPUs 的二級全掃描質譜圖見圖2。
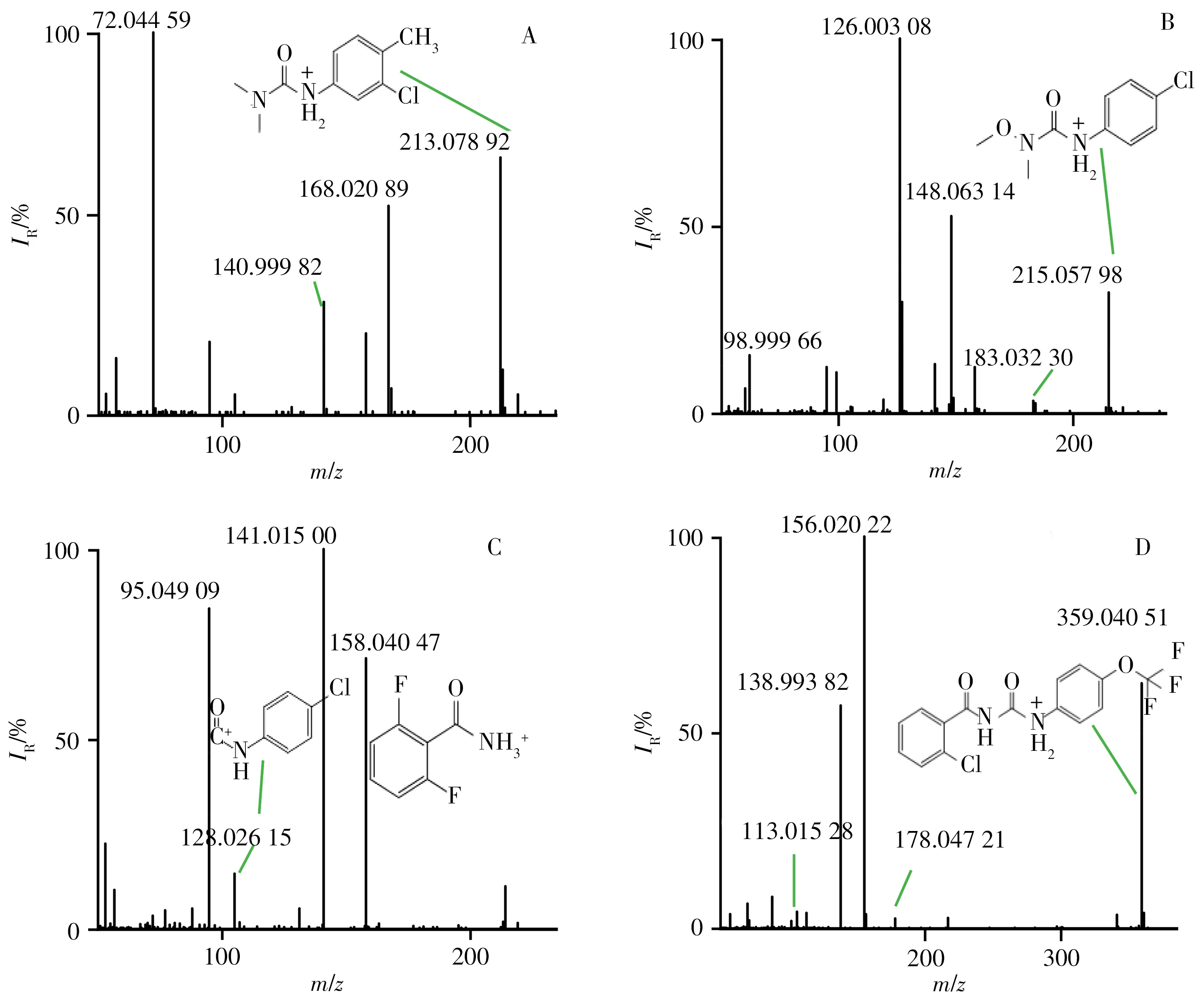
圖2 典型PUHs(A、B)和BPUs(C、D)的二級全掃描圖Fig.2 Secondary full scan spectra of typical PUHs(A,B)and BPUs(C,D)
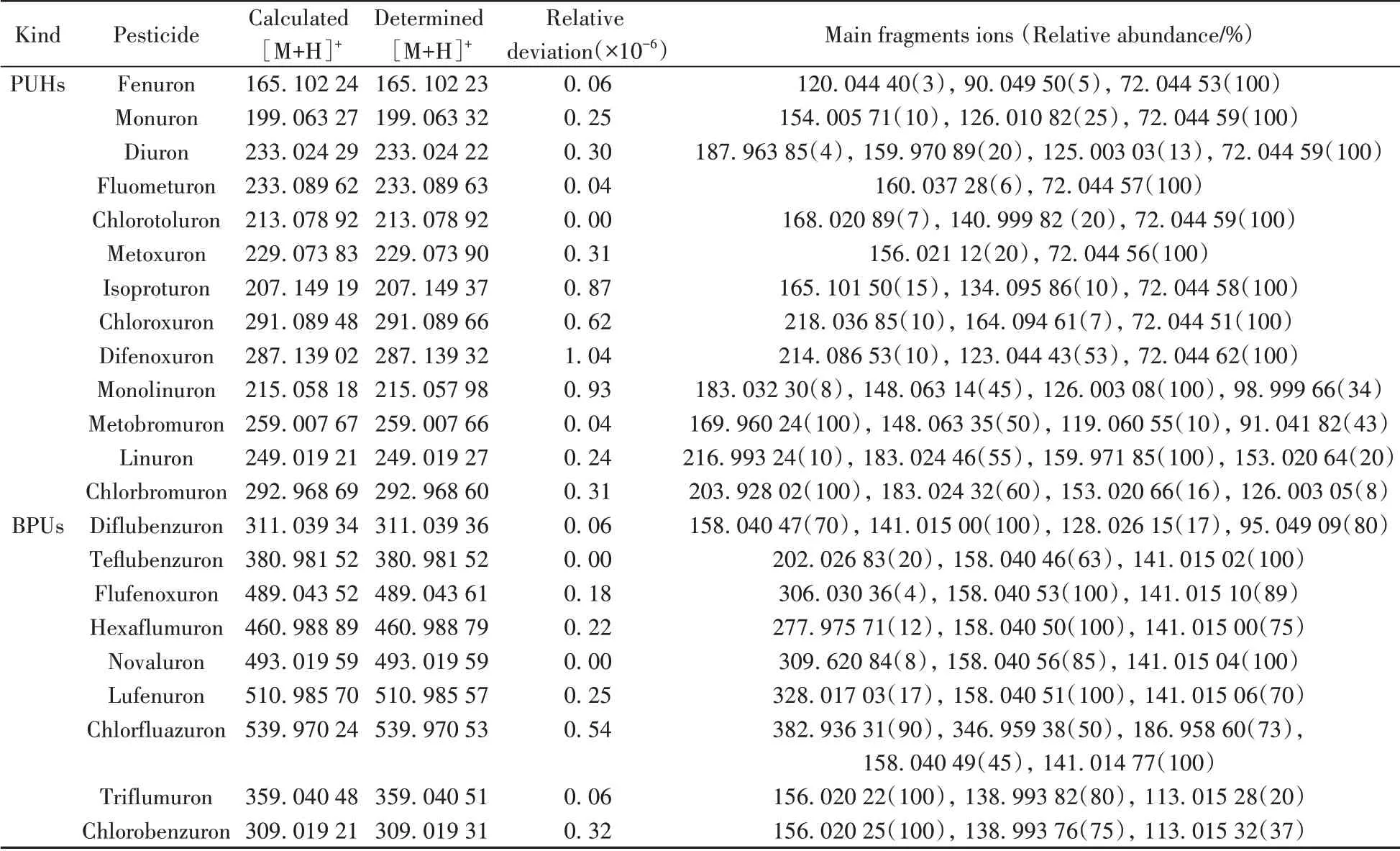
表2 13種苯脲類除草劑和9類苯甲酰脲類殺蟲劑的高分辨質譜數據Table 2 High resolution mass spectrometric data of 13 PUHs and 9 BPUs
2.2 質譜裂解途徑
2.2.1 PUHs 的主要裂解途徑根據取代基R3(甲基或甲氧基)的不同,PUHs可分為2種亞型。其中,綠麥隆等9 種PUHs 的取代基R3均為甲基,其準分子離子[M+H]+發生斷裂,產生特征碎片離子N,N-二甲基酰胺結構[(CH3)2NCO]+(m/z72.044 59);[M+H]+也可丟失中性分子二甲胺(m/z45.058 03)得到特征離子碎片[C6H3NHCOR1R2]+,或氫原子重排后發生脲基中碳氮鍵斷裂得到特征離子碎片[C6H3NH3R1R2]+。綠麥隆的特征離子碎片的主要裂解途徑見圖3。
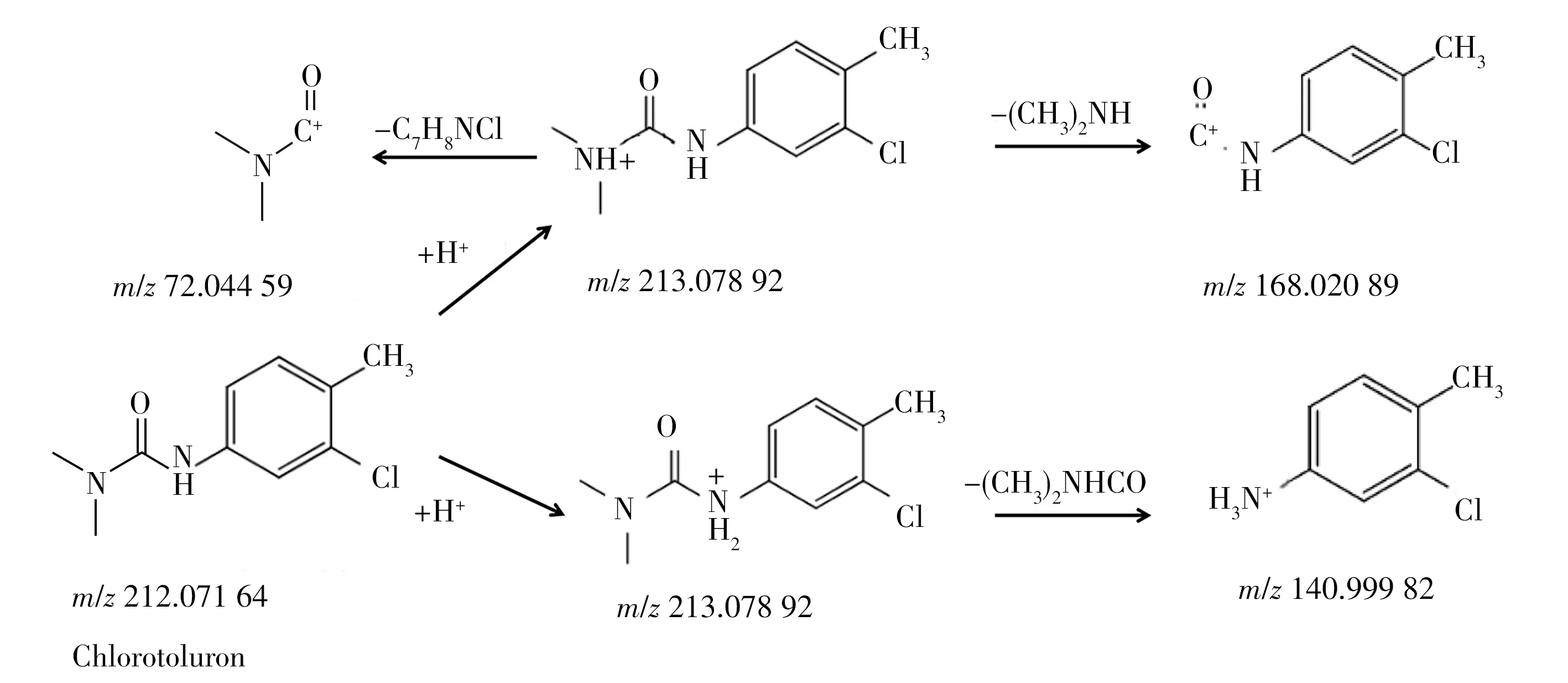
圖3 綠麥隆的主要裂解途徑Fig.3 Proposed fragmentation pathways of chlorotoluron
而綠谷隆、溴谷隆、利谷隆和氯溴隆等4 種PUHs 的取代基R3均為甲氧基。該亞類PUHs 的準分子[M+H]+的裂解與取代基為甲基的PUHs亞型相似,均發生N-甲氧基-N-甲基甲酰胺中氫原子重排,產生特征性離子碎片[C6H3NH3R1R2]+;與之不同的是,取代基R3均為甲氧基的4 種PUHs 的[M+H]+也可發生脲基中氮氧鍵斷裂,分別丟失中性分子甲醇[CH3OH]和鹵化氫[HR1],產生特征離子碎片[R1R2C7H6N2OCH3]+和[R2C7H6N2OCH3]+。以綠谷隆為例,特征離子碎片可能的裂解途徑見圖4。
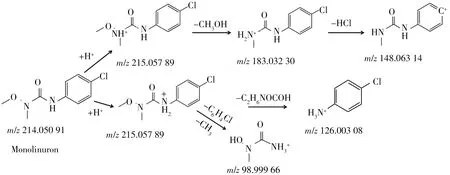
圖4 綠谷隆的主要裂解途徑Fig.4 Proposed fragmentation pathways of monolinuron
2.2.2 BPUs 的主要裂解途徑根據鹵素取代基的不同,BPUs 可分為含氟和含氯原子2 種亞型。其中,除蟲脲、氟苯脲、氟蟲脲、氟鈴脲、氟酰脲、虱螨脲和氟啶脲7種BPUs結構中苯甲酰基上的鹵素取代基均為氟原子。與PUHs 相比,含氟BPUs 的準分子離子[M+H]+也可發生脲橋中脲基碳氮鍵斷裂,產生特征離子碎片[C7H3F2ONH3]+(m/z158.040 47),該離子可進一步提示中性分子氨產生特征離子碎片[C7H3F2O]+(m/z141.015 00)。此外,[M+H]+也可丟失中性分子2,6-氟苯甲酰胺結構[C8H3F2O2NH2](m/z183.013 21),產生特征離子碎片[C7H2NOR1R2R3R4]+。以除蟲脲為例,特征離子碎片可能的裂解途徑見圖5。
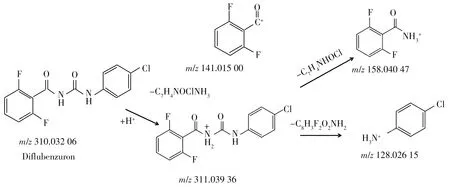
圖5 除蟲脲的主要裂解途徑Fig.5 Proposed fragmentation pathways of diflubenzuron
殺鈴脲和滅幼脲為含氯的BPUs,其準分子離子[M+H]+的裂解途徑與含氟的BPUs類似,但由于結構中苯甲酰基上的鹵素取代基與除蟲脲等不同,[M+H]+裂解產生的部分特征碎片離子的質荷比有所不同,分別為[C7H3ClONH3]+(m/z156.020 22)和[C7H3ClO]+(m/z138.993 82)。與上述苯脲類農藥不同的是,殺鈴脲和滅幼脲還存在特征碎片離子[C6H5Cl]+(m/z113.015 28),這可能是苯甲酰基結構中酰基與苯環相連的碳碳鍵斷裂后形成共軛結構所致。以殺鈴脲為例,特征離子碎片可能的裂解途徑見圖6。
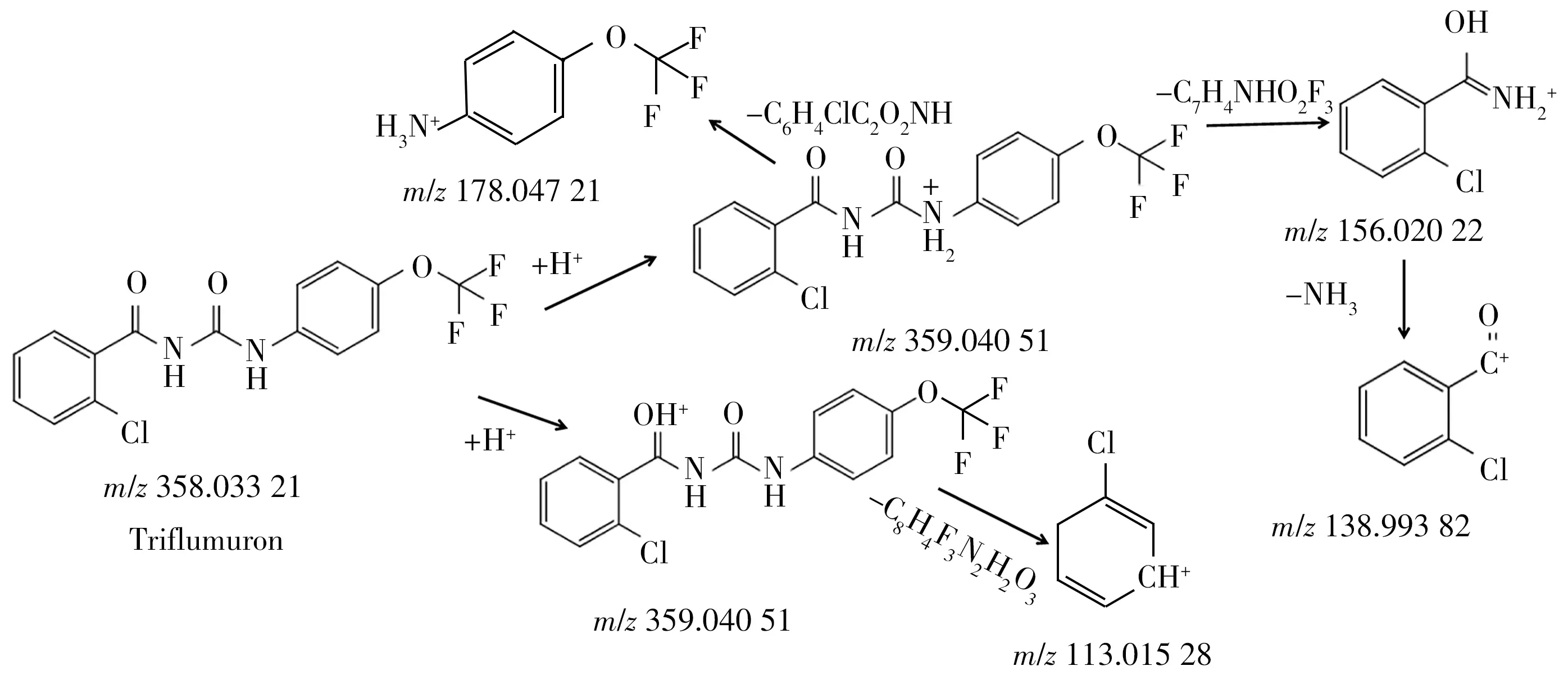
圖6 殺鈴脲的主要裂解途徑Fig.6 Proposed fragmentation pathways of triflumuron
2.3 實際樣品測定
應用上述裂解規律,對北京市售12 批蘋果樣品進行Full MS/dd-MS2模式下的二級離子碎片全掃描,在1 份蘋果樣品中檢測到離子碎片m/z72.044 59 和m/z168.020 85,準分子離子為m/z213.078 96的可疑化合物。根據標識性離子碎片m/z72.044 59推測,該化合物可能是一種苯脲類除草劑,推測碎片m/z168.026 85由準分子離子m/z213.078 96中性丟失(CH3)2NH(m/z45.058 03)產生,因此樣品中可能含有綠麥隆。進一步采用標準品進行驗證,綠麥隆標準品的保留時間為4.96 min,母離子為m/z213.078 90,子離子為m/z72.044 59、168.020 89、140.999 82。而在實際樣品中,該物質的保留時間為4.97 min,母離子為m/z213.078 96,子離子為m/z72.044 59、168.020 85,與標準品的保留時間以及二級質譜信息一致,由此確定樣品中含有綠麥隆,驗證了本文總結的苯脲類農藥的質譜裂解規律。
3 結 論
本文采用UPLC-Q/Orbitrap HRMS 技術在正離子模式下對22 種苯脲類農藥的裂解規律進行研究,根據取代基的不同,將22 種待測農藥分為4 類,以綠麥隆為代表的9 種含甲基的苯脲類除草劑的主要特征離子碎片為m/z72.044 59,特征丟失中性分子二甲胺(m/z45.058 03);以綠谷隆為代表的4種含甲氧基的苯脲類除草劑發生特征丟失中性分子甲醇或鹵化氫產生離子碎片;除蟲脲等7 種氟原子取代的苯甲酰脲類殺蟲劑的特征離子碎片為m/z158.040 47、m/z141.015 00,特征丟失中性分子2,6-氟苯甲酰胺結構(m/z183.013 21);殺鈴脲等2 種氯原子取代的苯甲酰脲類殺蟲劑的主要特征離子碎片為m/z156.020 25、m/z138.993 76 和m/z113.015 28。基于上述裂解規律,實現了蘋果中苯脲類農藥的非靶向篩查。