十二烷基三甲基溴化銨在磷灰石與鉀長石浮選分離中的捕收作用與機理
俞豪勇,朱陽戈,李松清,胡曉星
北京礦冶研究總院 礦物加工科學與技術國家重點實驗室,北京102628
引言
由于世界總人口的不斷增長,食品生產的迫切需求加劇了土地的高強度利用,進而促進了對化肥需求的長期增長[1-2]。作為磷肥的主要原料,磷礦資源開發利用受到了廣泛關注。磷灰石是一種具有六方晶系結構的磷酸鹽礦物,是富磷沉積巖礦床中的重要經濟礦物。沉積巖中常含有長石、石英等共伴生硅酸鹽雜質礦物,嚴重降低了磷礦石中磷灰石品位,使其無法直接用作化肥生產,因此通常需要對磷灰石進行選礦以提高磷礦品質[3-4]。隨著磷礦礦石性質的日益復雜,如何將磷灰石從硅酸鹽等脈石礦物中高效分離成為亟待解決的關鍵問題[5-7]。
為了實現硅質磷灰石的浮選分離,通常采用陰離子捕收劑正浮選法實現磷灰石與硅酸鹽脈石的分離[8-10],其中脂肪酸類捕收劑在磷礦正浮選中應用較為普遍。但脂肪酸捕收劑一般不耐硬水,在低溫條件下需升溫乳化導致選別成本升高,限制了其應用。與正浮選相比,使用陽離子捕收劑的反浮選更符合浮少抑多的原則[11],因而引起廣泛關注[12-14]。黃志強等[15]針對磷灰石反浮選合成了新型捕收劑N,N'-雙(十二烷基二甲基)-1,4-丁烷二溴化二銨(BDBD)作為硅酸鹽的捕收劑,結果表明,相較于常規胺類捕收劑,新型捕收劑具有更好的選擇性,精礦指標更好。劉鳴等人[16]采用醚多胺T609作捕收劑,通過反浮選工藝最終獲得了精礦P2O5品位33.64%、回收率為72.73%的良好指標。Pawlik M等[17]通過研究發現,季銨鹽捕收劑相較于傳統捕收劑選擇性更好,可以降低磷尾礦中P2O5品位。為深入研究硅質磷礦反浮選脫硅過程,本文考察了季銨鹽捕收劑十二烷基三甲基溴化銨(DTAB)對磷灰石和鉀長石的捕收性能與機理,以期為硅質低品位磷礦的開發提供借鑒。
1 樣品、藥劑與試驗方法
1.1 樣品與藥劑
磷灰石和鉀長石的單礦物樣品采自湖北宜昌,經過粉碎、研磨和篩分后獲得粒徑為-0.074 +0.038 mm的粉末樣品,用于微浮選試驗和微量熱研究。用于FTIR分析、Zeta電位測量和XPS分析的樣品研磨至約-20 μm。
磷灰石和鉀長石的化學成分如表1所示。結果表明,所制備的磷灰石和鉀長石礦物樣品純度較高,滿足試驗要求。

表1 磷灰石和鉀長石的化學成分 /%
捕收劑DTAB[C12H25(CH3)3NBr]為化學純,化學結構如圖1所示。H3PO4和NaOH為pH值調整劑,試驗用水為去離子水(ρ=18.3 μS/cm)。
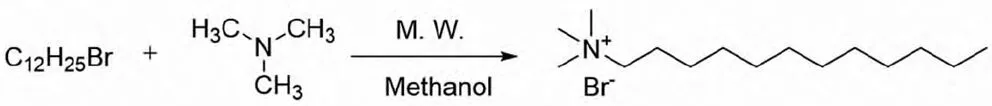
圖1 DTAB的化學結構
1.2 試驗方法
1.2.1 單礦物及人工混合礦浮選
使用XFG型(中國長春)浮選機(葉輪轉速為1 500 r/min)對單礦物樣品進行了浮選試驗。首先,將2 g礦物樣品置于40 mL浮選槽內;加入去離子水后攪拌1 min,向礦漿中添加pH調整劑(NaOH或H3PO4)以達到所需的pH值;隨后加入捕收劑攪拌3 min。每次浮選試驗進行5 min。浮選完成后,對獲得的泡沫與底流產品經過濾、干燥和稱重,計算回收率。對于人工混合礦浮選中,首先將磷灰石和鉀長石按照質量比31混合得到人工混合礦樣品,后續浮選過程與單礦物相同。
1.2.2 Zeta電位測定
采用顯微電泳法測量懸浮液中礦物表面的Zeta電位。試驗方法為:將礦物磨至粒徑小于2 μm,每次稱樣30 mg置于燒杯中,加入50 mL的蒸餾水并調節溶液pH值,按照與浮選試驗相同的調漿條件加藥劑,用磁力攪拌器攪拌3 min后在Zetasizer Nano Zs90分析儀上進行礦物表面ζ電位測量。測量重復三次取平均值。
1.2.3 微量熱測定
微量熱測定可通過礦物與捕收劑作用的凈反應熱量化其反應程度。在30 ℃恒溫環境中,使用SETARAM C80量熱計進行微量熱測量。每次測量前,100 mg礦物樣品和3.6×10-5mol/L DTAB分別放入量熱計池的兩個隔間中,兩個隔間由圓形聚四氟乙烯(PTFE)薄膜隔開。待量熱計基線完全穩定后,用可移動桿打破礦物顆粒與捕收劑之間的隔膜。測量過程中,在溫度穩定性為±0.000 1 ℃的基礎上保持±0.12 μW的基線。
1.2.4 紅外光譜分析
紅外光譜測試在Spectrum one傅立葉變換紅外光譜儀上進行測定。采用KBr壓片,測量范圍4 000~400 cm-1。紅外分析樣品制備過程如下:每次稱取2 g礦樣給入浮選槽,調節礦漿pH值后加入適量的藥劑,充分攪拌后固液分離,用相同pH值的蒸餾水溶液洗滌礦物兩次,所得樣品在真空干燥箱內60 ℃以下烘干,進行紅外光譜檢測。
1.2.5 X射線光電子能譜分析
每次稱取礦樣2 g,按照測試要求,根據相應單礦物浮選試驗一致的藥劑條件調漿、加藥,用離心機在3 500 r/min轉數下離心10 min后進行固液分離,并將離心后的固體礦物用蒸餾水反復清洗、攪拌再分離兩次,最后于真空干燥箱內60 ℃以下烘干,采用Thermo-ESCALAB 250XI型X射線光電子能譜儀檢測。
1.2.6 分子動力學模擬
為了比較十二烷基三甲基溴化銨在磷灰石和鉀長石表面浮選吸附過程中的異同,采用DFT計算的方法,初步構建了十二烷基三甲基溴化銨在磷灰石表面和鉀長石表面的吸附模型。在Material Studio軟件中,使用DMol3模塊,采用GGA-PW91泛函,幾何優化收斂標準如下:能量的收斂閾值為1.0×10-4Ha;原子位移的最大值為0.05 ?(1 ?=0.1 nm);原子間作用力的收斂閾值為0.02 Ha/?;SCF閾值為1.0×10-4Ha;電子處理方式為DSPP;DIIS size為6;smearing 值為0.005 Ha。
2 磷灰石與鉀長石的浮選行為
2.1 DTAB作用下磷灰石與鉀長石的可浮性
2.1.1 pH值對礦物可浮性的影響
在十二烷基三甲基溴化銨(DTAB)用量設定為3.0×10-5mol/L的條件下,考察了礦漿pH值對礦物可浮性的影響,試驗結果見圖2。從圖中可以看出,在弱酸性環境中,隨著pH值的上升,鉀長石回收率逐漸增大,在pH值6~11的區間里鉀長石回收率均在80%以上;而磷灰石則在2~12的pH范圍內幾乎不上浮。可見在pH值區間為5~11的弱酸性至堿性范圍中, DTAB對兩種礦物體現出良好的選擇性捕收作用。

圖2 pH值對鉀長石與磷灰石浮選的影響
2.1.2 DTAB用量對礦物可浮性的影響
在礦漿pH值為9.0時,DTAB用量對礦物的可浮性見圖3。由圖3可以看出,隨著用量的上升,鉀長石回收率逐漸上升,而磷灰石則幾乎無法上浮,當DTAB用量達到3.0×10-5mol/L以上時,二者可浮性差異較大。
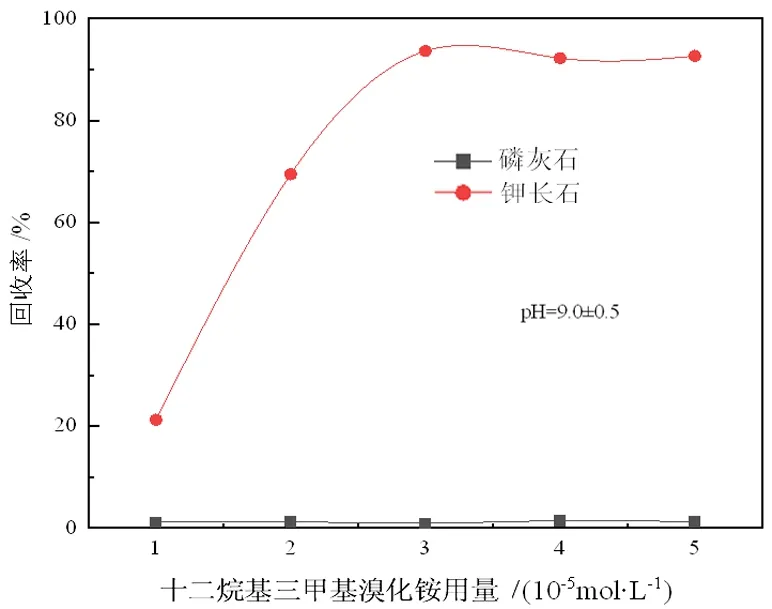
圖3 DTAB用量對鉀長石與磷灰石浮選回收率的影響
2.2 人工混合礦浮選
單礦物浮選試驗結果表明,DTAB為捕收劑時,磷灰石和鉀長石的可浮性差異較大,為進一步考察DTAB對二者的選擇性分離作用,進行了人工混合礦浮選試驗,試驗結果見表2。試驗過程中DTAB用量為3×10-5mol/L,礦漿pH值為9.0。人工混合礦浮選試驗最終獲得P2O5品位和回收率分別為34.85%和91.46%的磷精礦,精礦中Al2O3的含量為1.52%,表明DTAB具有良好的選擇性,可以實現鉀長石和磷灰石的選擇性分離。

表2 人工混合礦浮選試驗結果 /%
3 作用機理
3.1 Zeta 電位分析
在DTAB用量為3.0×10-5mol/L的條件下,通過Zeta電位測量考察了磷灰石和鉀長石在不同pH值環境中的藥劑吸附情況,試驗結果見圖4。如圖4所示,在試驗pH值區間, DTAB作用前后磷灰石的Zeta電位變化較小,表明在該pH值區間內,DTAB的吸附較弱;而對于鉀長石,其Zeta電位在試驗pH區間表面均荷負電,DTAB作用后Zeta電位明顯升高,表明陽離子捕收劑DTAB在鉀長石表面可通過靜電作用吸附在鉀長石表面,這與浮選結果吻合。

圖4 pH值對鉀長石與磷灰石Zeta電位的影響
3.2 微量熱測定
物理與化學反應的進行都伴隨著熱量的交換,而通過比不同反應間熱量交換的差異可以表征反應的強弱[18-20]。在本節中,我們使用微量熱分析來比較DTAB在磷灰石和鉀長石表面的吸附程度。
如圖5所示,兩種礦物與DTAB作用的反應熱差異較大,磷灰石的凈反應熱QDTAB(0.617 J/g)遠小于鉀長石的凈反應熱QDTAB(15.674 J/g),表明DTAB與鉀長石的反應劇烈程度遠大于磷灰石,這與浮選結果相吻合。

圖5 鉀長石與磷灰石的微量熱結果
3.3 紅外光譜分析
通過對DTAB作用前、后的磷灰石和鉀長石進行紅外光譜分析,研究其吸附機理。在圖6(a)DTAB的FTIR光譜中,2 923 cm-1和2 848 cm-1處為-CH2對稱和不對稱拉伸頻率,在1 654 cm-1處的特征峰歸屬于vR2NH,而1 050 cm-1處歸屬于 C-N 的伸縮振動[21]。
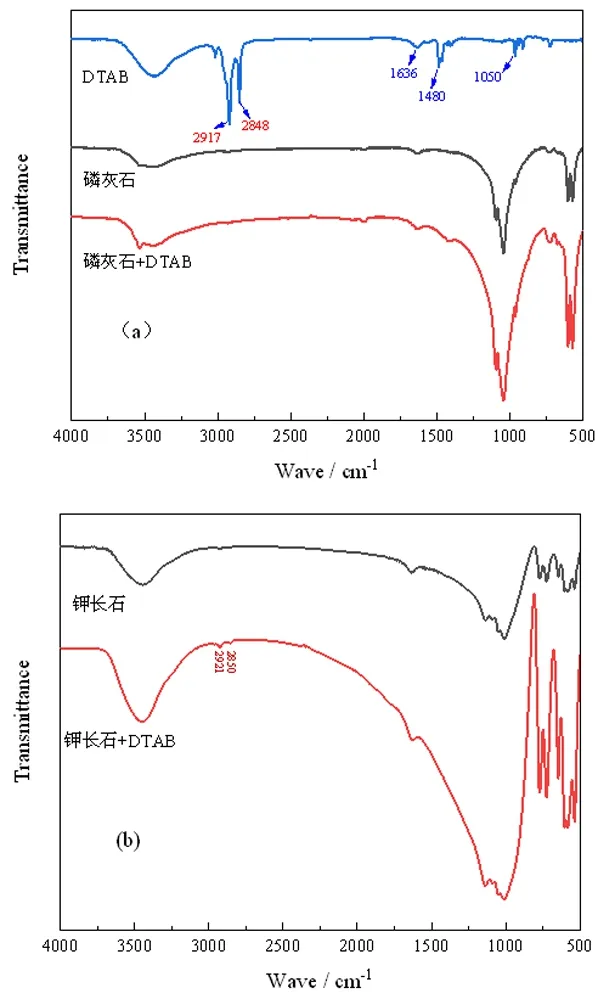
圖6 磷灰石(a)和鉀長石(b)與DTAB作用前后紅外光譜
如圖6(b)所示,在與DTAB作用后,磷灰石表面未檢測到DTAB的特征吸收峰,表明DTAB在磷灰石表面的吸附較弱,這一結果與浮選試驗結果一致。在鉀長石表面,DTAB處理后鉀長石的光譜中在2 923 cm-1和2 848 cm-1處出現-CH特征峰,表明DTAB在鉀長石表面發生物理吸附。
3.4 X射線光電子能譜分析
表3為DTAB處理前后的磷灰石和鉀長石表面上各種元素的相對含量。如表3所示,與DTAB作用后,磷灰石和鉀長石表面元素的分布密度發生不同程度的變化。與DTAB作用后,磷灰石表面N原子相對含量較低(0.12%)明顯低于鉀長石表面N原子相對含量(0.31%),證明DTAB在鉀長石表面的吸附量顯著大于磷灰石。
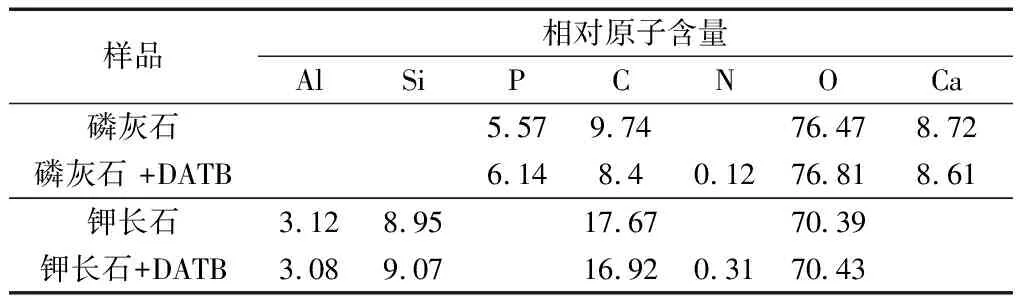
表3 與DTAB作用前后鉀長石和磷灰石表面的相對原子含量 /%
3.5 分子動力學模擬
采用分子動力學模擬分析了DTAB在兩種礦物表面的吸附。構建礦物表面模型過程中,磷灰石與鉀長石均取(001)面為實際解理面[22-23];十二烷基三甲基溴化銨溶液中,溴離子易解離,長鏈離子作為主要的作用單元,但長鏈離子作用基團中的核心N原子被3個-CH3基團包裹在中間,使長鏈離子與兩種礦物表面均存在較為明顯的空間位阻效果(位阻情況見圖7)。實際上,十二烷基三甲基溴化銨很難以兩個核心作用原子N-O之間的常態原子半徑之和1.36 ?為距離尺度,直接形成較強的化學吸附。

圖7 十二烷基三甲基溴化銨在鉀長石(001)面(左)和磷灰石(001)面(右)的空間位阻情況
為了驗證目標藥劑與不同礦物的吸附效果與吸附類型,測試了十二烷基三甲基溴化銨在磷灰石和鉀長石表面,在近、中、遠三種距離模式下的吸附結果,構建的基礎模型見圖8,數據見表4。

圖8 十二烷基三甲基溴化銨在鉀長石(001)面(左)和磷灰石(001)面(右)的基礎吸附模型

表4 十二烷基三甲基溴化銨在不同表面、不同距離條件下的吸附結果
如表4所示,十二烷基三甲基溴化銨在磷灰石和鉀長石表面的吸附計算說明,在近間距條件下,十二烷基三甲基溴化銨明顯受空間位阻和非極性基的排斥作用影響,長鏈離子均被明顯排斥較遠;在中間距條件下,排斥距離較短;在遠間距條件下,相比于常態原子半徑之和N-O 1.36 ?,作用后間距較大,已超出化學吸附作用范疇,但在靜電作用的吸引下,拉近了有限的距離。這組數據證明了在近、中、遠作用間距上,DTAB在礦物表面均存在靜電作用。在磷灰石表面,十二烷基三甲基溴化銨被排斥的效果更加突出,在鉀長石表面的吸附距離要明顯低于在磷灰石表面的吸附距離,這說明十二烷基三甲基溴化銨在鉀長石表面的吸附效果明顯強于在磷灰石表面的吸附效果。
4 結論
(1)季銨鹽捕收劑十二烷基三甲基溴化銨(DTAB)作捕收劑時,在pH值區間5~11范圍內鉀長石與磷灰石可浮性差異較大,人工混合礦浮選試驗可以獲得P2O5品位34.85%、回收率91.46%的磷精礦,精礦中Al2O3的含量為1.52%,表明DTAB可以實現鉀長石和磷灰石的選擇性分離。
(2)Zeta電位、微量熱分析、XPS測定、紅外光譜及分子模擬結果表明,DTAB在鉀長石和磷灰石表面吸附存在較大差異,DTAB可通過靜電作用在鉀長石表面吸附,而在磷灰石表面難以發生吸附。

