菱鎂礦氣泡模板法制備三水碳酸鎂晶體及其生長機理
劉珈伊,王余蓮,時天驕,王琪浩,朱益斌,張俊,于雨,袁志剛
沈陽理工大學 材料科學與工程學院,遼寧 沈陽 110159
引 言
三水碳酸鎂是一種重要的碳酸鎂水合物,主要以天然礦物、海水及鹽湖鹵水等為鎂源,二氧化碳、碳酸鹽等為碳源,經一系列反應制得,其對海洋中二氧化碳礦化和氯化鎂鹵水再利用具有重要意義[1-4]。由于純度高、熱分解溫度較低,三水碳酸鎂可作為制備硫酸鎂、硝酸鎂和氧化鎂等精細鎂鹽產品的前驅體。在熱分解過程中,三水碳酸鎂生成不燃燒的氧化鎂,釋放二氧化碳和水蒸氣,帶走大量熱量。因此,三水碳酸鎂是一種優(yōu)良的無機阻燃劑[5-7]。此外,因其穩(wěn)定性較為優(yōu)異,三水碳酸鎂可作為模板,制備氧化鋁、二氧化硅微米管與分級二氧化硅-二氧化鈦復合物。因其優(yōu)異的物理、化學和機械性能,三水碳酸鎂晶須可作為增強填料廣泛用于塑料、涂料、橡膠、玻璃、陶瓷和印刷工業(yè)領域[8-9]。
目前,制備三水碳酸鎂晶體的方法主要有沉淀法、水熱法、碳酸化法、微波法等。王余蓮等人[10]以MgCl2與(NH4)2CO3為原料,葡聚糖為晶形控制劑,在60 ℃反應3 h,合成了平均直徑為8 μm、比表面積為23.96 m2/g的多孔球狀MgCO3·3H2O晶體,并探究了葡聚糖作用下多孔結構構筑機理與生長模型。Skliros等人[11]在室溫條件下,將Na2CO3以3 mg/min的恒定速率加入至MgCl2·6H2O溶液中,混合均勻,再以1 000 r/min的轉速攪拌1 h,靜置24 h,獲得花環(huán)狀MgCO3·3H2O晶體。Harrison等人[12]利用K2CO3和MgCl2·6H2O為原料于恒溫間歇反應器中反應,獲得棒狀MgCO3·3H2O晶體。Cao等人[13]將純鎂樣品(99.99 wt%)經去離子水清洗、酒精脫脂、冷壓縮空氣干燥等預處理操作,再將其懸浮于高壓釜中,并通入高純度CO2,制備了傘狀結構MgCO3·3H2O保護膜。Cheng等人[14]以MgCl2·6H2O與NH3·H2O為原料,CO2為碳源,當反應溫度為40 ℃、反應時間為2 h、無水乙醇用量為30%時,制備了長度為25~30 μm、直徑為2~3 μm的光滑棒狀MgCO3·3H2O晶體;當乙醇用量超過40%時,棒狀MgCO3·3H2O開始溶解,形成更穩(wěn)定的花狀4MgCO3·Mg(OH)2·4H2O晶體。Yang等人[15]以MgCl2和Na2CO3為原料,在十二烷基硫酸鈉(SDS)作用下合成長徑比為55的MgCO3·3H2O晶須。高玉娟等人[16]以MgCl2·6H2O與NH4HCO3為原料,40 ℃下反應50 min合成棒狀MgCO3·3H2O晶體;研究發(fā)現(xiàn)反應物濃度增大,MgCO3·3H2O晶體由放射狀向棒狀轉變。閆平科等人[17-18]以MgCl2·6H2O與MgSO4·7H2O為原料,以NH4HCO3作為碳源,以Na2HPO4、AlCl3、SDBS、CTAB、AS等為表面活性劑,制備了棒狀、魚翅狀等多形貌MgCO3·3H2O晶體。吳丹等人[19]以MgCl2·6H2O和NH4HCO3為原料,通過低溫水熱法,于45~50 ℃反應70 min,陳化180 min,合成長徑比為29.6的一維針狀MgCO3·3H2O晶體。陳娟等人[20]以MgCl2和NH4HCO3為原料,通過水熱法制備長徑比為13~42的MgCO3·3H2O晶須,并證實晶須生長符合臺階生長機制。
綜上所述,研究者大多以可溶性鎂鹽和碳酸鹽等化學試劑為原料制備MgCO3·3H2O晶體,但上述工藝成本較高,難以實現(xiàn)工業(yè)化生產,且會產生含氯離子廢液,易污染環(huán)境。而以天然礦物為原料制備MgCO3·3H2O晶體,其原料廉價易得,工藝簡單,有利于工業(yè)放大。王余蓮等[21-24]以菱鎂礦為原料,經煅燒制得MgO,通過水化、碳化、熱解,合成不同形貌和長徑比的棒狀MgCO3·3H2O晶體,并研究了其結晶動力學;熱解過程中通過加入無機鹽類添加劑,獲得不同長徑比與光潔度的棒狀MgCO3·3H2O晶體,并深入探究了CaCl2對MgCO3·3H2O結晶過程的作用機理。Ding等[25]以天然滑石為原料,利用鹽酸酸浸獲得酸浸溶液,并將NH3·H2O和CO2加入至酸浸溶液中,60 ℃時制備了長為19.31 μm、直徑為0.96 μm的棒狀MgCO3·3H2O晶體。Hamilton等[26]在堆浸模擬試驗中,將尾礦樣品與酸溶液填充至聚氯乙烯柱中,再以0.06 L/min的流速通入N2(含10% CO2)至柱底部下方的空腔處,反應672 h,獲得以硫酸鹽沉淀物與棒狀MgCO3·3H2O晶體形式存在的產物。陳敏等人[27]以MgO含量為45.56%的低品位菱鎂礦為原料,采用水化碳酸化法,在50 ℃下熱解合成MgCO3·3H2O晶體;通過改變添加劑種類,制備了棒狀MgCO3·3H2O晶體。歐龍等人[28]以白云石為原料,60 ℃熱解Mg(HCO3)2,并通入空氣,制備長度為40~80 μm、長徑比為6~15的棒狀MgCO3·3H2O晶體。
綜上所述,目前國內外關于三水碳酸鎂的研究已取得豐碩成果。然而,上述研究鮮有利用氣泡輔助制備三水碳酸鎂晶體。本研究以菱鎂礦為原料制備重鎂水,并在其熱解過程中,引入氣泡制備不同形貌三水碳酸鎂晶體,主要探究氣泡種類、氣泡大小、氣泡通入時間對晶體物相組成和形貌的影響,并深入分析氣泡輔助下三水碳酸鎂晶體生長機理。
1 試驗
1.1 試驗原料
原料為遼寧岫巖菱鎂礦,經煅燒獲得輕燒氧化鎂粉。菱鎂礦與輕燒鎂粉的化學組成分析結果如表1所示;CO2、N2、空氣,沈陽景泉氣體廠;去離子水,實驗室自制。

表1 菱鎂礦與其煅燒所得輕燒氧化鎂的化學組成 /%
由表1可知,菱鎂礦中MgO含量為47.61%,純度相對較高;輕燒氧化鎂粉中MgO含量為82.70%,主要雜質為SiO2和CaO。
1.2 三水碳酸鎂晶體制備
將輕燒氧化鎂粉(-74 μm)與70~90 ℃去離子水在反應器中混合后置于60 ℃水浴中攪拌180 min,獲得水化溶液。再將CO2通入至水化溶液中,冰水水浴下碳化,待溶液pH值為7.75左右時,停止碳化,抽濾獲得Mg(HCO3)2溶液。
量取一定體積Mg(HCO3)2溶液置于反應器中,分別引入CO2、空氣與N2,于60 ℃攪拌反應20~120 min。抽濾、洗滌,將所得濾餅于恒溫干燥箱中干燥64 h,獲得白色粉末。
1.3 檢測與表征
利用UltimaⅣ型X射線衍射儀(XRD,Cu Kα,λ=0.154 1 nm)進行物相分析,管電壓為30 kV,管電流為20 mA,掃描范圍10°~90°,掃描速度8(°)/min;采用S-3400N型掃描電子顯微鏡(SEM,加速電壓20 kV)觀察產物微觀形貌;借助Escalab 250Xi型X光電子能譜儀(XPS,單色化X射線源,Al陽極)對樣品的化學組成與元素價態(tài)進行分析,以污染碳峰的C 1s(284.6 eV)為定標標準。
2 結果與討論
2.1 氣泡種類對三水碳酸鎂晶體制備的影響
試驗考察三種氣泡(CO2、空氣、N2)對三水碳酸鎂晶體制備的影響。固定反應溫度為60 ℃,氣泡尺寸為1 μm,氣泡通入時間為60 min。圖1和圖2為通入不同種類氣泡時所得產物的XRD圖譜與SEM圖像。
從圖1中可以看出,通入不同種類氣泡,所得產物衍射峰全部與三水碳酸鎂(MgCO3·3H2O,JCPDS 70-1433)標準特征峰一致,表明產物均為三水碳酸鎂晶體。通入空氣或CO2氣泡時,產物衍射峰強度高,基底平滑,且衍射峰對稱性好,表明此條件下三水碳酸鎂晶體結晶良好[16];N2氣泡作用下,所得產物衍射峰強度明顯降低,峰變寬,表明產物結晶度較差。

圖1 不同氣泡輔助下所得產物的XRD圖譜

(a) CO2;(b) 空氣;(c) N2
如圖2所示,CO2氣泡輔助下,所得產物為長徑比較小的光滑棒狀三水碳酸鎂晶體,其中棒狀晶體之間緊密貼合,并排生長(如圖2a)。根據重鎂水熱分解反應方程式(式1)可知,通入CO2氣泡會抑制重鎂水分解,阻礙反應正向進行,故所得產物中棒狀晶體長徑比較小。空氣氣泡輔助下,所得產物為長徑比較大的表面光滑的棒狀三水碳酸鎂晶體(如圖2b)。這是因為:一方面通入空氣會加快CO2逸出[28],促進反應正向進行;另一方面,通入空氣增大氣相與液相的接觸面積,在一定程度上提高反應速率,故二者共同作用下,所得棒狀晶體長徑比較大。N2氣泡輔助下,所得產物為光滑棒狀晶體和放射狀晶體;放射狀晶體表面較為粗糙,生長出細小棒狀分枝(如圖2c)。
重鎂水熱分解反應方程式:
Mg(HCO3)2+2H2O→MgCO3·3H2O↓+CO2↑
(1)
綜上可知,通入CO2或空氣氣泡時,所得產物形貌無明顯改變,均為常規(guī)光滑棒狀三水碳酸鎂晶體;而通入N2氣泡時,產物形貌變化明顯,表明熱解過程中引入N2氣泡對產物形貌具有調控作用。因此進一步研究N2氣泡對三水碳酸鎂晶體結晶過程的影響。
2.2 N2氣泡尺寸對三水碳酸鎂晶體制備的影響
保持其他條件不變,N2氣泡通入時間為60 min,反應溫度為60 ℃,考察不同尺寸 (1、5、10、20、50 μm) N2氣泡對三水碳酸鎂晶體形貌的影響。圖3為通入不同尺寸N2氣泡時所得產物的SEM圖像。

(a) 1 μm; (b) 5 μm; (c) 10 μm; (d) 20 μm; (e) 50 μm
從圖3可以看出,氣泡尺寸為1 μm時,所得產物由光滑棒狀與粗糙棒狀晶體組成,粗糙棒狀晶體表面附著許多棒狀分枝,主干與分枝之間相互搭建成放射狀晶體(如圖3a)。氣泡尺寸為5 μm時,產物均為棒狀晶體,其長短、粗細不一,短粗棒狀晶體表面較粗糙,附著許多細小晶須狀與不規(guī)則片狀晶體(如圖3b)。氣泡尺寸增加至10 μm時,產物由表面粗糙的短粗棒狀、光滑棒狀以及不規(guī)則片狀晶體組成,短粗棒狀晶體表面除附著晶須狀與不規(guī)則片狀晶體外,還生長出新的棒狀分枝(如圖3c)。氣泡尺寸為20 μm時,粗糙棒狀晶體明顯減少,產物多為光滑棒狀晶體,但其長短不一,且粒徑不均勻(如圖3d)。氣泡尺寸為50 μm時,產物多為光滑棒狀晶體,僅有少量粗糙棒狀晶體(如圖3e)。綜上所述,N2氣泡尺寸對晶體結晶形貌有著重要影響,且隨著N2氣泡尺寸增大,晶體形貌由不規(guī)則多面體狀向棒狀轉變,棒狀晶體表面由粗糙變光滑。
2.3 N2氣泡通入時間對三水碳酸鎂晶體制備的影響
N2氣泡尺寸為1 μm時,進一步考察其通入時間(20、40、60、80、120 min)對產物形貌的影響。
圖4為N2氣泡通入不同時間所得產物的SEM圖像。觀察圖4可知,氣泡通入時間為20 min,晶體粒徑不均、長短不一,產物由光滑棒狀、不規(guī)則片狀、無定形顆粒組成(如圖4a)。氣泡通入40 min時,粗糙棒狀晶體增加,產物由細長光滑棒狀與粗糙棒狀晶體組成,其平均長度約為50 μm,直徑為2~10 μm;粗糙棒狀晶體表面附著不規(guī)則碎片與棒狀晶須(如圖4b)。氣泡通入時間為60 min時,所得產物由光滑棒狀與粗糙棒狀晶體組成,后者表面存在棒狀分枝,其貫穿于晶體主干或附著在晶體主干上,主干與分枝之間相互搭建成放射狀晶體(如圖4c)。氣泡通入時間延長至80 min時,產物由光滑棒狀、放射狀與不規(guī)則多面體組成(如圖4d)。通氣120 min時,產物均為不規(guī)則多面體狀與放射狀晶體(如圖4e)。

(a) 20 min; (b) 40 min; (c) 60 min; (d) 80 min; (e) 120 min
綜上所述,隨著N2氣泡通入時間延長,所得產物形貌由棒狀向放射狀與不規(guī)則多面體狀轉變。
2.4 XPS分析
綜上可知,N2氣泡作用下,所得三水碳酸鎂晶體為放射棒狀以及不規(guī)則多面體狀,結晶度較差,故利用XPS對其化學價態(tài)進一步分析,結果如圖5所示。
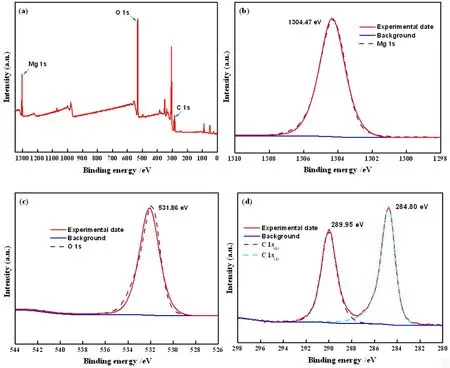
圖5 N2氣泡輔助下產物的XPS全圖譜和Mg 1s、O 1s、C 1s高分辨譜圖
圖5(a)為N2氣泡輔助下所得產物的XPS全譜圖。由圖可知,產物主要由Mg 1s、O 1s、C 1s構成。Mg 1s高分辨XPS譜如圖5(b)所示,Mg元素有一個特征峰,其結合能為1 304.47 eV。結合XPS數據庫分析可知,這與MgO的特征峰(1 304.5 eV)較為吻合。因此可確定產物中Mg元素是以Mg-O的形式存在。O 1s高分辨XPS譜圖如圖5(c)所示。由圖可見,O 1s峰形較為對稱,說明產物中可能只有一種結合態(tài)的氧,其價態(tài)是以O2-形式存在[29-30];結合XPS數據庫分析可知,圖中位于531.86 eV的峰對應于金屬碳酸鹽特征峰。圖5(d)所示為C 1s的高分辨XPS譜圖,結合XPS數據庫分析可知,位于電子結合能289.95 eV處C 1s(1)與284.80處C 1s(2)的特征峰分別與O-C=O鍵、與C-C鍵對應,其中O-C=O鍵的存在表明產物中可能存在碳酸根官能團,而C-C鍵則是被用于能量標定中的單質碳[31-32]。結合XRD表征結果,可進一步證明產物為MgCO3·3H2O。
3 N2氣泡輔助下三水碳酸鎂晶體生長機理研究
圖6為N2氣泡輔助下MgCO3·3H2O晶體生長示意圖。如圖6所示,基于負離子配位多面體理論,溶液中的Mg2+分別與CO32-基團中4個O原子、H2O中2個O原子通過[4+2]配位形成MgO6正八面體生長基元(如圖6a-6b)。MgO6正八面體生長基元通過共頂點的方式連接成長鏈狀結構[10,33]。長鏈狀結構中,由CO32-構成的平面三角形連接三個MgO6正八面體,兩個連接平面三角形頂點,另一個連接到平面三角形棱上(如圖6c)。根據鮑林規(guī)則,MgO6正八面體以共頂點、共棱和共面的連接方式形成生長面時,對應的晶體穩(wěn)定性與生長速率將依次降低。MgO6正八面體在[100]與[001]方向上,通過Mg-O鍵和C-O鍵以共頂點或共棱的方式連接,穩(wěn)定性與生長速度較低;而沿[010]方向,MgO6正八面體通過Mg-O鍵以共頂點方式連接,穩(wěn)定性高,生長速度最快,形成棒狀形貌[22,34-35](如圖6d)。反應時間延長,光滑棒狀三水碳酸鎂表面開始溶解,變得粗糙[36];為了減小粗糙表面的界面張力,大量N2氣泡將聚集此處[37-38](如圖6e)。隨著N2氣泡的不斷聚集,導致溶液中的離子匯聚至氣泡周圍,當溶液濃度達到過飽和度時,溶液中的離子發(fā)生反應,生成新的三水碳酸鎂晶核;以N2氣泡為泡界模板,晶體沿著氣泡表面生長形成新的棒狀三水碳酸鎂分枝[39-40](如圖6f)。最終,主干與新生成的棒狀分枝之間構筑成不規(guī)則多面體狀與放射狀形貌(如圖6g)。N2氣泡作為泡界模板時,氣泡表面呈圓弧狀;因晶體沿平面生長所需克服的能量勢壘遠小于沿曲面的,故三水碳酸鎂的生長總表現(xiàn)為一維棒狀,而非沿著氣泡圓弧狀表面形成彎曲狀形貌。

圖6 N2氣泡輔助下MgCO3·3H2O晶體生長示意圖
4 結論
(1)以菱鎂礦為原料,利用煅燒—水化—碳化法制備重鎂水,60 ℃熱解重鎂水過程中,分別通入CO2、空氣和N2氣泡,所得產物均為三水碳酸鎂晶體,但形貌稍有差異;當通入尺寸為1 μm的N2氣泡60~120 min時,獲得不規(guī)則多面體狀與放射狀三水碳酸鎂晶體。
(2)三水碳酸鎂晶體的生長基元為MgO6正八面體,沿[010]方向以共頂點方式緊密連接成長鏈,最終形成棒狀形貌。
(3)N2氣泡可充當泡界模板,誘導晶體沿能量勢壘低的平面生長成新的棒狀三水碳酸鎂晶體;N2氣泡作用下,新生成的棒狀晶體構筑成不規(guī)則多面體狀與放射狀三水碳酸鎂晶體。

