Up-to-7標準和米蘭標準對多發性肝細胞癌患者肝切除術后的預后預測價值分析
張宇,吳麗君,馬良,吳飛翔,向邦德,黎樂群△
我國肝細胞癌(hepatocellular carcinoma,HCC)的發病率較高,每年新發病例占全球50%以上[1-2]。目前,巴塞羅那肝癌(Barcelona clinic liver cancer,BCLC)分期系統是使用最廣泛的HCC分期系統[3-5]。在BCLC 分期系統中,參照米蘭標準將多發性HCC分為早期(BCLC-A 期)和中期(BCLC-B 期)[3]。我國《原發性肝癌診療規范》也參考了米蘭標準,將2~3個腫瘤且每個不超過3 cm的多發性HCC歸為中國肝癌臨床分期(China liver cancer staging,CNLC)Ⅰb期;將超越米蘭標準的多發性HCC歸為CNLCⅡa和CNLCⅡb 期[6]。米蘭標準是篩選HCC 患者進行肝移植手術的重要依據[4,7]。然而,Mazzaferro等[8]認為米蘭標準過于嚴格,通過分析1 556例接受肝移植治療的HCC 患者的預后與腫瘤大小、數目的關系,發現符合米蘭標準的患者與超越米蘭標準但符合up-to-7標準的患者有著相似的生存期,因此推薦采用up-to-7標準替代米蘭標準作為篩選HCC患者進行肝移植的依據。本研究擬比較up-to-7 標準和米蘭標準對多發性HCC 患者肝切除術后預后的預測能力。
1 資料與方法
1.1 一般資料 選取2006年1月—2013年10月于廣西醫科大學附屬腫瘤醫院肝膽外科接受肝切除術治療的252例多發性HCC 患者的臨床病理資料。納入標準:多發性HCC;接受HCC根治性切除術且術后病理證實為HCC。排除標準:合并大血管侵犯或肝外轉移;術前接受肝動脈化療栓塞、放療、射頻消融等抗腫瘤治療;合并嚴重的心肺腦疾病;合并其他惡性腫瘤。
1.2 治療方法和定義 252 例多發性HCC 患者均接受根治性肝切除術。多發性HCC的手術適應證參考我國《原發性肝癌診療規范》,即:腫瘤≤3個;腫瘤>3個,但腫瘤局限在同側半肝或可以局限切除者[6]。HCC根治性切除術定義為:完全切除術前和術中發現的所有病灶,且病理證實手術切緣無殘瘤的腫瘤細胞[9]。3個及以上的肝段的切除術定義為大范圍肝切除術。慢性乙型肝炎患者均接受規律抗病毒治療。
符合米蘭標準是指單個腫瘤不超過5 cm或2~3個腫瘤且每個不超過3 cm,同時無大血管侵犯和肝外轉移;超越米蘭標準是指單個腫瘤超過5 cm,或2~3個腫瘤且至少1個腫瘤超過3 cm,或腫瘤>3 個[3]。Up-to-7 標準的“7”指的是腫瘤數目+腫瘤最大直徑(cm)=7[8]。腫瘤數目+腫瘤最大直徑(cm)≤7 即為符合up-to-7 標準;腫瘤數目+腫瘤最大直徑(cm)>7即為超越up-to-7標準。
1.3 隨訪 術后囑患者定期返院隨訪。術后的前2 年,每3個月隨訪1次;此后每6個月隨訪1次,末次隨訪時間為2021年12月31日。在每次隨訪中,患者接受乙肝五項、甲胎蛋白(alpha-fetal protein,AFP)、肝腎功能、血常規、腹部增強CT或MRI等檢查。若患者在隨訪中出現腫瘤復發,根據患者復發時的腫瘤情況、肝功能狀態以及經濟情況,選擇進行二次手術、介入治療或分子靶向治療等。生存時間以手術日期至末次隨訪存活日期或者死亡日期計算;無瘤生存時間以手術日期至患者隨訪復發日期或者死亡日期計算。刪失:患者失訪,或患者在隨訪結束時未出現死亡或者腫瘤復發。
1.4 統計學方法 采用SPSS 23.0軟件和R軟件(版本3.4.4;http://www.r-project.org/)進行數據分析。符合正態分布的計量資料以均數±標準差(±s)表示,非正態分布的計量資料以中位數與四分位數[M(P25,P75)]表示;計數資料以例或例(%)表示。生存分析采用Kaplan-Meier法。單因素和多因素Cox回歸分析影響累積總生存率和無瘤生存率的獨立危險因素,單因素Cox 回歸分析中選擇P<0.15 的變量進入多因素Cox回歸模型。時間依賴的受試者工作特征(t-ROC)曲線和ROC曲線下面積(AUC)用于比較米蘭標準和up-to-7標準預測預后的準確性,AUC值越大表示該標準預測預后的準確度越高,t-ROC分析以R軟件完成[10-11]。P<0.05為差異有統計學意義。
2 結果
2.1 患者的一般特征 252 例多發性HCC 患者中,男222例(88.1%),女30例(11.9%);19.4%(49例)的患者年齡≥60歲;80.6%(203例)的患者年齡<60歲。88.8%(224 例)患者為乙肝相關性HCC。患者的總膽紅素、白蛋白、血小板計數、凝血酶原時間和谷草轉氨酶的水平分別為:12.4(8.6,17.0)μmol/L、(41±4)g/L、172(132,227)×109/L、12.8(12.0,13.7)s 和41(31,60)U/L。74.6%(188 例)的患者合并肝硬化,96.8%(244 例)的患者肝功能為Child-Pugh A 級,38.9%(98 例)的患者AFP ≥400 μg/L。患者腫瘤直徑為6(4,9)cm;腫瘤數目≥3 個的患者有96 例(38.1%),其余156 例(61.9%)患者腫瘤數目為2 個。有21.8%(55例)的患者接受了大范圍肝切除術。符合米蘭標準的多發性HCC 患者有36 例(14.3%),超越米蘭標準的有216 例(85.7%);符合up-to-7 標準的有92 例(36.5%),超越up-to-7 標準的有160 例(63.5%)。
2.2 不同標準分層后患者術后的累積總生存率比較 經過中位56(42,69)個月的隨訪,有116例患者死亡,162 例患者出現腫瘤復發。米蘭標準符合組和超越組累積總生存率的差異無統計學意義(P>0.05),見表1、圖1A。Up-to-7標準符合組和超越組累積總生存率的差異有統計學意義(P<0.05),見表1、圖1B。Up-to-7標準對累積總生存率具有更好的區分度。
2.3 不同標準分層后患者術后的累積無瘤生存率的比較 米蘭標準符合組和超越組累積無瘤生存率的差異無統計學意義(P>0.05),見表1、圖2A。Upto-7標準符合組和超越組累積無瘤生存率的差異有統計學意義(P<0.01),見表1、圖2B。Up-to-7標準對累積無瘤生存率具有更好的區分度。
2.4 影響多發性HCC 患者術后累積總生存率和無瘤生存率的多因素分析 以年齡(≥60 歲=1,<60歲=0)、總膽紅素、白蛋白、血小板計數、凝血酶原時間、AST、AFP(≥400μg/L=1,<400μg/L=0)、肝硬化(是=1,否=0)、大范圍肝切除(是=1,否=0)、米蘭標準(符合=0,超越=1)及up-to-7標準(符合=0,超越=1)為自變量,以生存和復發結局(死亡或復發=1,刪失=0)為因變量,分別進行累積總生存率和無瘤生存率的單因素Cox 回歸分析,并將單因素分析中P<0.15 的變量納入后續Cox 多因素分析。Cox 多因素分析結果顯示:年齡≥60 歲、AFP≥400 μg/L 和超越up-to-7 標準是影響多發性HCC 患者術后累積總生存率的獨立危險因素,見表2、3;較高水平AST 和超越up-to-7標準是影響多發性HCC患者術后累積無瘤生存率的獨立危險因素,見表4、5。
2.5 t-ROC 曲線分析比較不同標準預測多發性HCC 患者術后累積總生存率和無瘤生存率的準確性 Up-to-7標準預測多發性HCC患者術后累積總生存率和無瘤生存率的AUC 值在術后的各個時間點均優于米蘭標準,見圖3。
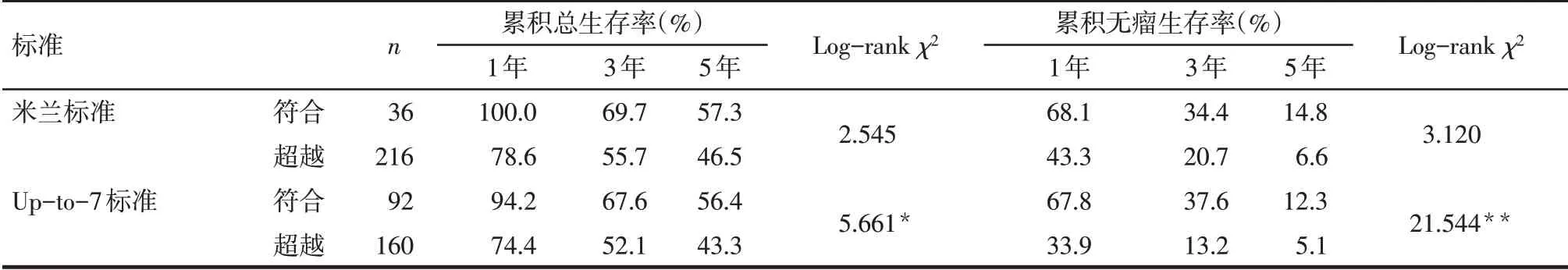
Tab.1 Overall survival and disease-free survival in multifocal HCC patients stratified by Milan criteria and up-to-7 criteria表1 米蘭標準和up-to-7標準分層后患者的累積總生存率和無瘤生存率
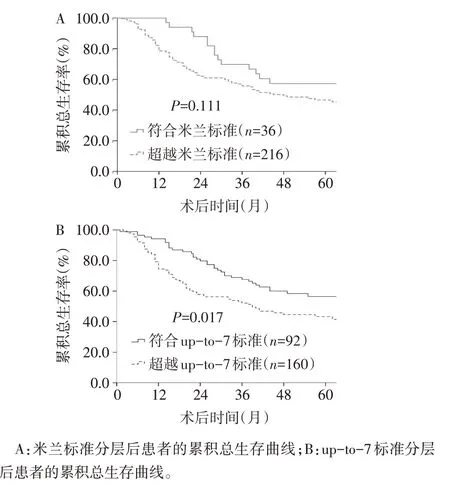
Fig.1 Overall survival curves stratified by Milan criteria and up-to-7 criteria圖1 米蘭標準和up-to-7標準分層后患者術后的累積總生存曲線
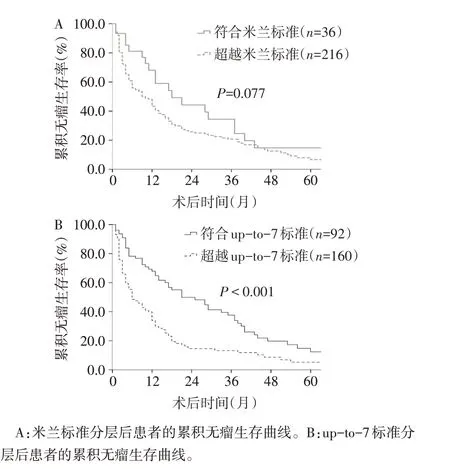
Fig.2 Disease-free survival curves stratified by Milan criteria and up-to-7 criteria圖2 米蘭標準和up-to-7標準分層后患者術后的累積無瘤生存曲線
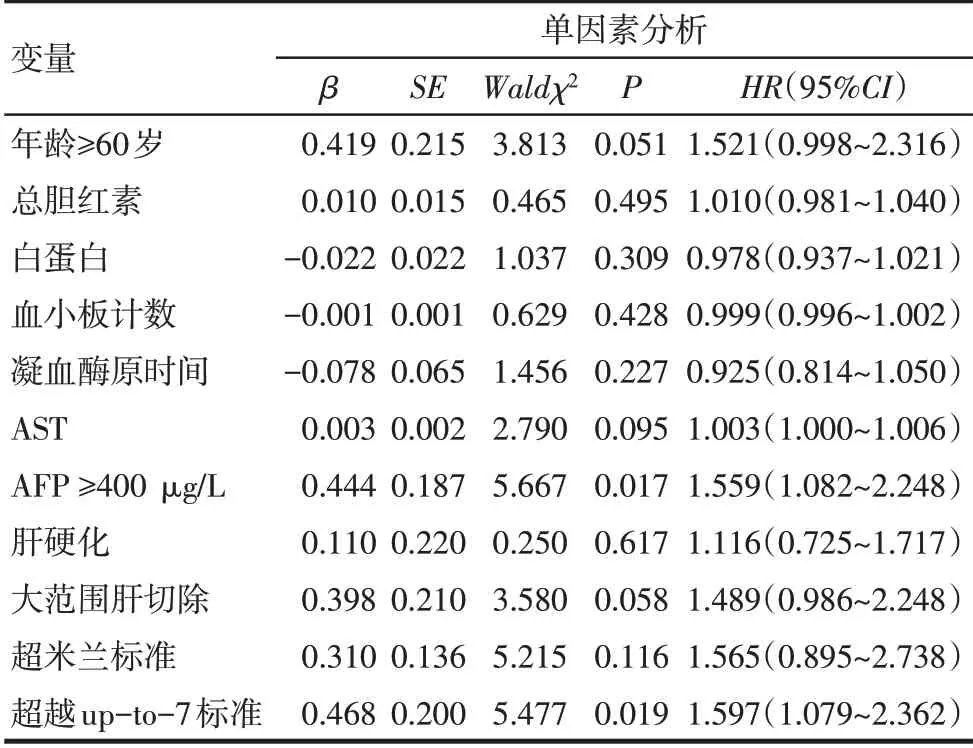
Tab.2 Univariate Cox regression analyses of factors affecting overall survival in patients with multifocal HCC表2 影響多發性肝細胞癌患者術后累積總生存率的單因素Cox回歸分析
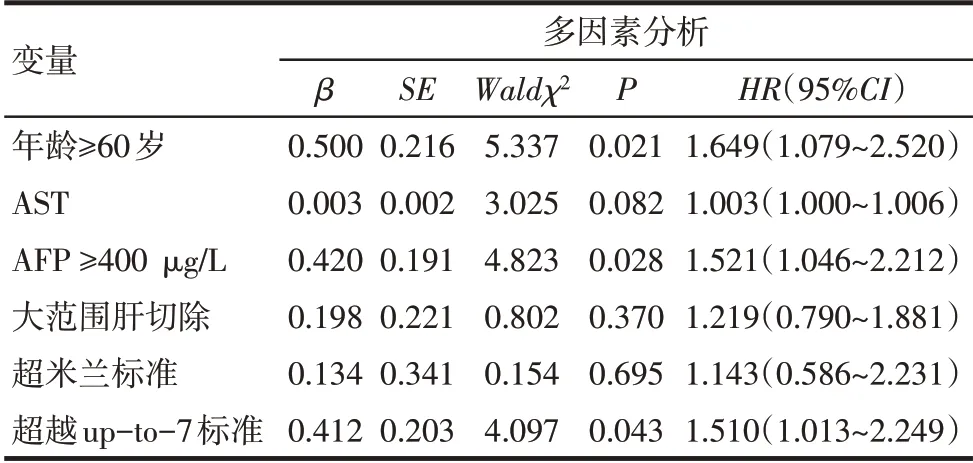
Tab.3 Multivariate Cox regression analyses of factors affecting overall survival in patients with multifocal HCC表3 影響多發性肝細胞癌患者術后累積總生存率的多因素Cox回歸分析
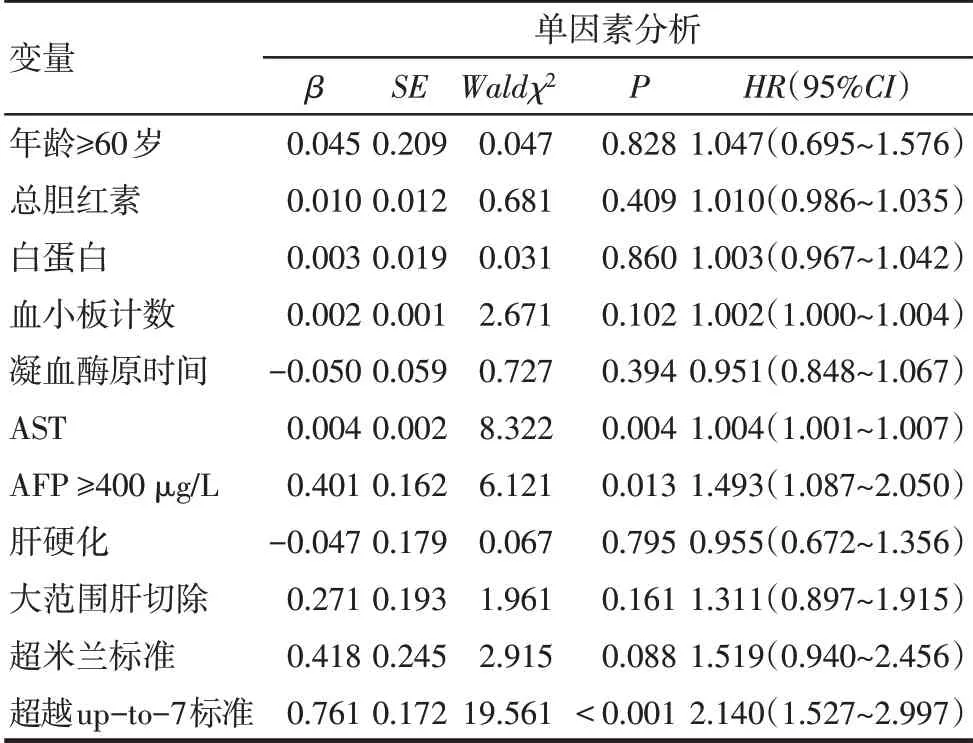
Tab.4 Univariate Cox regression analyses of factors affecting disease-free survival in patients with multifocal HCC表4 影響多發性肝細胞癌患者術后累積無瘤生存率的單因素Cox回歸分析

Tab.5 Multivariate Cox regression analyses of factors affecting disease-free survival in patients with multifocal HCC表5 影響多發性肝細胞癌患者術后累積無瘤生存率的多因素Cox回歸分析

Fig.3 Comparison of the accuracy of Milan criteria and up-to-7 criteria in predicting overall survival and disease-free survival using t-ROC curve analysis圖3 t-ROC曲線比較米蘭標準和up-to-7標準預測多發性肝細胞癌患者術后累積總生存率和無瘤生存率的準確性
3 討論
對于多發性HCC,米蘭標準不僅是篩選肝移植適宜對象的重要依據,也是劃分早、中期HCC 的界限。在BCLC分期系統中,中期HCC(多發性HCC超越米蘭標準)不推薦行肝移植和肝切除術治療。由于米蘭標準較為嚴格,越來越多的學者對這一標準提出了挑戰[8,12-14]。為了優化肝移植的選擇標準,Mazzaferro 等[8]開展了一項全球多中心的研究,并推薦采用up-to-7 標準替代米蘭標準。由于受傳統文化的影響,我國的器官捐獻率較低,導致肝移植的器官來源較少。所以,我國多發性HCC的根治性治療仍以肝切除術為主[9]。目前,分析up-to-7 標準與HCC 肝切除術后預后關系的研究較少,因此比較up-to-7 標準和米蘭標準在預測多發性HCC 患者肝切除術后預后方面的區分度和準確性非常有必要。
本研究結果顯示,米蘭標準符合組和超越組累積總生存率和累積無瘤生存率的差異均無統計學意義,而up-to-7標準符合組和超越組累積總生存率和無瘤生存率差異均有統計學意義,表明up-to-7標準對于多發性HCC患者預后的區分度優于米蘭標準。多因素分析結果顯示,超越up-to-7標準是影響多發性HCC 患者術后累積總生存率和無瘤生存率的獨立危險因素,但超越米蘭標準不是;在t-ROC曲線分析中,up-to-7 標準預測多發性HCC 患者術后累積總生存率和無瘤生存率的AUC 值也均大于米蘭標準,這些結果均進一步證實up-to-7標準在預測多發性HCC患者肝切除術后的預后方面優于米蘭標準。
另外,本研究符合米蘭標準的多發性HCC患者僅占14.3%(36 例),而符合up-to-7 標準的患者占36.5%(92例)。符合米蘭標準的多發性HCC患者的5年累積總生存率和無瘤生存率為57.3%和14.8%;而符合up-to-7 標準的多發性HCC 患者的5 年累積總生存率和無瘤生存率也達到了56.4%和12.3%,表明盡管up-to-7 標準比米蘭標準擴大了22.2%(56例)的患者,但患者總體的預后并沒有明顯的變化。在BCLC 分期系統中,超越米蘭標準的多發性HCC患者推薦肝動脈化療栓塞作為一線治療方案,不推薦手術治療。本研究進一步證實,米蘭標準過于嚴格,因為符合up-to-7標準和符合米蘭標準的多發性HCC 患者的預后相當,但up-to-7 標準明顯增加了手術的獲益人群。Mazzaferro 等[8]研究也發現,對于符合up-to-7 標準的接受肝移植治療的HCC 患者,超越米蘭標準的患者與符合米蘭標準的患者有相似的生存期。因此,對于多發性HCC 的早中期的劃分,up-to-7標準可能比米蘭標準更為合適。
綜上所述,up-to-7 標準在預測多發性HCC 患者肝切除術后的預后方面優于米蘭標準;up-to-7標準可以擴大手術的獲益人群,但本研究為單中心的回顧性研究,仍需多中心研究來證實。

