HPLC-QAMS同時測定屏風生脈膠囊中9個指標成分含量△
黃孝權,何人大,魏譚軍,周殿儒,肖成,陳飛,周曉維*,陳勇
1.達州市中西醫結合醫院,四川 達州 635000;2.成都地奧集團天府藥業有限公司,四川 達州 635027
屏風生脈膠囊由黃芪、防風、麥冬、人參、白術、五味子和附子組成,主要用于心悸氣短、表虛自汗、乏力眩暈、易感風邪。現代研究表明,屏風生脈膠囊對慢性蕁麻疹[1-2]、支氣管哮喘[3-4]、室性早搏[5]、病毒性心肌炎[6]及老年冠心病心絞痛[7]治療效果顯著,易被廣大患者接受。屏風生脈膠囊中黃芪補氣升陽、固表止汗、生津養血、行滯通痹;防風祛風解表、止痛止痙;麥冬養陰生津、潤肺清心;人參大補元氣、補脾益肺、生津養血、安神益智;白術健脾益氣、燥濕利水;五味子收斂固澀、益氣生津、補腎寧心;附子回陽救逆、散寒止痛。諸藥合用,共奏固衛御風、益氣養陰之功效。目前,屏風生脈膠囊國家藥品標準[8]及文獻[9-13]中僅以1或2個成分作為質量控制指標,均難以客觀評價其整體質量,也難以確保臨床療效的一致性,多指標控制模式已逐步應用于中藥及其制劑的質量評價中。傳統的多指標控制模式因某些對照品不易得到或部分對照品價格昂貴、穩定性差,推廣應用具有一定的局限性,而一測多評法(QAMS)以制劑中某一質量穩定、價格低廉、易得的指標成分作為內參物,通過相對校正因子(RCF)計算其他成分的含量,最終達到多個組分的同時測定,有效地解決了部分對照品不穩定、價格昂貴、不易獲得、檢驗成本過高等傳統多成分質量控制模式的不足。本研究以屏風生脈膠囊中毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B 為質量控制指標,采用高效液相色譜一測多評法(HPLC-QAMS)對上述9 個成分含量進行同步測定,建立屏風生脈膠囊多指標成分質量控制模式,以期為屏風生脈膠囊質量控制新體系提供參考。
1 材料
1.1 儀器
1260 型高效液相色譜儀(安捷倫公司)、LC-2030 型高效液相色譜儀(日本島津公司);AB265-S型十萬分之一電子天平(瑞士梅特勒-托利多公司);BRANSON 5510 型超聲提取器(上海滬沁儀器設備有限公司)。
1.2 試藥
對照品毛蕊異黃酮葡萄糖苷、升麻素苷(中國食品藥品檢定研究院,批號分別為111920-201907、111522-201913,純度分別為96.8%、94.6%);芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B(成都普瑞法科技開發有限公司,批號分別為PRF9060501、PRF8101143、PRF8091225、PRF9122902、PRF9121702、PRF8041122、PRF7102423,純度分別為99.6%、99.1%、99.9%、99.5%、99.1%、99.9%、98.3%);屏風生脈膠囊(每粒裝0.33 g)分別購于綿陽一康制藥有限公司(批號分別為191001、200501、201101、210201,編號為S1~S4)、廣州諾金制藥有限公司(批號分別為8421101、8421302、8421501、8421503,編號為S5~S8)和山西康威制藥有限責任公司(批號分別為1130109、1130111、1130118、1130311,編號為S9~S12);乙腈為色譜純;其余試劑均為分析純。
陰性對照試驗所用藥材黃芪(批號:210103-1)、防風(批號:210215-2)、麥冬(批號:210116-1)、人參(批號:210302-2)、白術(批號:210107-1)、五味子(批號:201201-1)和附子(批號:210211-2)均來源于四川仁禾中藥飲片有限公司,經達州市中西醫結合醫院周曉維主管藥師鑒定均為正品。
2 方法與結果
2.1 對照品溶液的制備
取9 個對照品各適量,精密稱定,用甲醇制成毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B 質量濃度分別為0.536、0.352、0.430、0.874、1.316、0.498、0.376、0.272、0.218 mg·mL–1的混合對照品儲備液。將混合對照品儲備液稀釋20 倍得對照品溶液(毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B 質量濃度分別為26.8、17.6、21.5、43.7、65.8、24.9、18.8、13.6、10.9 μg·mL–1)。
2.2 供試品溶液的制備
取屏風生脈膠囊內容物2 g,精密稱定,加甲醇20 mL,對供試品超聲處理45 min,放冷,甲醇稀釋至25 mL,搖勻,0.45 μm微孔濾膜濾過,續濾液作為屏風生脈膠囊供試品溶液。取按屏風生脈膠囊質量標準項下處方和制法制備的缺黃芪、缺防風、缺麥冬的陰性供試品各適量,按上述方法依次制得陰性供試品溶液。
2.3 色譜條件及系統適用性
色譜柱Agilent ZORAX StableBond C18(250 mm×4.6 mm,5 μm),柱溫為30 ℃;檢測波長分別為254 nm(0~36 min,毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷)[14-20]和296 nm(36~60 min,麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B)[21-23];流動相為乙腈(A)-0.1%甲酸(B),梯度洗脫(0~9 min,13%A;9~24 min,13%~33%A;24~36 min,33%~45%A;36~52 min,45%~68%A;52~60 min,68%~13%A);流速為1.0 mL·min–1;進樣量10μL。理論板數按9個指標成分計均應≥5500。
2.4 方法學考察
2.4.1 專屬性 精密吸取2.1、2.2項下溶液各10μL,按2.3項下色譜條件進樣檢測,記錄色譜圖(圖1)。結果屏風生脈膠囊供試品溶液中9 個指標成分與相鄰色譜峰分離良好,分離度均大于1.5;所檢測指標成分色譜峰峰形對稱,拖尾因子符合《中華人民共和國藥典》2020 年版(四部)規定;陰性供試品對9個指標成分的測定無干擾。
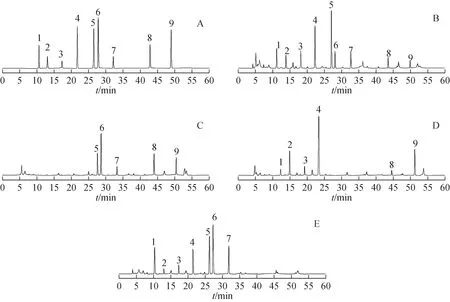
圖1 混合對照品、屏風生脈膠囊供試品及陰性供試品HPLC圖
2.4.2 線性關系考察 精密吸取2.1 項下混合對照品儲備液0.1、0.2、0.5、1.0、2.0、2.5 mL,置不同的20 mL 量瓶中,用甲醇定容制成6 個混合對照品溶液,按2.3項下色譜條件進樣10μL,以9 個指標成分質量濃度為橫坐標(X),以峰面積為縱坐標(Y)進行線性回歸(表1)。

表1 屏風生脈膠囊中9個指標成分的線性關系
2.4.3 精密度試驗 按2.3項下色譜條件進樣屏風生脈膠囊(編號:S1)同一份供試品溶液10μL,重復操作6 次,測得指標成分峰面積的RSD 分別為1.26%、1.33%、1.20%、0.87%、0.61%、1.19%、1.35%、1.29%、1.45%。
2.4.4 重復性試驗 按2.2 項下方法制備6 份屏風生脈膠囊(編號:S1)供試品溶液,依次進樣10μL分析,得指標成分含量的RSD 分別為1.57%、1.77%、1.69%、1.45%、1.09%、1.86%、1.74%、1.83%、1.91%。
2.4.5 穩定性試驗 分別于0、2、4、8、16、24 h按2.3項下色譜條件進樣屏風生脈膠囊(編號:S1)同一份供試品溶液10 μL,得指標成分峰面積的RSD分別為1.38%、1.41%、1.26%、0.95%、0.58%、1.12%、1.29%、1.31%、1.40%。
2.4.6 加樣回收率試驗 取已知9 個指標成分含量的屏風生脈膠囊內容物9 份,每份1 g,精密稱定,均分成3組,精密加入混合對照品溶液(毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B的質量濃度分別為0.309、0.195、0.246、0.583、0.934、0.261、0.225、0.149、0.108 mg·mL–1)0.8、1.0、1.2 mL,按2.2 項下方法制備供試品溶液,各精密吸取10 μL,按2.3項下方法進樣檢測,見表2。
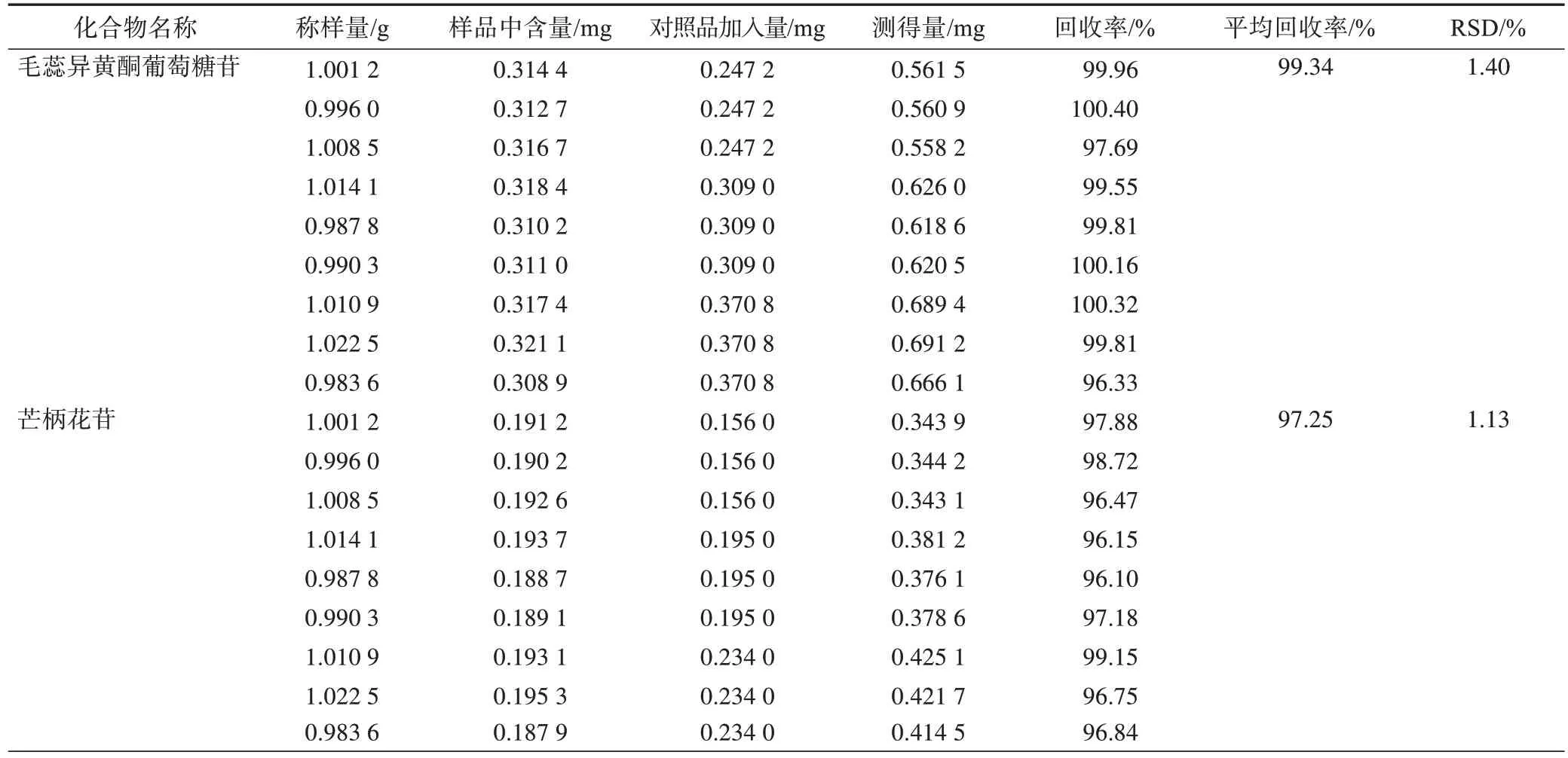
表2 屏風生脈膠囊中9個指標成分的加樣回收率試驗結果
2.5 QAMS評價模式的建立
2.5.1 RCF 的建立 按2.3項下色譜條件進樣2.4.2項下6 個混合對照品溶液各10 μL,按公式(1)計算各成分RCF。
式中?為校正因子,W為質量濃度,A為峰面積,k為其他待測成分,s為內參物。
以升麻素為內參物,分別計算其他8 個指標成分的RCF(表3)。
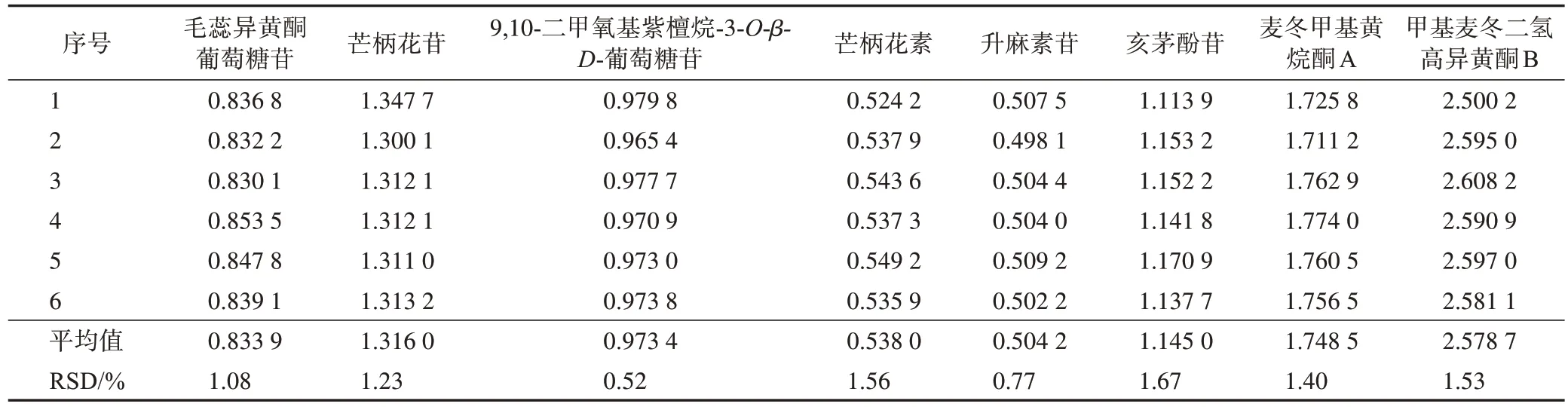
表3 屏風生脈膠囊中其他8個指標成分的RCF
2.5.2 不同儀器及色譜柱對RCF的影響 分別選用安捷倫1260 型、島津LC-2030 型高效液相色譜儀和色譜柱(Agilent ZORAX StableBond C18、Waters Nova-Pak C18、迪馬Spursil C18),進樣2.1 項下對照品溶液10 μL,得升麻素對其他8 個指標成分的RCF(表4)。

表4 儀器及色譜柱對屏風生脈膠囊中其他8個指標成分的RCF的影響
2.5.3 不同流速對RCF的影響 在不同流速(0.8、0.9、1.0、1.1、1.2 mL·min–1)條件下,按2.3項下色譜條件進樣2.1 項下對照品溶液10 μL,得升麻素對其他8個指標成分的RCF(表5)。
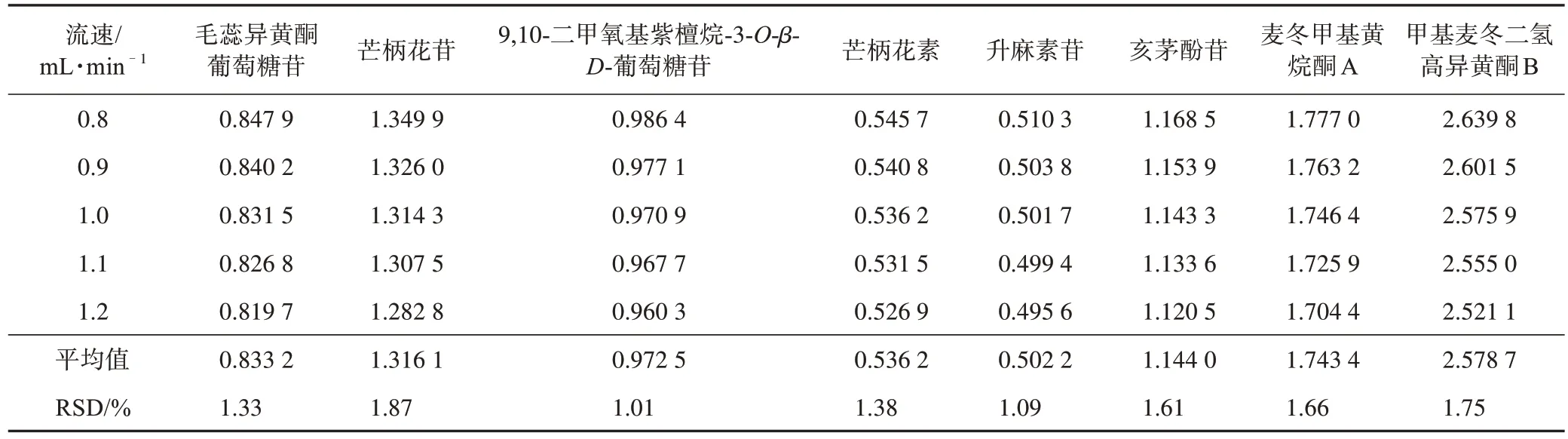
表5 流速對屏風生脈膠囊中其他8個指標成分的RCF的影響
2.5.4 不同柱溫對RCF 的影響 在不同柱溫(25、28、30、32、35 ℃)條件下,按2.3項下色譜條件進樣2.1 項下對照品溶液10μL,得升麻素對其他8 個指標成分的RCF(表6)。
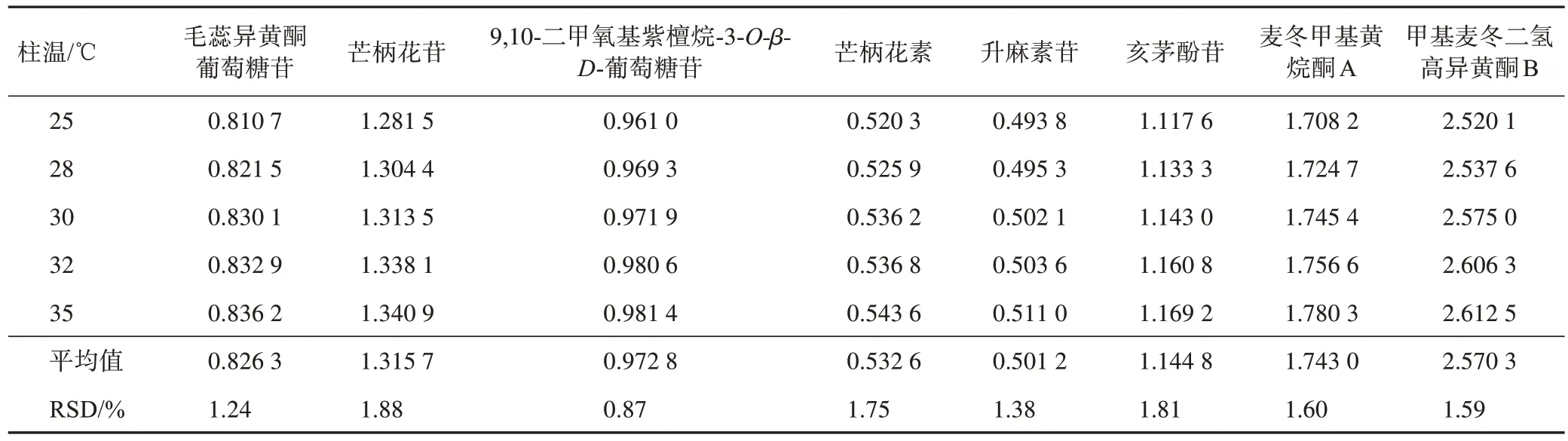
表6 柱溫對屏風生脈膠囊中其他8個指標成分的RCF的影響
2.5.5 色譜峰定位 按2.3項下色譜條件進樣2.1 項下對照品溶液10μL,采用相對保留時間值法對待測成分色譜峰進行定位,考察儀器(安捷倫1260 型、島津LC-2030 型高效液相色譜儀)和色譜柱(Agilent ZORAX StableBond C18、Waters Nova-Pak C18、迪馬Spursil C18)對相對保留時間的影響(表7)。
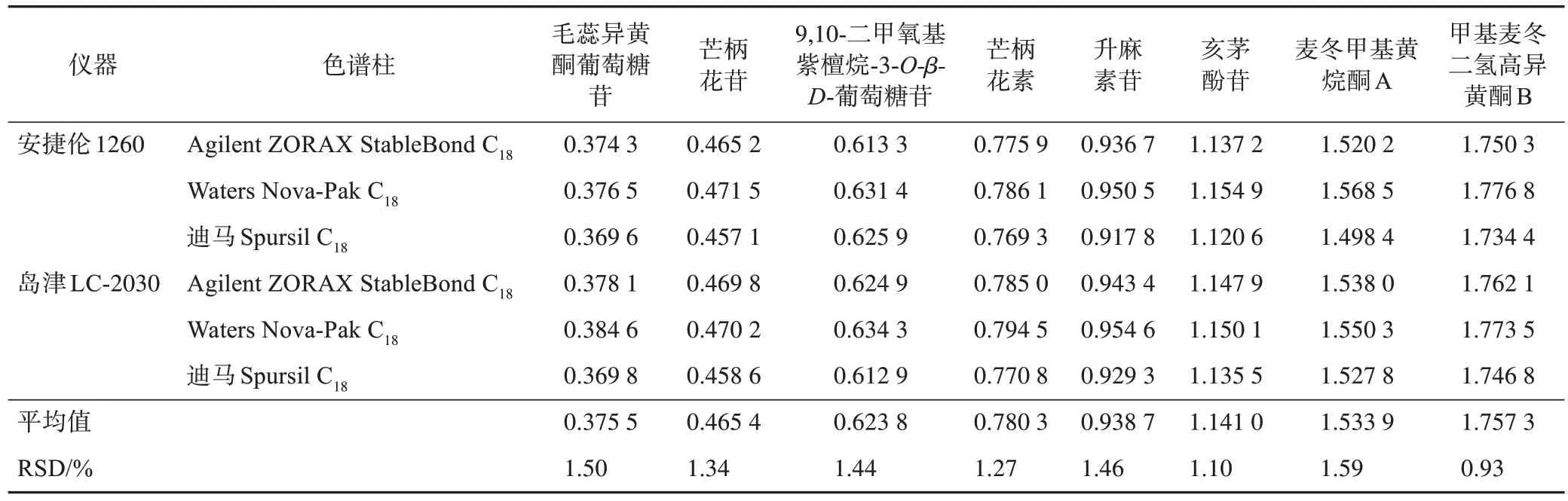
表7 不同儀器及色譜柱對屏風生脈膠囊中其他8個指標成分的相對保留時間的影響
2.6 QAMS與外標法(ESM)測定結果比較
為驗證所建立的QAMS 的準確性和可行性,取3 個廠家12 批屏風生脈膠囊,按2.2 項下方法制備屏風生脈膠囊供試品溶液,按2.3項下色譜條件進樣分析,分別運用ESM 和QAMS計算屏風生脈膠囊中9 個指標成分的含量,比較2 種方法檢測結果的差異(表8)。
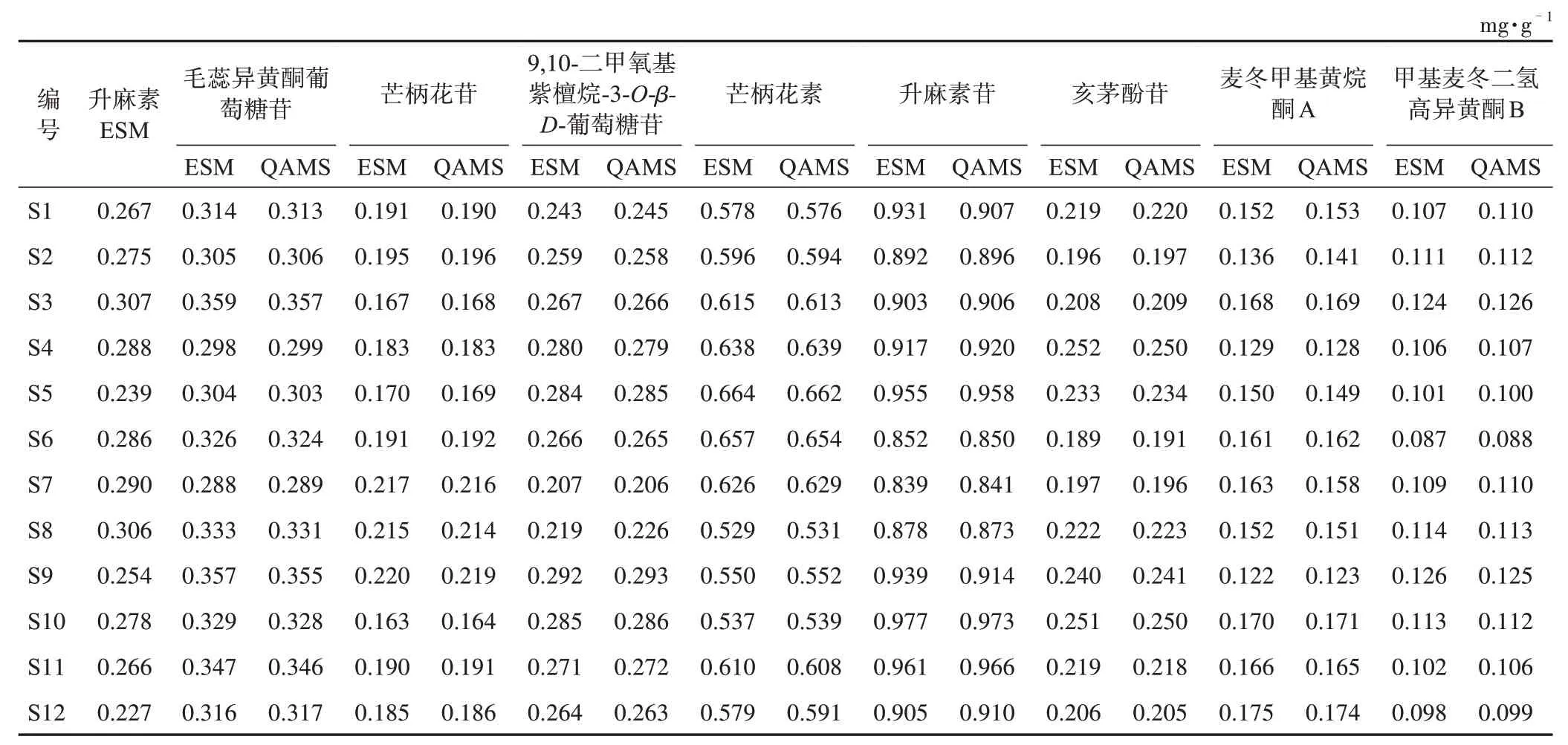
表8 屏風生脈膠囊中9個指標成分含量測定結果(n=3)
3 討論
3.1 目標成分的選擇
屏風生脈膠囊由黃芪、防風、麥冬、人參、白術、五味子、附子組成組方,方中黃芪和人參補益元氣、固表止汗為君藥;白術和防風健脾益氣為臣藥;五味子和麥冬斂陰止汗為佐藥;附子溫腎壯陽為使藥。本研究以君藥所含成分為主,兼顧臣佐藥所含成分,選取毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B共9個指標成分進行定量分析。
3.2 流動相的確定
首先取甲醇-水[18-20]和乙腈-水[21]為流動相,以屏風生脈膠囊中9 個指標成分的色譜峰峰形、分離效果、響應值為主要指標,兼顧檢驗用時、基線情況等,結果乙腈-水優于甲醇-水,但升麻素苷與升麻素不能有效分離。遂以乙腈為有機相,參考相關文獻對乙腈-0.1% 磷酸溶液、乙腈-0.1% 甲酸溶液[14-16,22-23]進行對比考察,最終乙腈-0.1%甲酸溶液為流動相梯度洗脫,對屏風生脈膠囊中毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B含量進行同時檢測。
3.3 供試品制備方法的確定
本研究在制備屏風生脈膠囊供試品溶液時,逐個考察了甲醇[14-15,17-21]、水[16]、80%甲醇[22]、70%甲醇[23]4 種提取溶劑及加熱回流[14,20]、超聲[15,17-19,21-23]2 種提取方式,以毛蕊異黃酮葡萄糖苷、芒柄花苷、9,10-二甲氧基紫檀烷-3-O-β-D-葡萄糖苷、芒柄花素、升麻素苷、升麻素、亥茅酚苷、麥冬甲基黃烷酮A、甲基麥冬二氫高異黃酮B 綜合提取率為首要指標,最終確定采用甲醇超聲處理45 min 為屏風生脈膠囊供試品制備方法[21]。
本研究所建立的HPLC-QAMS 結果準確,可用于對屏風生脈膠囊中9 個指標成分的同步定量分析,能夠作為屏風生脈膠囊多指標成分質量控制方法;同時也反映出9 個指標成分存在一定的批間差異,表明多指標成分質量控制對穩定屏風生脈膠囊產品質量,確保臨床用藥療效的一致性具有重要意義。

