光學體表監測系統Catalyst HD的cPosition與cMotion功能在乳腺癌調強放療中的應用
方涌文,劉鏢水,肖亮杰,王宇留,姚文燕,郭旋,何振宇,林承光,方鍵藍
中山大學腫瘤防治中心 華南國家腫瘤實驗室,廣東 廣州 510060
引言
在女性惡性腫瘤中,乳腺癌是目前最常見的惡性腫瘤之一,據世界衛生組織國際癌癥研究機構2020年調查數據顯示,全球女性癌癥中女性乳腺癌新增人數高達226萬,占全球癌癥新發病例的11.7%,正式取代肺癌全球第一大癌癥的地位,而乳腺癌死亡率在全球癌癥死亡率中排名第5,死亡率為6.9%[1]。目前乳腺癌也成為實體腫瘤治療中治療效果最佳的病種之一,放射治療中的每個流程步驟都非常重要,放射治療期間的乳腺癌患者體表的標記線是整個放療完美進行的保障[2]。乳腺癌患者體表標記點與標記線不僅影響放療實施的擺位精度,而且相對于左側乳腺癌患者放療中保護危及器官[3],如心臟、肺等也起到了重要的作用。光學體表監測系統(Optical Surface Monitoring System,OSMS)輔助擺位是近些年興起的新型擺位方式,其中Catalyst HD是利用光學表面成像技術,實時重建顯示所勾畫的感興趣區附近的三維體表輪廓。獲取實時患者體位誤差信息參數方便進行輔助擺位、治療實時監控和呼吸門控監視,實現患者放射治療全流程“三精”放療的標準[4]。本研究目的是比較Catalyst HD中cPosition與錐形束CT(Cone Beam CT,CBCT)校正兩個系統的一致性,在降低患者所受額外劑量的前提下,輔助患者放療體位的校正,探討能否替代CBCT作為淺層腫瘤患者放療的體位校正并且進行治療實時監控的分析,為光學體表實施提供臨床參考依據。
1 材料和方法
1.1 一般資料
選取在本中心Varian Vital_Beam進行調強放射治療的乳腺癌患者34例。本研究經醫院醫學倫理委員會批準,批準號:2020-379-01,所有患者均簽署知情同意書。
1.1.1 入選標準
年齡20~60歲;KPS大于50分;術后分期為Tis-2N0-2M0分期的乳腺癌保留乳房手術后患者;患側上臂上舉外展自如的患者;患者無通氣功能障礙,無慢性心肺疾病。患者接受4DCT、CBCT掃描并簽署知情同意書;患者接受KVCBCT圖像引導放療并簽署知情同意書。
1.1.2 排除標準
同時雙側乳腺癌;腋窩前哨淋巴結活檢,未做腋窩清掃;做過內乳淋巴引流區清掃;嚴重心功能不全;近3個月內出現心肌梗死或未糾正的不穩定型;既往胸壁或鎖骨上放療史;既往或同時第二原發惡性腫瘤。所選均為浸潤性癌并為保乳術后患者,行胸壁、內乳、鎖骨上淋巴引流區照射。
1.2 體位固定
發泡膠個體化仰臥固定,采用廣州福瑞人體定位墊發泡膠固定,將混合液平鋪倒到在防水布袋內,患者雙手上舉外展,采用發泡膠發泡固定的方式使手臂與手指充分塑形,患者面朝向健側,充分展開胸壁及腋窩淋巴結,發泡膠技術自動塑形的特性使得發泡膠固定墊更為貼合人體體表輪廓。發泡膠仰臥固定裝置如圖1所示。

圖1 發泡膠仰臥固定裝置
2 方法和數據采集
2.1 cPosition輔助擺位方法與誤差數據的采集
Catalyst HD OSMS的cPosition通過綠色光源和紅色光源來顯示乳腺癌患者體表實時三維輪廓與計劃參考輪廓的位移偏差且直接投射到患者體表輪廓上,并在顯示器上顯示出擺位的偏差數據。使用體表標記線擺位的方法如圖2a所示,使用Catalyst HD系統輔助擺位校正如圖2b所示。

圖2 cPosition輔助擺位方法與誤差數據的采集
放療前將患者從Eclipse計劃系統生成的體表外輪廓及放療計劃資料(RT Plan和RT Structure)導入到Catalyst HD系統中,在第1次CBCT驗證后捕獲新的放療體位輪廓,作為第二次及之后放射治療的參考輪廓,在每次治療前先按照患者體表的標記線進行擺位,接著使用OSMS輔助擺位校正功能進行體位校正,并在第2、3次及每隔5次CBCT進行體位驗證,記錄并觀察患者的標記線擺位治療床床值、Catalyst HD輔助擺位校正后治療床床值及CBCT校準后的體位誤差數據。具體的流程如圖3所示。
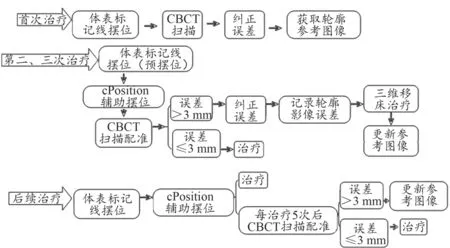
圖3 應用OSMS輔助擺位校正流程示意圖
2.2 cMotion治療實時監控與治療實時位移數據的采集
在患者放療實施前進入Catalyst HD中cMotion界面,治療時Catalyst HD系統對患者全程實時監控,當放療實施過程中出現意外運動即超出所限制的閾值時,控制加速器束流,暫停出束,保證治療的安全,在治療結束后導出患者分次內實時監控的位移數據。治療實時監控、位移閾值和位移矢量如圖4所示。
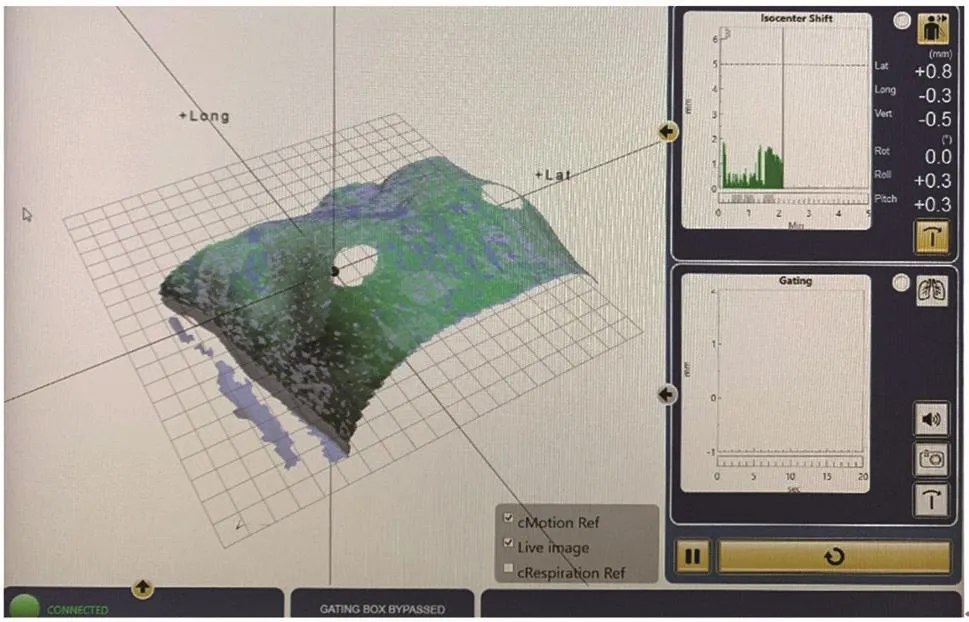
圖4 治療實時監控、位移閾值和位移矢量
2.3 統計學分析
使用SPSS 21.0的Pearson相關分析及配對樣本t檢驗分別對數據進行分析,根據Pearson相關分析得到:R≥0.8為極高度相關;0.6≤|R|<0.8為高度相關;0.4≤ |R|<0.6為中度相關;0.2≤|R|<0.4為低度相關;|R|<0.2基本不相關。計數資料采用n(%)表示,比較采用χ2檢驗,根據配對樣本t檢驗得到組均值和標準差,計量資料采用±s表示,其中P<0.05為差異有統計學意義。
3 結果
3.1 體表標記線擺位與OSMS輔助擺位校正的差異
體表標記線擺位與OSMS輔助擺位校正后進行CBCT體位校正在前后(Anterior Posterior,AP)、上下(Superior-Inferior,SI)、左右(Left Right,LR)方向的誤差,AP、SI和LR方向的t值分別為-3.438、-4.895和-3.473,P值均<0.05,差異有統計學意義;分析旋轉(RTN)、翻轉(Roll)和俯仰(Pitch)方向的誤差,RTN、Roll和Pitch方向的t值分別為-1.811、-3.608和4.273,RTN方向P值為0.072;Roll與Pitch方向P值均<0.05,差異有統計學意義(表1)。
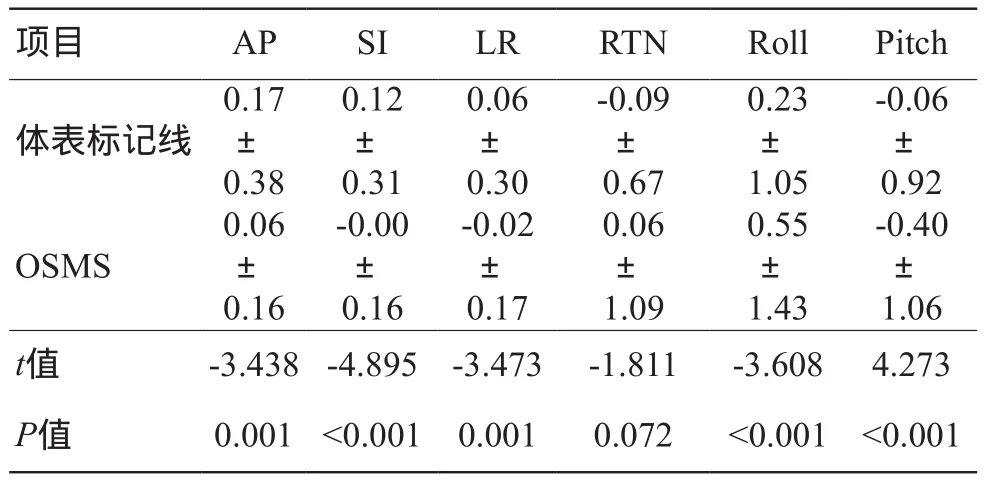
表1 體表標記線擺位與OSMS輔助擺位校正的差異(cm/°)
3.2 應用CBCT校正與Catalyst HD輔助擺位校正cPosition的差異
CBCT校正與Catalyst HD中cPosition校正功能的Pearson相關分析中AP、SI、LR方向相關性均表現為極高度相關,Pitch方向表現為低度相關,見表2。
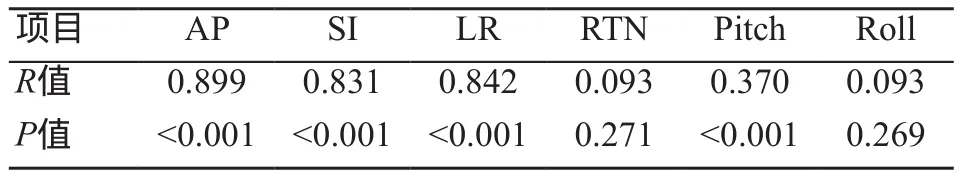
表2 CBCT校正與光學體表校正的Pearson相關分析
3.3 治療實時監控cMotion過程中位移誤差分析
cMotion過程中實時平移方向誤差的頻數分布如表3所示,實時旋轉方向誤差的頻數分布如表4所示,cMotion中平移方向誤差區間占比如圖5所示,cMotion中旋轉方向誤差區間占比如圖6所示。
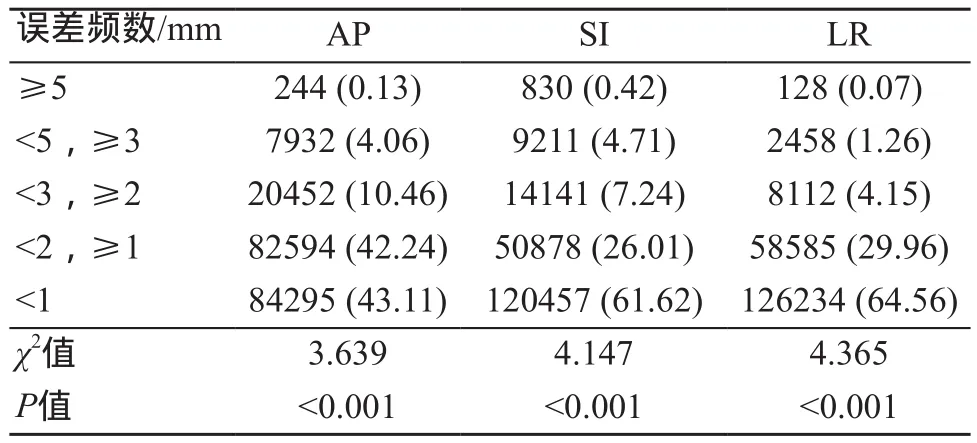
表3 cMotion過程中實時平移方向誤差頻數分布[n (%)]
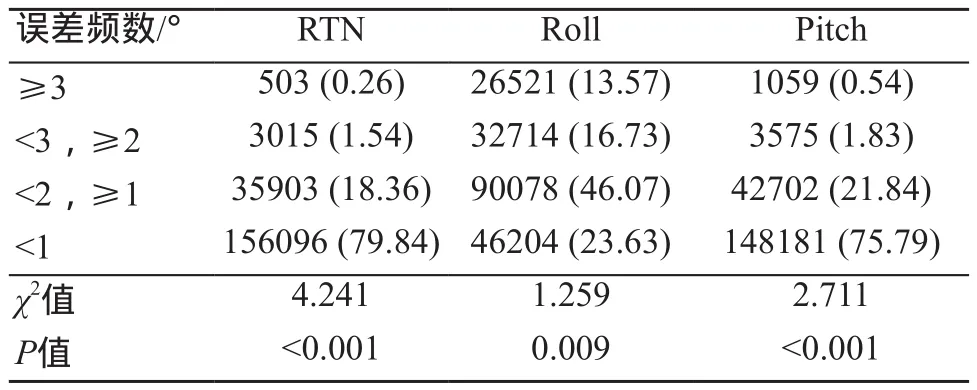
表4 cMotion過程中實時旋轉方向誤差頻數分布[n (%)]
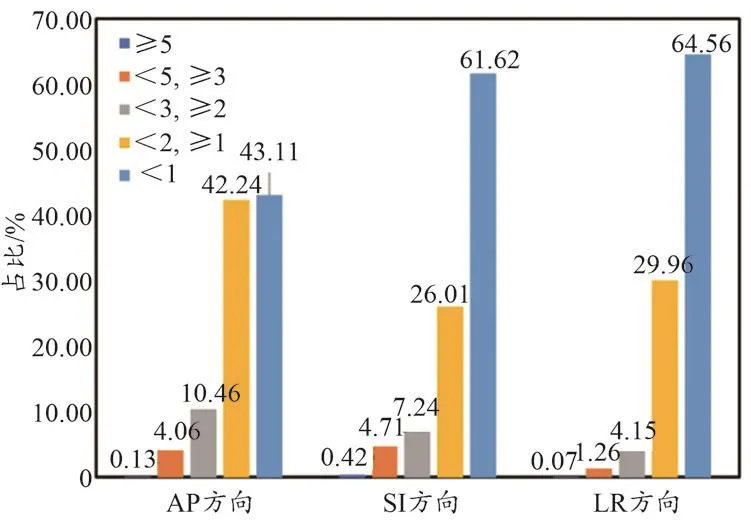
圖5 平移方向誤差區間占比
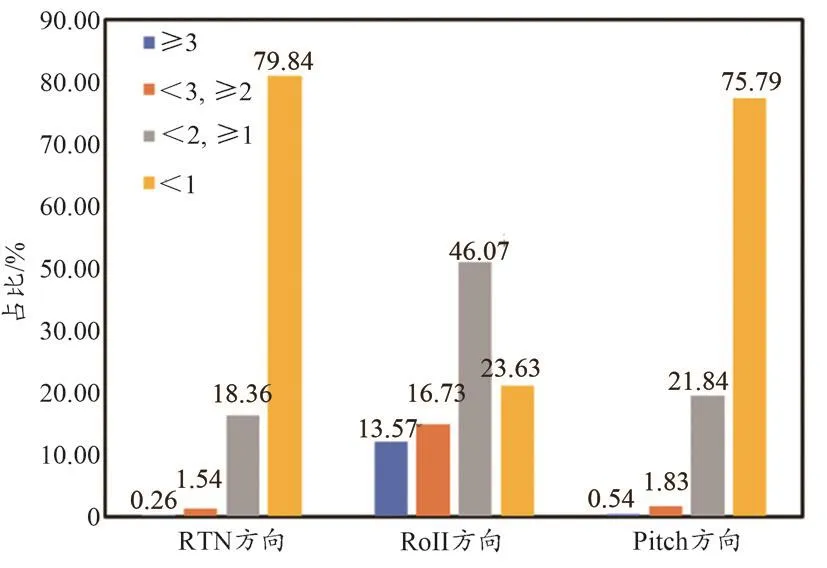
圖6 旋轉方向誤差區間占比
4 討論
C-RAD Catalyst HD獲取患者實時的三維體表輪廓信息,將這些三維體表輪廓信息與Eclipse計劃系統生成或者第一次治療時CBCT掃描校正后捕獲的體表外輪廓信息進行匹配比較,通過可視化的界面輔助引導放療擺位。目前OSMS廣泛應用到諸如乳腺癌、肺癌、鼻咽癌、腦瘤等的放療實施中[5],其中應用較為廣泛的是乳腺癌。目前CBCT具備的精確6維成像能力和較好的圖像分辨率,在體位誤差校正方面仍然作為癌癥患者體位誤差校正的“金標準”[6],本研究使用KV-CBCT對C-RAD Catalyst HD OSMS進行體表標志擺位與cPosition功能對乳腺癌擺位精度的對比發現,體表標記線及使用cPosition功能在3個平移方向比較差異均有統計學意義,光學體表擺位的應用能夠明顯減少三維方向的擺位誤差,與其他學者研究結果趨勢一致[7-8],而本研究也發現了在Pitch旋轉方向明顯減少擺位誤差,大大提高了擺位精度。相較于吳佳蔚等[9]基于美國CIVCO公司的全碳纖維乳腺托架固定的研究,本研究的體表標記線擺位誤差更小,原因在于本研究采用了發泡劑個體化體位固定技術,發泡膠個體化體位固定技術自動塑形的特性使得發泡膠固定墊是以患者的體表輪廓如上腹部、胸壁、手臂、頭頸部和手指等進行塑形,更為貼合人體體表輪廓,適形度高的同時也不存在漏氣變形的風險[10-13]。
本研究發現使用Varian Vital_Beam加速器進行胸部KV-CBCT掃描時掃描的視野為46.5 cm、范圍長度為17.5 cm、旋轉速度為6.0°/s、電壓125 kV和電流270 mAs,每次掃描存在的劑量加權為0.32 cGy,多次使用CBCT掃描將使患者受到額外的輻射劑量,延長患者的治療時間,同時也帶來一定的經濟壓力[14]。OSMS是一種無輻射且能輔助驗證患者放療體位的新興技術,應用CBCT校正與cPosition校正的Pearson相關分析中AP、SI、LR方向相關性均表現為極高度相關;Pitch方向表現為低度相關;直線加速器沒有聯合6維治療床治療的情況下,cPosition校正可以最大程度提高乳腺癌患者的擺位精度,直線加速器聯合6維治療床治療時,可以在AP、SI、LR以及Pitch等方向,進一步校正患者的放療體位,并且在一定程度上減少CBCT掃描的次數,縮短患者單次治療的時間,提高患者的放療舒適度。
在cMotion治療實時監控過程3個實時平移方向的位移距離在-2~2 mm占比大于95%,RTN實時旋轉角度在0°~1°占比為 79.84%,Roll實時旋轉角度在0°~1°占比為23.63%,Pitch實時旋轉角度在0°~1°占比75.79%,差異有統計學意義(P<0.05)。目前各位同行的研究關注點在于治療前的CBCT體位校正,但是無論是KV-CBCT、KV-4D CBCT或者是MV-CBCT體位校正基本都屬于擺位誤差的靜態體位校正技術[15-17],而忽略了患者治療過程中由于呼吸運動、咳嗽、打嗝、治療時間較長導致的肌肉疲勞[18]而發生的不自主移動等的誤差。目前患者的體位固定技術發展已相當成熟,體位固定效果也相對較為理想,并且患者治療過程中的體位變化沒有相關監控或校正的設備,造成目前相關研究的缺乏。本研究發現乳腺癌患者治療過程中不同方向會有不同的位移變化,在Roll方向的變化較大,1°以上的變化占比為76.37%,相對于左側乳腺癌患者來說,可能心臟、肺等危及器官的受量會隨之增加。本研究目前收集了在中山大學腫瘤防治中心Varian Vital_Beam進行調強放射治療的34例乳腺癌患者的治療實時監控位移數據,共195517組。后續研究方向是把cMotion位移數據代入Eclipse計劃系統進行劑量的分析,并研究不同的位移數據對靶區、危及器官劑量及覆蓋率的影響。并且后續研究將繼續擴大入組的患者數量,在表面引導放射治療(Surface Guided Radiation Therapy,SGRT)cPosition與cMotion的應用上為臨床治療提供更精確的支撐。
SGRT在提高了放療精準度的同時,也改善了患者的舒適度,目前在肺癌、膈肌腫瘤、肝癌、乳腺癌、四肢腫瘤放療中得到廣泛應用,已被證明具有亞毫米精度[19-20]。OSMS在分次內治療過程中,也能夠提供治療實時監控功能。患者在治療過程中可能會由于呼吸運動、治療時間較長導致的肌肉疲勞而發生的不自主移動等,造成放療體位的變化,OSMS可以及時反饋患者體位產生的變化,當患者治療實施過程中體位發生較大變化時會進行束流控制,超出設定的位移閾值時暫停出束,等待患者體位恢復正常后再進行出束治療。這樣不僅僅保證了放射治療的準確性,也大大提高了放射治療的治療精度。
綜上所述,OSMS的cPosition相對于傳統體表標記線擺位更加精確;OSMS的cPosition與CBCT校正有較強的一致性,OSMS的cPosition功能可以實時監測患者的體位變化,在乳腺癌保乳術患者放療時建議使用OSMS以提高擺位精度,減少額外劑量輻射,提高治療療效。

