甲醇和乙腈二元體系中奧美拉唑熱力學模型分析
戴明明,潘英敏,陶 寧,朱鳳梅,陳順平,吳海建,吳 剛,吳 偉
南京正大天晴制藥有限公司,江蘇 南京 210038
奧美拉唑是一種白色粉末或類白色粉末狀固體,分子式為C17H19N3O3S(圖1),其CAS 號為73590-58-6,由1 個亞砜基因連接苯并咪唑與取代吡啶環組成。作為胃質子泵H+/K+-ATP 酶的可逆抑制劑,奧美拉唑及其制劑常被廣泛使用于胃潰瘍、十二指腸潰瘍、反流性食管炎和卓-艾綜合征的治療[1-3]。奧美拉唑是目前國際上使用最廣泛的處方藥之一,同時在一些國家也作為非處方藥進行銷售。奧美拉唑及其衍生物具有較高的醫藥價值和工業生產前景。
圖1 奧美拉唑的化學結構式
眾所周知,藥物的純化處理、含量測定是藥品生產過程的重要組成部分。藥物的溶解度特性,特別是藥物的固-液相平衡、液-液相平衡常數對研究藥物的作用機制具有重要作用。本文旨在對奧美拉唑的固-液相平衡數據進行收集、擬合、分析,為奧美拉唑的藥學應用、分析純化研究提供基礎數據。此外,基于基礎數據還可以進一步探討奧美拉唑的萃取結晶、含量測定等工藝問題及其改進。
采用質量法測定常壓下奧美拉唑于5~60 ℃(278.15~333.15 K)下在甲醇和乙腈二元溶劑體系中的溶解度,并將溶解度數據采用修正的Apelblat 模型、近理想二元溶劑/Redich-Kister(CNIBS/R-K)模型和Jouyban-Acree 模型進行擬合,同時利用范德霍夫分析和吉布斯方程可以計算熱力學參數(包括焓、熵和吉布斯自由能)。根據實驗數據,從混合溶劑中找出奧美拉唑相平衡規律。此外,熱力學性質分析也有助于得出不同溫度、不同組分下溶解度的變化趨勢[4],以充實奧美拉唑基礎理論研究,為奧美拉唑的生產、應用、分析工藝提供一定指導,以期對奧美拉唑的使用、藥物制劑開發、色譜分析測定等方面提供參照。
1 實驗
1.1 材料與儀器
所用材料的詳細信息見表1。分析天平(BS124S 型,量程0~120 g,精度值±0.1 mg),賽多利斯科學儀器(北京)有限公司;循環恒溫水浴系統(WDC-0540 型,量程-5~100 ℃,精度值±0.1 ℃),南京舜瑪儀器設備有限公司。

表1 化學試劑屬性及來源
1.2 實驗方法
通過質量法進行溶解度測定[5-6]。將過量的奧美拉唑與不少于8 mL 的甲醇和乙腈的二元有機溶劑加入帶塞子的10 mL 玻璃試管中(以避免實驗過程中溶劑蒸發),將所有玻璃試管置于循環恒溫水浴系統并開啟磁力攪拌器連續攪拌24 h 以上(以確保玻璃試管中的液體達到平衡),然后關閉攪拌,并保持溫度至少6 h(以確保未溶解固體在玻璃試管底部沉淀)。用移液槍吸取1 mL 透明澄清的飽和溶液,迅速轉移至5 mL 已稱質量的燒杯中,立即稱量含有溶液的燒杯總質量,然后將燒杯置于室溫下的干燥器中,定期(如每星期一次)對燒杯稱質量,直至質量沒有變化。為了檢查溶解度測定的重復性,每個實驗至少重復3 次。用同樣的方法,在不同的溫度下測量了3 個樣品的溶解度,并用平均值計算了溶解度的摩爾分數。以摩爾分數表示溶質奧美拉唑的溶解度(x),數據計算見式(1)~(2)。
式中:xA為二元溶劑體系中甲醇的摩爾分數;i可為1、2、3,分別代表奧美拉唑、乙腈和甲醇;m1、m2、m3分別代表奧美拉唑、乙腈和甲醇的質量;M1、M2、M3分別代表奧美拉唑、乙腈和甲醇的摩爾質量。
2 結果與討論
2.1 數據與模型
測定在278.15~333.15 K 時奧美拉唑在甲醇和乙腈二元溶劑混合物中的溶解度(x),詳見表2,不同甲醇含量中溶解度與溫度的關系曲線見圖2。
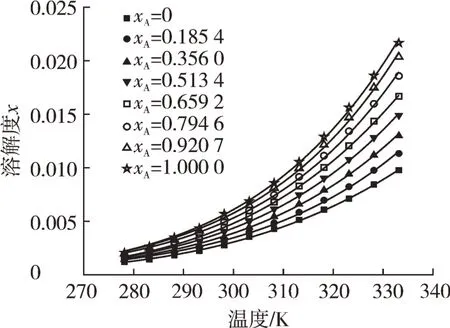
圖2 二元溶劑體系中奧美拉唑的摩爾分數溶解度(x)與溫度(T)關系
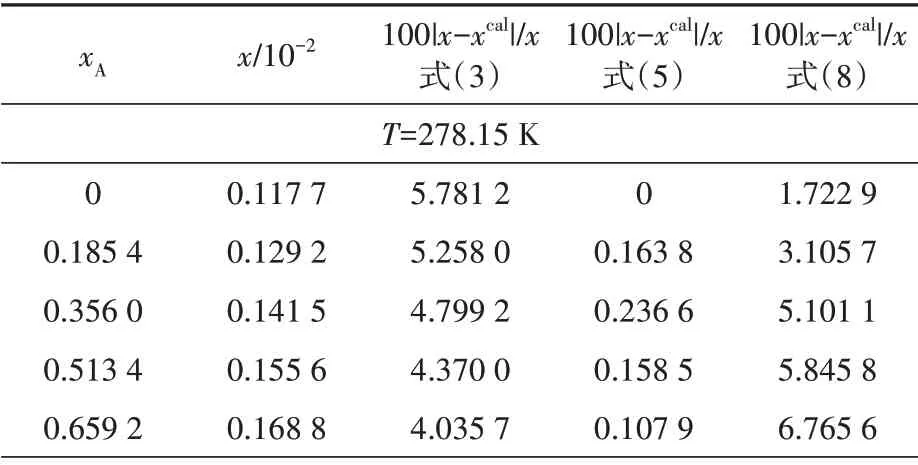
表2 奧美拉唑在甲醇和乙腈二元溶劑中的溶解度
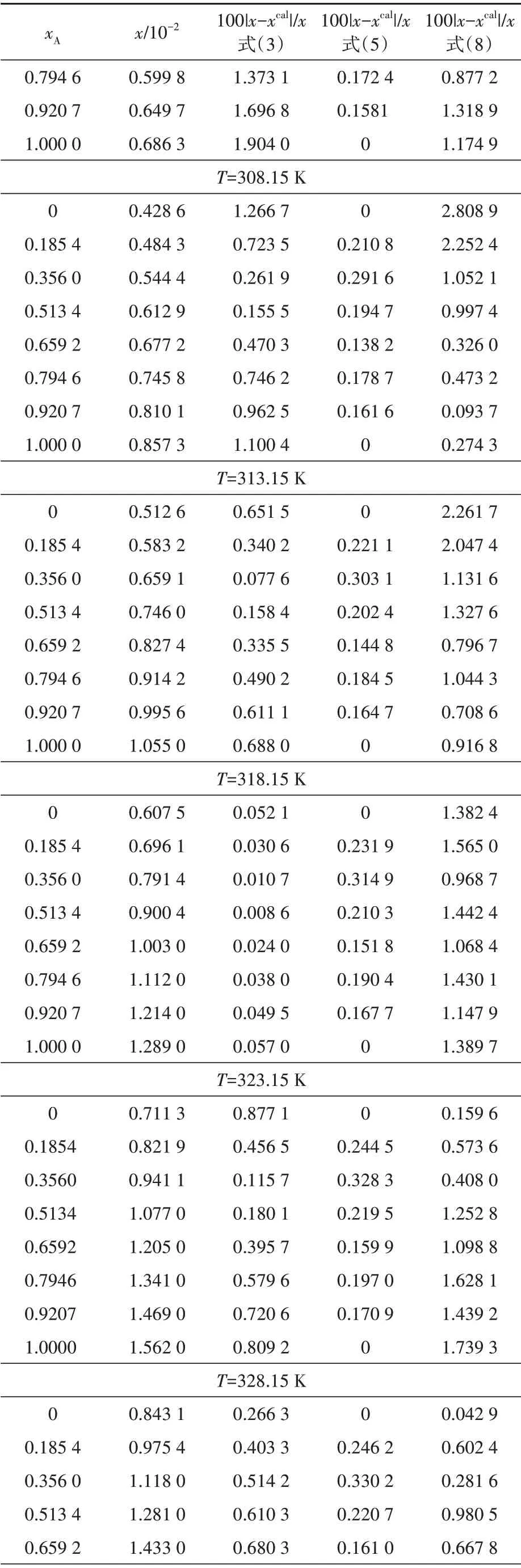
續表

續表
由表2和圖2可知:奧美拉唑在甲醇和乙腈二元溶劑體系中的溶解度隨溫度升高而增加;相同溫度時奧美拉唑的溶解度隨二元溶劑中甲醇含量的增加而增加。
2.2 修正的Apelblat模型
奧美拉唑的溶解度隨溫度的變化關系可利用修正的Apelblat模型進行擬合[7-9]。
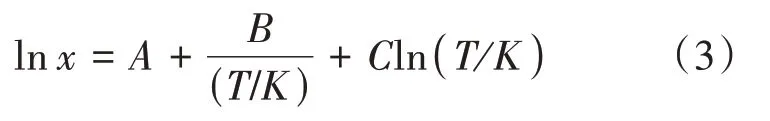
式中:T代表絕對溫度(K),A、B、C代表模型參數,x代表奧美拉唑在二元溶劑中的溶解度。參數A和B代表溶液活度系數的變化,表示溶質溶解度的非理想溶液效應,參數C表示溫度對熔融焓的影響,即熱容(△Cp)[10-11]的修正。修正后的Apelblat模型回歸曲線參數見表3。

表3 奧美拉唑在二元溶劑體系中修正的Apelblat模型的參數
2.3 CNIBS/R-K 模型
近理想二元溶劑/Redich-Kister(CNIBS/RK)模型也是計算二元溶劑體系中溶質溶解度的理論模型之一[12-16]。在等溫條件下溶解度隨混合溶劑中甲醇摩爾分數的變化趨勢常用CNIBS/R-K 模型進行擬合,CNIBS/R-K 模型可用式(4)表示。

式中:x代表奧美拉唑的溶解度,xA和xB代表未添加溶質時二元溶劑乙腈和甲醇的初始組成(以摩爾分數表示),XA和XB分別代表奧美拉唑在純乙腈和純甲醇中的溶解度。Si是模型常數,N可以等于0、1、2 和3。當N=2 時,可用(1-xA)代替xB,則式(4)可重排為
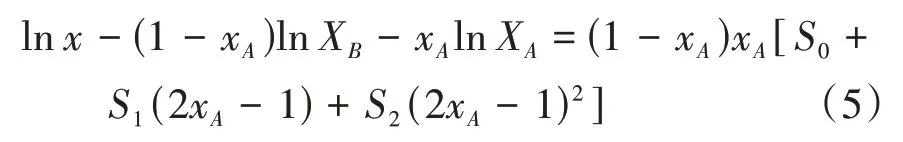
這是CNIBS/R-K 模型的一種變形,參數Si可以通過擬合[lnx-(1-xA)lnXB-xAlnXA]與{(1-xA)xA[S0+S1(2xA-1)+S2(2xA-1)2]}得到。
擬合得到的參數值見表4。然而,CNIBS/R-K模型只能用來描述溶解度數據和預測不同濃度混合溶劑在固定溫度下的溶解度數據。為了描述溶劑組成和溫度對奧美拉唑溶解度的影響,可采用Jouyban-Acree 模型。
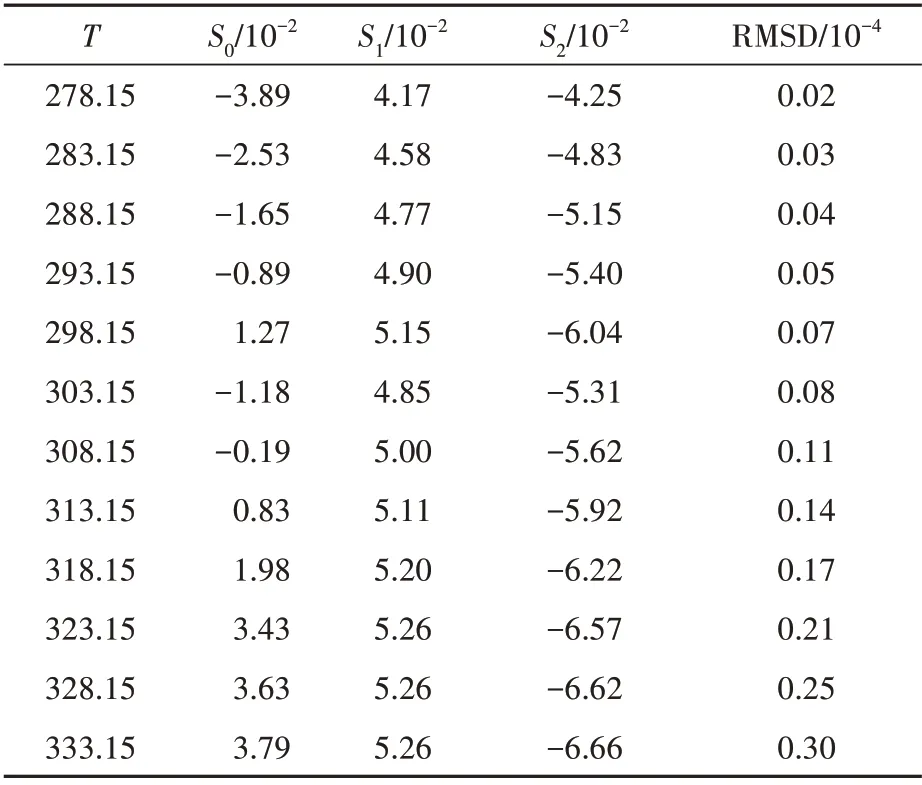
表4 奧美拉唑二元溶劑體系用CNIBS/R-K 模型擬合的參數
2.4 Jouyban-Acree 模型
Jouyban-Acree 模型是一種描述溶質溶解度隨溫度和二元溶劑初始組分的變化而變化的常見模型[17],具體計算見式(6)。
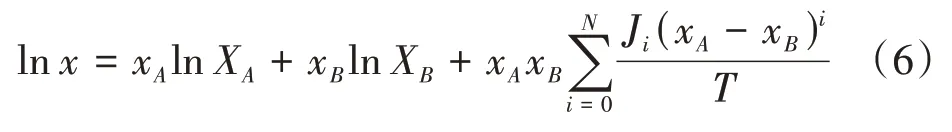
式中:Ji是模型常數。當N=2 時,可用(1-xA)代替xB,由式(6)可得到
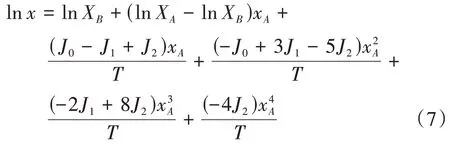
可以進一步簡化為
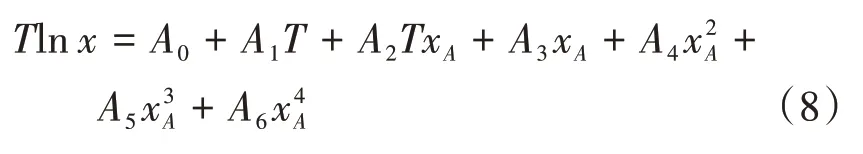
式中:A0、A1、A2、A3、A4、A5和A6是該模型的參數,可以通過最小二乘法將Tlnx與T、TxA、xA、x2A、x3A、x4A進行非線性回歸獲得,結果如表5所示。
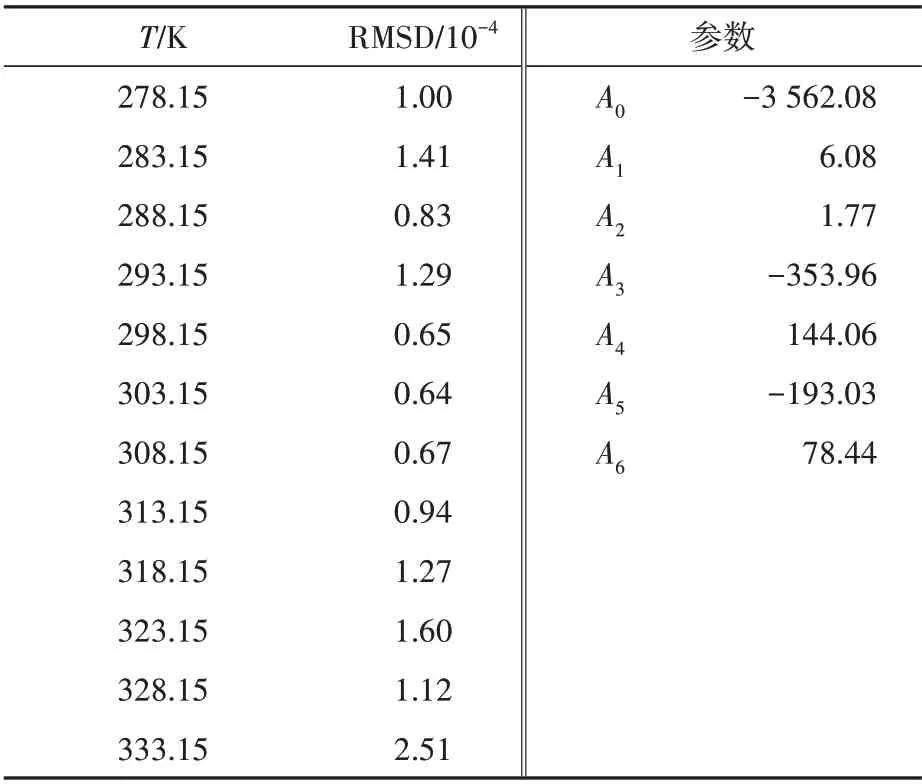
表5 奧美拉唑二元溶劑體系的Jouyban-Acree模型參數
2.5 標準偏差
通過模型擬合,可得到擬合計算數據xcal,通過實驗數據x和計算數據xcal之間相對偏差比較,可數據化表現出各模型擬合情況,相對偏差數據詳見表3~5。由表3~5 可知,修正的Apelblat 模型和Jouyban-Acree 模型在溫度較低情況下,其相對偏差值相對較大,隨著溫度的升高,相對偏差值逐漸變小。這可能是因為溶解度數值相對較小時,其相對偏差值可能相對較大。
相對標準偏差亦稱均方根誤差[18],可用來描述預測值與真實值的偏差情況,也常用于衡量實驗數據與計算數據的偏差。本研究中用其評估比較各模型與實驗數據的擬合適用情況。

式中:N表示實驗點的個數,x和xcal分別表示實驗數據和計算數據。表3~5 列出了相應模型的RMSD值。
由表3~5 可知,修正的Apelblat 模型、CNIBS/R-K 模型和Jouyban-Acree 模型的RMSD 值之和分別為4.66×10-4、1.47×10-4和1.393×10-3。由此可見,CNIBS/R-K 模型擬合效果最好。修正的Apelblat模型更關注于溫度對溶解度的影響,Jouyban-Acree 模型更多從整體闡述二元溶劑體系中的溶劑間比例對溶解度的影響,可以通過上述2 種模型實現對CNIBS/R-K模型的補充完善。
2.6 熱力學參數
范德霍夫分析是熱力學領域中常用的方法。標準摩爾溶解焓(ΔsolH0m)的表達式為
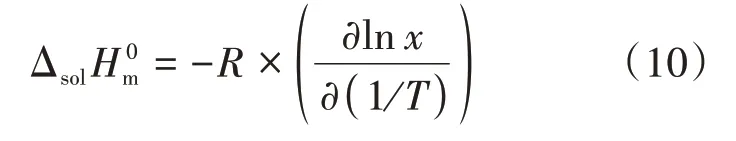
式中:R為通用氣體常數(8.314 J/(mol·K))。平均溫度時,標準摩爾溶解焓亦可用式(10)表達[19-20]。由此可以得到式(11)。
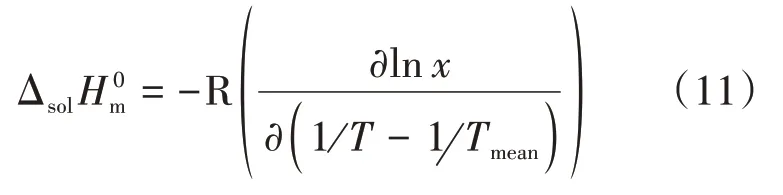
式中:Tmean表示實驗溫度范圍的平均溫度,即305.65 K。圖3即為奧美拉唑溶解度lnx與(1T-1Tmean)對應的曲線[21]。摩爾吉布斯能量方程(ΔsolG0m)可以表示為

根據吉布斯方程,可以得到溶液的標準摩爾熵(ΔsolS0m)。同時可以得出吉布斯能對應的焓和熵的貢獻度(分別以ξH和ξS表示)[22],為判斷溶解過程的狀態與自發性提供基礎。
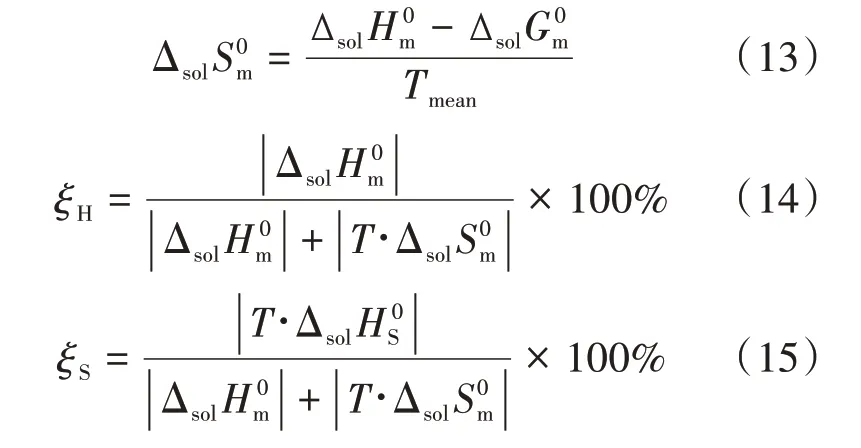
平均溫度下奧美拉唑在二元溶劑體系溶解過程的熱力學函數ΔsolH0m、ΔsolS0m、ΔsolG0m、ξH和ξS的值見圖3和表6。由圖3和表6可知,熱力學參數ΔsolH0m和ΔsolG0m均為正值,這說明奧美拉唑在所研究的二元溶劑體系中的溶解過程是吸熱和非自發的。此外,所有的ξH均高于61.45%,表明在溶解過程中焓是標準吉布斯能的主要貢獻者。同時,可以發現,伴隨著甲醇摩爾分數的梯度上升,標準摩爾熵梯度隨之增加,而標準吉布斯能呈現一定比例的等額下降,這說明在所研究的二元溶劑體系中,甲醇所占比例的上升在一定程度上增加了溶液體系混亂度,從而促進奧美拉唑的溶解過程。
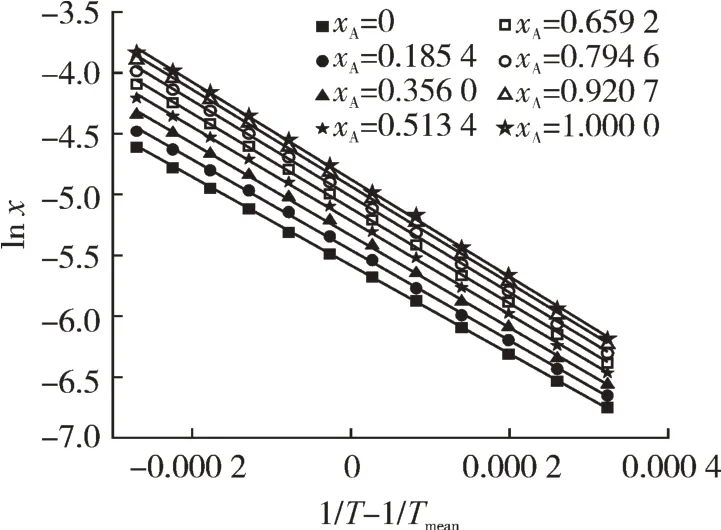
圖3 二元溶劑體系中奧美拉唑的摩爾分度溶解度(ln x)對應(1/T-1/Tmean)的范德霍夫分析
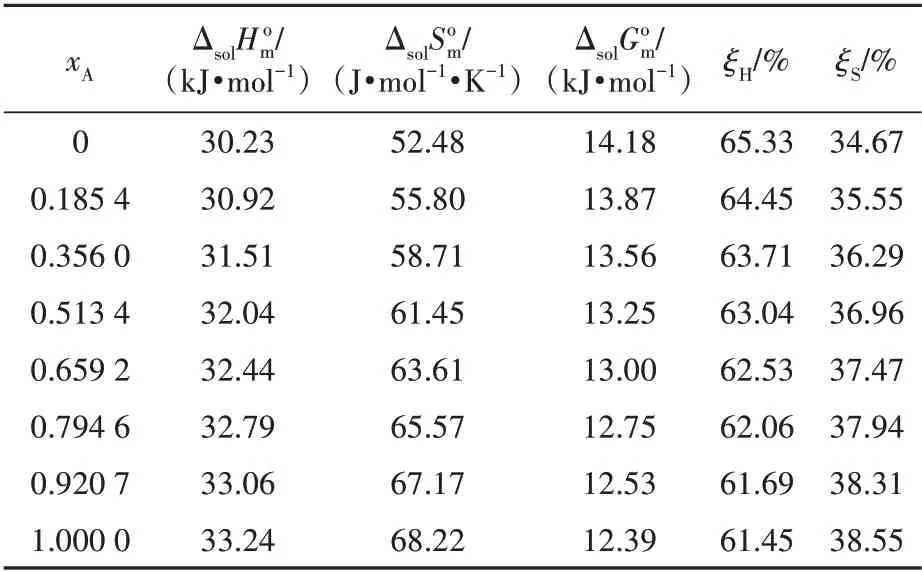
表6 平均溫度下奧美拉唑在二元溶劑體系溶解過程的熱力學函數
3 結論
1)奧美拉唑在甲醇和乙腈二元溶劑中的溶解度隨溫度升高而增加,隨甲醇比例增加而增加。
2)采用修正的Apelblat 模型、CNIBS/R-K 模型和Jouyban-Acree 模型均可成功擬合溶解度數據,其中CNIBS/R-K 模型因RMSD 值最小而擬合情況更好,并可以通過其他2 個模型實現對CNIBS/R-K模型的補充完善。
3)由范德霍夫分析的熱力學參數和吉布斯方程可知,奧美拉唑在甲醇和乙腈二元溶劑體系中的溶解過程是吸熱的、非自發的。
由此可見,本研究的實驗數據和參數能在奧美拉唑的純化分析工藝上提供一定指導,同時在實際工業生產中,在奧美拉唑的色譜分析、化合物純化等方面具有一定的參考意義。諸如利用熱力學數據,在色譜分析、化合物測定特別是檢驗方法學開發時,作為流動相的甲醇比例上升時,可一定程度上促進奧美拉唑的溶解,實現對奧美拉唑分離、測定的作用。

