乳塊散結顆粒制備工藝研究
周維利,孫銅,王坤
(山東省食品藥品檢驗研究院,山東 濟南 250101)
乳塊散結顆粒由丹參、川楝子、皂角刺、柴胡(醋制)、赤芍、醋香附、夏枯草、鱉甲(醋制)、橘葉、昆布、王不留行和淫羊藿組成,功能活血化瘀,疏肝理氣,軟堅散結。臨床上用于肝氣瘀滯,痰瘀互結所致的乳腺增生。本試驗以丹參素含量為指標,對其提取和制備工藝進行了研究,現報道如下。
1 儀器與材料
1.1 儀器 HS-337電子分析天平(邢臺慧思科技有限公司);ESJ203-S電子分析天平(洛陽美優實驗設備有限公司);KQ3200DE型數控超聲波清洗器(昆山市超聲儀器有限公司);島津LC-20高效液相色譜儀(島津);Shimpack VP-ODS(C18柱,4.6 mm×250 mm,5 μm);LC-RE-5000旋轉蒸發儀(上海力辰儀器科技有限公司);101-1AB電熱恒溫干燥箱(金壇市水北科普實驗儀器廠)。提取設備、離心機。
1.2 試劑 丹參、川楝子、皂角刺、柴胡(醋制)等藥材飲片(濟南漱玉平民大藥房有限公司)、丹參素對照品(110855-201614,20 mg/支,標示含量98.1%,中國食品藥品檢定研究院);乳塊散結顆粒(自制);陰性對樣品(自制);乙腈、甲醇和冰醋酸為色譜純,水為重蒸去離子水,草酸為分析純。
2 方法與結果
2.1 丹參素含量測定方法
2.1.1 色譜條件與系統適應性試驗[1-6]以十八烷基硅烷鍵合硅膠為填充劑;以乙腈-甲醇-水-冰醋酸(0.5∶8∶92∶1)為流動相;檢測波長為280 nm。理論板數按丹參素峰計算不得低于3 500。
2.1.2 對照品溶液 取丹參素鈉對照品適量,精密稱定,加50%甲醇溶液制成每1 mL含50 μg的溶液(相當于每1含丹參素45 μg),即得[7]。
2.1.3 供試品溶液 ①取乳塊散結顆粒適量,研細,取約1.0 g,精密稱定,置離心管中,加水2 mL及中性氧化鋁(100~200目)1.5 g,攪拌均勻,用水洗滌3次,每次10 mL,離心(3 000 r·min-1)棄去水洗液,再用5%草酸溶液攪拌提取3次,每次8 mL,離心,合并5%草酸溶液,置25 mL量瓶中,加5%草酸溶液至刻度,搖勻,濾過,取續濾液,即得[7];②取工藝研究試驗得清膏2 mL,置離心管中,中性氧化鋁(100~200目)1.5 g,攪拌均勻,同①操作,即得。
2.1.4 陰性溶液 制備不含丹參的乳塊散結顆粒,按“2.1.3”項下操作,即得陰性樣品。
2.1.5 專屬性 分別取乳塊散結顆粒供試品、丹參素對照品以及陰性對照3種溶液,按“2.1.1”項下色譜條件進樣、測定,不含丹參的陰性對照在丹參素峰處無干擾,見圖1~3。
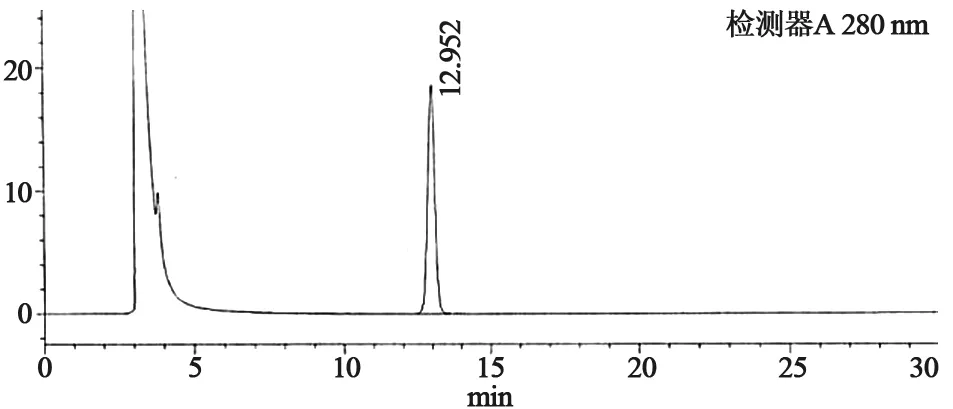
圖1 丹參素對照品HPLC圖
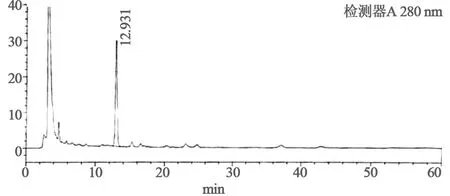
圖2 乳塊散結顆粒HPLC圖
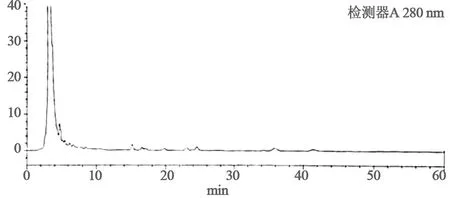
圖3 不含丹參陰性HPLC圖
2.1.6 線性與范圍 取丹參素鈉對照品適量,精密稱定,加5%草酸溶液溶解并稀釋至刻度,作為丹參素鈉對照品貯備液(相當于含丹參素264.55 g·mL-1);分別精密量取1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0 mL貯備液置25 mL量瓶中,用5%草酸溶液稀釋至刻度,搖勻,作為丹參素對照品溶液。分別吸取上述對照品溶液,按“2.1.1”項下條件進樣、測定,以濃度C和峰面積A計算,得回歸方程為A=78 937C+928.57,R2=0.999 3;丹參素在10.58~84.65 μg·mL-1范圍內,峰面積與濃度呈良好線性關系。
2.1.7 精密度試驗 取丹參素對照品溶液(42.33 μg·mL-1)按“2.1.1”項下色譜條件進樣、測定,連續進樣6次,峰面積RSD為1.21%。
2.1.8 重復性試驗 取20200502批乳塊散結顆粒(1.02 mg·g-1)樣品6份,按“2.1.3”項下制備,按“2.1.1”項下色譜條件進樣、測定,重復測定6次,丹參素含量的RSD為0.996%。
2.1.9 穩定性試驗 取20200502批乳塊散結顆粒供試品溶液分別于0、2、4、6、8和12 h進樣測定,丹參素峰面積RSD為0.867%,供試品溶液在室溫條件下在12 h內穩定。
2.1.10 回收率試驗 取20200502批乳塊散結顆粒適量,研細,取約0.5 g,精密稱定,取6份,照“2.1.3”項下方法處理,并分別加入丹參素對照品溶液(52.91 μg·mL-1)10.0 mL,混勻,按“2.1.1”項下色譜條件進樣、測定,丹參素平均回收率為97.45%,RSD為1.56%。
2.2 工藝研究
2.2.1 提取工藝研究 通過預試驗及參考相關文獻,經預試驗后以水為提取溶劑。分別稱取丹參200 g、川楝子40 g、皂角刺64 g、柴胡(醋制)48 g、赤芍56 g、醋香附40 g、夏枯草40 g、鱉甲(醋制)40 g、王不留行64 g、橘葉64 g、昆布64 g、淫羊藿80 g,共9份,每份計800 g,按表1進行試驗,以丹參素含量為評價指標進行試驗,因素水平見表1~3。

表1 水提因素水平表
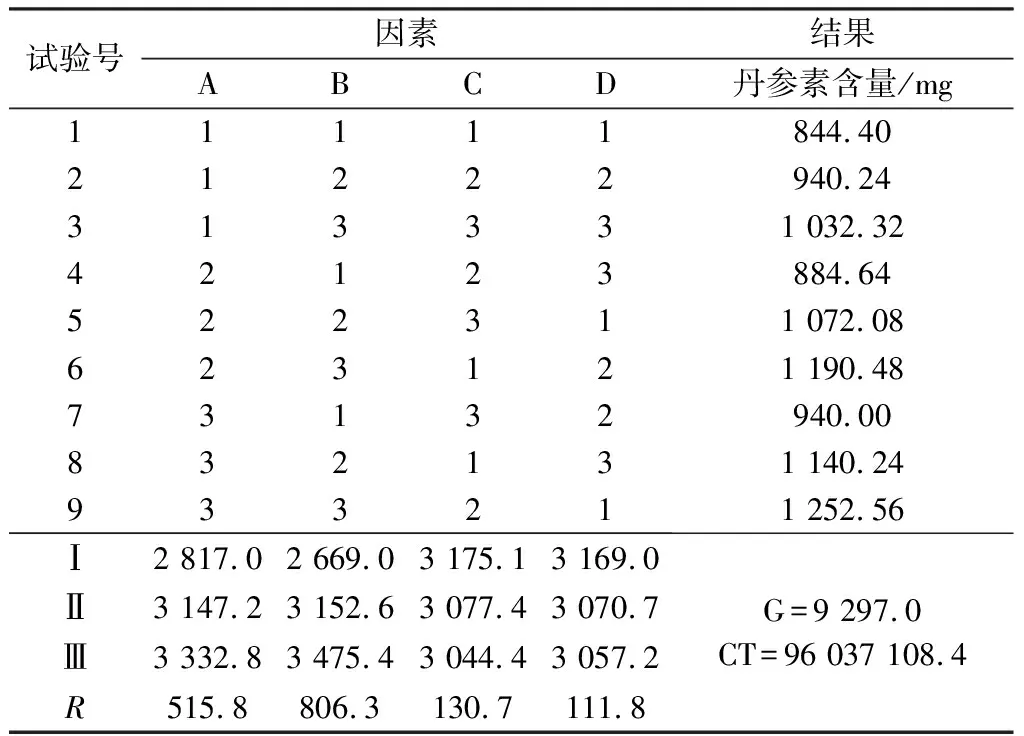
表2 L9(34)正交試驗設計與結果
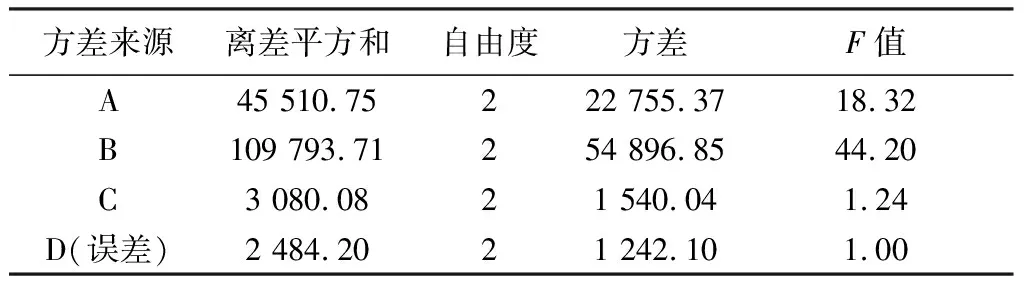
表3 水提方差分析
由直觀分析可知,各因素影響依次為B>A>C,最佳為A3B3C2(藥材加8倍量水提取3次,每次3 h);考慮到生產成本、效率和人工等因素,綜合考慮選擇A2B2C1(藥材加8倍量水提取2次,每次2 h)。
2.2.2 提取工藝驗證 稱取乳塊散結顆粒處方中各藥材飲片6份,每份800 g,分別按A3B3C1和A2B2C1各提取3次,濃縮為1.26(80 ℃)的清膏,測定丹參素含量,結果見表4。
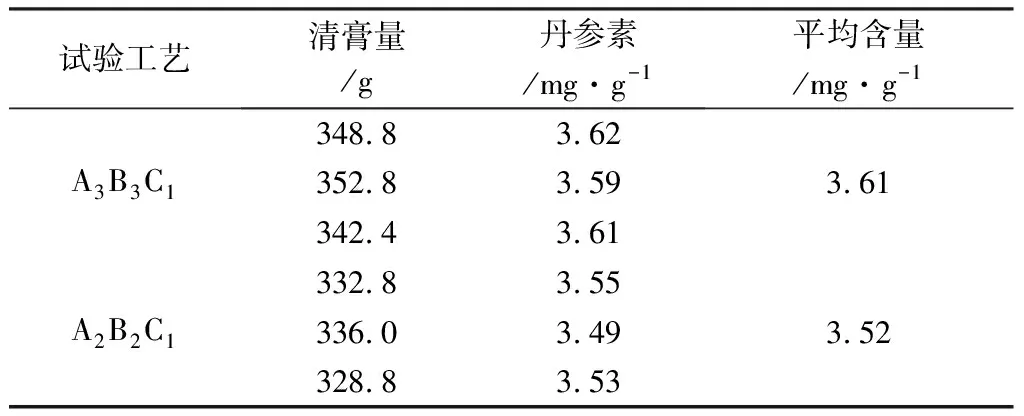
表4 提取工藝驗證試驗結果表
按A3B3C1與A2B2C1工藝各提取3次,工藝A2B2C1與工藝A3B3C1相比,丹參素含量基本無差別,故選擇按A2B2C1進行提取。
2.2.3 醇沉工藝研究
2.2.3.1 醇沉濃度試驗 稱取乳塊散結顆粒處方中各藥材飲片4份,每份800 g,按A2B2C1提取,提取液濾過,濾液合并濃縮至1.27(80 ℃)的清膏,分成4份,以不同含醇量進行醇沉,攪勻,靜置48 h,濾取上清液,回收乙醇,濃縮為稠膏,測定丹參素含量與稠膏率,結果見表5。

表5 醇沉濃度試驗結果表
乙醇濃度為75%進行醇沉時丹參素含量與出稠膏均合適,故選擇醇沉濃度為75%。
2.2.3.2 靜置時間試驗 按“2.2.3.1”項下方法制備清膏,測定含量,分成4份,加乙醇進行醇沉,靜置不同時間,濾取上清液,回收乙醇,濃縮為稠膏,測定丹參素含量與稠膏率,結果見表6。
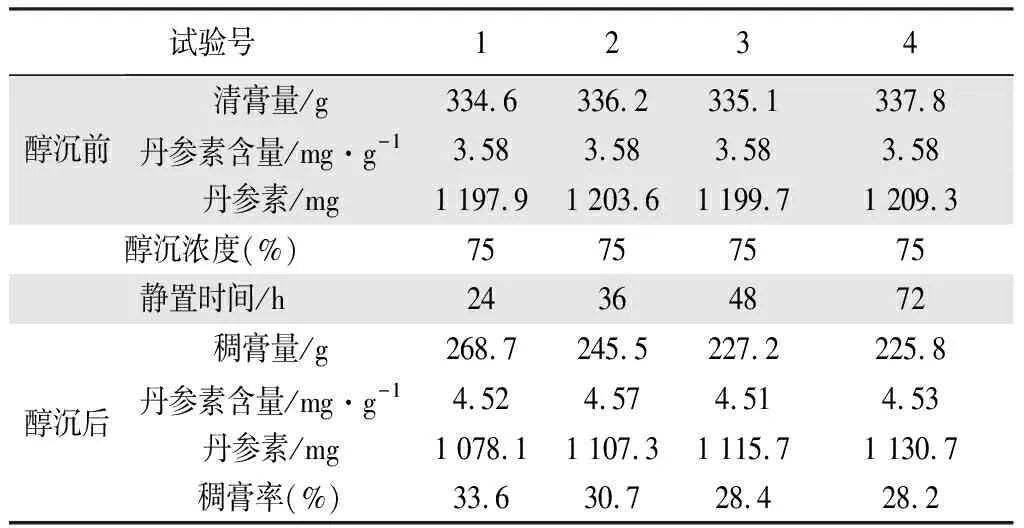
表6 醇沉后靜置時間試驗結果表
藥液靜置48 h,分層明顯,容易過濾,故選擇靜置時間為48 h。
2.2.4 成型工藝研究 取丹參200 g、川楝子40 g、皂角刺64 g、柴胡(醋制)48 g、赤芍56 g、醋香附40 g、夏枯草40 g、鱉甲(醋制)40 g、王不留行64 g、橘葉64 g、昆布64 g、淫羊藿80 g,每份計800 g,4份,按“2.2.3.1”項下方法制備清膏,使乙醇濃度達75%,醇沉,靜置,濾過,回收乙醇,濃縮為稠膏,分成4份,加入不賦形劑制軟材,以14目尼龍網篩制粒,75 ℃干燥,16目篩整粒。
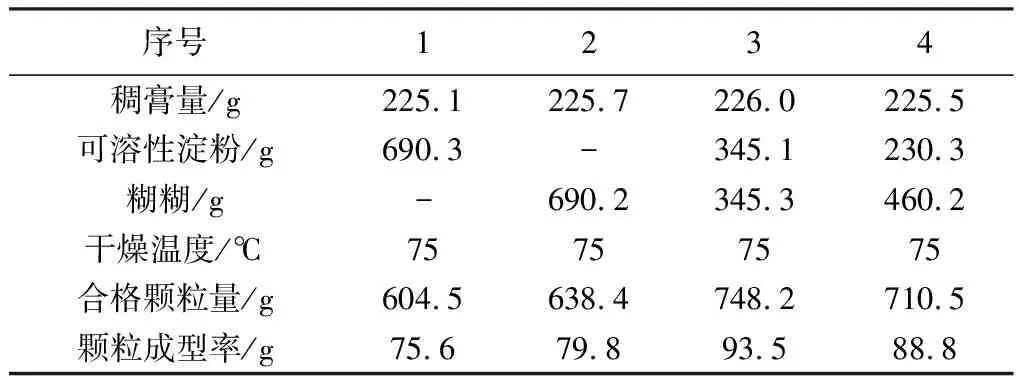
表7 賦形劑試驗結果表
結果:在成型試驗中,以可溶性淀粉與糊精(1∶1)賦形劑時易制粒,顆粒成型率最佳。
3 討論
3.1 處方中藥材飲片的各主要藥理成分均溶于水,以水溶性成分丹參素含量為指標,經預試驗后以水為溶劑進行了正交優選,對乳塊散結顆粒的最佳直觀工藝和綜合考慮后提取工藝各進行3批驗證試驗,最終選定提取工藝為藥材飲片加8倍量水提取2次,每次2 h。為最大可能保留有效成分,易于成型,減少顆粒裝量,便于患者服用,水提液濃縮至相對密度為1.25~1.30(80 ℃)時進行了醇沉,減少出膏量。
3.2 可溶性淀粉為白色細膩粉末,是可溶顆粒的良好稀釋劑,并有矯味及黏合作用;糊精為白色或微帶黃色的細膩粉末,不溶于醇,微溶于水,能溶于沸水成黏膠狀溶液,黏性強,并呈弱酸性[8]。在顆粒的成型試驗中,醇沉后上清液濃縮成稠膏,加入可溶性淀粉與糊精(1∶1)為賦形劑制粒,在賦形劑與稠膏比大于3時易于制粒,顆粒成型性好,簡化了清膏干燥、粉碎的工序,可節約資源與人工,提高生產效率。

