植物內生真菌Fusarium guttiforme次生代謝產物研究
李慧媛,岳婧怡,王舉濤,2*,蔡百祥*
1安徽中醫藥大學藥學院;2安徽省中藥研究與開發重點實驗室,合肥 230012;3蕪湖職業技術學院,蕪湖 241006
內生真菌指一類生活在健康植物組織體內但不引起植物感染病害的微生物,其具有獨特的生物學特性,與宿主植物互生互利,且產生多種重要的次生代謝產物,可用于制藥、農業,以及具有一系列生物活性的食品工業[1-3]。
鐮刀菌屬(Fusarium)是一類廣泛分布于土壤和植物體內的絲狀真菌,近年來,諸多學者對鐮刀菌屬真菌次生代謝產物進行研究,發現其不僅能產生伏馬毒素(fumonis)、單端孢霉烯族毒素(trichothecenes)和玉米赤霉烯酮(zearalenones)三類主要真菌毒素,還能產生萜類、酰胺、醌類和聚酮類等具有廣泛的顯著的生物活性的次生代謝產物[4-9]。調研相關文獻,發現植物內生菌Fusariumguttiforme次生代謝產物的研究較少,為進一步豐富Fusariumguttiforme代謝產物的化學成分,同時考慮固體發酵對其次生代謝產物的影響,本文利用多種色譜分離方法和現代波譜技術,對植物內生真菌Fusariumguttiforme大米發酵次生代謝產物進行化學成分研究,并同時對所獲得的化合物進行體外抗炎活性篩選,旨在發現結構新穎和活性較好的先導分子,以期豐富鐮刀屬內生真菌次生代謝產物。
1 材料與方法
1.1 儀器和材料
AV-500 MHz型核磁共振譜儀(Bruker公司,德國);UPLC-IT-TOF 質譜(Shimadzu Crop公司,日本);LC-3000半制備型HPLC(北京同恒創新科技有限公司,中國);Waters Xbridge C18(250 mm ×20mm,5 μmol/L)色譜柱(Waters公司,美國);ODS C18(45~60 μmol/L)(日本京都YMC株式會社,日本);Sephadex LH-20凝膠(GE公司,瑞士);柱層析硅膠200~300目(青島海洋化工廠,中國);HSGF254 薄層層析硅膠板(煙臺江有硅膠開發有限公司,中國)。
1.2 菌種來源
內生真菌Fusariumguttiforme(GenBank accession No.KC464629.1)來源于安徽中醫藥大學天然藥化教研室,4 ℃保存。
1.3 菌種的發酵提取與分離
將保存在斜面試管中的待發酵菌株接種到滅菌后的PDA培養基(馬鈴薯浸粉3 g/L、葡萄糖20 g/L、瓊脂14.0 g/L)上,于28 ℃恒溫培養箱中培養活化5~7天,用滅菌后的5 mm打孔器打孔取其菌餅,將菌餅置于滅菌后的大米固體培養基(100 g大米和110 mL蒸餾水置于1 L的錐形瓶中,121 ℃高壓滅菌20 min)中,于28 ℃恒溫發酵25天。25天后停止發酵,在每個錐形瓶中加入500 mL乙酸乙酯進行提取,連續減壓回流3次后得到待分離浸膏。
該乙酸乙酯部位(20 g)經硅膠柱色譜(200~300目),依次以石油醚-丙酮系統梯度洗脫(100∶0→0∶1,V/V)和二氯甲烷-甲醇系統洗脫(1∶1,V/V),共得到9個組分(A~I)。Fr.B(0.5 g)經Sephadex LH-20柱(MeOH,100%)處理并通過半制備型HPLC(MeOH-H2O,50∶50 V/V)分離得到化合物7(10 mg)。Fr.D(5 g)經MCI(MeOH-H2O,1∶1→0:1,V/V),RP-C18柱(MeOH-H2O,30∶70→100∶00,V/V)洗脫得到S1~S3三個亞組分。S2(0.6 g)經Sephadex LH-20柱(CHCl3-MeOH,1∶1,V/V和MeOH)洗脫,并采用pre-HPLC(MeCN-H2O,60∶40 V/V)得到化合物2(5 mg)、3(8 mg)。Fr.E7(6 g)經Sephadex LH-2柱(MeOH,100%)洗脫,并通過pre-HPLC(MeOH-H2O,60∶40 V/V)純化,得到化合物1(6 mg)和5(11 mg)。Fr.F(3g)經ODS柱(MeOH-H2O,10∶90→100∶0,V/V)梯度洗脫,得到四個亞組分SF1~SF4。SF2(0.2 g)通過pre-HPLC(MeCN-H2O,60∶40 V/V)純化,得到化合物4(5 mg)和化合物6(4 mg)。
1.4 化合物NO抑制活性的測試
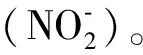
NO生成抑制率 = (OD非藥物處理組-OD樣品組)/
OD非藥物處理組× 100%
2 結果
2.1 結構鑒定
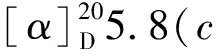

表1 化合物1的1H和13C NMR數據(500和125 MHz,CDCl3)
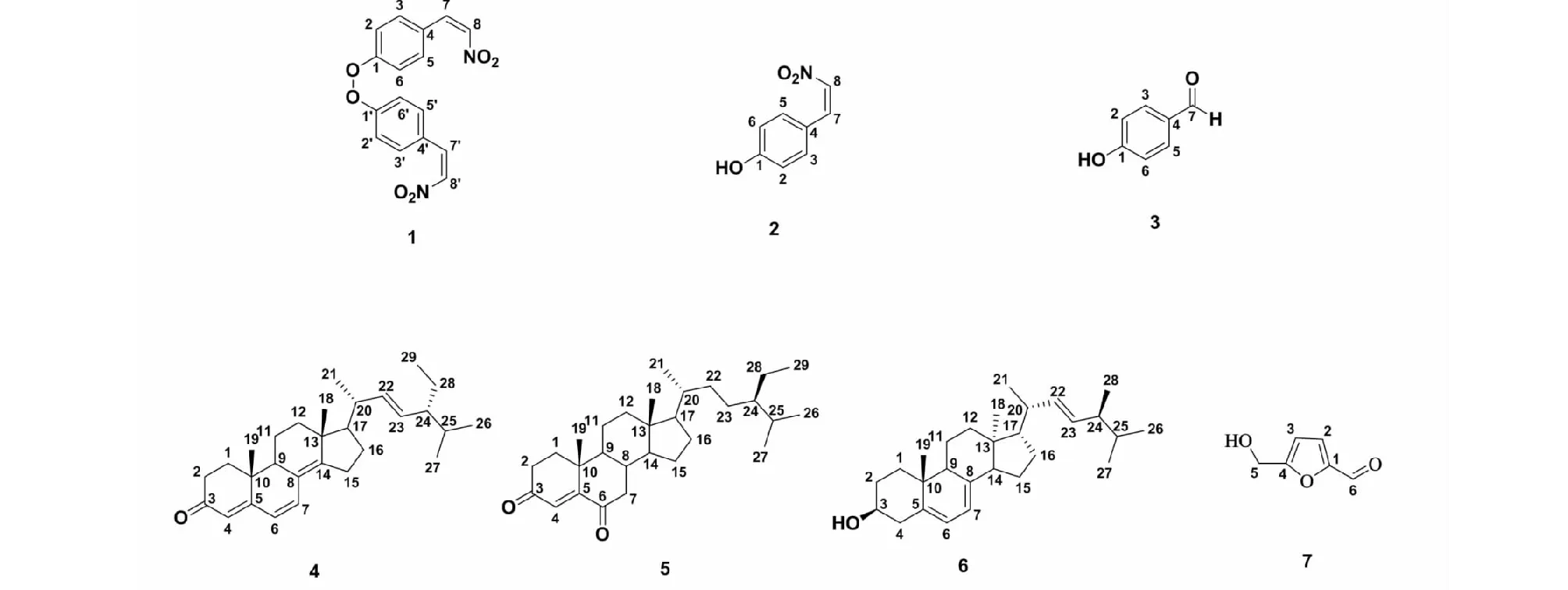
圖1 化合物1~7的結構Fig.1 Structures of compounds 1-7
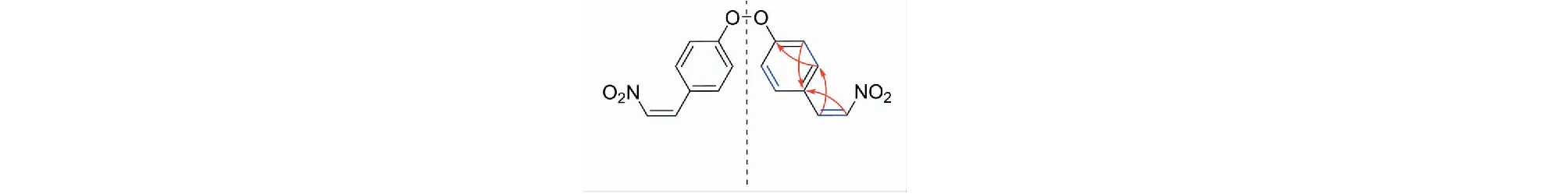
圖2 化合物1的關鍵1H-1H COSY (-) 和 HMBC (→) 相關性Fig.2 The key 1H-1H COSY (-) and HMBC (→) correlations of compound 1
化合物2白色粉末;分子式為C8H7NO2。1H NMR(400 MHz,(CD3)2CO)δ:9.26(1H,br s,1-OH),8.05(1H,d,J= 13.5 Hz,H-7),7.85(1H,d,J= 13.5 Hz,H-8),7.72(2H,d,J= 8.0 Hz,H-3,5),6.98(2H,d,J= 8.0 Hz,H-2,6);13C NMR(125 MHz,(CD3)2CO);δ:162.2(C-1),117.1(C-2,C-6),132.7(C-3,C-5),122.7(C-4),140.0(C-7),135.9(C-8)。上述數據與文獻[10]報道基本一致,因此確定化合物2為(Z)-1-hydroxy-4-(2-nitroethenyl)-benzene。
化合物3無色粉末;易溶于甲醇,分子式C7H6O2為。ESI-MS:121 [M-H]-;1H NMR(400 MHz,CD3OD)δ:9.85(1H,s,CHO),7.81(2H,d,J= 8.4 Hz,H-2,6),7.01(2H,d,J= 8.4 Hz,H-3,5);13C NMR(125 MHz,CD3OD)δ:129.8(C-1),132.6(C-2,6),116.0(C-3,5),161.7(C-4),191.4(C-7)。上述數據與文獻[11]報道基本一致,因此確定化合物3為對羥基苯甲醛。
化合物4白色針狀結晶;分子式為C29H43O。1H NMR(500 MHz,CDCl3)δ:6.59(1H,d,J= 9.5 Hz,H-6),6.02(1H,d,J= 9.5 Hz,H-7),5.73(1H,br s,H-4),5.25(1H,dd,J= 16.5,6.7 Hz,H-23),5.18(1H,dd,J= 16.5,6.3 Hz,H-22),2.54(1H,m,H-2α),2.48(1H,m,H-2β),2.02(1H,m,H-1α),1.82(1H,m,H-1β),1.05(3H,d,J= 6.0Hz,H-21),0.96(3H,s,H-19),0.94(3H,s,H-18),0.92(3H,d,J= 7.0 Hz,H-27),0.86(3H,d,J= 7.0 Hz,H-26),0.83(3H,t,J= 6.2 Hz,H-29);13C NMR(125 MHz,CDCl3)δ:35.6(C-1),19.0(C-2),199.6(C-3),123.0(C-4),164.4(C-5),124.4(C-6),134.0(C-7),124.5(C-8),44.3(C-9),36.8(C-10),25.4(C-11),34.1(C-12),44.0(C-13),156.1(C-14),34.1(C-15),27.7(C-16),55.7(C-17),16.6(C-18),18.9(C-19),39.3(C-20),21.2(C-21),132.5(C-22),135.0(C-23),42.8(C-24),33.1(C-25),19.6(C-26),20.0(C-27),29.7(C-28),17.6(C-29)。上述數據與文獻[12]報道基本一致,因此確定化合物4為stigmasta-4,6,8(14),22-tetraen-3-one。
化合物5無色晶體;分子式為C29H46O2。ESI-MS:427 [M+H]+;1H NMR(400 MHz,CDCl3)δ:6.17(1H,s,H-4),2.53(1H,m,H-2α),2.46(1H,m,H-2β),2.14(1H,dd,J= 5.0,2.8 Hz,H-1β),1.91(1H,dd,J= 9.9,5.7 Hz,H-1α),1.17(3H,s,H-19),0.93(3H,d,J= 6.4 Hz,H-21),0.85(3H,t,J= 7.5 Hz,H-29),0.84(3H,d,J= 7.1 Hz,H-26),0.81(3H,d,J= 6.8 Hz,H-27),0.72(3H,s,H-18);13C NMR(150 MHz,CDCl3)δ:35.5(C-1),33.9(C-2),199.5(C-3),125.4(C-4),161.1(C-5),202.4(C-6),46.8(C-7),34.2(C-8),51.0(C-9),39.8(C-10),20.9(C-11),39.1(C-12),42.5(C-13),55.8(C-14),23.9(C-15),28.0(C-16),56.5(C-17),11.9(C-18),17.5(C-19),36.0(C-20),18.7(C-21),33.8(C-22),26.0(C-23),45.8(C-24),29.1(C-25),19.8(C-26),18.9(C-27),23.0(C-28),11.8(C-29)。上述數據與文獻[13]報道基本一致,因此確定化合物5為stigmast-4-ene-3,6-dione。
化合物6無色針狀結晶;分子式為C28H43O。1H NMR(500 MHz,CDCl3),δ:5.57(1H,dd,J= 6.6,2.5 Hz,H-6),5.38(1H,m,H-7),5.21(1H,dd,J= 15.9,6.6 Hz,H-23),5.18(1H,dd,J= 15.9,6.6 Hz,H-22),1.03(3H,d,J= 6.6 Hz,H-21),0.94(3H,s,H-19),0.91(3H,d,J= 7.2 Hz,H-28),0.84(3H,d,J= 6.4 Hz,H-27),0.82(3H,d,J= 6.4 Hz,H-26),0.63(3H,s,H-18);13C NMR(125 MHz,CDCl3),δ:38.4(C-1),32.0(C-2),70.5(C-3),40.8(C-4),139.8(C-5),119.6(C-6),116.3(C-7),141.4(C-8),46.3(C-9),37.0(C-10),21.1(C-11),39.1(C-12),42.8(C-13),54.6(C-14),23.0(C-15),28.3(C-16),55.7(C-17),12.1(C-18),16.3(C-19),40.4(C-20),21.1(C-21),135.6(C-22),132.0(C-23),42.3(C-24),33.1(C-25),20.0(C-26),19.7(C-27),17.6(C-28)。上述數據與文獻[14]報道基本一致,因此確定化合物6為麥角甾醇。
化合物7白色粉末;分子式為C6H6O3。1H NMR(400 MHz,CD3OD),δ:9.43(1H,s,CHO),7.28(1H,d,J= 3.2 Hz,H-3),6.48(1H,d,J= 3.6 Hz,H-4),4.51(2H,s,H-6);13C NMR(100 MHz,CD3OD),179.5(C-1),153.8(C-2),124.8(C-3),110.9(C-4),163.2(C-5),57.6(C-6)。上述數據與文獻[15]報道基本一致,因此確定化合物7為5-羥甲基糠醛。
2.2 生物活性
評估化合物1~7在LPS刺激的RAW 264.7細胞中抑制NO產生的能力。結果(見表2)顯示化合物1和2表現出較弱的NO抑制活性,IC50值為48.1和46.6 μmol/L,陽性對照LNMMA(NG-單甲基-L-精氨酸鹽酸鹽)的IC50為38.2 μmol/L。
3 討論
本研究從植物內生菌F.guttiforme大米發酵物的乙酸乙酯部位分離鑒定了7個化合物,其中化合物1為一種新型的含過氧鍵的二聚苯衍生物,化合物2~7分別為苯衍生物、酚酸類、甾體類化合物、麥角甾醇及糠醛類化合物,均首次從該真菌中分離得到,極大地豐富了鐮刀菌屬次生代謝產物結構的多樣性。同時,二聚體或多聚體衍生物大多具有較強的藥理活性和穩定性,其中對二聚體類衍生物研究偏多,Paik等[16]報道了一系列含有苯環結構的二聚體衍生物,其中鄰苯二甲酸酯二聚體對人子宮頸癌具有很好的選擇性和殺傷性,對正常宮頸細胞沒有細胞毒性作用。烷基、酯基、醚鍵等連接的青蒿素二聚體往往比單核化合物具有更高體內外抗瘧疾的活性、更低的毒副作用和穩定的理化性質[17,18]。此外,已有報道表明苯環衍生物、酚類和甾體類化合物等具有抗炎、抗氧化、抗腫瘤、抑菌等活性,因此本文對從F.guttiforme中分離所得到的化合物1~7抗炎活性進行體外初步評估,結果表明化合物1和2表現出一定的NO生成抑制活性,IC50值為48.1和46.6 μmol/L,初步闡明了鐮刀菌F.guttiforme的活性物質基礎,為后續藥理實驗的開展提供參考,同時亦可為鐮刀菌相關研究提供一定科學價值。
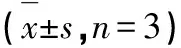
表2 化合物1~7在RAW 246.7細胞中抑制NO產生的IC50值

