2-二氟溴甲基-1,3-苯并噻唑的簡便合成
徐榮福, 廖富民, 蔡 穎, 劉晉彪
(江西理工大學 材料冶金化學學部 江西省功能分子材料化學重點實驗室,江西 贛州 341000)
分子中引入二氟亞甲基(—CF2—),不僅能改變分子的物理、化學性質,并且二氟亞甲基作為氧原子的等極體和等電體,均能很好地替代—C=O, CHOH和CH2等基團[1],隨著含偕二氟取代高活性化合物的出現,使得含偕二氟亞甲基結構單元化合物的高效合成倍受關注[2-4]。因此,科學家們越來越關注將偕二氟亞甲基引入到有機化合物中,從而試圖改善化合物的理化性能。
2-二氟溴甲基-1,3-苯并噻唑是一類非常重要的含二氟亞甲基的有機合成子,2-二氟溴甲基-1,3-苯并噻唑可在銅的催化或促進下發生芳(烷、烯)基化反應[5-15],aldol反應[16-21],氧(硫)取代反應[9,22]來構建二氟亞甲基連接的含1,3-苯并噻唑化合物,在作為二氟亞甲基連接體的同時,也引入了苯并噻唑這一藥效基團和光電性能基團。目前,2-二氟溴甲基-1,3-苯并噻唑的主要合成方法是由2-巰基芳胺與二氟(溴)乙酸的縮合反應來獲得[9,23],但還存在需多步反應以及底物范圍有待拓展的不足。因此,研究2-二氟溴甲基-1,3-苯并噻唑的高效、簡便合成方法具有重要的意義。
基于實驗室前期及前人的研究[9,23],本文以2-巰基芳胺1與二氟溴乙酸2為原料,在不外加催化劑條件下,以氯苯為溶劑,于100 ℃下發生縮合反應,簡便合成了8個2-二氟溴甲基-1,3-苯并噻唑化合物(3a~3i, Scheme 1),產率39%~88%,產物結構經1H NMR,13C NMR,19F NMR和HR-MS(ESI)表征確認。
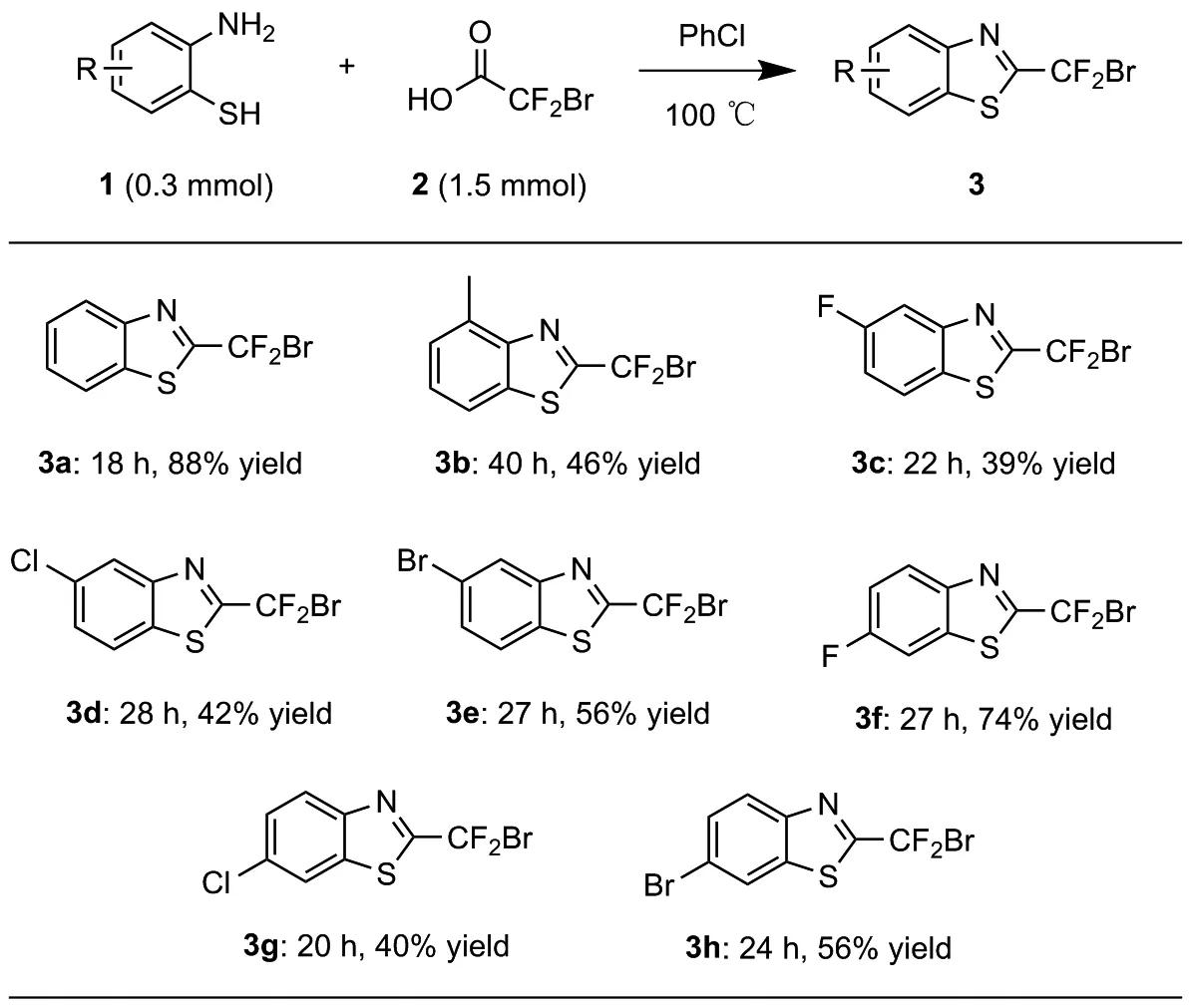
Scheme 1
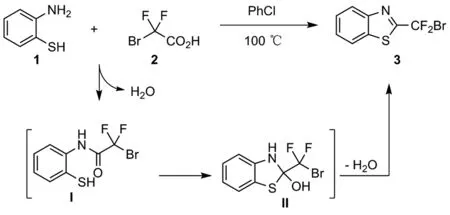
Scheme 2
1 實驗部分
1.1 儀器與試劑
Bruker-500M型超導核磁共振儀(TMS為內標);Thermo Scientific Q Exactive組合型四極桿Orbitrap質譜儀。
試劑或溶劑皆為市售分析純或化學純試劑。
1.2 3的合成通法
依次將2-巰基芳胺1(0.3 mmol)和二氟溴乙酸2(1.5 mmol)加入盛有3 mL氯苯的封管中,100 ℃下加熱攪拌反應18~40 h。經薄層色譜法監測反應進程,反應完畢后,反應液冷卻至室溫后直接上樣柱層析分離得純品3。
2-二氟溴甲基-1,3-苯并噻唑(3a): 黃色油狀液體,產率88%;1H NMR(500 MHz, CDCl3)δ:8.19(d,J=5.0 Hz, 1H), 7.96(s, 1H), 7.60~7.53(m, 2H);13C NMR(125 MHz, CDCl3)δ: 162.12(t,J=31.3 Hz, 1C), 151.87, 135.19, 127.36, 127.33, 124.98, 121.99, 113.45(t,J=301.3 Hz, 1C);19F NMR(471 MHz, CDCl3)δ: -43.28, -43.30。
4-甲基-2-二氟溴甲基-1,3-苯并噻唑(3b): 白色固體,m.p.55~56 ℃,產率46%;1H NMR(500 MHz, CDCl3)δ: 7.77(d,J=10.0 Hz, 1H), 7.43~7.40(m, 1H), 7.38(d,J=10.0 Hz, 1H), 2.79(s, 3H);13C NMR(125 MHz, CDCl3)δ:160.70(t,J=31.3 Hz, 1C), 151.51, 135.33, 135.21, 127.64, 127.30, 119.25, 113.64(t,J=302.5 Hz, 1C), 18.25;19F NMR(471 MHz, CDCl3)δ: -43.00; HR-MS(ESI):Exact mass calcd for C9H7BrF2NS {[M+H]+}:277.9445, found 277.9439。
5-氟-2-二氟溴甲基-1,3-苯并噻唑(3c): 白色固體,m.p.62~65 ℃,產率39%;1H NMR(500 MHz, CDCl3)δ:7.92~7.91(m, 1H), 7.86(d,J=10.0 Hz, 1H), 7.35~7.31(m, 1H);13C NMR(125 MHz, CDCl3)δ: 164.42, 162.21(d,J=243.8 Hz, 1C), 152.84(d,J=12.5 Hz, ̄1C), 130.69, 122.95(d,J=8.8 Hz, 1C), 116.62(d,J=25.0 Hz, 1C), 113.09(t,J=301.3 Hz, 1C), 110.97(d,J=23.8 Hz, 1C);19F NMR(471 MHz, CDCl3)δ: -43.80, -113.18; HRMS(ESI):Exact mass calcd for C8H4BrF3NS{[M+H]+}: 281.9194, found 281.9186.
5-氯-2-二氟溴甲基-1,3-苯并噻唑(3d): 白色固體,m.p.57~58 ℃,產率42%;1H NMR(500 MHz, CDCl3)δ: 8.16(s, 1H), 7.88(d,J=10.0 Hz, 1H), 7.52(d,J=10.0 Hz, 1H);13C NMR(125 MHz, CDCl3)δ: 163.86(t,J=31.3 Hz, 1C), 152.67, 133.58, 133.40, 128.07, 124.72, 122.77, 113.04(t,J=300.0 Hz, 1C);19F NMR(471 MHz, CDCl3)δ: -43.81; HR-MS(ESI):Exact mass calcd for C8H4BrClF2NS{[M+H]+}:297.8899, found 297.8892。
5-溴-2-二氟溴甲基-1,3-苯并噻唑(3e): 白色固體,m.p.60~61 ℃,產率56%;.1H NMR(500 MHz, CDCl3)δ: 8.33(s, 1H), 7.83(d,J=10.0 Hz, 1H), 7.65(d,J=10.0 Hz, 1H);13C NMR(125 MHz, CDCl3)δ: 163.63(t,J=31.3 Hz, 1C), 152.96, 133.94, 130.66, 127.82, 123.05, 121.06, 113.00(t,J=301.3 Hz, 1C);19F NMR(471 MHz, CDCl3)δ: -43.80; HR-MS(ESI):Exact mass calcd for C8H4Br2F2NS{[M+H]+}:341.8394, found 341.8380.
6-氟-2-二氟溴甲基-1,3-苯并噻唑(3f): 白色固體,m.p.57~60 ℃,產率74%;1H NMR(500 MHz, CDCl3)δ: 8.15~8.14(m, 1H), 7.64(d,J=10.0 Hz, 1H), 7.36~7.33(m, 1H);13C NMR(125 MHz, CDCl3)δ:162.51, 160.52, 148.52, 136.40(d,J=11.3 Hz, 1C), 126.31(d,J=10.0 Hz, 1C), 116.57(d,J=25.0 Hz, 1C), 113.10(d,J=301.3 Hz, 1C), 108.11(d,J=27.5 Hz, 1C);19F NMR(471 MHz, CDCl3)δ: -43.39, -111.52; HR-MS(ESI):Exact mass calcd for C8H4BrF3NS{[M+H]+}:281.9194, found 281.9188。
6-氯-2-二氟溴甲基-1,3-苯并噻唑(3g): 白色固體,m.p.74~75 ℃,產率40%;1H NMR(500 MHz, CDCl3)δ: 8.10(d,J=5.0 Hz, 1H), 7.95(s, 1H), 7.57(d,J=5.0 Hz, 1H);13C NMR(125 MHz, CDCl3)δ: 162.50(t,J=31.3 Hz, 1C), 150.40, 136.34, 133.58, 128.42, 125.79, 121.58, 113.08(t,J=301.3 Hz, 1C);19F NMR(471 MHz, CDCl3)δ: -43.59; HR-MS(ESI):Exact mass calcd for C8H4BrClF2NS{[M+H]+}: 297.8899, found 297.8891。
6-溴-2-二氟溴甲基-1,3-苯并噻唑(3h): 白色固體,m.p.74~76 ℃,產率56%;1H NMR(500 MHz, CDCl3)δ: 8.10(s, 1H), 8.03(d,J=5.0 Hz, 1H), 7.70(d,J=10.0 Hz, 1H);13C NMR(125 MHz, CDCl3)δ: 162.48(t,J=30.0 Hz, 1C), 150.69, 136.72, 131.08, 126.05, 124.54, 121.28, 113.03(t,J=301.3 Hz, 1C);19F NMR(471 MHz, CDCl3)δ: -43.61; HR-MS(ESI):Exact mass calcd for C8H4Br2F2NS{[M+H]+}:341.8394, found 341.8383。
2 結果與討論
基于2-巰基芳胺與二氟溴乙酸發生縮合反應得到苯并噻唑類化合物,經條件篩選,發現以氯苯作為溶劑,2-巰基苯胺能與5當量二氟溴乙酸在100 ℃下即可發生反應,生成2-二氟溴甲基-1,3-苯并噻唑3a,產率可達88%。因此,在上述條件下,我們考察了一系列2-巰基芳胺的反應(Scheme 1)。芳環上不同位置取代的芳胺均能順利發生反應,以中等的產率得到產物3b~3h。此外,不管是給電子的甲基還是吸電子的鹵素原子取代,反應均能兼容,這是由于鹵素原子的引入,有助于產物進行后續交叉偶聯衍生化反應。
根據上述反應結果及文獻報道[6],本文提出了該反應可能經歷的途徑如Scheme 2所示。在酸性條件下,原料1與二氟溴乙酸發生脫水反應,生成酰胺中間體I。隨后,中間體I在酸性條件下發生分子內環化生成中間體II,繼而脫水得到目標產物3。
3 結論
在100℃的氯苯溶劑中,2-巰基芳胺能與二氟溴乙酸發生一步縮合反應,該反應高效、簡便地合成了一系列2-二氟溴甲基-1,3-苯并噻唑,且操作簡便,底物兼容性較好,為合成2-二氟溴甲基-1,3-苯并噻唑衍生物提供了新的方法選擇。

