改性纖維素碳源對序批式生物膜反應器系統的脫氮效能影響*
徐 麗 董 月 崔 鵬
(沈陽建筑大學市政與環境工程學院,遼寧 沈陽 110168)
目前我國的污水處理廠大多采用生物法來處理污水中過量的氮磷物質,但是由于城市排放的污水逐漸呈現低碳氮比的特點[1],在處理過程中碳源不足,出水就難以達標,因此,為改善出水水質補充外加碳源十分必要[2]。現階段的有機碳源可分為兩大類:一是以葡萄糖、甲醇等液態有機物為主的傳統液體碳源;二是以天然植物纖維素及人工合成高聚物為主的新型固體碳源[3-4]。傳統的液體碳源,具有投加量難以控制、投放頻繁、運行成本高等缺陷,而人工合成高聚物,如聚酯類、聚烴類,雖釋碳穩定但是價格高昂營養成分單一,也不適宜大規模應用[5];基于安全性和經濟性等方面的考慮,價廉易得的天然纖維素類碳源成為廣大研究人員的共同研究目標。目前,研究較多的纖維素碳源為農業廢棄物中的杏仁殼、花生殼等殼類,蘆葦、樹葉等天然植物類,麥稈、玉米稈等秸稈類以及玉米芯、甘蔗渣、稻草等[6],[7]39-44,[8]2967-2971,[9]748-754,[10]39,[11]40-43,[12]992-995,[13-14]。結合諸位學者的研究成果可知,殼類碳源如花生殼,存在前期釋碳過快、后期釋碳不足或者釋碳總量不足等問題[7]42,[8]2968,[9]750;而蘆葦等植物初期釋放的氮磷較多,需要進行有效的預處理[8]2969,[10]39;秸稈類及玉米芯、稻殼等碳源前期的反硝化效果良好,但中后期也會出現供碳不足的現象[9]754,[11]43,[12]995。
纖維素類碳源普遍存在釋碳量不足、釋碳不穩定等問題,需要破壞木質素的包裹使更多的纖維素與半纖維素酶解釋放,以此提高釋碳量與縮短釋碳周期,所以對改性預處理方法的探究具有重要的研究意義。筆者選擇了不同濃度的NaOH與K2S2O8為改性試劑對纖維素類碳源玉米芯和稻殼進行改性處理,探究改性前后碳源表面結構特征、靜態釋放能力、可生化性等,篩選出改性后的最適宜碳源及改性條件,并將最適宜的改性碳源投入序批式生物膜反應器 (SBBR),探究它對系統脫氮效能的影響。為纖維素碳源的改性方法及條件研究提供參考,為SBBR工藝處理低碳氮比污水提供理論和參數支撐。
1 材料與方法
1.1 材 料
(1) 碳源材料:選取纖維素類碳源玉米芯和稻殼作為碳源材料。將玉米去粒后切割成若干個2~3 cm 的小段,利用0.9 mm的篩網對稻殼進行篩選。兩者均用蒸餾水清洗2~3遍,放置于85 ℃鼓風干燥箱中烘干,密封保存備用。
(2) 實驗用水:采用人工模擬低碳氮比污水作為實驗用水,模擬污水以葡萄糖作為碳源、氯化銨作為氮源、磷酸二氫鉀作為磷源,再加入少量的營養元素維持微生物活動,并投加NaOH和HCl維持進水pH為7.5±0.1。
(3) 接種污泥:反應器使用的污泥取自沈陽市上夾河污水處理廠的二沉池,污泥含水率約為90%,污泥沉降性能良好。污泥沉淀后倒掉上清液,取底部活性污泥作為接種污泥。
1.2 實驗裝置
實驗裝置如圖1所示。反應器主體是由有機玻璃制成的圓柱體,總高1.1 m,內徑30.0 cm,有效水深為80.0 cm,反應器的有效容積約為10.0 L,投加填料填充率約為30%,反應器運行由計時器進行自動控制。反應器下端進水,中端出水;底部設有曝氣裝置,采用氣體流量計控制,好氧段的DO控制在 (3.0±0.1) mg/L;容器內設有攪拌裝置,攪拌轉速為70 r/min,以保證反應器內填料處于流化狀態。

1—儲水箱;2—蠕動泵;3—攪拌裝置;4—SBBR主體;5—微孔曝氣盤;6—氣體流量計;7—電磁氣泵;8—排水口;9—填料;10—取樣口圖1 實驗裝置示意圖Fig.1 Diagram of experimental setup
1.3 實驗方法
(1) 改性纖維素碳源制備:分別用質量分數為3%、5%、7%的NaOH溶液和 K2S2O8溶液浸泡玉米芯和稻殼48 h,并用經過蒸餾水浸泡48 h的玉米芯和稻殼作為對照組(未改性組),按照1 g固體配50 mL溶液的比例對材料進行改性,48 h后取出,振蕩去除表面殘液,并用去離子水沖洗干凈,用烘箱烘干,冷卻后密封保存。
(2) 靜態釋放能力研究:稱取對照組以及不同改性處理后的玉米芯和稻殼各(3.0±0.2) g,置于250 mL的錐形瓶中,加入100 mL經過殺菌處理的蒸餾水。選用磨砂口錐形瓶,保持瓶內密封狀態,將錐形瓶置于恒溫培養箱中,溫度為25 ℃,每間隔24 h分析瓶內上清液中COD、氨氮、TN、TP的釋放情況。
(3) 表面特征分析:將干燥后的未改性組與經NaOH溶液和 K2S2O8溶液處理后的玉米芯和稻殼材料,利用HITACHI S-4800型掃描電子顯微鏡進行觀察分析,放大倍數為300倍,抽真空后拍照保存。
(4) 可生化性研究:以蒸餾水浸泡過的玉米芯和稻殼材料作為對照組,對不同改性處理后的玉米芯和稻殼進行可生化性實驗。所用培養液為人工模擬低碳氮比污水,COD為180 mg/L,用NaOH溶液調節培養液pH至7.5±0.1,將配置好的培養液置于高壓蒸汽滅菌器中121 ℃ 滅菌30 min。將不同處理組的固體碳源材料各1 g置于250 mL錐形瓶中,分別加入100 mL培養液和5 mL接種污泥,用保鮮膜封住瓶口保持瓶內密封環境。最后置于恒溫培養箱中,溫度設置為25 ℃,以24 h為周期檢測培養液在600 nm波長處的吸光值(OD600)。
(5) 反硝化效果研究:首先對反應器內接種的污泥進行低碳環境的培養馴化,接著投入篩選出的最適宜的改性碳源以及人工模擬的低碳氮比污水,完成SBBR系統的啟動運行。對比投加前后反應器的出水效果,探究改性纖維素碳源對系統的反硝化效能的影響。
(6) 分析方法:水質主要檢測項目為COD、TN、TP、氨氮。COD采用快速密閉催化消解法測定;TN采用過硫酸鉀氧化—紫外分光光度法測定;TP采用過硫酸鉀消解法測定;氨氮采用納氏試劑分光光度法測定。
2 結果與討論
2.1 改性前后纖維素碳源靜態釋放性能
實驗過程中,以蒸餾水浸泡后的玉米芯和稻殼作為未改性組,用 W 表示;以 NaOH 溶液浸泡后的玉米芯和稻殼作為堿處理組,7% NaOH 溶液記為 J1;5% NaOH 溶液記為 J2;3% NaOH 溶液記為 J3;以 K2S2O8溶液浸泡后的玉米芯和稻殼作為氧化處理組,7% K2S2O8溶液記為Y1;5% K2S2O8溶液記為Y2;3% K2S2O8溶液記為Y3。
從圖2可以看出,經過改性處理后的稻殼和玉米芯的 COD 釋放速率均有不同程度的增長。由7% NaOH 改性后的稻殼和玉米芯第一天的COD釋放速率最高,分別為 26.5、109.5 mg/(g·d)。對比未改性組,經 7% NaOH 改性后稻殼的COD釋放速率提高了2 倍多,而玉米芯則提高了5 倍多。觀察改性前后兩種材料的COD釋放速率,均表現為前期釋放速率較快,后期逐漸降低至平穩,這與趙民[15]、史曉林[16]、任玉銳[17]的研究結論一致。對比不同濃度K2S2O8溶液改性后的稻殼和玉米芯的 COD 釋放速率可知,NaOH溶液的改性效果更優。
推測原因是在實驗初期,稻殼與玉米芯材料表面覆蓋的可溶性小分子有機物能夠迅速溶解于水中,導致浸出液中COD含量增長迅速。隨時間的推移,稻殼與玉米芯的本底有機物逐漸分解且釋放,但可溶性碳的釋放程度較低,進而造成浸出液中COD釋放速率減緩,最后趨于穩定。因為稻殼與玉米芯含有的纖維素水解后,產生的可溶性碳可供微生物活動,所以兩種固體材料能夠緩慢釋碳。高濃度 NaOH 溶液改性后碳源釋放速率增長最為明顯,是因為 OH-可以破壞固體碳源材料的木質素,有研究指出,木質素會抑制纖維素的水解作用[18]。破壞木質素后可減少對纖維素水解酶的影響,促進纖維素酶解糖化過程,對比改性前后稻殼與玉米芯浸出液中COD的釋放效果,經由NaOH溶液浸泡后固體碳源材料纖維素的水解能力得以提升。改性后的玉米芯COD釋放速率最高,是因為相比稻殼的木質結構,玉米芯的木質纖維結構更加松散,木質素更容易被破壞。由此可見,改性后的玉米芯更加適用于作為緩釋碳源。
如圖3所示,實驗初期,各組碳源材料浸出液中氨氮基本溶出,且隨時間推移增幅明顯下降,最后趨于平緩,與文獻[19]報道一致。對比未改性的玉米芯和稻殼,改性處理能減少氨氮的釋放量。在整個實驗檢測過程中,對照組的稻殼浸出液中氨氮釋放量從0.94 mg/L增加至3.59 mg/L,玉米芯則從1.01 mg/L增加至2.29 mg/L。對比改性組,發現經由7% NaOH溶液改性后的玉米芯和稻殼的氨氮釋放量減少最明顯,其中7% NaOH改性后的稻殼氨氮釋放量由0.43 mg/L增加至2.34 mg/L,玉米芯由0.76 mg/L增加至1.42 mg/L。稻殼的氮源含量高于玉米芯,主要是因為稻殼本身的含氮量較高,經過堿液改性后結構變得松散,氮的釋放更加快速。
由圖4可見,經過不同試劑改性后玉米芯與稻殼的TN釋放量均有所減少且增加速率緩慢。對比兩種材料浸出液的氨氮釋放曲線特征,TN的釋放特征與其具有一定程度的相似性,同時可以看出改性后玉米芯和稻殼浸出液中TN釋放量低至可以忽略不計(《城鎮污水處理廠污染物排放標準》(GB 18918-2002)一級A標準TN限值為15 mg/L)。可見玉米芯與稻殼作為后續實驗處理的緩釋碳源,不會增加氮素負荷。
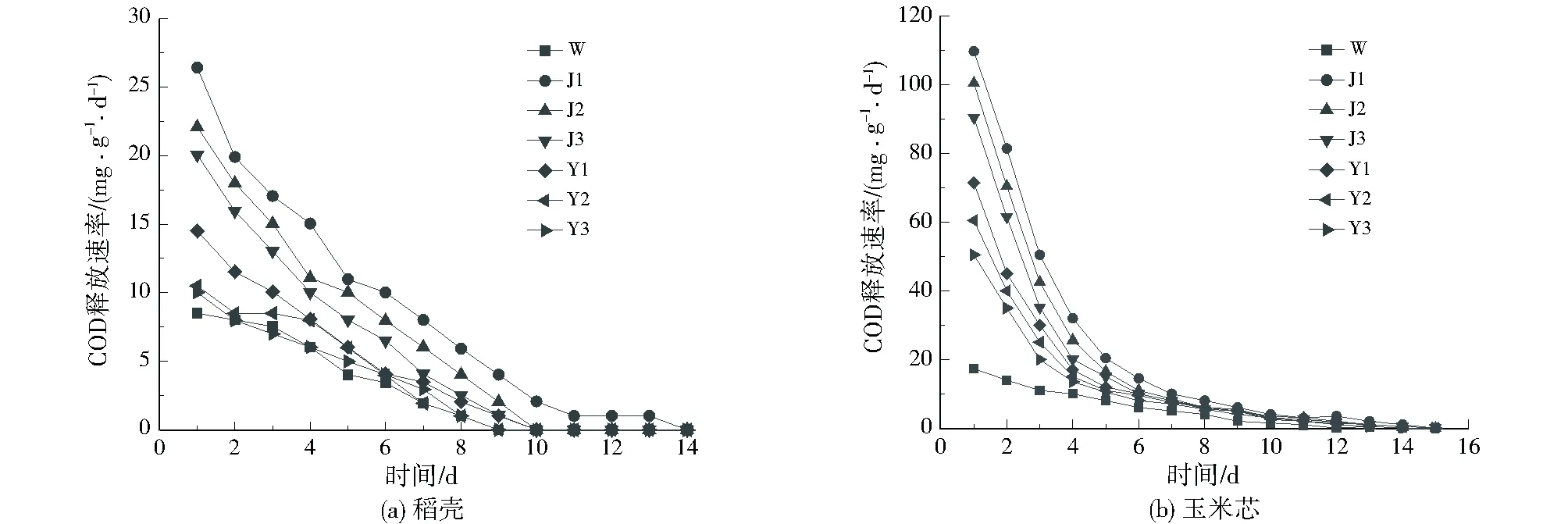
圖2 稻殼、玉米芯浸出液碳源釋放規律Fig.2 Carbon source release law of rice husk and corn cob leaching solution
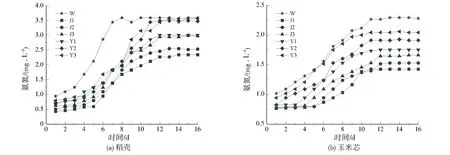
圖3 稻殼、玉米芯浸出液氨氮釋放量Fig.3 Ammonia nitrogen concentration of leaching solution of rice husk and corn cob

圖4 稻殼、玉米芯浸出液TN釋放量Fig.4 TN concentration of rice husk and corn cob leaching solution

圖5 稻殼、玉米芯浸出液TP釋放量Fig.5 TP concentration of rice husk and corn cob leaching solution
由圖5可見,經由不同改性溶劑浸泡后,玉米芯與稻殼的 TP 釋放量均有明顯降低。對比兩種固體碳源材料,發現經由7% NaOH溶液改性后的兩種材料浸出液中 TP 釋放量最低,其中稻殼TP釋放量為0.108 mg/L,玉米芯 TP 釋放量為0.095 mg/L,但改性前后稻殼的TP釋放量始終高于玉米芯。7% NaOH溶液改性后的玉米芯所釋放的 TP偏低且可忽略不計,不會增加系統磷素的負荷。
2.2 改性前后纖維素碳源表面特征分析
通過不同改性方式處理固體碳源材料均可改變其表面結構。由圖 6 可以看出,未經改性的玉米芯表面結構未被破壞且較平坦,但經改性后玉米芯表面結構都發生不同程度的破壞。經由 NaOH 溶液浸泡后的玉米芯,孔隙尺寸與孔隙間距顯著增加,并且表面結構發生明顯破壞;使用 K2S2O8溶液改性后的玉米芯,孔隙尺寸與孔隙間距沒有明顯增加,雖表面結構也被破壞但程度不及NaOH溶液改性。分析認為這種現象是堿性溶液溶解半纖維素和木質素等物質所導致的[20-22]。根據李輝勇[23]的研究得知,原料中木質素的含量不是影響纖維素酶解的唯一限制因素,改性前后比表面積的變化也有著一定的影響,比表面積變大更有利于微生物附著生長。

圖6 改性處理前后稻殼與玉米芯材料的表征Fig.6 Characterization of rice husk and corn cob materials before and after modification
對照組的稻殼表面凹凸不平,經改性處理后的稻殼表面結構發生明顯變化。其中經由 7% NaOH 溶液處理后的稻殼,表面凸起大量消失,且形成不規則孔狀結構,表面結構更加粗糙。對比高濃度NaOH溶液,低濃度的 NaOH 溶液破壞效果一般。經 K2S2O8溶液處理后,也能觀察到表面結構被破壞,但破壞程度不大。綜上可以得出,7% NaOH 溶液處理后的玉米芯和稻殼更適宜作為緩釋碳源。
2.3 改性前后纖維素碳源的可生化性
綜合前面的研究結果,因7% NaOH溶液對玉米芯和稻殼的改性處理均具有明顯提升作用,所以選擇7% NaOH溶液處理后的玉米芯和稻殼與對照組進行深入研究。
由圖7可知,7% NaOH改性后的玉米芯和稻殼浸出液中微生物含量均高于對照組,且趨勢均為先增長后下降。在第5天時,改性玉米芯的OD600為0.461而改性稻殼為0.346,經由7% NaOH改性處理后玉米芯的可生化性能顯著提升。分析原因是經過堿處理后玉米芯和稻殼的可溶性碳釋放程度不同,并且對比改性處理后的碳源表面結構也可發現,玉米芯表面出現大面積褶皺,提高了比表面積,進而導致改性玉米芯的纖維素酶解糖化反應要強于改性稻殼,所以7% NaOH改性處理后玉米芯的可生化性能最佳。

圖7 改性前后玉米芯和稻殼浸出液可生化性能Fig.7 Biochemical properties of corn cob and rice husk leaching solution before and after modification
2.4 改性纖維素碳源的投加對系統脫氮效能的影響
經過前期的實驗篩選發現,7% NaOH改性后的玉米芯在碳釋放、可生化性等方面均具有一定的優勢,故選擇其作為SBBR系統的緩釋碳源進行后續實驗。
2.4.1 污泥馴化階段系統的脫氮能力
反應器接種污泥含水率為90%,活性污泥質量濃度(MLSS)為4 153 mg/L,pH為7.2;反應器內溫度控制在20 ℃左右,DO控制在(3.0±0.2) mg/L,pH控制在7.0±0.2。SBBR工藝啟動運行模式為進水—攪拌—曝氣—攪拌—靜置—出水,以厭氧(2 h)—好氧(5 h)—靜置(1 h)運行方式對反應器內污泥進行60 d的培養馴化。根據反應器的進水濃度,可以將整個反應階段分為污泥培養階段Ⅰ:COD為180 mg/L(圖8中0~20 d);污泥低負荷馴化階段Ⅱ:COD為140 mg/L(圖8中20~40 d);污泥低負荷馴化階段Ⅲ:COD為100 mg/L(圖8中40~60 d)。
對反應器內接種的活性污泥進行為期60 d的培養與馴化,反應初期因反應器內營養物質偏少,污泥活性及沉降性不佳,污泥呈淡黃色[24-25]。由圖8可見,初期系統出水COD濃度變化幅度很大,去除效果并不穩定,這是由于與污泥原本適應的水質相比反應器內COD濃度突然下降,活性污泥中的微生物還未適應進水水質;系統運行至10 d之后COD去除率可以穩定在85%以上,說明此時反應器內微生物適應了進水水質,且對有機物的去除具有一定的穩定性和高效性;反應器進水中氮的組成主要是氨氮,進水質量濃度為35 mg/L,從第1天到第5天氨氮去除效果不理想,這同樣與微生物對反應器的適應過程有關,由于初始階段水環境發生變化,污泥活性較差,所以前期系統處理效能較低。隨著系統的運行,反應器內微生物逐漸適應新的污水環境,氨氮去除率逐漸增加,最后穩定在60%以上且無明顯波動;TN的去除主要是由于反應器內硝化細菌的同化作用,利用氨氮作為自身細胞內合成物質,當反應器內微生物含量保持一定時,對反應器內氨氮的處理能力基本不再變化,則反應器內的TN濃度也趨于穩定。

圖8 污泥馴化階段各指標變化情況Fig.8 Changes of indicators in the domestication stage of sludge
2.4.2 投加碳源啟動階段系統的脫氮能力
反應器進水COD為(100±5) mg/L,TN為50 mg/L,其碳氮比(質量比)約為2,難以滿足微生物進一步脫氮除磷的需求。設定碳氮比為6,此時改性玉米芯釋碳能力為25 mg/(g·L·d),所以需投加20 g改性玉米芯材料。填料填充率為30%,反應器進水氨氮為35 mg/L,SBBR系統進出水COD、氨氮、TN變化如圖9所示。
投加改性玉米芯后,SBBR系統的處理效果得到提高。對比投加改性玉米芯前的反應器出水效果可以發現,SBBR系統對COD仍具有較高的去除率(80%),氨氮去除率由原來的60%提升至73%左右,TN去除率由原來的50%提高到60%左右。由此說明改性玉米芯釋放的可溶性碳能被反應器內微生物有效利用,進而提高系統的脫氮效能。
3 結 論
(1) 經過不同濃度的NaOH和K2S2O8改性的玉米芯和稻殼均可作為緩釋碳源,NaOH對兩種碳源改性的效果優于K2S2O8。7% NaOH改性后的玉米芯和稻殼相比同組最優。
(2) 經由7% NaOH溶液處理后的玉米芯第1天的COD釋放速率最高,達到了109.5 mg/(g·d),并且浸出液中釋放的氮、磷較少;通過表面特征分析發現,經7% NaOH溶液改性后的玉米芯表面孔隙結構最為明顯,且表面粗糙褶皺最多;對比7% NaOH溶液改性前后的玉米芯和稻殼可生化性能,發現經7% NaOH處理后的玉米芯可生化性能顯著增強。因此7% NaOH改性處理后的玉米芯可作為調節低碳氮比污水的緩釋碳源。
(3) 投加改性玉米芯后的SBBR系統,出水效果相比未投加時的出水效果得到明顯提升。系統穩定運行20 d后,COD去除率穩定在80%,氨氮的去除率由60%提升到73%左右,TN的去除率由50%提升到60%左右。這表明7% NaOH改性處理后的玉米芯是良好的緩釋碳源,能有效地提高系統的脫氮效能。
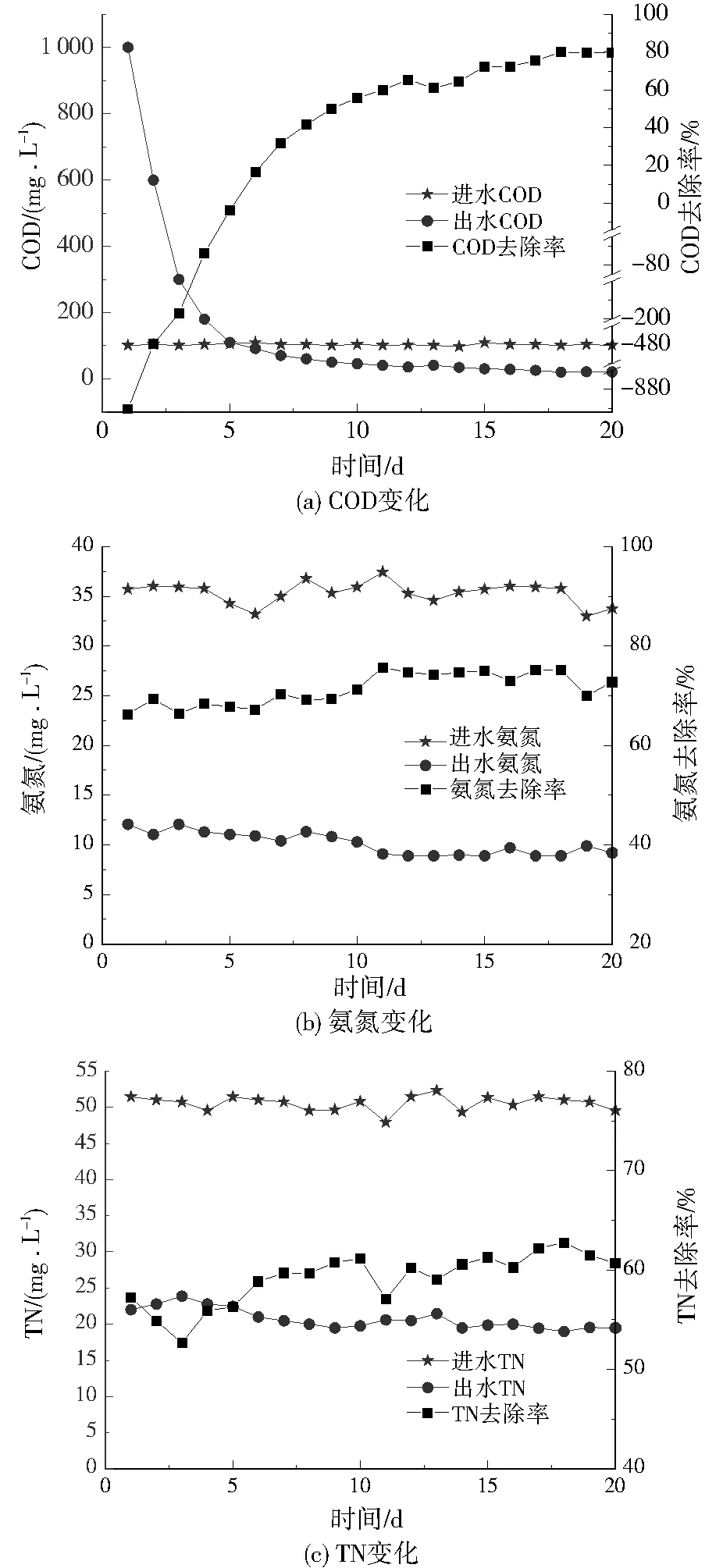
圖9 SBBR啟動階段各指標變化情況Fig.9 Changes of various indicators in the SBBR startup stage

