西格列汀聯合賴諾普利治療早期糖尿病腎病的臨床研究
羅雯璐
(上海市徐匯區長橋街道社區衛生服務中心全科,上海 200231)
隨著病情進展,糖尿病患者相關的各大血管、微血管并發癥隨之而來,糖尿病腎病即其中重要的微血管并發癥之一,如果不能給予患者及時有效的對癥治療,有可能發展為終末期腎衰竭,嚴重危害患者身體健康。目前,對于早期糖尿病腎病的臨床治療,多采用藥物干預,西格列汀作為二肽基肽酶4(DPP-4)抑制劑,其能夠通過抑制DPP-4 的活性,從而升高患者體內胰高糖素樣肽 -1(GLP-1)水平。而GLP-1 具有促進胰島素分泌,增加機體對葡萄糖的攝取的作用,起到降糖效果,但對腎功能的改善作用效果不佳[1]。賴諾普利作為一種長效血管緊張素轉換酶抑制劑藥物,可通過提高腎內一氧化氮(NO)的活性,清除體內多余的游離氧自由基,從而起到擴張血管、改善濾過膜通透性、延緩腎小球濾過率(eGFR)下降及減輕腎小球細胞肥大的作用[2]。因此本研究旨在探討西格列汀聯合賴諾普利治療早期糖尿病腎病患者,對其胱抑素C(CysC)、24 h 尿微量白蛋白(24 h-UmALB)、血肌酐(Scr)、尿素氮(BUN)、eGFR 水平的影響,現報道如下。
1 資料與方法
1.1 一般資料 將上海市徐匯區長橋街道社區衛生服務中心于2018 年10 月至2020 年10 月期間診治的112 例早期糖尿病腎病患者,按隨機數字表法分為對照組和觀察組,每組56 例。對照組患者中男性29 例,女性27 例;年齡46~75 歲,平均(65.61±3.84)歲;糖尿病病程2~8年,平均(3.82±1.26)年。觀察組患者中男性30 例,女性26 例;年齡45~74 歲,平均(65.47±4.05)歲;糖尿病病程2~8 年,平均(3.78±1.32)年。對比兩組患者一般資料,差異無統計學意義(P>0.05),組間可比。納入標準:符合《糖尿病腎病防治專家共識(2014 年版)》[3]中的相關診斷標準者;糖尿病病程在2 年以上者;尿白蛋白排泄率(UAER)為20~199 μg/min 者等。排除標準:4周內曾發生過糖尿病酮癥酸中毒及其他并發癥者;繼發性腎臟疾病或有泌尿系統疾病者;近期有服用腎毒性藥物史者或口服生長激素、糖皮質激素者等。患者均簽署知情同意書,且院內醫學倫理委員會已批準此研究。
1.2 治療方法 所有患者采用常規治療+輔助治療[降糖藥物或者皮下注射胰島素進行治療,同時行低蛋白、低鈉的合理飲食,以及適量的運動]。在此基礎上,對照組患者口服磷酸西格列汀片(Merck Sharp & Dohme Ltd.,注冊證號J20140095,規格:100 mg/片)治療,100 mg/次,1 次/d。在對照組患者治療的基礎上,觀察組患者口服賴諾普利片(浙江華海藥業股份有限公司,國藥準字H20094033,規格:10 mg/片)治療,10 mg/次,1 次/d,兩組患者均連續治療1 個月。
1.3 觀察指標 ①治療效果,顯效:治療后患者臨床癥狀消失,血糖降幅≥ 30%,UAER 降幅≥ 50%或達到正常水平;有效:治療后患者臨床癥狀有所改善,血糖降幅≥ 10%但 < 30%,UAER 降幅≥ 10%但 < 50%;無效:患者臨床癥狀無改善甚至加重,血糖降幅 < 10%,UAER降幅 < 10%[3]。總有效率=顯效率+有效率。②血管內皮功能,抽取兩組患者治療前后空腹靜脈血3 mL,經3 000 r/min 轉速離心10 min 后取血清,采用放射免疫法測定內皮素-1(ET-1)水平,采用硝酸還原酶法測定NO水平,采用酶聯免疫吸附實驗法檢測可溶性血管細胞黏附分子 -1(sVCAM-1)水平。③腎功能,血液采集、血清制備方式同②,采用全自動生化分析儀檢測CysC、Scr水平,采用放射免疫法檢測BUN 水平,并計算eGFR,eGFR=186×(Scr)-1.154×(年齡)-0.203×0.742(女性);收集24 h 尿液,混勻后采用免疫比濁法測定24 h-UmALB。④凝血與血脂指標,血液采集方式同②,經抗凝處理,進行離心操作(3 000 r/min,10 min)后取血漿,經凝血分析儀檢測活化部分凝血活酶時間(APTT)、纖維蛋白原(FIB)水平;血液采集、血清制備方式同②,使用全自動生化分析儀檢測血清總膽固醇(TC)、三酰甘油(TG)水平。⑤不良反應,比較兩組患者頭暈頭痛、胃腸道反應、皮疹等不良反應發生情況。
1.4 統計學方法 采用SPSS 23.0 統計軟件分析數據,計數資料[治療后治療效果、治療期間不良反應]以[ 例(%)]表示,采用χ2檢驗;本研究計量資料[治療前后血管內皮功能指標(ET-1、sVCAM-1、NO)、腎功能指標(CysC、Scr、BUN、24 h-UmALB、eGFR)、凝血功能及血脂指標(FIB、TC、TG、APTT)]均經K-S 法檢驗證實符合正態分布,以(±s)表示,兩組間比較采用獨立樣本t檢驗。以P<0.05 為差異有統計學意義。
2 結果
2.1 兩組患者治療效果比較 觀察組患者臨床總有效率顯著高于對照組,差異有統計學意義(P<0.05),見表1。
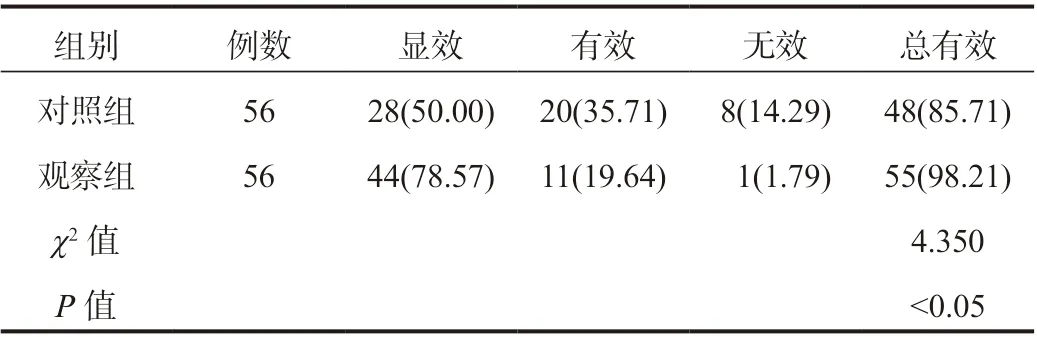
表1 兩組患者治療效果比較[ 例(%)]
2.2 兩組患者血管內皮功能指標比較 相較于治療前,治療后兩組患者ET-1、sVCAM-1 水平均顯著降低,觀察組顯著低于對照組;NO 水平顯著升高,觀察組顯著高于對照組,差異均有統計學意義(均P<0.05),見表2。
表2 兩組患者血管內皮功能指標比較( ±s)
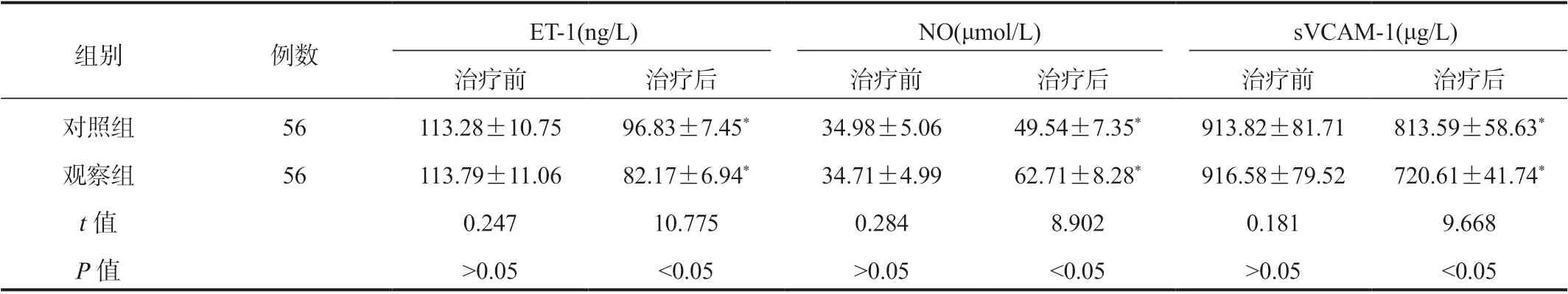
表2 兩組患者血管內皮功能指標比較( ±s)
注:與治療前比,*P<0.05。ET-1:內皮素 -1;NO:一氧化氮;sVCAM-1:可溶性血管細胞黏附分子 -1。
組別 例數 ET-1(ng/L) NO(μmol/L) sVCAM-1(μg/L)治療前 治療后 治療前 治療后 治療前 治療后對照組 56 113.28±10.75 96.83±7.45* 34.98±5.06 49.54±7.35* 913.82±81.71 813.59±58.63*觀察組 56 113.79±11.06 82.17±6.94* 34.71±4.99 62.71±8.28* 916.58±79.52 720.61±41.74*t 值 0.247 10.775 0.284 8.902 0.181 9.668 P 值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.3 兩組患者腎功能指標比較 相較于治療前,治療后兩組患者血清CysC、Scr、BUN 及24 h-UmALB 水平均顯著降低,觀察組顯著低于對照組;eGFR 顯著升高,觀察組顯著高于對照組,差異均有統計學意義(均P<0.05),見表3。
表3 兩組患者腎功能指標比較( ±s)
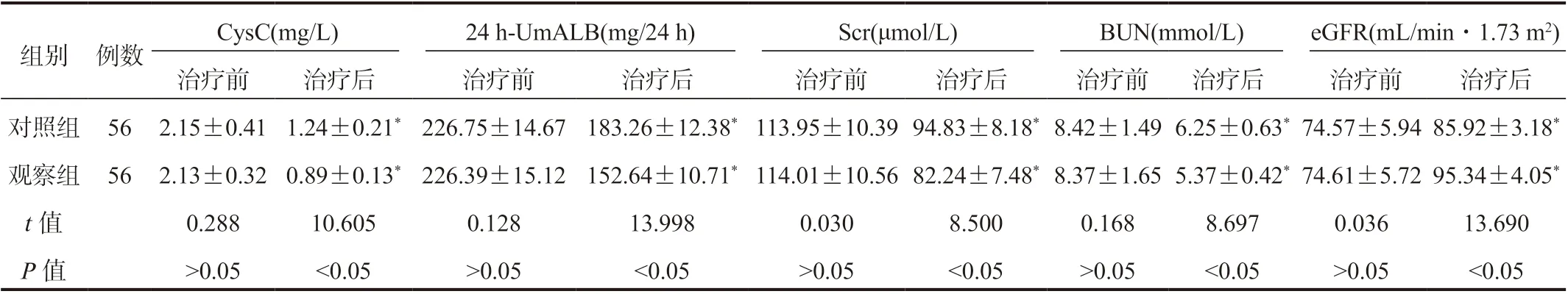
表3 兩組患者腎功能指標比較( ±s)
注:與治療前比,*P<0.05。CysC:胱抑素C;24 h-UmALB:24 h 尿微量白蛋白;Scr:血肌酐;BUN:尿素氮;eGFR:腎小球濾過率。
組別 例數 CysC(mg/L) 24 h-UmALB(mg/24 h) Scr(μmol/L) BUN(mmol/L) eGFR(mL/min·1.73 m2)治療前 治療后 治療前 治療后 治療前 治療后 治療前 治療后 治療前 治療后對照組 56 2.15±0.41 1.24±0.21* 226.75±14.67 183.26±12.38* 113.95±10.39 94.83±8.18* 8.42±1.49 6.25±0.63* 74.57±5.94 85.92±3.18*觀察組 56 2.13±0.32 0.89±0.13* 226.39±15.12 152.64±10.71* 114.01±10.56 82.24±7.48* 8.37±1.65 5.37±0.42* 74.61±5.72 95.34±4.05*t 值 0.288 10.605 0.128 13.998 0.030 8.500 0.168 8.697 0.036 13.690 P 值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.4 兩組患者凝血指標與血脂水平比較 相較于治療前,治療后兩組患者FIB、TC、TG 水平均顯著降低,觀察組顯著低于對照組;APTT 顯著延長,觀察組顯著長于對照組,差異均有統計學意義(均P<0.05),見表4。
表4 兩組患者凝血指標與血脂水平比較( ±s)
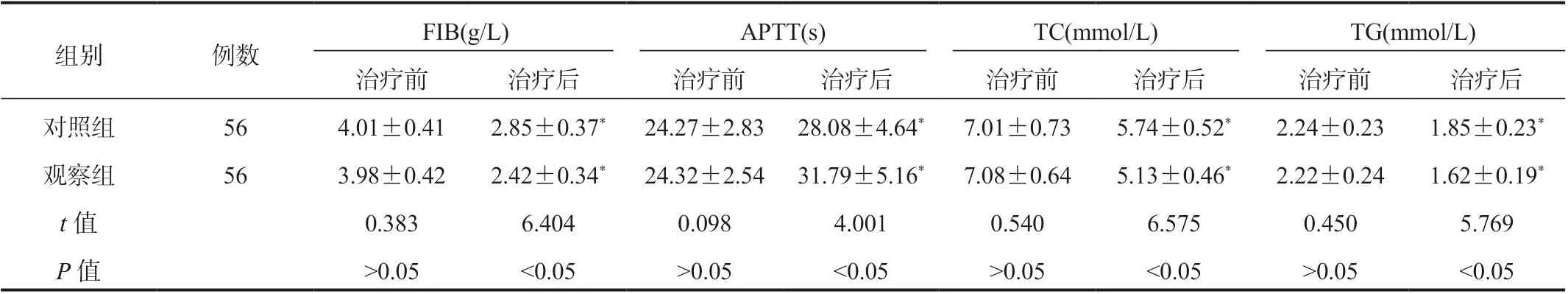
表4 兩組患者凝血指標與血脂水平比較( ±s)
注:與治療前比,*P<0.05。FIB:纖維蛋白原;APTT:活化部分凝血活酶時間;TC:總膽固醇;TG:三酰甘油。
組別 例數FIB(g/L) APTT(s) TC(mmol/L) TG(mmol/L)治療前 治療后 治療前 治療后 治療前 治療后 治療前 治療后對照組 56 4.01±0.41 2.85±0.37* 24.27±2.83 28.08±4.64* 7.01±0.73 5.74±0.52* 2.24±0.23 1.85±0.23*觀察組 56 3.98±0.42 2.42±0.34* 24.32±2.54 31.79±5.16* 7.08±0.64 5.13±0.46* 2.22±0.24 1.62±0.19*t 值 0.383 6.404 0.098 4.001 0.540 6.575 0.450 5.769 P 值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.5 兩組患者不良反應發生率比較 兩組患者不良反應總發生率比較,差異無統計學意義(P>0.05),見表5。
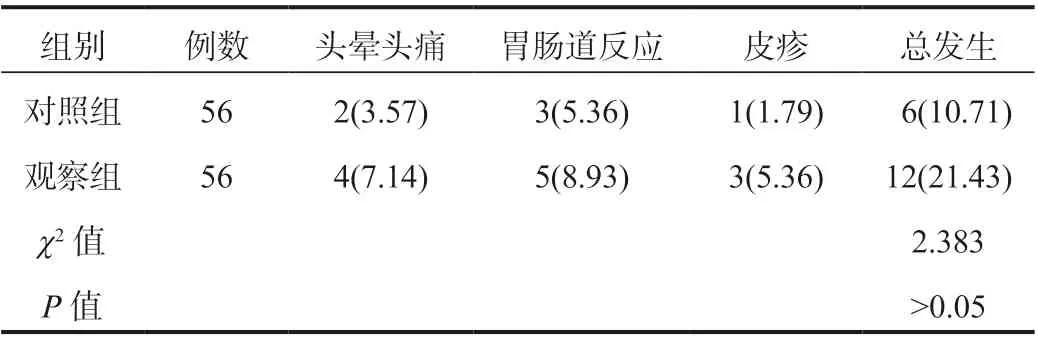
表5 兩組患者不良反應發生率比較[ 例(%)]
3 討論
糖尿病腎病主要以持續性蛋白尿、漸進性腎功能損害及高血壓為臨床表現,是糖尿病代謝異常引起的微血管并發癥,盡早診斷與治療對于患者預后具有重大意義。西格列汀可大幅提高胰腺β 細胞對葡萄糖的反應性,進一步促進胰島素的合成與釋放,從而強化了機體的攝糖作用,實現有效的血糖調控[4];同時GLP-1 對胰腺α 細胞也具有抑制作用,限制其對胰高糖素的分泌作用,而胰高糖素濃度與胰島素水平在肝葡萄糖的合成中發揮著重要作用,能進一步降低血糖水平,但長期應用容易使患者肝酶升高,腎功能減退[5]。
糖尿病患者在高血糖狀態下導致機體內氧化應激加強,進而引起脂質氧化和蛋白質修飾,從而促進動脈粥樣硬化的發生。ET-1 主要由上皮細胞、肝細胞、血管平滑肌細胞、內皮細胞、神經細胞及星形膠質細胞分泌,能刺激腎小管上皮細胞生成醛固酮增多,進一步加重病情;sVCAM-1介導了白細胞與內皮細胞黏附,導致內皮細胞損傷,細胞外基質大量堆積,增加血管通透性,同時促使白細胞在腎小球和腎間質浸潤,加速腎小球硬化;NO 是一種重要的內源性血管舒張因子,主要作用是舒張血管,抑制白細胞黏附于血管內皮細胞的表面,進一步抑制血管內皮細胞釋放ET-1、血管緊張素Ⅱ等血管活性物質,減少血管內皮損傷。血管內皮本身對外界刺激的敏感性高,易受到來自血液和組織的各種理化因子的刺激,而上述因子可以對內皮細胞的增殖進行抑制,激活核轉錄因子 -κB,利于許多靶基因的表達,可加強內皮細胞與白細胞的相互作用,進而對血管內皮功能損傷的發生和發展起到促進作用[6]。賴諾普利作為一種可使緩激肽積聚的血管緊張素轉化酶抑制劑,可降低超氧陰離子的水平,促進NO 在冠狀動脈微血管中的積累,從而改善血管內皮功能[7];同時其在機體中無需通過肝臟轉化,可直接產生藥理效應,安全性良好。本研究中,相較于對照組,觀察組患者治療總有效率顯著升高,ET-1、sVCAM-1 水平均顯著降低,NO 水平顯著升高;兩組患者不良反應總發生率組間經比較,差異無統計學意義,提示將西格列汀聯合賴諾普利應用于早期糖尿病腎病患者的治療中,有助于血管內皮功能的改善,提高臨床療效,且不增加不良反應,安全性較好。
高血糖可以導致腎血流的增加,使得腎小球濾過率增高,激活腎素 - 血管緊張素系統,進而引起腎小球高灌注、高壓及高濾過的異常狀態。本研究中,治療后,觀察組患者CysC、24 h-UmALB、Scr、BUN 水平均顯著低于對照組,eGFR顯著高于對照組,提示將西格列汀聯合賴諾普利應用于早期糖尿病腎病患者的治療中,有助于腎功能的改善,促進病情恢復。分析其原因可能為,賴諾普利不僅可以提高機體血漿腎素活性,下調血管緊張素Ⅱ和醛固酮的表達水平,還可通過抑制緩激肽降解酶的活性,延長腎臟內緩激肽的作用時間,增加其擴張血管、改善血流動力學,提高eGFR,減少尿蛋白排泄,恢復患者腎臟功能[8-9]。
相關研究顯示,長期高血糖引起全身血管內皮損傷,并且會降低功能性脂蛋白脂酶水平,導致TC、TG 水平升高[10];由于糖尿病患者早期體內的糖代謝發生了紊亂,會導致血脂水平升高,同時由于各種致炎因子持續存在,并且造成血管內皮組織損傷,而血管內皮受損后,血小板開始聚集并形變,形成血小板血栓,導致冠心病、腦梗塞、糖尿病眼病、糖尿病腎病等各種血管并發癥,從而導致FIB 水平升高,APTT 縮短,凝血功能進一步受損[11]。本研究中,相較于對照組,觀察組患者FIB、TC、TG 水平均顯著降低,APTT 水平顯著延長,提示將西格列汀聯合賴諾普利應用于早期糖尿病腎病患者的治療中,可對其凝血功能指標與血脂水平進行調節,控制病情發展。分析原因可能為,由于巨噬細胞可以刺激腎小球系膜細胞產生纖維連接蛋白,進而影響凝血功能指標,西格列汀能夠降低巨噬細胞的濾過性并阻止其聚集,從而降低FIB 水平,延長APTT[12];賴諾普利可通過對血管緊張素轉換酶的活性進行抑制,降低醛固酮、血管緊張素Ⅱ的濃度,增強血漿腎素活性(PRA),導致外周血管的擴張和血管阻力降低,減少心肌耗氧,促進側支循環,降低血液黏度,進而改善血脂狀況和凝血功能[13-14]。
綜上,將西格列汀聯合賴諾普利應用于早期糖尿病腎病患者的治療中,有助于血管內皮功能與腎功能的改善,同時可對凝血功能指標與血脂水平進行調節,療效顯著,且安全性良好,可促進病情恢復,值得臨床推廣應用。

