低氧處理的hAMSCs外泌體對巨噬細胞M1/M2分型影響及其分子機制
江鑫銘,李霄霞,趙春華
(青島大學基礎醫學院,山東 青島 266071)
間充質干細胞(MSCs)是一類具有高度自我更新能力、多向分化潛能、低免疫原性及重要免疫調節能力的多能成體干細胞[1]。因較易獲取且易于分離提取,人脂肪間充質干細胞(hAMSCs)的臨床研究較為廣泛。由于MSCs在體外培養時,通常處于常氧狀態中,即培養環境中氧氣的體積分數為0.209左右,但是在自然生理條件下,體內環境中氧氣的體積分數只有0.02~0.08,甚至更低。所以,研究低氧狀態下的MSCs更有利于將來其臨床應用。
外泌體是由細胞分泌的來自細胞內多囊泡體的一種脂質雙分子層組成的囊泡,是MSCs旁分泌作用和細胞間通訊的重要遞質[2]。它們可以通過轉移分子貨物來影響受體細胞的功能,例如蛋白質、微小RNA(miRNA)和mRNA等[3-4]。與干細胞相比,源自MSCs的外泌體具有很多優點,例如更容易通過組織屏障,能減少排斥反應的風險[5]。
巨噬細胞作為人體內重要的抗原呈遞細胞和免疫調節細胞,在多種疾病中發揮重要作用[6]。巨噬細胞根據其不同的激活方式和發揮免疫功能方式,分為M1型和M2型。M1型巨噬細胞為促炎性的,M2型巨噬細胞為抑炎性的[7]。MSCs能調節巨噬細胞由M1型向M2型轉化來減輕炎癥反應以及加速損傷修復[8]。有研究表明,在硫酸葡聚糖誘導炎癥性腸病小鼠模型中,腹腔注射MSCs可誘導 M2 型巨噬細胞產生從而明顯改善結腸炎癥[9];在腎動脈狹窄損傷模型中,MSCs可以通過調控巨噬細胞表型改善腎功能[10]。本研究旨在探討低氧狀態下hAMSCs外泌體對巨噬細胞M1/M2分型的影響及其分子機制,為其將來應用于臨床治療奠定基礎。現將結果報告如下。
1 材料與方法
1.1 細胞和試劑
本實驗所用的hAMSCs來自于吸脂術病人術后廢棄的脂肪組織(已經征得病人的知情同意),經提取原代細胞后擴增所得。巨噬細胞RAW264.7為實驗室自存細胞系。本實驗所用的RPMI、高糖DMEM和DME/F12培養液均購自美國Hyclone公司;胎牛血清購自Ex-cell公司;青霉素、鏈霉素、總RNA提取試劑、胰蛋白酶、RIPA裂解液、抗體稀釋液均購自新賽美公司;膠原酶P購自美國Roche公司;脂多糖(LPS)購自美國Sigma公司;逆轉錄試劑盒、SYBR Green Master Mix試劑盒購自上海翊圣公司;PBS緩沖液購自biosharp公司;直標抗體CD80、CD206購自美國BD公司。
1.2 hAMSCs的分離培養
取廢棄脂肪組織用PBS沖洗后分裝至離心管中,以700 r/min離心3 min后吸棄PBS,加入2 g/L膠原酶P適量,置37 ℃恒溫搖床中消化30 min,消化液經過100目濾網過濾濾去未消化組織后加入足量PBS,以1 000 r/min離心5 min,棄上清,留底部細胞沉淀。重復2次后,將細胞沉淀重懸接種于含體積分數0.10胎牛血清的DME/F12培養液中,置于37 ℃恒溫CO2培養箱內培養,每2 d換液1次,待細胞生長至約80%融合時進行傳代培養。
1.3 hAMSCs外泌體的提取及鑒定
將第5代hAMSCs細胞接種于10 cm培養皿中,待細胞生長至80%~90%融合時,換無血清高糖DMEM培養液,將細胞置于低氧小室(氧氣的體積分數為0.025)培養24 h,取上清液置于分子量為100 000規格的離心過濾器內,以3 500 r/min離心30 min,收集離心過濾器內的外泌體。使用透射電子顯微鏡觀察并拍攝外泌體,使用納米顆粒追蹤分析儀進行外泌體粒徑檢測,采用Western blot方法檢測外泌體相關標志蛋白表達。
1.4 巨噬細胞M1/M2表型誘導以及流式細胞術鑒定
巨噬細胞正常生長至80%左右融合時進行傳代,接種于6孔板中,培養48 h后換無血清RPMI培養液。設置2孔為對照組(A組),2孔為單純LPS誘導組(B組),2孔為LPS和hAMSCs外泌體共處理組(C組)。對照組無處理措施;單純LPS誘導組加入濃度為1 mg/L的LPS誘導12 h,以PBS洗去LPS,換無血清RPMI培養液繼續培養24 h;LPS和hAMSCs外泌體共處理組首先加入濃度為1 mg/L的LPS誘導12 h,以PBS洗去LPS后換無血清RPMI培養液,然后加入濃度為50 mg/L的hAMSCs外泌體繼續培養24 h。收集細胞、RNA和蛋白進行鑒定。用胰蛋白酶消化后收集細胞,以PBS清洗、重懸,加入CD80直標抗體4 ℃下孵育30 min,以PBS清洗2次,洗去未結合直標抗體,用PBS重懸細胞;以PBS清洗、重懸,用40 g/L多聚甲醛固定3 min,以PBS洗去多聚甲醛后用體積分數0.001的tritonX重懸細胞,同時加入CD206直標抗體4 ℃孵育30 min,以PBS洗2次洗去殘留的tritonX和直標抗體后用PBS重懸。采用流式細胞術檢測CD80和CD206在各組細胞的表達。實驗重復3次。
1.5 實時熒光定量PCR(qPCR)檢測巨噬細胞炎癥因子表達
按總RNA提取試劑說明書提取各組RNA,隨后按照逆轉錄試劑說明書進行總RNA的逆轉錄。先進行殘留組基因的去除,條件為42 ℃、2 min;然后進行逆轉錄,條件為25 ℃、5 min,42 ℃、30 min,85 ℃、5 min。按照熒光定量所需的SYBR Green Master Mix試劑盒使用說明配制反應體系,設置反應條件:預變性95 ℃、5 min,變性95 ℃、10 s;退火/延伸60 ℃、30 s,循環39次。實驗所用基因引物序列見表1。以GAPDH為內參照基因,采用2-△△Ct方法計算腫瘤壞死因子α(TNF-α)、白細胞介素1β(IL-1β)、一氧化氮合酶2(NOS-2)和白細胞介素12(IL-12)的mRNA表達水平。每組樣本設置3個副孔,實驗獨立重復3次。

表1 PCR引物及其序列
1.6 Western blot檢測核因子κB(NF-κB)通路相關蛋白表達
細胞加入RIPA裂解液裂解后提取細胞總蛋白,參照SDS-PAGE凝膠試劑盒操作說明書在制膠后采用恒壓電泳將所提取的蛋白樣品分離,然后將蛋白轉移到硝酸纖維素膜上。使用100 g/L的脫脂奶粉室溫封閉90 min,加入一抗(β-actin、P65、p-P65,以1∶1 000抗體稀釋液稀釋)4 ℃孵育過夜,加入羊抗兔二抗(以1∶5 000抗體稀釋液稀釋)室溫孵育60 min。使用超敏ECL發光檢測試劑盒進行顯影。應用Image J軟件分析蛋白電泳條帶灰度值,以β-actin作為內參照蛋白,計算P65、p-P65蛋白的相對表達量。實驗獨立重復3次。
1.7 統計學分析
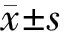
2 結 果
2.1 低氧處理的hAMSCs外泌體的鑒定
應用超速離心法提取了低氧處理的hAMSCs的外泌體,在電鏡下觀察其形態為盤狀囊泡形(圖1A)。使用納米粒徑分析儀檢測外泌體直徑分布,結果顯示直徑118.5 nm的外泌體占比為95.8%(圖1B和表2)。Western blot方法檢測外泌體相關標志蛋白的表達,結果顯示,只能檢測到外泌體標志蛋白TSG101的表達,而沒有檢測到細胞質特異性蛋白CALNEXIN的表達(圖1C),表明所提取的盤狀囊泡是外泌體而非胞質部分。
2.2 巨噬細胞炎癥因子表達情況和流式細胞術檢測細胞表型
qPCR檢測結果顯示,相較于對照組,加入LPS誘導后巨噬細胞炎癥因子TNF-α、IL-1β、NOS-2和IL-12的mRNA相對表達量顯著升高;而LPS和hAMSCs外泌體共處理組細胞與單純LPS誘導組細胞相比較,上述炎癥因子mRNA的相對表達量明顯下降,差異均有統計學意義(F=10.820~222.942,P<0.05)。表明經低氧處理的hAMSCs外泌體可以降低M1型巨噬細胞炎癥因子的表達。見表3。
流式細胞術檢測結果顯示,與單純LPS誘導組相比,LPS和hAMSCs外泌體共處理組M1型巨噬細胞比例下降,M2型巨噬細胞比例增加(t=3.293、10.242,P<0.05)。見表4和圖2。

表2 hAMSCs外泌體粒徑峰值分析

表3 各組巨噬細胞炎癥因子mRNA相對表達水平的比較

表4 兩組M1型、M2型巨噬細胞標志物表達的比較
2.3 巨噬細胞NF-κB信號通路蛋白的變化
本文Western blot檢測結果顯示,對照組、單純LPS誘導組、LPS和hAMSCs外泌體共處理組細胞的p-P65/P-65蛋白表達比值分別為0.602±0.032、1.560±0.035和1.251±0.059(n=3)。與單純LPS誘導組相比,LPS和hAMSCs外泌體共處理組細胞p-P65蛋白表達減少(圖3),p-P65/P-65蛋白表達比值下降,差異具有統計學意義(F=375.634,P<0.05)。表明M1巨噬細胞經外泌體處理后其NF-κB信號通路受到抑制。

A:低氧處理的hAMSCs外泌體電鏡下形態;B:納米粒徑分析儀檢測低氧處理的hAMSCs外泌體的直徑分布;C:Western blot方法檢測TSG101蛋白和CALNEXIN蛋白表達情況。

流式細胞術檢測兩組細胞CD80、CD206表達,CD80為M1型巨噬細胞標志物,CD206為M2型巨噬細胞標志物。

A、B、C分別為對照組、單純LPS誘導組、LPS和hAMSCs外泌體共處理組。
3 討 論
MSCs是一種多潛能干細胞,具有免疫調節特性(包括免疫抑制和免疫促進)和低免疫原性[11-13],已被應用于多種治療中。但是MSCs的體內治療的效果與體外實驗結果存在差異,體內治療效果通常不如體外實驗結果[14-16],所以越來越多的研究選擇將MSCs進行預處理以后再應用于治療。本研究對MSCs進行低氧處理以模擬其在體內條件下所處的氣體環境。
有研究表明,MSCs在全身給藥后存活不到1周,但其治療效果可以持續產生,由此可見MSCs的免疫抑制功能至少部分是由旁分泌介導的,其中外泌體可能是主要的活性媒介[17-19]。外泌體是細胞間通訊中獨特的分泌性囊泡,是具有雙層膜結構的膜囊,含有復雜而豐富的蛋白質、核酸和其他活性分子[20],其功能涉及多個方面,包括免疫應答、抗原提呈、細胞遷移、細胞分化和腫瘤侵襲等。與細胞相比,外泌體具有較低的免疫原性、更強的跨越生物屏障能力以及較少的安全問題等優點[21-23]。MSCs是一種可以產生大量外泌體的細胞,其中骨髓MSCs來源的外泌體正在被探索作為MSCs的治療替代方案,因為它們可能與細胞具有類似的治療效果[24]。
本研究旨在探討低氧處理后的MSCs外泌體對巨噬細胞表型的影響。正常MSCs外泌體對免疫細胞具有免疫抑制作用,如誘導促炎表型Th1細胞向Th2細胞轉變、減少促炎因子的分泌、增加抗炎因子的分泌等[25]。MSCs外泌體的免疫抑制作用與其生物活性分子如miRNA和蛋白質有關[26]。已證實,含有miR-142-3p、miR-223-3p和miR-126-3p的MSCs外泌體調控樹突狀細胞成熟,并在其他疾病模型中促進其抗炎潛能[27]。巨噬細胞作為免疫細胞的一員,同樣受MSCs外泌體的免疫調控。巨噬細胞作為天然的免疫細胞,在免疫反應和組織修復中起重要作用[7,28]。MSCs外泌體通過誘導抗炎M2巨噬細胞的產生和抑制促炎因子的表達來觸發免疫抑制效應[29]。本研究結果顯示,低氧處理的hAMSCs外泌體同樣可以誘導巨噬細胞由促炎M1型向抑炎M2型轉化,并且可以使巨噬細胞炎性因子表達下降。本研究同時檢測了NF-κB信號通路的P65和p-P65蛋白的表達情況,結果顯示,與單純LPS誘導組相比,LPS和hAMSCs外泌體共處理組細胞p-P65/P65蛋白表達比值明顯降低,表明M1型巨噬細胞NF-κB信號通路受到抑制。提示MSCs外泌體對巨噬細胞表型的影響是通過抑制NF-κB信號通路實現的,但這一信號通路更精確的影響因子仍需進一步的實驗來探究。例如已有研究發現,三結構域蛋白(TRIM)家族是天然免疫系統不可或缺的組成成分,作為E3泛素連接酶的成員可以使視黃酸誘導基因蛋白Ⅰ(RIG-Ⅰ)降解[30-32],而RIG-Ⅰ是NF-κB信號通路的重要成員[33]。低氧處理的MSCs外泌體是否是通過RIG-Ⅰ抑制NF-κB信號通路仍需進一步實驗研究。
總而言之,MSCs具有抗炎和免疫調節能力,長期以來科研人員一直致力于將MSCs應用于多種免疫性疾病的治療。由于MSCs體內外治療效果不同,因而在體外對MSCs進行預處理以及使用有類似處理效果的MSCs外泌體進行體外實驗是近年來的研究熱點。完善與此相關的免疫調節機制信號通路的實驗研究有利于MSCs將來的臨床應用,從而提升臨床治療效果。

