伴有腦白質高信號的多系統萎縮患者臨床特征分析
黃晶晶, 陳志剛, 張新寧, 王 垚, 薛 靜 冉維正, 田文楊, 趙倩煜, 郭冰玉, 李學軍
多系統萎縮(multiple system atrophy,MSA)是一種罕見的且具有致死性的神經退行性疾病,臨床表現可見帕金森樣癥狀、小腦性共濟失調和自主神經功能障礙[1]。其主要病理特征是少突膠質細胞內α-突觸核蛋白聚集形成包涵體,導致了少突膠質細胞功能障礙,從而引起脫髓鞘改變以及對神經元營養支持作用的減少[2]。因此,除神經元丟失外,白質退行性變可能是MSA的核心特征。腦小血管病(cerebral small vessel diseases,CSVD)是臨床常見的腦血管病之一,腦白質高信號(white matter hyperintensity,WMH)是其常見的影像學表現,臨床表現可見認知障礙、步態障礙、情感障礙及二便障礙。因此,CSVD共患病可能加重MSA患者的臨床癥狀。本研究通過觀察MSA伴WMH患者的臨床特征,進一步對不同程度的WMH進行劃分,旨在探討WMH與MSA患者臨床癥狀的相關性,以及MSA患者出現WMH的危險因素。
1 資料與方法
1.1 研究對象 選取2018年5月-2021年8月北京中醫藥大學東方醫院就診的MSA患者88例。納入標準:(1)符合2008年Gilman等[1]提出的第二版診斷標準中可能或很可能的MSA;(2)年齡30~80歲。排除標準:(1)其他原因導致的腦白質病變:如多發性硬化、中樞神經系統感染、一氧化碳中毒、腦積水、腦部腫瘤、顱腦外傷等;(2)卒中或心肌梗死病史;(3)合并嚴重心肝腎臟器功能障礙或惡性腫瘤;(4)有精神疾病或不能配合認知測試者。本研究通過了北京中醫藥大學東方醫院倫理委員會批準,所有患者均簽署了知情同意書。
1.2 資料采集 收集患者的一般人口學信息和腦血管病危險因素相關的既往病史。
采用統一多系統萎縮量表(unified multiple system atrophy rating scale,UMSARS)總分、UMSARS第四部分整體失能等級(UMSARS Ⅳ)評估患者整體病情嚴重程度。采用蒙特利爾認知評估量表(the Montreal cognitive assessment scale,MoCA)評估認知功能。運動癥狀評估采用UMSARS第二部分運動檢查(UMSARS Ⅱ),分別記錄UMSARSⅡ總分及震顫、強直、運動遲緩、共濟失調、步態姿勢異常的亞分數。其中震顫=2.4靜止性震顫+2.5動作性震顫;強直=2.6張力增高;運動遲緩=2.7快速輪替+2.8輕叩對指+2.9腿部靈活度+2.11從座位上站起;共濟失調=2.7快速輪替+2.8輕叩對指+2.9腿部靈活度+2.10跟膝脛試驗;步態姿勢異常=2.12姿勢+2.13身體搖晃+2.14步態。
采用膀胱過度活動癥癥狀評分(the overactive bladder symptom score,OABSS)評估受試者尿頻尿急癥狀,采用國際尿失禁咨詢問卷簡表(the International Consultation on Incontinence Questionnaire-Short Form,ICIQ-SF)評估尿失禁癥狀,采用Wexner便秘評分評估便秘癥狀,并統計受試者有無大便失禁癥狀。
回顧患者量表評估前后3個月內的MRI檢查結果,結合T1WI、T2WI和T2FLAIR序列,由兩名經過培訓的神經內科醫生進行Fazekas量表評分,分為腦室周圍白質高信號(periventricular white matter hyperintensity,PVH)0~3分,和深部白質高信號(deep white matter hyperintensity,DWMH)0~3分[3,4]。
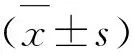
2 結 果
2.1 基線資料分析 本研究共納入研究對象88例,男性61例,女性27例;年齡40~78歲,平均(56.57±8.14)歲;發病年齡39~77歲,平均(53.95±7.93)歲;MSA-帕金森型(MSA-Parkinsonian subtype,MSA-P)27例(30.68%),MSA-小腦共濟失調型(MSA-cerebellar ataxia,MSA-C)61例(69.32%);可能的MSA29例(32.95%),很可能的MSA59例(67.05%)。PVH評分0分23例(26.14%),1分57例(64.77%),2分8例(9.09%),無3分患者。DWMH評分0分41例(46.59%),1分39例(44.32%),2分8例(9.09%),無3分患者(見表1、表3)。

表1 PVH不同等級患者一般資料的比較

表2 PVH不同等級患者臨床特征的比較

表3 DWMH不同等級患者一般資料的比較
2.2 PVH不同等級患者臨床特征的比較 PVH不同等級患者在UMSARS總分、UMSARS Ⅱ、UMSARS Ⅳ評分方面存在顯著性差異(P<0.05),在病程、臨床亞型、診斷等級、UMSARS Ⅰ、震顫、強直、運動遲緩、共濟失調、步態姿勢異常、MoCA、OABSS、ICIQ-SF、Wexner得分、大便失禁方面差異無統計學意義(見表2)。
2.3 DWMH不同等級患者臨床特征的比較 DWMH不同等級患者在UMSARS總分、UMSARSⅠ、UMSARSⅡ、UMSARS Ⅳ評分方面存在顯著性差異(P<0.05),在病程、臨床亞型、診斷等級、震顫、強直、運動遲緩、共濟失調、步態姿勢異常、MoCA、OABSS、ICIQ-SF、Wexner得分、大便失禁方面差異無統計學意義(見表4)。

表4 DWMH不同等級患者臨床特征的比較
2.4 MSA患者發生WMH危險因素的有序Logistic回歸分析 分別以PVH、DWMH評分作為因變量,對一般資料的單因素分析中P<0.05的指標進一步行有序Logistic回歸分析。因發病年齡與入組年齡存在相關性,因而只納入入組年齡。結果顯示,入組年齡、高血壓史是MSA患者發生PVH或DWMH的獨立危險因素(見表5、表6)。

表5 MSA患者發生PVH危險因素的有序Logistic回歸分析

表6 MSA患者發生DWMH危險因素的有序Logistic回歸分析
3 討 論
MSA是一種進行性神經退行性疾病,以自主神經功能障礙、帕金森綜合征、小腦性共濟失調為特征,病情進展迅速,目前缺乏有效的治療手段,預后極差[5]。既往研究發現,MSA患者中存在廣泛的白質損害,這是MSA特有的表現。一種解釋是,MSA中的白質異常最初可能高度局限于大腦的脆弱區域,隨疾病的發展而擴大;另一種觀點認為,白質異常一開始就是彌散性的,隨著疾病的發展變得越來越嚴重[6]。這反映了α-syn在少突膠質細胞中的廣泛聚集,從而導致少突膠質細胞功能障礙和進行性脫髓鞘[7]。Del Campo等研究表明,MSA患者存在普遍的白質微結構異常,與運動癥狀和認知功能相關[6]。因此,MSA患者的白質損害值得重視。
本研究納入88例MSA患者,其中65例(73.86%)伴PVH,47例(53.41%)伴DWMH。Hatakeyama等納入59例MSA患者,進行PVH分級的中位數為1(1~2),DWMH分級的中位數為1(0.75~2)[8]。Rulseh等納入20名MSA患者和20名健康對照組行DTI檢查,發現兩組受試者間的白質存在廣泛的差異,主要體現在增加的RD值和MD值上,MD值是白質的敏感性但非特異性標記,RD值已被證明與髓鞘的完整性相關[9]。這提示白質可能是MSA患者不良預后的重要因素。
本研究發現,PVH、DWMH分級均與患者的UMSARS總分及Ⅳ分數相關,DWMH分級又與UMSARSⅠ相關,提示WMH與患者的病情嚴重程度相關。未發現WMH評分與病程、臨床亞型、診斷等級間的相關性,提示白質損害在不同分型、不同診斷等級的MSA患者中普遍存在。白質受損可能參與了MSA的發病過程,且與病程無關,提示可能是發病因素,并非繼發性改變,可能是預測MSA進展和預后的潛在生物標志物。
已有研究表明,MSA患者存在全腦彌散性白質異常,與運動癥狀(UMSARS Ⅱ)有關[6]。一項基于體素的形態計量學研究對14例MSA患者和14例健康對照組研究發現,小腦和部分皮質區的灰質減少,小腦、小腦腳和腦干的白質減少,進一步隨訪1 y發現,MSA患者有額外的胼胝體白質受損,這可能反映了神經退行性變和皮質萎縮的一種特異性疾病模式,也與MSA患者的運動功能損害相符[10]。本研究發現,腦室旁WMH和深部WMH均與MSA患者的運動癥狀相關,隨WMH評分升高運動癥狀加重。其機制可能與WMH累及與運動相關的神經網絡有關,白質纖維束損傷影響脊髓對運動的控制[11~13],白質纖維束微結構的完整性被破壞,導致結構網絡效率降低,從而影響運動任務中最佳信息的處理和整合[11,14,15]。
既往研究表明,MSA的認知損害可能與皮質下網絡功能障礙與皮質萎縮之前的腦白質變性相關[16]。Hatakeyama等研究發現,WMH是MSA患者額葉功能障礙的預測因子,但并未發現白質退行性變與快速進展性認知障礙之間的關聯,可能是由于白質損傷的特點更容易引起額葉功能障礙而不是整體認知功能受損[8]。Griffanti等具體研究WMH不同的病變部位對認知功能發現,相比DWMH而言,PVH與認知水平及下降速度顯著相關[17],其病理機制可能與胼胝體、后扣帶白質纖維改變、楔葉和額中回功能連接受損密切相關。本研究結果提示,高PVH分級、高DWMH分級均與MSA患者的認知功能無關,可能與本研究選用MoCA量表評估患者的整體認知功能有關,今后的研究中需要更詳盡的認知測評,且進行隨訪以探索WMH與患者認知障礙進展的關系。
WMH的發生存在多種潛在的危險因素,加深對其危險因素的了解有助于進行早期臨床干預。Indelicato等研究發現,MSA患者的臥位高血壓與腦白質損害有關[18]。Lim等研究也表明,臥位收縮壓是WMH嚴重程度的主要影響因素,提示MSA患者存在腦靶器官損害[19]。本研究對MSA患者不同部位、不同嚴重程度WMH的危險因素進行單獨探究發現,年齡、高血壓史均是MSA患者伴發PVH或DWMH的獨立危險因素。但值得注意的是,對MSA患者血壓的管理要更為謹慎,尤其是體位性低血壓嚴重的患者,臥位血壓非常高,而立位血壓卻低于正常范圍,盲目降壓可能會給患者帶來生命危險,未來需要進一步開發有效的超高血壓和低血壓的治療策略。此外,動態血壓波動對腦血流灌注及WMH的影響尚需進一步研究,也不應排除少突膠質細胞退變與WMH相關的可能性[20]。
綜上所述,本研究結果顯示,部分MSA患者可見WMH、PVH、DWMH分級與患者的運動癥狀及病情嚴重程度相關。年齡和高血壓病史是MSA伴發PVH、DWMH的獨立危險因素,可能與其發病機制和預后有關。目前MSA的病因和發病機制尚不明確,治療手段有限,研究MSA發生、進展和預后的影響因素可為明確其發病機制和治療策略提供依據。由于本研究為單中心的回顧性研究,且MSA為罕見病,樣本量較少,研究結果存在一定的局限性,未來還需要更全面的縱向研究支持。

