2015—2020年某院腸球菌臨床分布及耐藥性分析
巴林其木格 董海榮
呼和浩特市第一醫院醫學檢驗科,內蒙古呼和浩特 010010
腸球菌是一類人體腸道中的正常菌群,作為條件致病菌,腸球菌屬具有較強的生存力和傳播力,而且易獲得抗菌藥物的耐藥性。腸球菌可引起泌尿系統、腹腔和傷口感染,甚至可導致血流感染,已成為院內感染的重要致病菌[1]。有相關研究發現腸球菌作為與醫院感染有關的致病菌,近年來的檢出率不斷增長,在美國,腸球菌已經是第二或第三位導致醫院內泌尿道感染、傷口感染和菌血癥的致病菌[2],在我國,屎腸球菌的檢出率從2014年的2.5%上升到2019年的3.0%[3]。因此,臨床微生物實驗室監測腸球菌藥物耐藥性,對臨床醫師根據細菌藥敏結果制訂正確用藥方案具有重要意義。為了解2015—2020年呼和浩特市第一醫院(本院)分離的腸球菌臨床分布特征、耐藥情況,本研究進行了相關實驗分析,現報道如下。
1 材料與方法
1.1 菌株來源
收集2015—2020年本院就診患者臨床樣本中分離的1697株腸球菌,去除同一患者3 d內同類標本的重復菌株。
1.2 細菌鑒定及藥敏試驗
按照《全國臨床檢驗操作規程》第4版[4]處理本研究實驗標本及菌株。標本接種在哥倫比亞血平板(安圖公司)進行分離培養18~24 h。細菌鑒定及藥敏試驗使用VITEK2-Compact。
1.3 統計學處理
菌株藥物耐藥性統計采用WHONET 5.6統計學軟件,統計學分析應用SPSS 22.0統計學軟件,計數資料以[n(%)]表示,采用χ2檢驗或Fisher確切概率法進行分析,P< 0.05為差異有統計學意義。
2 結果
2.1 腸球菌的分離率
2015—2020年共分離出1697株腸球菌,占同年細菌總數的8.71%,其中2015年7.81%、2016年7.95%、2017年7.47%、2018年8.18%、2019年9.32%、2020年10.28%,腸球菌分離率呈上升趨勢。2015—2020年共檢出的1697株腸球菌中有571株糞腸球菌,占33.65%;1081株屎腸球菌,占63.70%;45株其他腸球菌,占2.65%。糞腸球菌和屎腸球菌年分離率無顯著變化。
2.2 腸球菌樣本來源情況
2015—2020年糞腸球菌和屎腸球菌主要分離自患者中段尿,分泌物和膿液的糞腸球菌分離率顯著高于屎腸球菌,而血液、膽汁和腹水的屎腸球菌分離率明顯高于糞腸球菌。見表1。

表1 2015—2020年糞腸球菌和屎腸球菌標本來源情況
2.3 糞腸球菌和屎腸球菌耐藥率
2015—2020年糞腸球菌對氨芐西林(AMP)、青霉素(P)、呋喃妥因(F)、利奈唑胺(LZD)和萬古霉素(VA)的耐藥率<17.63%,保持較高的敏感性,而對紅霉素(E)和四環素(TE)的耐藥率>66.17%,保持較低的敏感性,對喹諾酮類抗菌藥物[左氧氟沙星(LEV)、環丙沙星(CIP)]的耐藥率波動在26.14%~52.12%;2015—2020年屎腸球菌對利奈唑胺、萬古霉素和奎奴普汀/達福普汀保持著較高的敏感性,其耐藥率均<6.21%,而對青霉素類、喹諾酮類抗菌藥物和大環內酯類的耐藥情況較嚴重,其耐藥率>80.00%,見表2~3。
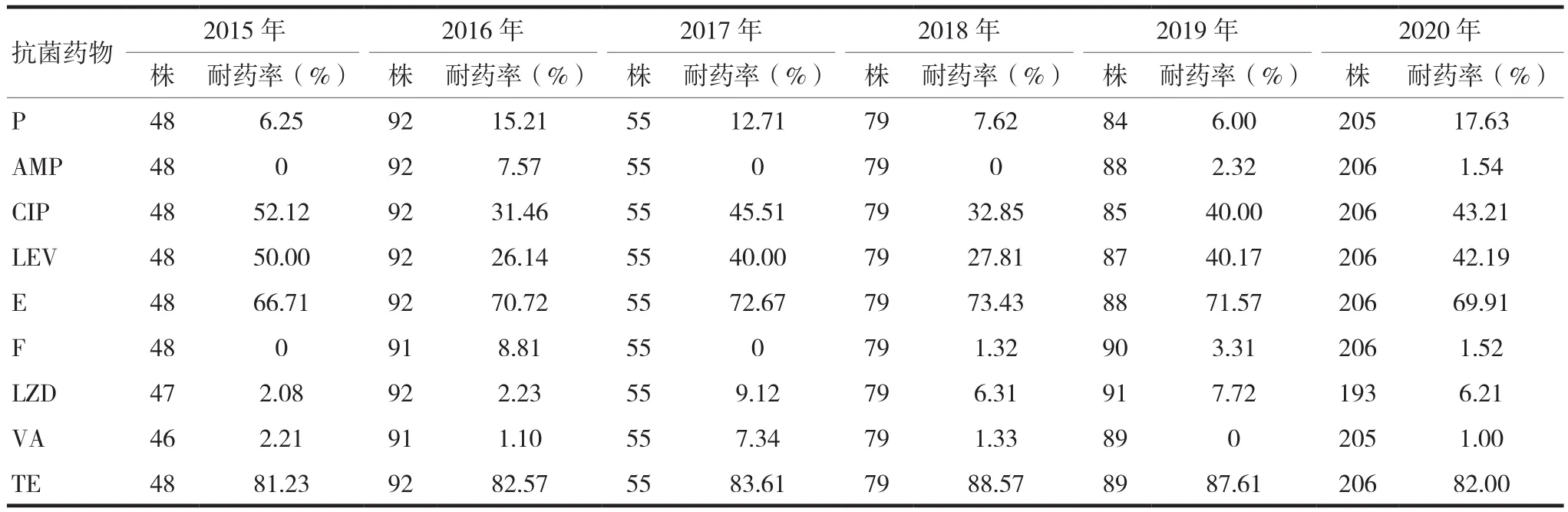
表2 2015—2020年糞腸球菌耐藥率
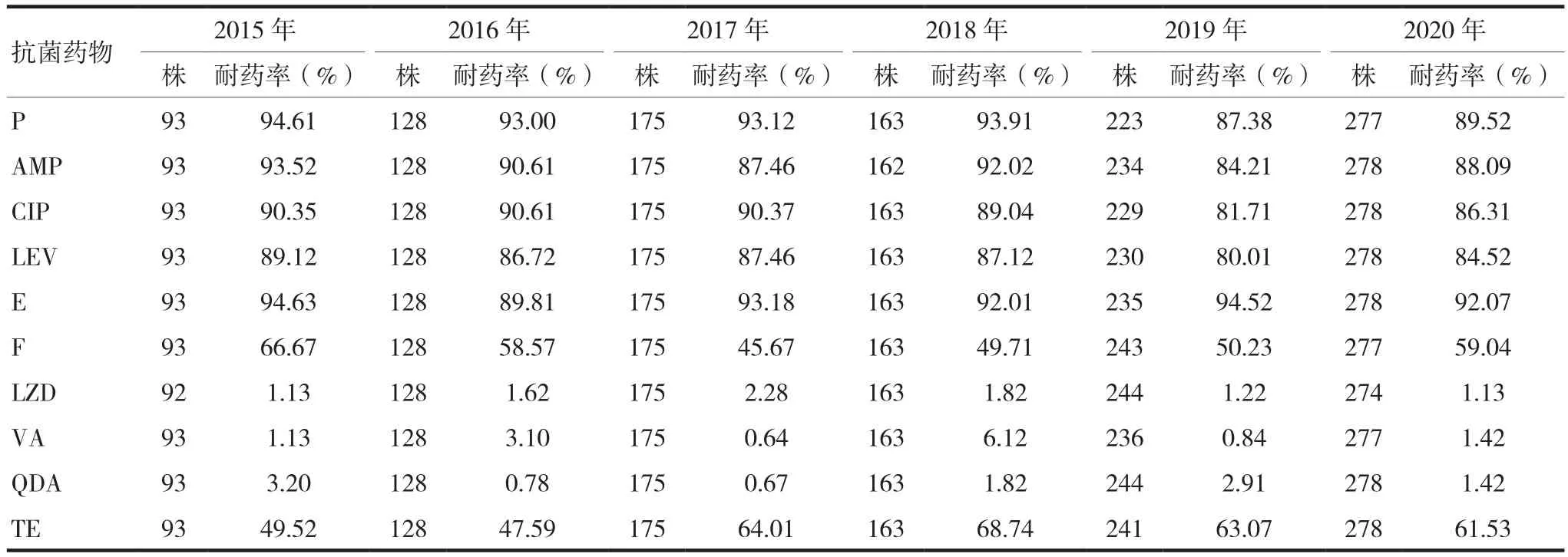
表3 2015—2020年屎腸球菌耐藥率
2.4 糞腸球菌和屎腸球菌耐藥率比較
2015—2020年屎腸球菌對除萬古霉素之外的其他抗菌藥物耐藥率明顯高于糞腸球菌,差異有統計學意義(P< 0.05),見表 4。
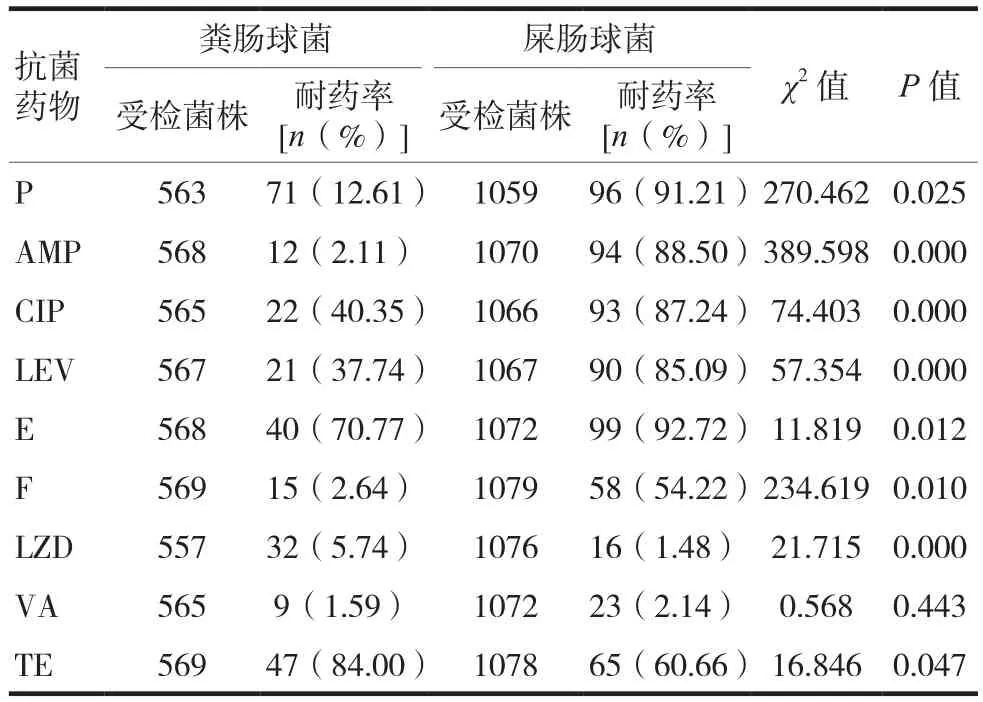
表4 糞腸球菌和屎腸球菌耐藥率比較
2.5 萬古霉素耐藥腸球菌(VRE)檢出情況
2015—2020年共檢出31株VRE,占腸球菌總數的1.85%,其中有22株屎腸球菌,占屎腸球菌總數的2.03%,9株糞腸球菌,占糞腸球菌總數的1.58%。
3 討論
醫院內感染不僅會使住院患者的病情加重,而且會造成醫療資源嚴重浪費。院內感染主要是由對多種抗菌藥物耐藥的病原菌引起的,如MRSA、VRE所引起的醫院感染,而且因可選用的抗菌藥物有限導致臨床治療較為棘手。近年來,因廣譜抗菌藥物的廣泛應用以及侵入性診療操作的增加,腸球菌的醫院感染率逐年增加[3-4]。
2015—2020年本院腸球菌檢出率總體呈逐年上升趨勢,屎腸球菌分離率顯著高于糞腸球菌,與國內有關報道[5-6]結果類似,但與許尊仲等[7]研究的深圳地區腸球菌臨床分布有所差異,這種監測結果差異可能與醫院級別、標本來源、地區差異、醫生用藥習慣等因素有關。
2015—2020年本院腸球菌從標本來源情況分析:腸球菌主要來源于中段尿。所以,腸球菌是本院引起泌尿系感染的重要病原菌。本研究結顯示,糞腸球菌從分泌物中檢出率明顯高于屎腸球菌,提示糞腸球菌引起手術切口及軟組織感染的概率比屎腸球菌高,而屎腸球菌從全血和腹水中的檢出率明顯高于糞腸球菌,國內曾有類似的標本來源情況的報道[8-9]。本研究結果提示腸球菌引起的血流感染占一定比例,且屎腸球菌引起的血流感染率顯著高于糞腸球菌。2014—2019年全國耐藥監測網[10]顯示,腸球菌在血培養分離菌病原菌中居前10位,腸球菌引起的尿路感染和腹腔感染可繼發導致血流感染,因此,臨床醫師做侵入性操作時應嚴格遵守無菌操作原則,防止交叉感染及院內感染。
腸球菌屬細菌對頭孢菌素類、克林霉素、低濃度氨基糖苷類、磺胺類等天然耐藥[11],而且隨著耐多藥(MDR)腸球菌、VRE的檢出,使腸球菌感染治療更為棘手。WHO的全球病原體優先級列表顯示,VRE為高優先級病原體,MDR腸球菌為重要威脅[12]。本研究結果表明,2015—2020年腸球菌屬內除萬古霉素之外的其他抗菌藥物耐藥率存在顯著差異。屎腸球菌對抗菌藥物的耐藥率高于糞腸球菌,與全國2019年細菌耐藥監測數據[13]相符,提示屎腸球菌相對于糞腸球菌,在抗菌藥物的選擇及敏感性方面較低,故治療屎腸球菌引起的感染時,其抗菌藥物的選擇范圍窄,治療難度增加。糞腸球菌對β-內酰胺類抗菌藥物有著較低的耐藥率,其耐藥率<17.63%,結果與譚枝微等[8]研究一致,提示對于嚴重感染,特別是基礎疾病較多的患者,臨床上可聯合使用抗菌藥物,如β-內酰胺類或萬古霉素與氨基糖苷類藥物,以抵抗腸球菌的天然耐藥性,達到最佳治療效果。
本研究結果顯示,2015—2020年屎腸球菌對奎奴普汀/達福普汀耐藥率<5.00%,與熊域皎等[14]的研究結果不同,導致這種不同的原因與不同地區醫院收治患者的病種、臨床醫生的經驗用藥習慣等有關。2015—2020年本院糞腸球菌對呋喃妥因保持較低的耐藥率,且此藥在尿液中濃度很高,可用于治療糞腸球菌引起的尿路感染。腸球菌對喹諾酮類和四環素類的耐藥率波動在中等水平,醫生可根據藥敏結果聯合用藥治療。
隨著VRE的出現,其臨床分離率逐漸增多。本研究結果顯示腸球菌對萬古霉素和利奈唑胺的耐藥率保持較低水平,但仍檢出VRE,占1.85%,雖然低于國內部分報道[15]的檢出率,但仍高于全國三級醫院耐藥水平[13],以屎腸球菌為主,且腸球菌能轉移耐藥基因給其他細菌,所以臨床醫師應嚴格控制萬古霉素的適應證,防止或延緩VRE的產生與院內傳播。
利奈唑胺主要用于治療MRSA、VRE的感染。有關報道顯示在全世界范圍內利奈唑胺耐藥率<2%[16],但本院1697株腸球菌中48株耐利奈唑胺腸球菌,占2.82%,主要以糞腸球菌為主,臨床醫師選用利奈唑胺治療時需嚴格把控用藥指征,防止利奈唑胺耐藥菌株的院內感染及流行。

