高劑量維生素D3對進展期胃癌術后合并營養風險患者營養狀態、腸道菌群和應激炎性反應的影響
劉艷玲 楊玉霞 楊玉敬
1 河南省鶴壁市人民醫院急診科 458030; 2 河南省腫瘤醫院疼痛康復與姑息醫學科; 3 河南省腫瘤醫院普外科
我國胃癌患者中有60%~80%處于進展期,一經確診,絕大多數需手術治療。手術是一種強烈應激,其通過心理上的懼怕、生理上的創傷直接影響身心和腸道組織功能重建,進而降低蛋白質、礦物質及維生素的吸收和代謝,最終導致患者營養不良,嚴重影響患者術后康復效果。術后給予患者維生素D3治療,維生素D可充分與維生素D3結合調節細胞的增殖、分化、存活、凋亡等多種生物功能,可有效預防胃癌進一步發生發展。本文旨在觀察標準劑量、高劑量維生素D3對進展期胃癌術后合并營養風險患者的療效。
1 資料與方法
1.1 一般資料 選取我科2019年10月—2020年5月收治的97例進展期胃癌術后合并營養風險患者,按隨機數字表法分為對照組和觀察組。對照組48例,男27例,女21例,平均年齡(51.01±4.79)歲;觀察組49例,男29例,女20例,平均年齡(51.53±4.82)歲。兩組一般資料對比差異無統計學意義(P>0.05)。納入標準:所有患者均符合胃癌診斷標準[1],具備胃癌根治術手術指征,NRS-200評分≥3分,患者知情。排除標準:伴有風濕免疫系統疾病、甲狀腺功能亢進疾病,對本研究藥物過敏者。
1.2 方法 兩組患者均給予術后短期腸外營養支持,術后第1天開始全腸外營養支持,連續治療5d,以“全合一”方式經過頸內靜脈置管進行輸注,輸注時間為12~16h,脂肪乳占30%~40%,蛋白質以1.5~2.0g/(kg·d)補充,非蛋白熱量為30kcal/(kg·d),熱氮比為150∶1。對照組在此基礎上給予標準劑量維生素D3(國藥控股星鯊制藥有限公司,H35021450)口服治療,400IU/次,1次/d。觀察組在營養支持基礎上給予高劑量維生素D3口服治療,4 000IU/次,1次/d。兩組均治療3個月。
1.3 觀察指標 (1)營養狀態:采集患者空腹靜脈血,用酶聯免疫吸附法(ELISA)檢測25羥維生素D[25(OH)D],采用免疫比濁法檢測白蛋白(Alb)、血鈣(Ca)水平,采用全自動血細胞分析儀檢測血紅蛋白(Hb)水平。(2)腸道菌群:采集兩組患者糞便標本,采用細菌三級鑒定法對細菌鑒定至菌屬水平,比較兩組患者雙歧桿菌、腸球菌、大腸桿菌數量。(3)應激炎性反應:抽取患者空腹靜脈血,采用免疫層析法檢測血清C反應蛋白(CRP),采用ELISA檢測白細胞介素-6(IL-6)、皮質醇(Cor)水平。
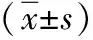
2 結果
2.1 兩組治療前后營養狀態對比 治療后觀察組25(OH)D、Alb、Ca、Hb水平高于對照組(P<0.05)。見表1。
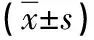
表1 兩組營養狀態對比
2.2 兩組治療前后腸道菌群對比 治療后觀察組雙歧桿菌數量略高于對照組,腸球菌、大腸桿菌數量略低于對照組,但差異無統計學意義(P>0.05)。見表2。

表2 兩組腸道菌群對比
2.3 兩組治療前后應激炎性指標水平對比 治療后觀察組CRP、IL-6、Cor水平低于對照組(P<0.05)。見表3。
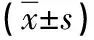
表3 兩組應激炎性指標水平對比
3 討論
進展期胃癌患者機體在腫瘤的負荷作用下,三大營養物質代謝吸收均會發生異常變化,再加上外科手術治療后對機體的創傷及術后禁食、胃腸減壓等均會增大患者機體的分解代謝,進而加重其營養不良狀況,增大術后發生營養風險。本文結果顯示,治療后兩組腸道菌群數量均有改善,但組間無明顯差異,提示經標準劑量維生素D3或高劑量維生素D3聯合短期腸外營養支持治療糾正患者腸道菌群紊亂效果相當。短期腸外營養支持通過靜脈輸注給予脂肪、礦物質、碳水化合物、蛋白質等營養物質,可分解出大量脂肪酸被腸道黏膜細胞利用,發揮降低腸道pH值、保護腸道黏膜屏障的作用,防止腸道內細菌移位,進而調節腸道菌群紊亂,促進腸道功能恢復。維生素D3是人體必需的營養素,其通過維生素D受體相結合可誘導胃癌腫瘤細胞信號傳導和基因調控的瀑聯效應,進而抑制腫瘤細胞增殖,刺激其自噬和凋亡,在抗腫瘤機制中發揮重要作用。維生素D對維持患者正常腸道功能具有重要作用,通過補充不同劑量維生素D3可增大腸道內乳酸桿菌和雙歧桿菌等有益菌的表達,增強腸道黏膜上皮細胞間相連的蛋白穩定性,降低腸球菌、大腸埃希菌數量,有效糾正腸道菌群失調現象,有助于胃腸功能恢復。經標準劑量維生素D3治療仍存在血鈣降低現象[2],相較于高劑量維生素D3,其使大量蛋白尿丟失造成血液中CABP、DBP等相關載體蛋白隨尿液排出體外,進而使腸道對鈣的吸收降低并出現低蛋白癥,影響進展期胃癌患者預后效果。
本文結果顯示,治療后觀察組25(OH)D、Alb、Ca、Hb水平優于對照組,提示經高劑量維生素D3聯合短期腸外營養支持可改善營養狀態,提高機體內25(OH)D水平。短期腸外營養支持通過靜脈系統輸注營養物質,可增大患者機體攝入大量的氮和熱量,糾正機體負氮平衡狀態,降低了手術創傷后高代謝和應激反應,促進腸道對營養物質的充分吸收,進而改善患者營養狀態。在患者術后給予標準劑量維生素D3治療,可促進營養物質的吸收,提高營養狀態,而鈣敏感受體(CASR)是調節血鈣的關鍵因素,胃癌患者機體內血鈣水平輕微的波動均會被CASR感知,并對其產生調節作用,當血鈣水平降低時,CASR可經減低自身活性促使改調定點上移,但其對血清游離鈣難以調節,并當血液鈣水平降到一定程度CASR的調節作用會受到嚴重損害,進而影響患者對營養物質的吸收,營養狀態改善效果不顯著[3]。進展期胃癌術后患者給予高劑量維生素D3治療,其代謝產物主要包含骨化三醇[1,25(OH)2D3]和阿法骨化醇[1α-(OH)D3],通過與維生素D受體相結合,維生素D3可增加患者胃腸道對鈣、鎂、鐵和磷酸鹽等營養素的吸收,可提高抵抗力,減低血液內鐵調素濃度調節鐵循環,進而緩解貧血癥狀,提升25(OH)D水平,有效改善營養狀態[3]。
本文結果顯示,觀察組CRP、IL-6、Cor水平均低于對照組,提示經高劑量維生素D3與短期腸外營養支持聯合治療,可有效降低進展期胃癌術后患者機體應激炎癥反應。維生素D缺乏在胃癌患者中非常普遍,而對于給予標準劑量維生素D3治療的患者而言,通過作用于維生素D受體上,可調節巨噬細胞、T淋巴細胞、樹突細胞等免疫細胞的分化、增殖過程,減少了炎癥因子的釋放與分泌,但人體細胞在維生素D3的激素刺激作用下會產生明顯的耐受性,特別是T細胞分泌多種白細胞介素的功效不足,促使細胞功能下降,對降低患者機體炎癥應激反應效果欠佳。相較于標準劑量維生素D3,高劑量維生素D3可通過減少Nephrin蛋白的丟失,減少足細胞的脫落等作用來減少尿蛋白的生成,并抑制炎癥細胞浸潤、減少炎性因子分泌、下調腎素—血管緊張素系統(RAS)等機制來保護胃腸道功能;同時長時間服用高劑量維生素D3其生成的代謝產物1,25(OH)2D3可調節腸道基因和生理穩態環境,進而提高宿主對病原微生物的防御能力,減少有害菌的大量滋生,減低機體炎癥應激反應[4]。
綜上所述,高劑量維生素D3聯合短期腸外營養支持治療進展期胃癌術后合并營養風險患者,可有效降低機體應激炎癥反應,調節腸道菌群,改善營養狀態。

