獼猴桃組織培養繁殖苗木
劉永利
(朝陽縣臺子鎮林業站,遼寧 朝陽 122625)
獼猴桃的繁殖方式多種多樣,有實生繁殖、嫁接繁殖、扦插繁殖等。這3種方式比較常見且容易操作,需要的硬件條件也不高。組織培養雖然相對要復雜一些,上手難度較大,但是如果遇到不能量產的稀有品種,采用此種方法卻能夠取得巨大的效果,所以了解其過程以及繁殖方法十分必要。
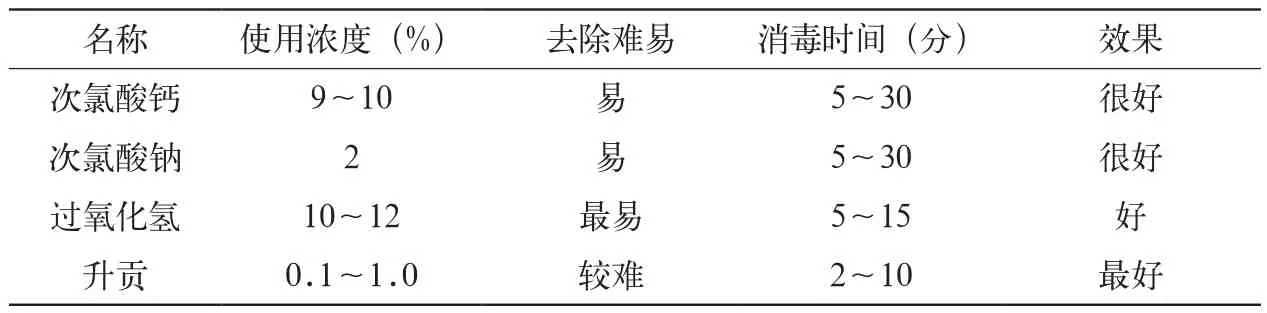
表1 常用消毒滅菌劑及效果比較
從理論上講,植物的每一個細胞都具有成長為一個完整植株的功能。因此,植物組織培養是一種十分重要的繁殖技術。
獼猴桃組織也同其他植物組織一樣,具有無限增殖和產生不定芽及不定根的能力,在適宜的培養條件下,用一部分組織可以培養出許多植株,并能保持原有植物的種性,特別是對于數量稀少的優良品種和砧木,采用組織培養來進行工廠化育苗具有重要意義。
1 材料及材料消毒
1.1 材料
組織培養的材料可以選用獼猴桃的莖段、莖尖、腋芽、葉片、葉梗、下胚軸、胚乳、幼胚、原生質體等。在國外也有用根、果實組織(幼果果皮附近的組織)作接種材料的。常用的組織培養材料為獼猴桃莖段、莖尖和腋芽。
1.2 滅菌消毒
因各個器官組織的特性不同,需要無菌操作所用消毒藥品、濃度,具體操作方法、處理時間等也有所差異。常用消毒滅菌劑有多種,效果不盡相同,在實踐中應根據材料摸索試驗,采用既能達到消毒滅菌目的,又不損傷材料的藥劑。
2 基本培養基
基本培養基為MS培養基,但培養材料不同,其組分也有所變化。蔗糖和瓊脂的用量可根據不同需要進行調整,培養基的酸堿度調至pH5.8。配好培養基,分裝于玻璃容器內,在120℃高壓蒸氣下滅菌30分鐘后備用。

圖1 繼代培養切莖
3 外植體接種與培養
外植體選取健壯的當年生嫩枝上的莖段、莖尖或腋芽。將外植體用自來水沖洗2小時,用75%乙醇漂30秒鐘,用0.1%氯化汞溶液滅菌5~8分鐘,倒凈滅菌液,用無菌水沖洗3~4次。如果是莖段接種,則用消毒解剖刀刮去表皮,露出綠色皮層,再縱劈成2~4片,并剪成0.5~1.0厘米長的小段,小段不能帶有節部,接種在試管中的培養基上,每管2~4小段(試管為30毫米×160毫米)。
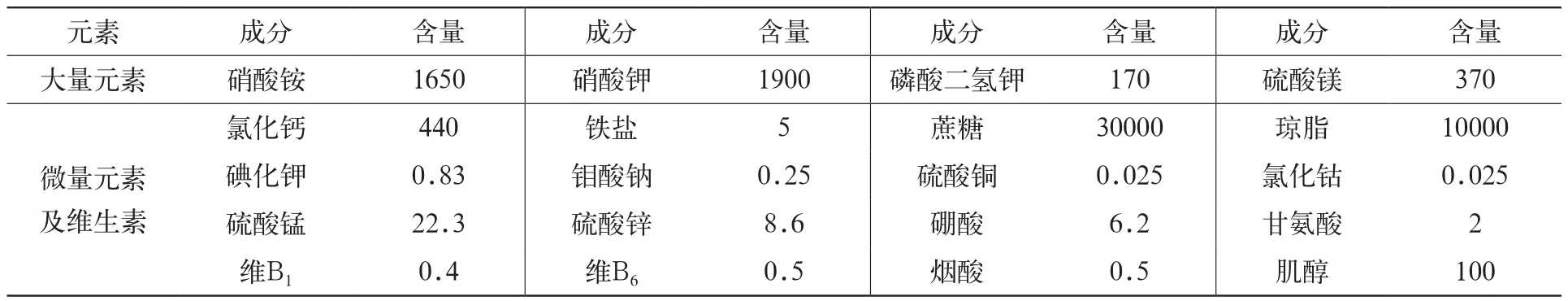
表2 MS培養基的基本組分 毫克/升
如果是莖尖或腋芽培養,每個試管的培養基上接種一個芽。莖尖應剝去毛被及葉片,留下黃綠色帶有1~2個葉原基的小葉片作培養材料。
上述外植體接種的基本培養基為MS,蔗糖濃度2%,pH5.8,添加玉米素0.1~30毫克/升、6-BA(6-芐基腺嘌呤)0.1~5毫克/升、IBA(吲哚丁酸)0.1~5毫克/升和NAA(萘乙酸)0.1~5毫克/升。接種后將試管放在培養室的培養架上,培養溫度25±1℃,光強度1000勒克斯,每日照光12小時。
4 繼代培養
外植體培養一周后會產生愈傷組織,一個月可見到分化出來的小植株。待莖長到1~3厘米,即可進行繼代培養。采用切斷法,將其剪成約1厘米長莖段,接種到新的培養基中。以后每隔約30天進行一次繼代培養,每次的莖段增殖量為3~4倍。反復進行,直到所需繁殖數量。根據成都生物所的試驗,待試管苗伸長到4~5厘米時進行剪切,每次切成4段,每隔60天切一次,一年可切6次,即1個芽的繁殖系數為4的6次方,即4096株。
5 誘導生根
試管內繼代培養的小植株長到2厘米左右時,從基部切下,用吲哚丁酸(IBA)20~30毫克/升液浸泡2小時,再轉接在生根培養基上誘導生根。生根培養基的成分為MS培養基的大量元素減半,包括激素和蔗糖也要減半,其他成分不變。轉接生根培養時,要防止葉片接觸培養基,以利生根。經培養10天左右,在基部切口即可產生不定根,20天左右成為真根,變成完整幼苗。待植株長到3~5厘米,則可進行鍛煉、移栽。
6 鍛煉與移栽
組培苗是在嚴格的人工操控條件下長成的,對自然生態環境條件下能否適應,還需要一個過渡階段,這個過渡階段就是鍛煉。方法是,將試管苗轉移到較大的容器中培養,使小苗生長健壯;或將有苗的試管移到自然光照下2~3天,打開試管口2~3天,使試管苗得到鍛煉,然后移栽。
試管苗移栽時先用30℃左右溫水,洗凈苗上的瓊脂等培養基,再移入溫室栽植,不要直接移入露地栽植,因成活率很低。溫室保持20~25℃的溫度,95%的空氣相對濕度,土壤為腐殖土或人工配制的營養土。溫室中生長80天左右,葉可長到8片以上,株高6厘米以上,新根數量500條以上,長17厘米以上。然后再移栽到露地苗圃,成活率極高。
7 結語
獼猴桃的實生繁殖、嫁接繁殖、扦插繁殖與組織培養繁殖等4種繁殖方法,是目前中國和其他國家普遍采用的繁殖方法。除此之外,還有其他繁殖方法,如利用枝蔓進行壓條繁殖,包括地面壓條和空中壓條;利用根際萌蘗進行分株繁殖。這兩種繁殖技術因為繁殖率低,不便操作,因此不常采用。

