喹啉腈熒光微球構建及在熒光免疫層析中對SAA 的檢測應用
李 強, 徐建新, 郭志前
(1. 上海奧普生物醫藥股份有限公司, 上海即時檢測醫學工程技術研究中心, 上海 200201;2. 華東理工大學化學與分子工程學院, 精細化工研究所, 上海 200237)
聚集誘導發光(Aggregation-Induced Emission,AIE)材料是近年來新興的熱點研究領域,因其具備獨特的聚集態發光性質而倍受關注。傳統發光材料多受到“濃度猝滅(Aggregation-Caused Quenching,ACQ)”效應的制約,其分子在高濃度下表現出明顯的熒光猝滅性質;相比之下,AIE 熒光材料在稀溶液中的分子態下幾乎不發光,而當其處于分子聚集態時表現出顯著的熒光增強效應[1-3]。AIE 材料具有發光效率高且光穩定性強的特性,因而能在細胞成像及相關生物成像中應用,獲得更好的圖像分辨率,特別是在高濃度態或聚集態下,AIE 材料表現出更高的靈敏度,并且能通過化學修飾來實現發光波長的調控等[4-6]。AIE 熒光材料的設計及應用等基礎研究得到了廣泛的關注。
目前,AIE 熒光材料在熒光探針、生物成像、診斷以及治療等領域具有廣泛的應用前景[7-8]。AIE 熒光材料應用于檢測的生物分子包括氨基酸、糖類、DNA/RNA、蛋白質、肽等;應用于監測的生物過程有蛋白纖維顫動、細胞凋亡、成骨分化、自噬/有絲分裂等;此外,還可應用于特定細胞器、細胞、微生物、組織甚至動物的成像等方面[9-12]。
由病原菌和病毒等引起的傳染病感染,通常是指細菌、病毒、真菌、寄生蟲等病原體侵入人體所引起的局部組織和全身性的炎癥反應,一直是全球公共衛生關注的重要焦點問題,并且往往伴隨著較高的死亡率[13-14]。如何快速、準確地鑒別細菌或者病毒感染的類型是臨床醫學診斷中面臨的最大困難和挑戰之一,盡管它們在臨床癥狀表現上缺乏特異性,但在臨床用藥上卻存在顯著的差異。傳統的感染診斷方法包括紅細胞沉降率、病原培養、白細胞計數和聚合酶鏈反應等[15-18],但這些方法受到檢測時間長、樣品預處理過程復雜、設備昂貴或技術人員操作水平低等制約,無法滿足臨床即時檢測POCT(Point-of-Care Testing)的需求,從而無法實現快速、便捷、高效的診斷。
血清淀粉樣蛋白A(Serum Amyloid A,SAA)[19-21]是一種由肝細胞產生后被分泌到血清中的一種急性時相蛋白,當機體發生感染或損傷時,其濃度可在4~6 h 內迅速升高約1 000 倍,當機體抗原清除后則迅速降低回復至正常水平。目前,臨床對于炎癥檢測的研究主要集中在炎性疾病急性反應期間的SAA類型[22],亦有專家學者發現SAA 異常可以作為新冠患者病癥診斷的一個重要指標[23]。臨床診斷中SAA具有如下顯著特點:(1)SAA 作為急性時相反應蛋白之一,臨床上可用于監測急性期反應,是反映機體感染情況和炎癥恢復情況的重要靈敏指標之一,已有研究表明在新冠患者中SAA 的變化表現較為明顯;(2)與目前臨床廣泛使用的炎癥指標CRP(C-Reactive Protein)相比較,SAA 的升高見于病毒、支原體感染,且其敏感性高于CRP; CRP 升高多見于細菌感染,但對病毒及支原體等病原體感染因其濃度變化幅度小而敏感性較低[24-25],因而SAA 與CRP 的聯合檢測可以互補應用,能夠更有效地提高感染性疾病的檢出率。因此,快速、準確地檢測到SAA 的含量,可以為醫護人員對病患進行有效診斷、評估、監控及治療提供更敏感的診斷依據。
目前體外快速檢測SAA 的方法主要分為金標法、膠乳免疫比濁法、熒光免疫層析法、化學發光法等[26-28]。熒光檢測技術[29-30]因其操作簡單、靈敏度高、方便攜帶、可家用等優點受到廣泛關注。本文采用溶脹包埋的方法,制備了基于喹啉腈(QM)[31-32]熒光染料衍生物QM-OH 的AIE 熒光微球QM-OH@PS-COOH(羧基聚苯乙烯),發展了基于熒光免疫層析的檢測技術,實現了對臨床樣本中SAA 的定性、定量靈敏檢測,以及對病毒感染患者的體外快速診斷。
1 實驗部分
1.1 主要材料
實驗所用的SAA 標記抗體、涂層抗體均購自莫迪斯公司,SAA 抗原購自上海普欣生物技術有限公司。過硫酸鉀、苯乙烯、甲基丙烯酸、四氫呋喃(THF)、十二烷基苯磺酸鈉、多聚磷酸鈉、硝酸,N-羥基硫代琥珀酰亞胺(NHS),均為分析純,購自上海泰坦科技股份有限公司;SAA 檢測試劑卡購自上海奧普生物醫藥股份有限公司。
1.2 測試與表征
核磁共振氫譜和碳譜的測定采用德國Bruker公司的超導傅里葉變換核磁共振波譜儀(Bruker AvanceIII 400 MHz),以四甲基硅烷 (TMS,摩爾分數0.03%) 為內標溶劑測定,并以氘代二甲基亞砜(DMSOd6)為溶劑;質譜測試為美國沃特世公司的質譜分析儀(Waters LCT Premier XE);紫外-可見光光譜采用美國安捷倫公司的紫外-可見光吸收光譜儀器(Agilent Cary 60)進行測定。熒光光譜采用日本Horiba 公司熒光光譜儀(Floromax-4 Spectrofluorometer)進行檢測;粒度大小采用Malvern 公司粒徑儀(Zetasizer Nano S90)進行檢測;電導率(G)采用上海雷磁公司的電導率儀(DDS-307A)檢測;試劑卡采用上海奧普生物醫藥股份有限公司MAYA 免疫熒光定量分析儀(MAYA-500)開展檢測研究。
1.3 實驗方法
1.3.1 喹啉腈衍生物QM-OH 的合成 QM-OH 的具體合成方法參照文獻[31]。
1.3.2 熒光微球QM-OH@PS-COOH 的合成 在500 mL 燒杯中,分別加入十二烷基苯磺酸鈉0.4 g、過硫酸鉀0.25 g 和多聚磷酸鈉0.25 g,然后再加入250 mL 超純水,混合均勻至溶解。將上述溶液倒入500 mL 三頸瓶中(水浴預先加熱到85 ℃),在攪拌(300 r/min)和通氮氣情況下逐滴加入25 mL 苯乙烯,滴加完全30 min 后再逐滴加入甲基丙烯酸溶液1.5 mL,然后在水浴85 ℃加熱攪拌和通氮氣情況下持續反應6 h。當反應結束冷卻后,用布氏漏斗抽濾,得到的濾液即為PS-COOH。在50 mL 圓底燒瓶中,加入四氫呋喃和水的混合溶液約25 mL,再加入PS-COOH 5 mL和QM-OH 50 mg,在60 ℃水浴中溶脹包埋6 h 后,得到AIE 熒光微球QM-OH@PS-COOH。
1.3.3 QM-OH@PS-COOH 微球羧基含量的測定在250 mL 的燒杯中,加入100 mL 超純水,稱取1 g熒光微球QM-OH@PS-COOH 分散于水相中,用NaOH 溶液調節pH 約為10。以0.2 mol/L 的稀硝酸溶液進行滴定,每次滴定加入20 μL 稀硝酸,記錄溶液的電導率變化并作圖計算得到QM-OH@PS-COOH熒光微球上的羧基含量。
1.3.4 QM-OH@PS-COOH 和標記抗體偶聯儲備液的制備 在10 mL 試管中分別加入超純水1.3 mL、磷酸鹽緩沖液(PBS)1 mL、熒光微球QM-OH@PSCOOH 1 mL、標記抗體1.4 mL,在室溫下混和均勻15 min;然后加入1 mL 1-(3-二甲氨基丙基)-3-乙基碳二亞胺鹽酸鹽(EDC)溶液(10 mg/mL),室溫下繼續混勻30 min;接著加入2 mL、0.03 g/mL 的牛血清蛋白(BSA)溶液進行封閉,室溫下繼續混勻30 min;離心除去上清液,向得到的固體中加入2 mL 熒光恢復液,并將其超聲分散,得到單分散的QM-OH@PS-COOH和標記抗體偶聯的熒光儲備液。
1.3.5 QM-OH@PS-COOH 和標記抗體偶聯的熒光儲備液檢測SAA 移取SAA 抗原5 μL 加入到1 mL 1.3.4 節制備的QM-OH@PS-COOH 和標記抗體偶聯熒光儲備液中,均勻混合1 min,然后滴加0.3 mL 到試紙卡上,放置1 min 后,再將試紙卡插入MAYA 熒光免疫定量分析儀進行讀數。
2 結果與討論
2.1 QM-OH 的核磁波譜及高分辨質譜表征
在100 mL 的圓底燒瓶中,分別加入QM(1.2 g,5.1 mmol)和4-羥基苯甲醛(671 mg,5.5 mmol),同時加入30 mL 乙腈溶解固體,磁力攪拌下滴加1 mL 哌啶,氬氣保護下加熱回流反應10 h。反應過程中,反應液逐漸由黃色變為橙紅色。反應結束冷卻至室溫,觀察到有大量的橙紅色固體析出。用旋轉蒸發儀濃縮有機相,并利用硅膠柱層析分離得到粗產品(硅膠200~300 目(48~74 μm),展開劑二氯甲烷和甲醇的體積比為20∶1),最終得到橘色固體對羥基喹啉腈(985 mg,2.9 mmol),產率 56.6%。1H-NMR(400 MHz, DMSO-d6,δ): 10.05 (s, 1H, -OH), 8.94 (d,J=8.8 Hz, 1H, phenyl-H), 8.10 (d,J= 9.2 Hz, 1H, phenyl-H), 7.92 (t,J= 7.6 Hz, 1H, phenyl-H), 7.69 (d,J= 8.4 Hz,2H, phenyl-H), 7.61 (t,J= 7.6 Hz, 1H, phenyl-H),7.39~7.29 (m, 2H, alkene-H), 7.02 (s, 1H, quinoline-H),6.87 (d,J= 8.4 Hz, 2H, phenyl-H), 4.56 (q,J= 6.8 Hz,2H, -CH2CH3), 1.40 (t,J= 8.0 Hz, 3H, -CH2CH3)。13CNMR (100 MHz, DMSO-d6,δ): 13.63, 24.63, 26.28,43.71, 46.24, 46.53, 106.42, 115.82, 116.58, 118.07,120.60, 124.85, 125.09, 126.04, 130.04, 133.60, 137.84,140.06, 149.68, 152.05, 159.80。 Mass spectrometry(ESI for [M + Na]+): Calcd. for C22H17N3ONa: 362.126 9;found: 362.126 8。
2.2 QM-OH 的紫外-熒光光譜圖
激發波長(λex)為440 nm 下QM-OH 在水和THF混合體系中的紫外-熒光光譜圖如圖1 所示。在水和THF 的混合溶液中,QM-OH 的紫外吸收光譜在320~500 nm 之間有一組寬的雙重吸收峰(吸收波長(λabs)為365 nm 和440 nm),隨著混合溶劑中水體積分數(fw,0~95%)的不斷增加,其雙重吸收峰位置沒有發生明顯變化,相比之下其熒光光譜隨著fw的增加而顯著增強。當fw處于0~70%時,QM-OH 表現為明顯的熒光淬滅效應;當fw> 70%時,其在550 nm處的熒光強度表現出顯著的增強,并且伴隨著fw的逐漸增大其熒光不斷增強,當fw= 95%時,熒光強度達到最大值。這些結果表明分子QM-OH 本身具有明顯的AIE 聚集誘導發光性質。
2.3 AIE 熒光微球QM-OH@PS-COOH 的結構表征和分析
首先由粒徑儀測試得到AIE 熒光微球QM-OH@PS-COOH 的粒徑約為100 nm 左右。然后利用掃描電子顯微鏡(SEM)對熒光微球QM-OH@PS-COOH進行結構表征,結果如圖2 所示,該熒光微球呈現出規則的球狀形貌。在體外診斷試劑中通常采用球形熒光微球作為修飾材料,通過微球表面修飾羧基后與抗體偶聯達到最佳效果,有利于提升檢測準確性。圖2 插圖是AIE 熒光微球QM-OH@PS-COOH的乳液圖片,通過肉眼可以清晰地觀察到該AIE 熒光微球是亮黃色的,其吸光度變化便于體外診斷過程中的定性判斷。
2.4 AIE 熒光微球QM-OH@PS-COOH 的密度、固含量及羧基含量的測定

圖1 λ ex =440 nm 下QM-OH 在水和THF 混合體系(不同水體積分數)中的紫外吸收光譜圖(a)和熒光光譜圖(b)Fig. 1 Ultraviolet absorption (a) and fluorescence (b) spectra of QM-OH in H2O/THF mixtures with different volume fractions of water (fw)under λex = 440 nm

圖2 QM-OH@PS-COOH 的TEM 圖(插圖是QM-OH@PS-COOH 的乳液圖片)Fig. 2 TEM image of QM-OH@PS-COOH (Illustrated by emulsion image of QM-OH@PS-COOH)
在干凈的小稱量杯(質量3.132 1 g)中,加入1 mL制備的熒光微球QM-OH@PS-COOH,稱量得到兩者總質量為4.135 1 g,然后放入70 ℃的烘箱中烘6 h,將水分烘干,稱取質量為3.232 9 g。經計算,熒光微球QM-OH@PS-COOH 的密度為1.003 g/mL,固含量(質量分數)為10.08%。
根據文獻[33],對合成的微球進行電導率滴定,具體操作見1.3.3 節。溶液的電導率隨著稀硝酸溶液加入體積的不同呈現如圖3 所示的變化。羧基含量(DC)的計算公式如下;
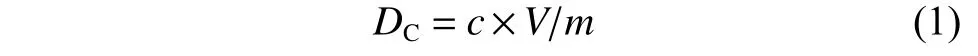
其中:c為滴定稀硝酸的濃度;V為所用稀硝酸的體積;m為滴定中微球的質量。
熒光微球的表面羧基密度(PA)計算公式為:

其中:ρ為該批次微球密度;d為微球粒徑。
圖3 中AB 段示出了過量堿滴定時的電導率變化;BC 段示出了對微球上羧基滴定引起的電導率變化;CD 段示出了過量的稀硝酸溶液引起的電導率變化。經計算,BC 段所用稀硝酸的物質的量為5.6×10-5mol,微球的羧基含量為0.056 meq/g,PA 值為177.3。
2.5 QM-OH@PS-COOH 在熒光免疫層析中對SAA 的檢測
在對AIE 熒光微球QM-OH@PS-COOH 的結構進行表征后,將該AIE 熒光微球用于熒光免疫層析中,對病毒感染中產生的SAA 抗原進行一系列的相關檢測,其原理如圖4 所示。首先將QM-OH@PSCOOH 與SAA 標記抗體偶聯,得到熒光標記抗體(熒光液);然后待測樣本在流動相的作用下先與熒光標記抗體結合,并在硝酸纖維素(NC)膜的層析作用下到達檢測線再與涂層抗體結合,形成雙抗夾心的“三明治”型。檢測線處的信號變化采用與設計配套的熒光儀器進行定量測定,其熒光強度變化與樣品中SAA 質量濃度呈正相關。通過檢測線上的熒光液和質控線進一步獲取檢測到的熒光信號,利用檢測儀器放大信號,得到SAA 質量的具體數值,從而實現對病毒感染患者的體外快速診斷。
SAA 更適用于小兒感染性疾病的診斷,是病毒感染早期檢測的靈敏指標。因此,對于病毒感染標志物SAA 來說,高靈敏度的檢測至關重要。首先,使用AIE 熒光微球QM-OH@PS-COOH 標記的抗體熒光液對SAA 質控品進行定標,得到如表1 所示的數據。表中數據1 和數據2 分別是2 次的儀器熒光測試值,當SAA 測試值高于50 mg/L 時,適用于定標的A 線;反之,適用于定標的B 線。對應的A、B 定標曲線如圖5 所示,由圖可見,當SAA 質量濃度從0 升高到216 mg/L 時,熒光強度與質控品中SAA 質量濃度呈正相關,說明AIE 熒光微球QM-OH@PS-COOH 標記的抗體熒光液對SAA 質控品進行了有效定標,其中A 線相關系數為0.992 1,B 線的相關系數為0.984 0,體現了良好的線性關系。
SAA 是反映感染性疾病早期炎癥的敏感指標,有助于炎癥診斷、評估、監控及治療。因此在對SAA 質控品進行有效定標后,使用AIE 熒光微球QM-OH@PS-COOH 標記的抗體熒光液對病毒感染的血液樣本進行測試。10 份血液樣本來自上海中醫藥大學附屬龍華醫院。所有的測試均在MAYA 熒光免疫定量分析儀和SAA 樣板條上測定,如圖6 所示。將使用AIE 熒光微球QM-OH@PS-COOH 標記的抗體熒光液測試的10 份血液樣本的測試數值與龍華醫院的測試數值進行了對比,結果如表2 所示。臨床上,當SAA 質量濃度低于10 mg/L 時為正常水平;當SAA 質量濃度高于10 mg/L 時預示感染;當SAA質量濃度高于50 mg/L 時為陽性高值樣本。由表2可知,有4 份陰性樣本和6 份陽性樣本,其中陽性樣本有2 份陽性高值樣本。該AIE 熒光微球標記的體系能夠有效區分血液樣本中的陰性和陽性樣本,與龍華醫院測試值一致。同時,該體系測試值與龍華醫院的測試值偏差在±15%之內,符合測試要求。
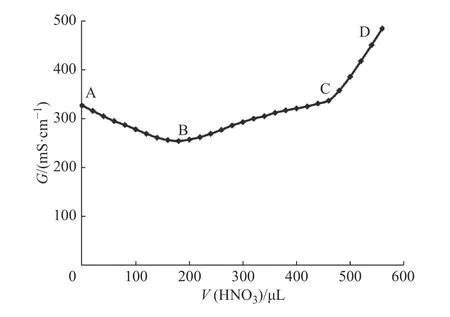
圖3 QM-OH@PS-COOH 的表面羧基電導率滴定變化圖Fig. 3 Surface carboxyl electric conductivity titration of QMOH@PS-COOH
SAA 樣本條上有質控線(C 線)和檢測線(T 線)兩條。檢測合格有效的樣本條必須滿足以下條件:(1)C 線處有顏色和熒光呈現;(2)陰性樣本在T 線處無顏色且無熒光呈現,陽性樣本在T 線處有顏色和熒光呈現。
如圖6(b)所示,在日光下,可以看到SAA 的陰性樣本在樣板條上的T 線處沒有顏色;陽性低值則在T 線處呈現淡黃色;而SAA 的陽性高值樣本在T 線處有較為明顯的黃色。在紫外燈下,如圖6(c)所示,SAA 的陽性高值(115.14 mg/L)樣本在T 線處有較為明顯的黃色熒光;SAA 的陽性低值(23.73 mg/L)樣本在T 線處呈現較弱的黃色熒光;SAA 的陰性樣本則沒有熒光呈現。肉眼可見的判定適用于對SAA 的定性分析。熒光數值可以通過MAYA 熒光免疫定量分析儀放大處理得到,適用于對SAA 的定量分析。
目前市面上的體外診斷自測試劑(如新冠自測試紙條)主要是膠體金法和彩色微球法,以定性檢測為主,實驗結果顯示基于AIE 熒光微球的檢測SAA試紙條既可以定性檢測,還能借助MAYA 熒光儀器來定量檢測。該AIE 熒光微球QM-OH@PS-COOH標記的抗體熒光液對SAA 具有良好的檢測效果,在體外診斷領域尤其是自測試劑方面具有一定的潛在應用價值。
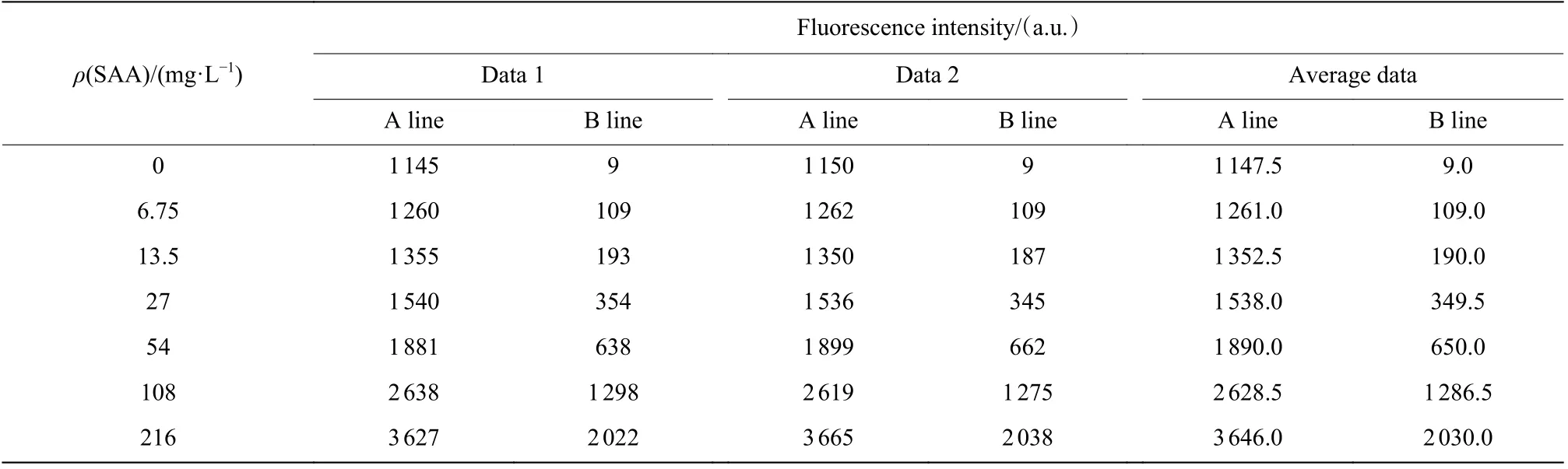
表1 SAA 質控品定標的數據Table 1 SAA quality control product calibration data

圖4 喹啉腈AIE 熒光微球QM-OH@PS-COOH 熒光免疫層析檢測SAA 原理示意圖Fig. 4 Schematic diagram of quinoline-malononitrile AIE fluorescent microsphere QM-OH@PS-COOH for SAA detection in fluorescent immunochromatography
3 結 論
選取AIE 熒光染料QM-OH,通過簡單的溶脹包埋方法,得到了能夠用于熒光免疫層析的AIE 熒光微球QM-OH@PS-COOH。該AIE 熒光微球大小均一、形狀規整,其密度、固含量、羧基含量等與市售熒光微球基本一致,同時與SAA 抗體具有優異的偶聯效果,且穩定性好。該AIE熒光微球QM-OH@PSCOOH 作為熒光免疫層析中的主要載體,能夠有效區分臨床樣本中SAA 的陰性和陽性樣本,不僅可以肉眼定性判斷,還可以對SAA 定量分析得到準確數值,具有潛在的應用價值。
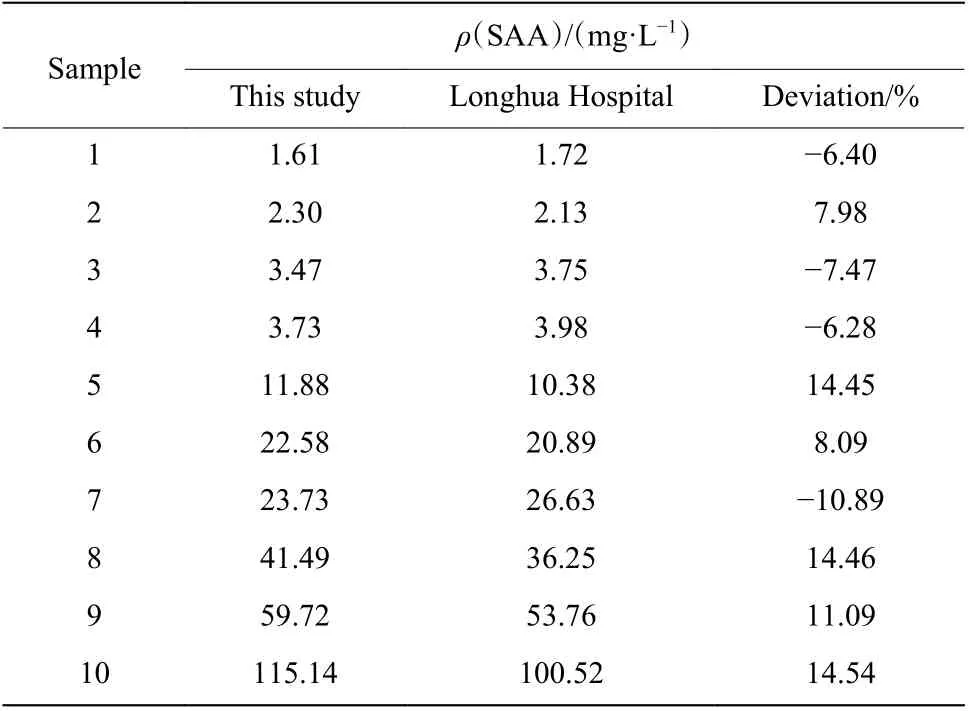
表2 本文和龍華醫院臨床測試樣本SAA 測值比較Table 2 Comparation of SAA value between this study and Longhua Hospital

圖5 SAA 質控品定標的曲線Fig. 5 Calibration curve of SAA quality control product

圖6 MAYA 熒光免疫定量分析儀(a);日光燈下陰性、陽性低值、陽性高值樣本的檢測條(b);熒光燈下陰性、陽性低值、陽性高值樣本的檢測條(c)Fig. 6 MAYA fluorescence immunoquantitative analyzer(a); Test strips for negative, low positive and high positive samples under daylight lamps(b); Test strips for negative, low positive and high positive samples under fluorescent lamps(c)

