電氧化法制備APT的新工藝研究
馬鑫銘,張正陽,楊永強
(礦冶科技集團有限公司,北京 100160)
仲鎢酸銨(APT)是鎢冶金及鎢化工領域的重要中間產品,絕大部分鎢冶金的終端產品需要通過APT來制取,如硬質合金、金屬鎢材、偏鎢酸銨等。因此,從鎢酸銨溶液中結晶制備APT是鎢冶煉過程中重要的工序之一。
現在工業上應用的APT制備工藝有蒸發結晶法、酸中和法和冷凍結晶法。蒸發結晶法是現在工業應用的主流工藝,該工藝利用高溫(工業上一般為90~100 ℃)下氨氣(NH)易揮發的性質,脫除溶液中的氨氣從而降低鎢酸銨溶液的pH。當鎢酸銨溶液pH為8.5時,仲鎢酸根迅速生成,仲鎢酸根聚合并且和銨根離子結合形成APT沉淀。蒸發結晶法工藝及設備簡單,易實現大型化,同時還有一定的提純作用。但是,蒸發結晶需要鼓入大量熱氣將氨氮吹脫成氨氣帶離溶液,因此其效率較低且能耗高,同時吹脫的氨氣容易造成污染且回收處理成本較高。酸中和法也是生產APT的重要方法,該工藝的原理是:將鹽酸加入鎢酸銨溶液進行中和,控制溶液pH在7.0~7.5,靜置一段時間,溶液中的(NH)WO轉化為APT沉淀析出。酸中和法具有工藝簡單、產品粒度易于控制的優點,但是需要加入鹽酸,相應地帶入HCl中所含的雜質,故生產的APT純度較低。冷凍結晶法先用液氮將鎢酸銨溶液全部迅速冷凍,然后在真空條件下適當升高溫度(不能導致解凍),使其中的HO、NH升華,最終得到仲鎢酸銨粉末。冷凍結晶法固化時間極短,因此不發生偏析現象,生產的APT粒度較細且成分均勻,可以用于制備超細鎢粉。但是,冷凍結晶法的缺點顯而易見,制備過程用到液氮,因此成本較高,且制備的APT中雜質含量較多。因此,開發一種既不影響鎢結晶又能解決氨氮問題的低能耗新工藝具有較大的研究價值。
鎢酸銨溶液可以看作一種含有氨氮與氯離子的溶液,其中含有一定濃度的氯離子。電氧化法電解制備APT,是利用電氧化產酸的原理使鎢酸銨溶液的pH降低,進而結晶析出APT。此方法既避免引入雜質離子,又可以去除鎢酸銨溶液中的氨氮(氨分子),避免因蒸發結晶而導致高能耗問題,實現鎢酸銨溶液結晶過程的高效清潔生產。本試驗擬從時間、氯離子濃度、電流密度、溫度和轉速等方面對鎢結晶進行研究。
1 試驗原料、設備裝置及操作方法
1.1 試劑及儀器
試驗使用的主要試劑及儀器如表1和表2所示。試劑主要有氯化銨、硫代硫酸鈉、酒石酸鉀鈉、氫氧化鉀、二氯化汞和碘化鉀,儀器主要有電子節能控溫儀、水浴鍋、可見分光光度計、電感耦合等離子體發射光譜儀(ICP-OES)和電熱恒溫干燥箱。

表1 主要試劑

表2 主要儀器
1.2 試驗裝置及操作方法
1.2.1 鎢酸銨溶液配制
首先,按照1.2∶1.0至1.5∶1.0(鎢酸∶水)的比例,將鎢酸加水調和成漿并加熱,使其保持在70~80 ℃。然后,將鎢酸加入劇烈攪拌的濃氨水中,在50 ℃的溫度下反應0.5 h。用布氏漏斗進行真空抽濾,得到濾液,然后將一定質量的氯化銨固體溶解在濾液中,配制成模擬鎢酸銨溶液。
1.2.2 電解
電解試驗裝置如圖1所示,取氨溶所得到的鎢酸銨溶液40 mL置于燒杯中,放入轉子并插入電極(陽極為Ti/RuO組成的尺寸穩定陽極,陰極為鈦片),然后將燒杯放入水浴鍋中并通過向內插置的水銀溫度計讀取溶液的真實溫度。首先打開水溫鍋進行加熱,燒杯內鎢酸銨溶液達到設定溫度值時,打開直流電源并控制電流恒定進行電解。隔一段時間用注射器(頂端接濾膜過濾器)吸取1 mL溶液,分析其鎢濃度,計算鎢的結晶率。試驗完畢關閉電源,用抽濾機進行真空抽濾。
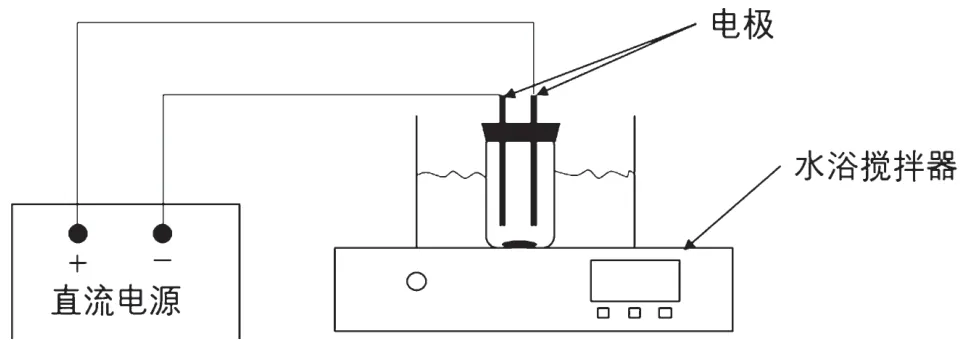
圖1 純鎢化合物制備試驗裝置
1.3 分析方法
采用納氏試劑比色法測定氨氮,采用電感耦合等離子體光譜儀(ICP)測定鎢含量。
2 試驗結果與討論
2.1 時間對鎢結晶的影響

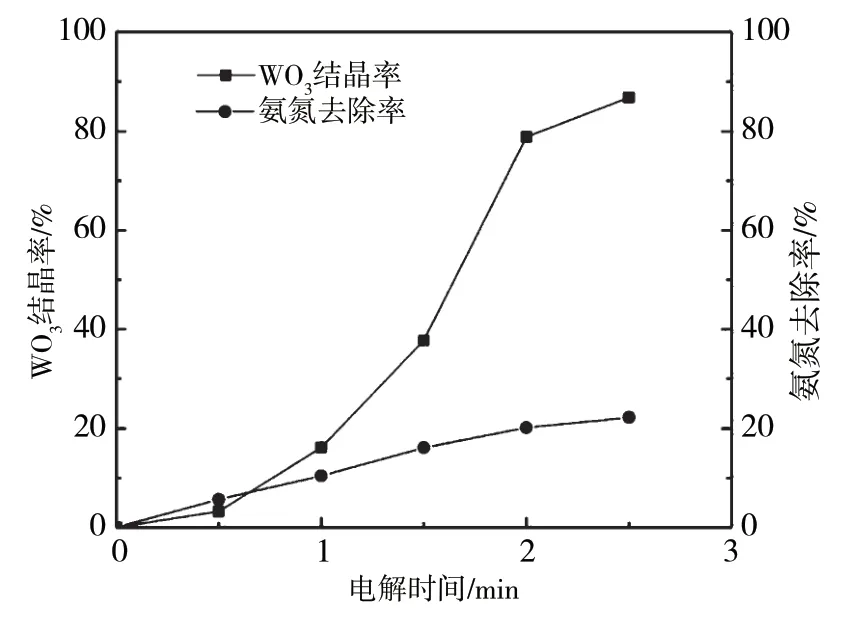
圖2 反應時間對鎢結晶和氨氮降解的影響
從氨氮脫除率變化趨勢可以看出,當電解時間為0~2 h時,隨著反應時間的延長,氨氮脫除率以較快的趨勢上升,但是電解時間超過2 h后,氨氮脫除率逐漸減緩。研究發現,pH對電化學氧化降解氨氮的效果影響較大,反應開始時,鎢酸銨溶液pH較高,通過電氧化的作用,氨氮在氧化脫除過程將產生活性氯,使溶液pH不斷下降,從而導致電化學氧化氨氮的速率降低。當電解時間為0.5~2.0 h時,pH下降雖然能夠導致電化學氧化氨氮的速率下降,但同時也促進了鎢酸銨溶液的中和結晶,使其析出仲鎢酸銨沉淀,所以氨氮氧化速率基本不變。當電解時間超過2 h后,氨氮脫除速率明顯變緩。
2.2 水溫對鎢結晶的影響
在反應時間為2.5 h、電流為1.5 A、氯離子濃度為1 mol/L、轉速為400 r/min的條件下,考察了不同溫度對鎢結晶的影響,試驗結果如圖3所示。從圖3可以看出,反應溫度為10~40 ℃時,隨著溫度的升高,鎢的結晶率有所提高,原因可能是反應溫度升高導致溶液中游離氨分子揮發成氨氣的速率加快,溶液pH下降速率加快,促進了晶粒的形成與長大。這說明在此溫度范圍內溫度對鎢結晶及氨氮脫除的影響較小。然而,溫度從20 ℃升高至40 ℃,鎢的結晶率只提高6%,提升幅度較小。升高溫度會加劇反應能耗,因此反應在常溫下進行即可。
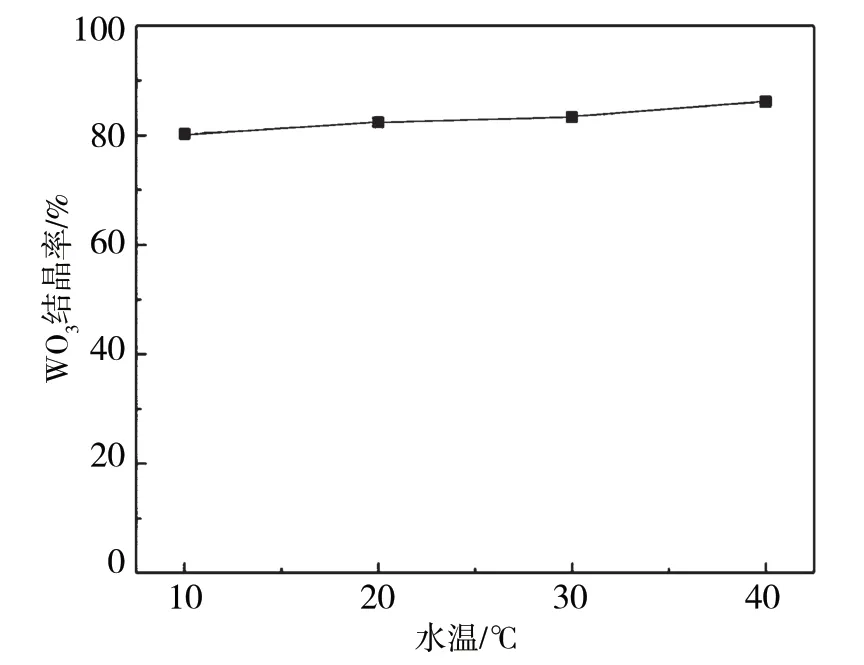
圖3 水溫對鎢結晶的影響
2.3 轉速對鎢結晶的影響
在反應時間為2.5 h、水溫為30 ℃、電流為1.5 A、氯離子濃度為1 mol/L的條件下,考察了不同轉速條件對鎢結晶的影響,試驗結果如圖4所示。
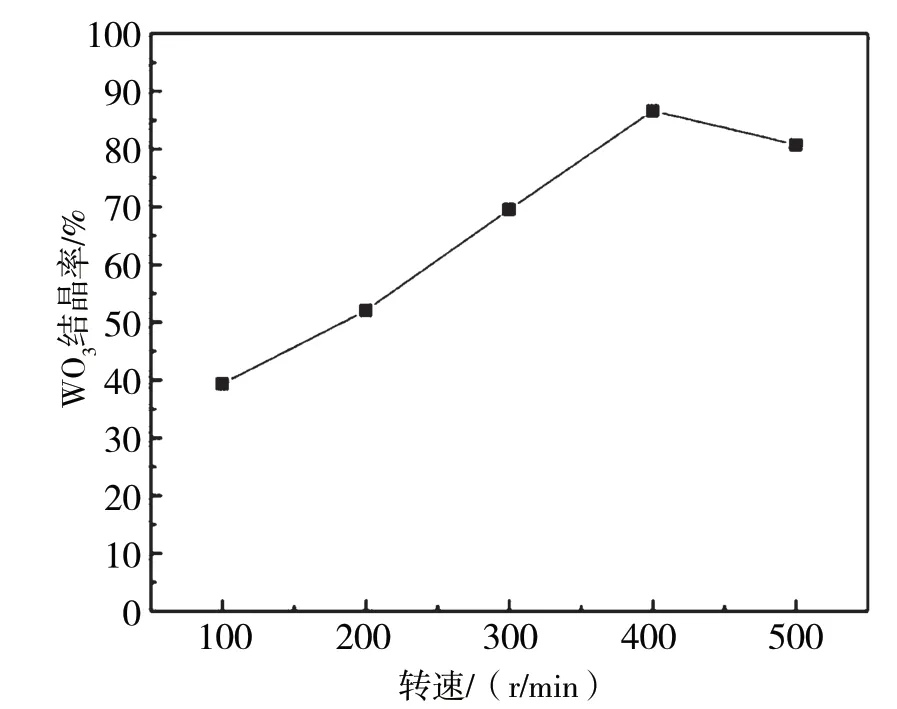
圖4 轉速對鎢結晶的影響
從圖4可以看出,在轉速為100~400 r/min的條件下,鎢的結晶率隨轉速的提升而逐漸升高,轉速為400 r/min時,結晶率達到最高,為86.3%。繼續提高轉速至500 r/min,鎢的結晶率反而下降。經分析,在轉速較低的情況下,提高轉速可以使陽極產生的氯氣與鎢酸銨溶液充分混合,促進氯氣在水中溶解,也可以增加溶液的混合程度,在結晶過程中提升晶粒長大速度,所以鎢的結晶率有所提高,但是當轉速過快時,氯氣在溶液中的溶解率反而降低,一部分氯氣逸出,導致電流效率降低,鎢的結晶率有所下降。
2.4 電流對鎢結晶的影響
在反應時間為2.5 h、水溫為30 ℃、電流為1.5 A、氯離子濃度為1 mol/L的條件下,考察了電流對鎢結晶的影響,試驗結果如圖5所示。從圖5可以看出,在電流較低的情況下,鎢的結晶率隨電流的增大而增大,但總體維持在較低的水平。但是,當電流從1 A提升至1.5 A時,鎢的結晶率有了明顯提升,從20%增長到85%。之后繼續提高電流,鎢的結晶率變化不大,維持在86%左右。這可能是因為在電流較低的情況下,施加在電極的電壓偏低,鎢酸銨溶液pH又較高,所以導致陽極的副反應析氧反應作用較強,溶液pH下降緩慢導致鎢的結晶率不高。當電流增大至一定程度時,陽極的析氯反應占據主導地位,因此鎢的結晶率有了顯著提高。當電流進一步提高時,反應速度有所加快,但是對鎢的結晶率影響不大。電流過大時,試驗觀察到陽極表面吸附有白色與黃色固體。經分析,電流增大可能導致電極表面電流密度增大,陽極附近活性氯濃度過高,APT結晶并吸附在陽極上轉化為鎢酸,或者是鎢酸根直接在陽極表面與H結合為鎢酸析出。綜合分析后,選用1.5 A作為試驗電流。
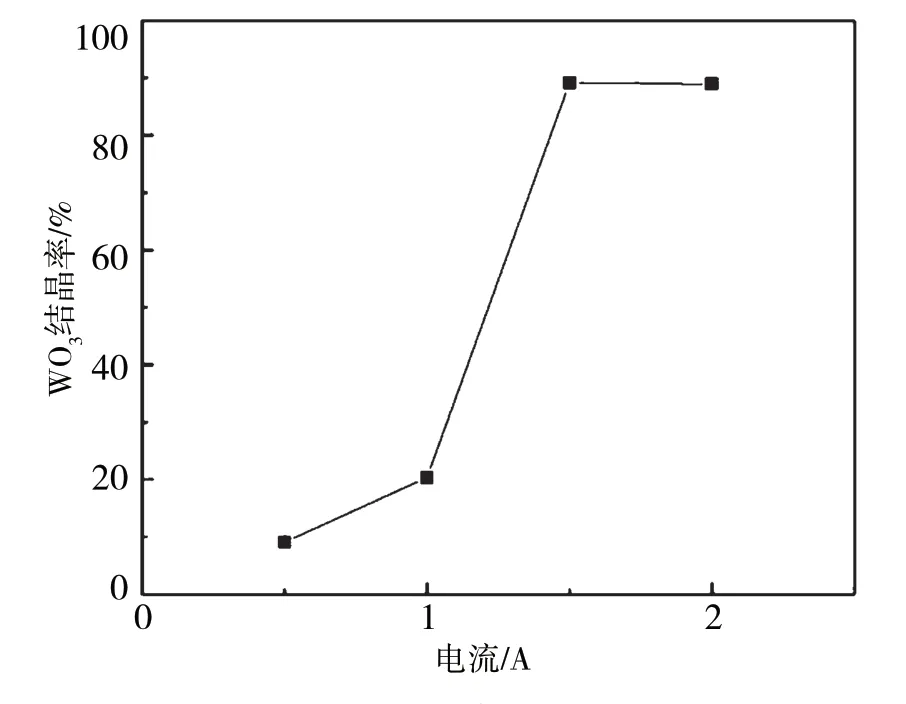
圖5 電流對鎢結晶的影響
從圖6可以看出,隨著電流的增大,結晶產物中(NH)(HWO)(HO)衍射峰強度增大,電流提高至1.5 A后,衍射峰強度更是提升明顯。但是,觀察發現,這時也出現許多雜峰,結合結晶產物由白色逐漸變為黃色的試驗現象可以推測,當電解反應進行時,一部分(NH)(HWO)(HO)與H反應生成無定形的鎢酸沉淀或者是鎢酸根直接與H結合形成鎢酸。
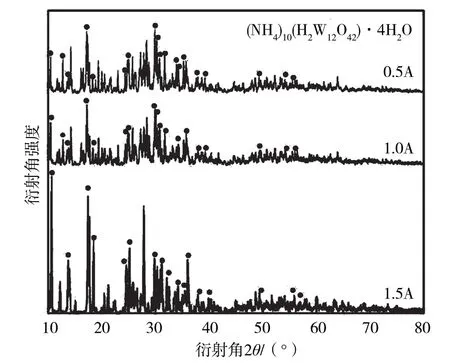
圖6 不同電流條件下鎢結晶產物的X射線衍射(XRD)光譜圖
2.5 氯離子濃度對鎢結晶的影響
在反應時間為2.5 h、水溫為30 ℃、轉速為400 r/min、電流為1.5 A的條件下,考察了氯離子濃度對鎢結晶的影響,試驗結果如圖7所示。從圖7可以看出,在溶液中沒有氯離子存在的情況下,鎢的結晶率為0%,這是因為電氧化過程中只有氯離子存在的間接氧化才能產生氯氣,從而降低鎢酸銨溶液的pH,析出APT。從圖7可以看出,當氯離子濃度為0~1 mol/L時,隨著氯離子濃度的增大,鎢的結晶率升高。這是因為氯離子濃度增大能夠顯著提高電化學氧化過程的活性氯濃度,使得pH下降速率增大,所以電解2.5 h后有了較高的結晶率。當氯離子濃度超過1 mol/L時,反應速率提升不大,因此鎢的結晶率基本不變。
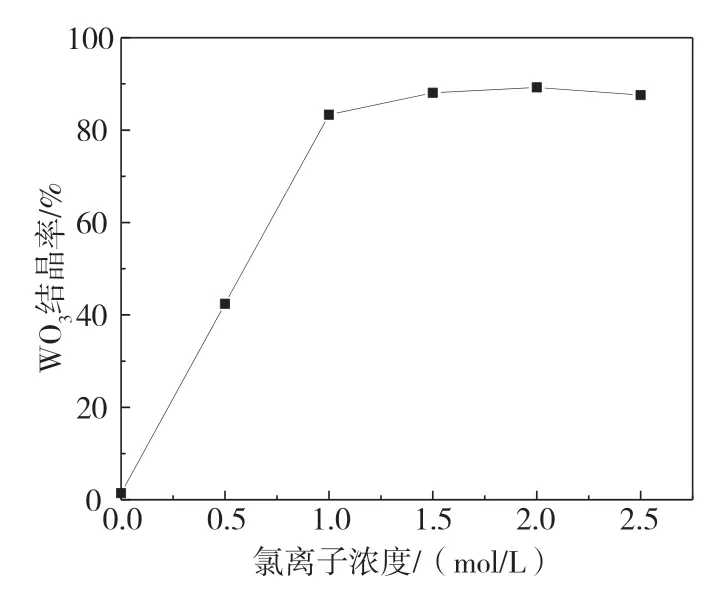
圖7 氯離子濃度對鎢結晶的影響
3 結論
基于電化學氧化產酸原理,將蒸發結晶過程改為電化學氧化酸化結晶過程,取得較好效果。隨著反應時間的延長,鎢的結晶率和氨氮的去除率均呈上升趨勢。在一定范圍內,提高反應的轉速能夠提升鎢的結晶率,但是當轉速超過400 r/min時,提高轉速反而降低了鎢的結晶率。在10~40 ℃的溫度范圍內,溫度升高能提高鎢的結晶率,但是提升幅度較小。在一定范圍內,隨著電流的增大與氯離子濃度的提高,鎢的結晶率逐漸上升,但是當電流超過2 A,氯離子濃度超過1 mol/L時,鎢的結晶率變化不大。電化學氧化結晶過程鎢的結晶率較高,控制反應條件可得到結晶產物(NH)(HWO)(HO)或鎢酸。

