Lp-PLA2、hs-CRP與急性腦梗死及動脈粥樣硬化的相關性
郭繼強 丁興龍 徐金格
(徐州醫科大學第二附屬醫院(徐州礦務集團總醫院)檢驗科,江蘇 徐州 221006)
急性腦梗死(ACI)是一種常見腦血管疾病,嚴重危害人類生命健康,其中大動脈粥樣硬化(LAA)型ACI是其重要分型之一,動脈粥樣硬化(AS)為主要發病機制〔1,2〕。近年來隨著人們對AS研究的進一步深入,對于炎癥參與AS形成已達成廣泛共識〔3,4〕。脂蛋白相關磷脂酶(Lp-PL)A2是一種主要經巨噬細胞與中性粒細胞分泌的新型炎癥介質,超敏C反應蛋白(hs-CRP)是反映機體炎癥反應的敏感指標,二者均為誘發AS的重要危險因素〔5,6〕。目前對于血清Lp-PLA2、hs-CRP水平在腦血管疾病中的臨床意義及其與ACI的相關性還存在很多爭議。本研究旨在探討血清Lp-PLA2、hs-CRP與ACI及AS的相關性。
1 材料與方法
1.1一般資料 選取2019年1月至2020年12月在徐州醫學院第二附屬醫院神經內科住院治療的ACI患者126例。納入標準:①符合《中國急性缺血性腦卒中診治指南2014》有關ACI的診斷標準〔7〕并經頭顱CT或磁共振成像(MRI)確診;②初次發病且發病至就診時間<72 h,入院后3 d內行頸動脈超聲檢查;③未合并腦損傷、腦炎、腦部腫瘤等腦部疾病。排除標準:①出血性或混合型腦卒中;②心源性腦梗死者;③合并急性心血管疾病、重癥腦梗死、腦動靜脈畸形或顱內腫瘤者;④近期正使用或曾使用可能影響Lp-PLA2、hs-CRP水平的相關藥物者;⑤合并嚴重心、肝、腎功能不全、血液疾病或有精神病史者。同期入院60例體檢健康人群作為對照,兩組性別、年齡、體重指數(BMI)、高血壓史、糖尿病史差異無統計學意義(P>0.05),見表1。納入患者均簽署知情同意書,研究經醫院倫理委員會審核同意。
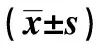
表1 兩組一般資料比較
1.2分組方法 依據美國國立衛生研究院腦卒中量表(NIHSS)評分將ACI患者分為輕度(NIHISS評分<4分)、中度(NIHISS評分為4~22分)和重度神經功能缺損(NIHISS評分為≥23分)3組,行頸動脈超聲檢查并依據頸動脈斑塊位置、形態及回聲特點分為無斑塊、穩定斑塊和不穩定斑塊3組〔8〕。按照中國缺血性腦卒中亞型分型(CISS)將126例ACI患者分為LAA組90例、非LAA組36例,LAA組男52例,女38例,年齡52~78歲,平均(64.11±7.83)歲,BMI為(23.91±2.37)kg/m2,高血壓史35例,糖尿病史23例。非LAA組男23例,女13例,年齡53~75歲,平均(63.29±7.54)歲,BMI為(23.52±2.29)kg/m2,高血壓史27例,糖尿病史17例。LAA組、非LAA組和對照組基本資料差異均無統計學意義(P>0.05)。
1.3標本采集及測定 ACI患者均于入院次日(對照組于體檢當日)清晨空腹下抽取靜脈血4 ml,2 500 r/min離心10 min,離心半徑12 cm,然后分離血清,置于4℃冰箱待檢。采用免疫比濁法測定血清Lp-PLA2、hs-CRP水平,所用儀器為美國雅培AEROSET型全自動生化分析儀,檢測試劑及配套質控品均來自北京九強生物技術有限公司,批號:2018092601,2019020702,均嚴格按試劑盒說明書操作。
1.4統計學方法 采用SPSS20.0統計學軟件進行t檢驗、秩和檢驗、F檢驗、χ2檢驗及Spearman相關性分析。
2 結 果
2.1ACI組與對照組Lp-PLA2、hs-CRP水平比較 ACI組血清Lp-PLA2、hs-CRP水平〔(243.60±57.81)、(8.14±2.59)mg/L〕均明顯高于對照組〔(122.70±44.63)、(1.24±0.33)mg/L;t=14.291、20.528,均P<0.001〕。
2.2不同神經功能缺損和斑塊性質ACI患者Lp-PLA2、hs-CRP水平比較 輕、中、重度神經功能缺損患者Lp-PLA2、hs-CRP水平差異均有統計學意義(P<0.001),重度組明顯高于輕、中度組(P<0.05),中度組明顯高于輕度組(P<0.05)。不同斑塊性質患者血清Lp-PLA2、hs-CRP水平比較差異均有統計學意義(P<0.001),不穩定斑塊組明顯高于無斑塊組、穩定斑塊組(P<0.05),穩定斑塊組明顯高于無斑塊組(P<0.05),見表2、表3。
2.33組Lp-PLA2、hs-CRP水平比較 LAA組血清Lp-PLA2水平〔(251.72±59.90)mg/L〕明顯高于非LAA組〔(189.44±49.52)mg/L〕與對照組(P<0.05),非LAA組明顯高于對照組(P<0.05)。LAA組、非LAA組血清hs-CRP水平〔(8.56±2.70)、(7.84±2.32)mg/L〕明顯高于對照組(P<0.05),LAA組、非LAA組差異無統計學意義(P>0.05)。
2.4相關性分析 ACI組Lp-PLA2、hs-CRP水平均與神經功能缺損程度(r=0.911、0.864,均P<0.001)、頸動脈斑塊性質呈正相關(r=0.752、0.699,均P<0.001)。

表2 不同神經功能缺損程度患者Lp-PLA2、hs-CRP水平比較

表3 不同斑塊性質患者Lp-PLA2、hs-CRP水平比較
3 討 論
ACI是因腦AS及血栓形成造成血管管腔狹窄或阻塞,進而致腦供血不足或中斷而引發腦組織壞死及神經功能受損的一類腦血管疾病,具有發病急驟、致殘率和病死率高等特點,及早進行診治對于改善預后至關重要〔9〕。AS是一種常見慢性炎癥性疾病,隨著年齡增長AS發病率亦呈增長趨勢,主要有動脈管壁增厚、硬化及失去彈性、血管內膜下粥樣斑塊形成或破裂。血管管腔狹窄或閉塞等病理表現,嚴重影響動脈供血功能,并誘發動脈粥樣硬化性心血管疾病(ASCVD)〔10〕。ACI為ASCVD常見疾病之一,AS是其基礎病理改變〔11〕。現有研究證實,AS發生與機體內炎癥因子介導的相關炎癥反應關系密切〔12〕,因此ACI發生、發展可能與炎癥因子過表達、血脂代謝紊亂等因素有關。
Lp-PLA2是一種主要經巨噬細胞與中性粒細胞分泌的新型炎癥介質,可通過氧化型低密度脂蛋白(LDL)生成溶血磷脂酰膽堿,進而在炎癥反應中發揮重要作用,可損害血管正常保護機制受損并誘發頸AS〔13〕。C反應蛋白(CRP)是一種非特異性炎癥標志物,可通過誘導細胞因子釋放及黏附因子表達誘發內皮功能障礙,影響內皮細胞通透性,并可能參與斑塊發生、發展。hs-CRP與CRP為同一物質,是一種由肝細胞合成的非特異性急性期反應蛋白,一旦微生物入侵機體、遭受炎性刺激或出現組織損傷時肝細胞會大量釋放hs-CRP并進入人體血液〔14〕。本研究結果提示此類患者機體Lp-PLA2、hs-CRP水平均異常升高并可能參與了該病的病理生理過程,與既往研究〔15〕結論一致。Lp-PLA2可通過結合LDL分解氧化卵磷脂,促進炎癥介質與溶血卵磷脂生成,造成血管內皮細胞損傷、單核巨噬細胞浸潤、粥樣斑塊形成并影響其穩定性,增加缺血性腦卒中發生風險。hs-CRP能誘導炎癥與黏附因子并使其聚集于血管內皮層下,促進泡沫細胞生成,同時能通過激活炎癥通路促進細胞間質降解與血管平滑肌細胞凋亡,增加AS及斑塊破裂風險。
本研究還發現,ACI患者神經功能缺損程度越重、斑塊性質越不穩定,其Lp-PLA2、hs-CRP水平也越高,且相關性分析顯示上述指標與神經功能缺損程度、斑塊性質呈正相關,與郝澤林等〔8〕結論一致。提示血清Lp-PLA2、hs-CRP水平可能是預測ACI患者早期神經功能缺損和斑塊性質穩定性的重要生物學指標,在判斷ACI患者神經功能缺損程度、斑塊性質中發揮重要作用。其原因可能為:Lp-PLA2、hs-CRP等炎癥介質能通過激活補體系統、激發氧化應激反應、促使單核細胞朝巨噬細胞轉化和產生促凝血活性等作用機制促進血栓生成并發展,進而加大斑塊破裂、出血、脫落乃至栓塞等風險,導致腦血管管腔狹窄并誘發ACI。
LAA是缺血性腦卒中(IS)的重要病因及發病機制之一,腦血管狹窄、AS斑塊形成及其不穩定性是誘發缺血性腦卒中的重要原因,其中斑塊不穩定性的危害較血管狹窄更大〔16〕。炎癥反應是AS形成和發展的關鍵因素,與AS斑塊及其穩定性密切相關。本研究結果提示Lp-PLA2與ACI患者AS病理過程密切相關,可能發揮促進AS的作用,而hs-CRP可能與AS病理過程無顯著關系,該結論與既往報道基本一致。其機制在于,LDL在動脈壁內轉變為氧化型LDL時,Lp-PLA2水解氧化型LDL并生成氧化型游離脂肪酸與溶血卵磷脂等促炎介質,進而促使黏附因子、細胞因子生成,單核細胞大量聚集于內膜并轉變為巨噬細胞,通過吞噬氧化型LDL形成泡沫細胞,造成AS性斑塊聚集,大量釋放細胞因子與蛋白酶,影響斑塊穩定性,促使斑塊破裂,最終導致血栓形成并誘發心血管事件。
綜上,Lp-PLA2、hs-CRP與NIHSS評分、頸動脈斑塊性質相關,可能是預測ACI患者早期神經功能缺損和斑塊性質穩定性的重要生物學指標,高水平的Lp-PLA2、hs-CRP可能參與了腦梗死的發生及發展過程,對于預測疾病風險有重要意義;Lp-PLA2與AS病理過程密切相關,在ACI的診治過程中具有指導意義。

