血清TNF-α、IL-6、IL-8水平與老年高血壓性視網膜病變的相關性
楊秀麗 李爽樂 彭璟 曾洪波 劉利麗
(自貢市第一人民醫院眼科,四川 自貢 643000)
高血壓性視網膜病變(HRP)是高血壓患者常見并發癥之一,是因長期高動脈血壓導致的眼底血管結構和功能改變,可嚴重損傷患者視力〔1〕;另外,HRP也與腦卒中、冠心病等疾病密切相關,用于部分心腦血管疾病的風險預測〔2〕。老年因基礎疾病較多、血壓更難控制等因素,HRP發病風險相對更高,病情也更重〔3〕,因此,對老年患者進行HRP篩查具有重要臨床意義。目前,HRP病因病機尚不完全明晰,近年來有研究認為慢性炎癥可能參與HRP的發生〔4〕。腫瘤壞死因子(TNF)-α、白細胞介素(IL)-6、IL-8是常見的炎癥因子指標,臨床獲取便捷,已被證實參與糖尿病視網膜病變(DR)、增生性玻璃體視網膜病變(PVR)等多種眼科疾病的發生發展〔5,6〕。本研究旨在探究血清TNF-α、IL-6、IL-8水平與老年HRP的相關性。
1 對象與方法
1.1研究對象 本研究為前瞻性研究,所有入組患者知情、同意且自愿參與研究。選取2020年5月至2021年10月自貢市第一人民醫院收治的96例老年高血壓患者。納入標準:(1)確診為原發性高血壓〔7〕;(2)完成眼底檢查;(3)各項生理病理資料清晰完整。排除標準:(1)繼發性高血壓;(2)伴嚴重肺腎功能不全、糖尿病或急慢性感染、心腦血管意外等急性并發癥;(3)合并白內障、青光眼等其他眼科疾病者。
1.2診斷標準與分組 HRP診斷標準〔8〕:(1)有高血壓病史;(2)經45°眼底數碼照相檢查明確存在視網膜動脈管壁、管徑及血管滲透性改變等導致的視網膜滲出、出血、視盤水腫等;(3)排除DR、視盤神經炎、視網膜中央靜脈阻塞、前部缺血性視神經病變、顱內壓增高導致的視乳頭水腫等具有類似表現疾病。分組:根據是否合并HRP分為HRP組(n=43)和非HRP組(n=53)。另選取同期體檢的健康老年人群為對照組(n=40)。
1.3觀察指標與檢測方法 (1)一般資料:包括性別、年齡、吸煙飲酒情況、體重指數(BMI)、高血壓病程、收縮壓(SBP)、舒張壓(DBP)等;(2)生化指標:包括空腹血糖(FPG)、糖化血紅蛋白(HbA1c)、總膽固醇(TC)、三酰甘油(TG)、低密度脂蛋白膽固醇(LDL-C)、高密度脂蛋白膽固醇(HDL-C)、TNF-α、IL-6、IL-8。其中,FPG用葡萄糖氧化酶法檢測,HbA1c用高效液相色譜法檢測,TC、TG、LDL-C、HDL-C用全自動生化分析儀(AU5800,Beckman Coulter)檢測,TNF-α、IL-6、IL-8用酶聯免疫吸附試驗(ELISA)檢測,試劑盒為R&D Systems公司產品,血樣均為空腹外周靜脈血。
1.4統計學方法 采用SPSS23.0軟件進行t檢驗、F檢驗、χ2檢驗及Logistic回歸分析;采用受試者工作特征(ROC)曲線評價血清TNF-α、IL-6、IL-8對HRP的診斷價值。
2 結 果
2.13組一般資料比較 HRP組高血壓病程明顯長于非HRP組(P<0.05);HRP組和非HRP組SBP、DBP明顯高于對照組(P<0.05);但HRP組和非HRP組SBP、DBP比較差異無統計學意義(P>0.05)。見表1。
2.23組生化指標比較 HRP組和非HRP組血清TNF-α、IL-6、IL-8水平明顯高于對照組(P<0.05);且HRP組均明顯高于非HRP組(P<0.05)。3組FPG、HbA1c及血清TC、TG、LDL-C、HDL-C水平差異均無統計學意義(P>0.05)。見表2。
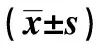
表1 3組一般資料比較
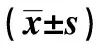
表2 3組生化指標比較
2.3Logistic多因素回歸分析 以高血壓患者是否合并HRP為因變量,以單因素分析中有統計學意義的指標為自變量,行Logistic回歸分析結果顯示,高血壓病程、TNF-α、IL-6、IL-8均是HRP發生的獨立影響因素(P<0.05)。見表3。
2.4血清TNF-α、IL-6、IL-8對HRP的診斷價值 ROC曲線分析顯示,血清TNF-α、IL-6、IL-8診斷HRP的曲線下面積(AUC)分別為0.682、0.779、0.691;且以三者聯合的AUC最大。見表4、圖1。

表3 影響HRP的Logistic多因素回歸分析

表4 血清TNF-α、IL-6、IL-8對HRP的診斷價值

圖1 血清TNF-α、IL-6、IL-8診斷HRP的ROC曲線
3 討 論
HRP在高血壓群體中具有較高的發病率,可對患者視力造成難以逆轉的損傷〔9〕。高血壓引起的視網膜動脈硬化、管徑狹窄及靜脈阻塞等微血管損傷是HRP的主要病理基礎,近年有學者發現多種炎癥因子也可能參與其中,HRP也可看作是炎性疾病的一種〔10〕。
TNF-α為促炎因子,可趨化和聚集炎癥細胞,導致血管通透性增加而損傷血-視網膜屏障〔11〕。Liu等〔12〕研究發現,重度子癇前期患者的視網膜中TNF-α的表達明顯增加,提示TNF-α可能在子癇前期引起的眼底病變中具有重要作用。TNF-α也可作為一種促血管生成因子提高血管內皮生長因子(VEGF)的表達促進視網膜微血管新生或增厚〔13〕;另外,TNF-α也可通過激活死亡受體通路來誘導細胞凋亡,進而加重視網膜損傷〔14〕。本研究結果提示TNF-α參與了HRP的發生發展。
IL-6可由多種細胞分泌,其生物功能復雜多樣。研究發現,IL-6不僅可通過激活T細胞、促進B細胞分化、提高急性期蛋白和免疫球蛋白的分泌、擾亂氧化-抗氧化平衡等多種途徑協助炎癥反應、氧化應激反應,損傷血管內皮細胞〔15〕;還可通過促進血管緊張素受體基因的表達來刺激血管收縮,引起內皮細胞障礙,增加細胞間通透性〔16〕。基礎實驗發現,IL-6可促進視網膜色素上皮(RPE)細胞的增殖,抑制IL-6的分泌可有效緩解這一作用〔17〕。有研究也提示,IL-6可能通過參與炎癥反應、誘導血管新生、提高內皮細胞通透性等多種途徑來促進及加重糖尿病患者的DR病情〔18〕。本研究結果提示IL-6與HRP的發生發展關系密切。
IL-8是重要的趨化因子及炎癥反應標志物,與高血壓患者的病情進展、轉歸等聯系緊密〔19〕。研究發現,中性粒細胞、單核細胞、巨噬細胞等多種炎癥細胞可在TNF-α的刺激下釋放IL-8,參與患者全身炎癥狀態的維持,且IL-8將進一步刺激RPE細胞進行增殖、移行,加重視網膜損傷〔20〕。季美霞等〔21〕研究也發現,IL-8與DR患者的VEGF水平呈正相關,作為炎癥因子和促血管新生因子參與了DR的進展。本研究結果顯示,IL-8是HRP發生的獨立影響因素,原因可能是IL-8在HRP的發生發展中不僅可通過趨化炎癥細胞破壞血-視網膜屏障、加重炎癥損傷,還可促進細胞黏附分子和貯存酶的釋放,激起呼吸爆發,大量生成的活性氧代謝產物將加重氧化應激損傷、引起細胞浸潤等,最終損傷視網膜微血管〔22〕。
綜上,血清TNF-α、IL-6、IL-8均與HRP的發生發展關系密切,是HRP發生的獨立影響因素,三者聯合用于HRP診斷中具有較高的診斷效能。臨床在診療高血壓患者時應密切關注患者的血清炎癥因子水平,叮囑高風險患者定期進行眼底檢查,發揮其診斷、病情監測的積極作用,盡可能改善患者預后。

