土壤中三價銻的老化對秀麗隱桿線蟲毒性的影響
宋子杰,趙 龍,黨秀麗,侯 紅,蔡世鑫,王京原
1. 中國環境科學研究院,環境基準與風險評估國家重點實驗室,北京 100012
2. 沈陽農業大學土地與環境學院,農業農村部東北耕地保育重點實驗室,土肥高效利用國家工程研究中心,遼寧 沈陽 110866
作為類金屬元素,銻(Sb)在阻燃、鉛合金、對苯二甲酸二甲酯生產等領域得到了廣泛應用[1-2]. 未受污染的天然土壤中,Sb 以相對較低的濃度(0.3~8.6 mg/kg)存在[3]. 然而,隨著采礦冶煉作業、化石燃料燃燒、含Sb 產品生產應用等一系列人類活動的開展,土壤環境中的Sb 濃度急劇上升[4]. Sb 不具備生物學功能且對生物體具有毒害作用,被美國環境保護局視為優先污染物[5-6]. 中國作為世界Sb 儲量最大的國家(占全球78%的Sb 產能)[7],土壤Sb 污染形勢尤為嚴峻. 莫昌琍等[8]在湖南省錫礦山冶煉廠周邊調查發現,土壤中Sb 平均含量高達6 070.08 mg/kg.
土壤Sb 污染引起了國內外研究者的關注,并陸續開展了一系列Sb 的生態毒性研究. 林祥龍等[9]研究土壤外源Sb(Ⅲ)對白符跳的毒性,結果顯示,經過7 d 老化的北京潮土中外源Sb(Ⅲ)對白符跳慢性致死毒性的LC50(50%致死濃度)值和慢性繁殖毒性的EC50(50%效應濃度)值分別為703 和307 mg/kg. Lin等[10]研究表明,經Sb(Ⅲ)處理后老化1 d 的黑龍江黑土和重慶紫土對大麥根伸長毒性的EC50值分別為5 561 和5 958 mg/kg. 多數Sb 毒性研究沒有考慮長時間老化對土壤中外源Sb(Ⅲ)毒性的影響. 林蕾等[11]研究發現,隨著老化時間的推移,Zn 對小白菜的生長毒性和有效態Zn 濃度均呈下降趨勢. Lock 等[12]研究指出,利用未經老化處理的重金屬污染物進行生物毒性測試會在一定程度上高估土壤中重金屬的毒性. 三價銻〔Sb(Ⅲ)〕和五價銻〔Sb(Ⅴ)〕是土壤中Sb 的主要氧化態[6],已有研究[13]指出,Sb(Ⅲ)的生物毒性高于Sb(Ⅴ),但土壤環境中的Sb 以Sb(Ⅴ)為主. 如果不充分考慮Sb(Ⅲ)進入土壤環境后的價態變化會誤判其對生物的真實毒性. 此外,土壤性質對重金屬的毒性和老化過程同樣存在影響. 何飛等[14]研究指出,土壤有機質、全氮、陽離子交換量、鐵、錳是影響外源Sb(Ⅲ)對甘藍根伸長毒性的主要因素. 孫碩等[15]研究發現,土壤性質的不同會導致重金屬老化過程的差異,EDTA 提取態Pb 濃度與土壤pH 和電導率均具有極顯著的相關性.
得益于短生命周期和易培養的優勢,模式生物秀麗隱桿線蟲(Caenorhabditis elegans)被廣泛應用于生物毒性測試. H?ss 等[16]對22 種具有不同性質和污染模式的土壤以及9 種無污染的參考土壤進行了基于ISO 10872 指南的線蟲毒性測試,結果表明,該方法適用于測試土壤中污染物的毒性. Kim 等[17]研究顯示,土壤中Cd、Cu、Ni、Zn 濃度分別達637、429、744、669 mg/kg 時,線蟲的后代個體數量均降低50%,并指出基于ISO 10872 指南的毒性測試是評價土壤污染物毒性的一種簡單快速方法.
相較發達國家,我國土壤環境基準研究相對滯后[18],沒有充分考慮土壤污染物對不同生態受體的毒性[19]. 目前,圍繞土壤中Sb 對生物毒性的測試多以陸生植物、蚯蚓、跳蟲為受試生物[14,20-21],有關Sb 對土壤線蟲毒性的研究較為鮮見,從而導致研究基礎數據較為匱乏,不能較好地服務于土壤環境基準研究. 因此,該研究選用2 種性質的農田土壤(安徽黃棕壤和新疆灰漠土),以秀麗隱桿線蟲為受試生物,研究7和56 d 老化對土壤中外源Sb(Ⅲ)的價態變化、可提取態Sb 濃度以及對線蟲毒性的影響,探討不同土壤中外源Sb(Ⅲ)老化過程的差異,以期為我國土壤基準研究以及Sb 污染風險管控提供理論依據和數據支撐.
1 材料與方法
1.1 供試材料
1.1.1 供試試劑
該研究選用酒石酸銻鉀(C8H4K2O12Sb2·3H2O)作為外源Sb(Ⅲ)化合物,其為分析純(>99%)白色粉末狀固體顆粒,購自上海麥克林生化科技有限公司.
1.1.2 供試土壤
該研究選用的黃棕壤和灰漠土分別采集自安徽省宣城市(安徽黃棕壤)和新疆維吾爾自治區烏魯木齊市的農田表層(0~20 cm)(新疆灰漠土),土壤于自然條件下風干,過2 mm 尼龍篩網后備用. 土壤性質及測定方法如表1 所示.

表1 土壤性質及測定方法Table 1 Soil properties and determination methods
1.1.3 供試生物
該研究選用秀麗隱桿線蟲(Caenorhabditis elegansvar. Bristol,strain N2)和 大 腸 桿 菌(Escherichia coli,strain OP50)作為毒性測試生物和食物源,均購自福建上源生物科技有限公司.
1.2 試驗方法
1.2.1 土壤中外源Sb(Ⅲ)的添加和老化
土壤中外源Sb(Ⅲ)的添加通過噴灑酒石酸銻鉀溶液的方式進行,使土壤中的理論總Sb 濃度分別達400、800、1 600、3 200、6 400 mg/kg,對照組土壤中僅添加去離子水. 充分攪拌使土壤與酒石酸銻鉀溶液混勻,調節土壤含水量至田間持水量的55%~60%,裝入自封袋中進行老化并取土壤樣品測定實際總Sb 濃度,老化過程中通過稱重法補充去離子水以維持土壤含水量. 經過7 和56 d 的老化后,取土壤樣品測定不同價態Sb 和可提取態Sb 濃度,并進行土壤中外源Sb(Ⅲ)對線蟲毒性的測試.
1.2.2 線蟲毒性測試
1.2.2.1 線蟲的培養和同步化
食物源的培養:接種單克隆大腸桿菌菌株至LB培養基(稱取0.5 g 酪蛋白胨、0.5 g NaCl、0.25 g 酵母抽提物溶解于50 mL 去離子水中,121 ℃蒸汽滅菌后冷卻備用),振蕩培養(37 ℃,160 r/min)17 h 后,備用于線蟲的培養和毒性測試.
線蟲的培養:線蟲在20 ℃條件下生長于線蟲生長培養基(nematode growth-medium,NGM)瓊脂(稱取6.8 g 瓊脂粉、1.2 g NaCl、1.0 g 酪蛋白胨溶解于300 mL 去離子水中,121 ℃蒸汽滅菌后冷卻至55 ℃,加入0.4 mL 1 mol/L CaCl2溶液、0.4 mL 1 mol/L MgSO4溶液、10 mL 1 mol/L pH=6.0 的KH2PO4溶液和0.4 mL 5 g/L 的膽固醇乙醇溶液,用無菌水定容至400 mL 后,轉移15~20 mL 瓊脂至培養皿冷卻備用),通過更換接種有大腸桿菌的NGM 瓊脂以維持線蟲的生存.
線蟲的同步化:經過約72 h 的培養,NGM 瓊脂表面分布大量的線蟲幼蟲,用M9 培養基(稱取6 g Na2HPO4、5 g NaCl、3 g KH2PO4和0.25 g MgSO4·7H2O溶解于1 000 mL 去離子水后備用)將瓊脂表面的線蟲沖洗至管口布置有5 μm 尼龍篩網的離心管內,利用線蟲不同生長時期的體型差異過濾出同步的一齡期線蟲幼蟲,備用于線蟲毒性測試.
1.2.2.2 線蟲的毒性暴露和回收
根據ISO 10872 指南[26]和文獻[27]進行線蟲的毒性暴露和回收. 轉移0.5 g 的風干土壤樣品至培養板的測試孔中,添加100 μL 大腸桿菌菌液(15 mg/mL)與土壤樣品充分混合,并調節土壤含水量至田間持水量的80%,以滿足毒性暴露期間線蟲對食物和水分的需求. 通過毛細管向土壤樣品中添加10 條同步的一齡期線蟲幼蟲后密封培養板. 在20 ℃無光照條件下中進行96 h 的毒性暴露. 毒性暴露完成后,向培養板中添加500 μL 0.3 g/L 的虎紅(C20H2Cl4I4Na2O5)溶液以染色線蟲角質層,將培養板置于電熱鼓風干燥箱中,通過高溫(80 ℃)殺死線蟲以終止毒性測試. 通過液態氧化硅懸浮法將培養板中的線蟲回收于離心管內低溫(4 ℃)保存,備用于生長量、生育率、繁殖數的測定. 每個試驗處理設置3 次重復.
1.2.2.3 線蟲生長量、生育率和繁殖數的測定
將回收于離心管內的線蟲倒入培養皿中,在顯微鏡下完成線蟲軀體長度測量、生育能力檢查(線蟲軀體內至少有一顆蟲卵,則被認為具備生育能力)、個體數量計數后,計算線蟲的生長量、生育率、繁殖數.
生長量計算公式:
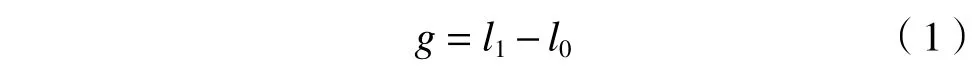
式中:g為 線蟲的生長量,μm;l1為毒性測試結束時的線蟲體長,μm;l0為毒性測試開始時的線蟲體長,μm.取30 條一齡期線蟲幼蟲體長的平均值作為毒性測試開始時的線蟲體長〔(274.2±7.5) μm〕.
生育率計算公式:
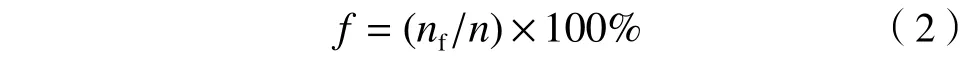
式中:f為線蟲生育率,%;nf為具備生育能力的線蟲數量,條;n為引入毒性測試的線蟲數量,條.
繁殖數計算公式:
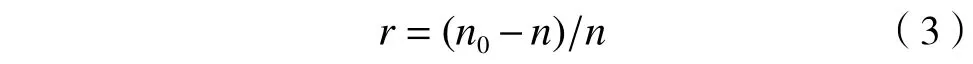
式中:r為線蟲繁殖數,條;n0為回收的線蟲數量,條.
1.2.3 土壤中Sb 濃度的測定
實際總Sb 濃度的測定參考Fan 等[24]研究,稱取0.1 g 風干的土壤樣品于消解管內,添加8 mL HF-HClO4-HNO3(三者體積比為3∶1∶1)混合液體,微波消解(180 ℃) 45 min 后趕酸,經過0.5% HNO3溶液適當稀釋后,利用電感耦合等離子體發射光譜儀(IRIS Advantage 型,Thermo Electron Corporation,美國)測定溶液中的Sb 濃度.
可提取態Sb 濃度的測定參考Ettler 等[28]研究,稱取1 g 風干的土壤樣品于離心管內,添加10 mL 1 mol/L Na2HPO4溶液,振蕩(25 ℃和200 r/min)2 h后離心(4 000 r/min)10 min,上層清液過0.45 μm 濾膜后,利用電感耦合等離子體質譜儀(Agilent 7500 型,安捷倫科技有限公司,美國)測定濾液中的Sb 濃度.
不同價態Sb 濃度的測定參考文獻[29],稱取0.5 g 風干土壤樣品于離心管內,添加5 mL 0.1 mol/L C6H8O7溶液,振蕩(60 ℃和200 r/min)30 min 后離心(4 000 r/min)10 min,上層清液過0.45 μm 濾膜后,通過原子熒光光度計(AFS-920,北京吉天儀器有限公司)測定濾液中的Sb(Ⅲ)和Sb(Ⅴ)濃度.
1.3 數據處理與分析
試驗數據的統計分析通過SPSS 22.0 軟件進行,土壤總Sb 濃度實測值與線蟲生長量、生育率、繁殖數間劑量效應方程的擬合以及毒性閾值(EC50值)的計算通過Sigmaplot 14.0 軟件進行,圖和表的繪制分別通過Origin Pro 2021 和Excel 2020 軟件進行.
2 結果與分析
2.1 老化過程中外源Sb(Ⅲ)的價態變化
由圖1 可見,安徽黃棕壤和新疆灰漠土中Sb(Ⅴ)在總Sb 的占比均隨Sb(Ⅲ)處理濃度的上升而降低. 經過7 d 的老化,各Sb(Ⅲ)處理濃度下新疆灰漠土中Sb(Ⅴ)的占比均高于安徽黃棕壤,在Sb(Ⅲ)處理濃度為800 和1 600 mg/kg 時達極顯著水平(P<0.01),在Sb(Ⅲ)處理濃度為6 400 mg/kg 時達顯著水平(P<0.05). 與7 d 老化相比,經過56 d 老化的安徽黃棕壤和新疆灰漠土中Sb(Ⅴ)的占比均出現極顯著提升(P<0.01). Sb(Ⅲ)處理濃度(400 和800 mg/kg)較低時,安徽黃棕壤和新疆灰漠土中的Sb 主要以Sb(Ⅴ)形態存在;Sb(Ⅲ)處理濃度為1 600、3 200、6 400 mg/kg 時,新疆灰漠土中Sb(Ⅴ)的占比顯著(P<0.05)或極顯著(P<0.01)高于安徽黃棕壤. 綜上,土壤中Sb(Ⅲ)的氧化效率與Sb(Ⅲ)的處理濃度、老化時間以及土壤性質有關.
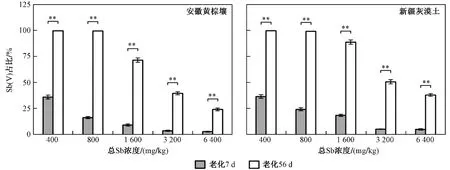
圖1 不同老化時間的安徽黃棕壤和新疆灰漠土中Sb(Ⅴ)占總Sb 比例Fig.1 Proportion of Sb(Ⅴ) in total Sb in Anhui yellow-brown soil and Xinjiang grey dessert soil with different aging time
2.2 老化過程中可提取態Sb 濃度的變化
由圖2 可見:整體而言,土壤可提取態Sb 濃度隨Sb(Ⅲ)處理濃度的提高呈上升趨勢. 經過7 d 的老化,新疆灰漠土中可提取態Sb 濃度顯著高于安徽黃棕壤(P<0.05). 經過56 d 的老化,經3 200 和6 400 mg/kg 處理的安徽黃棕壤中可提取態Sb 濃度分別出現顯著(P<0.05)和極顯著(P<0.01)的降低;經800 mg/kg 處理的新疆灰漠土中可提取態Sb 濃度出現顯著(P<0.05)的降低;Sb(Ⅲ)處理濃度為1 600、3 200 和6 400 mg/kg 時,新疆灰漠土中可提取態Sb 濃度出現極顯著(P<0.01)的降低,Sb(Ⅲ)處理濃度相同時新疆灰漠土中可提取態Sb 濃度仍高于安徽黃棕壤. 結果表明,土壤中可提取態Sb 的提取比例與老化時間及土壤性質有關.
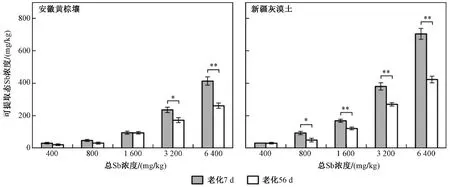
圖2 不同老化時間的安徽黃棕壤和新疆灰漠土中可提取態Sb 濃度Fig.2 Extracted Sb concentration in Anhui yellow-brown soil and Xinjiang grey dessert soil with different aging time
2.3 老化土壤中Sb 對線蟲的毒性
根據ISO 10872 指南中關于線蟲毒性測試的有效性標準進行毒性測試結果的檢驗. 由表2 可見,該研究的線蟲毒性測試結果符合有效性標準.
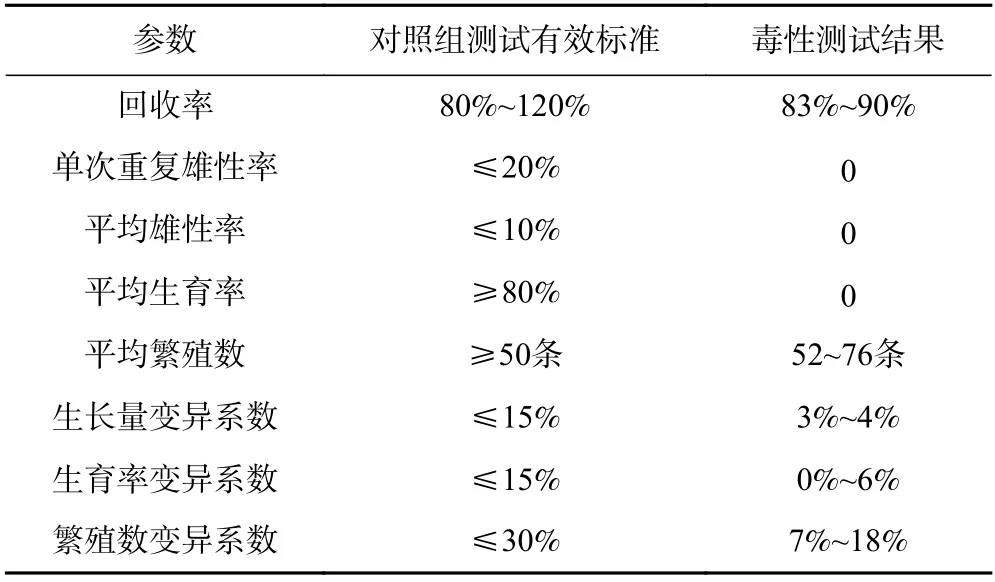
表2 毒性測試有效性Table 2 Validity of toxicity test
2.3.1 老化土壤中Sb 對線蟲的生長毒性
由圖3 可見:總Sb 濃度為6 400 mg/kg 時,經過7 d 老化的安徽黃棕壤和新疆灰漠土中線蟲的生長量均不足各對照組的10%;而老化56 d 時,線蟲的生長量分別為各對照組的41.2%和17.7%. 根據外源Sb(Ⅲ)對線蟲生長毒性的EC50值以及老化因子(見表3)可以發現,經過7 和56 d 老化處理的安徽黃棕壤中,外源Sb(Ⅲ)對線蟲的生長毒性低于新疆灰漠土,新疆灰漠土中外源Sb(Ⅲ)表現出更明顯的老化效應.
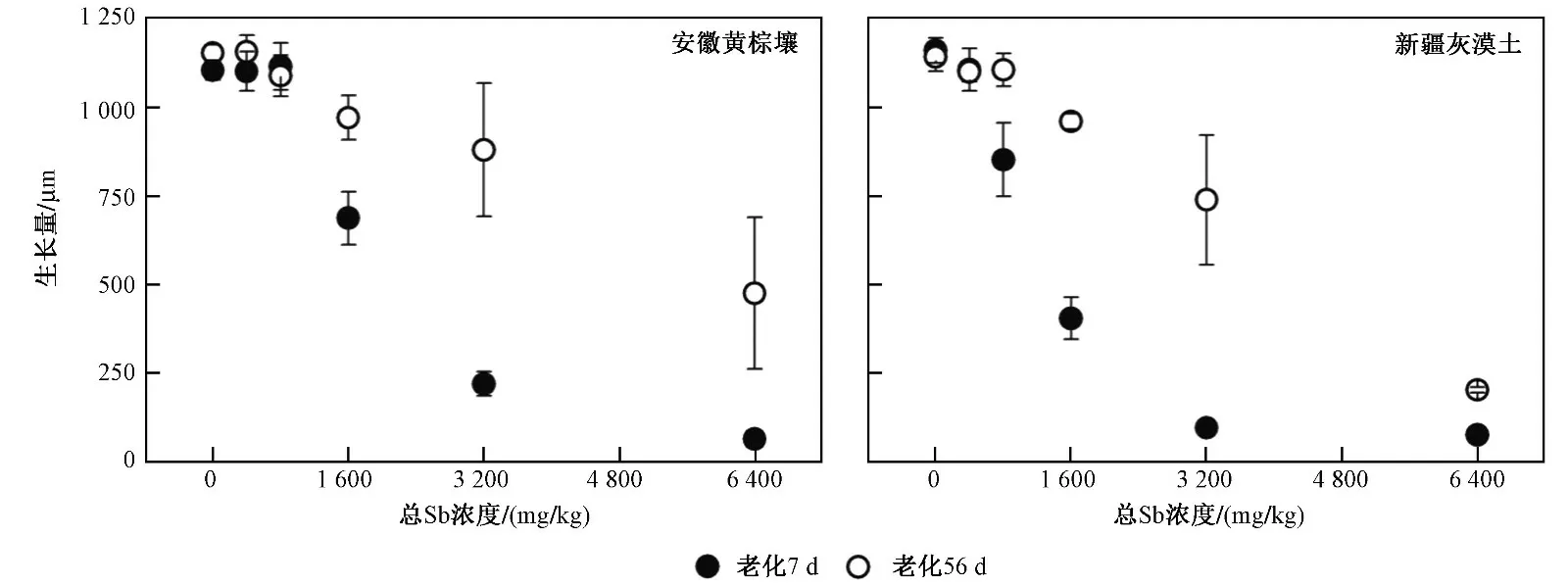
圖3 不同老化時間的安徽黃棕壤和新疆灰漠土中Sb 對線蟲的生長毒性Fig.3 Growth toxicity of Sb to C. elegans in Anhui yellow-brown soil and Xinjiang grey dessert soil with different aging time
2.3.2 老化土壤中Sb 對線蟲的生育毒性
由圖4 可見,經3 200 mg/kg Sb(Ⅲ)處理的安徽黃棕壤和新疆灰漠土老化7 d 后完全抑制了線蟲的生育能力,而經過56 d 的老化,線蟲的生育率分別為51.7%和46.7%. Sb(Ⅲ)處理濃度(6 400 mg/kg)最高時,2 種土壤中僅有16.7%和3.7%的線蟲具備生育能力. 由外源Sb(Ⅲ)對線蟲生育毒性的EC50值以及老化因子(見表3)可知,經Sb(Ⅲ)處理后老化7 和56 d 的新疆灰漠土均表現出對線蟲較高的生育毒性和較強的老化效應,外源Sb(Ⅲ)對線蟲生育毒性的閾值均低于其對生長毒性的閾值,毒性評價終點的敏感性差異整體表現為生育毒性高于生長毒性.

表3 土壤中Sb 對線蟲生長、生育、繁殖毒性的EC50 值及老化因子Table 3 EC50 values of Sb in soil and aging factors derived from the growth, fertility, and reproduction of C. elegans
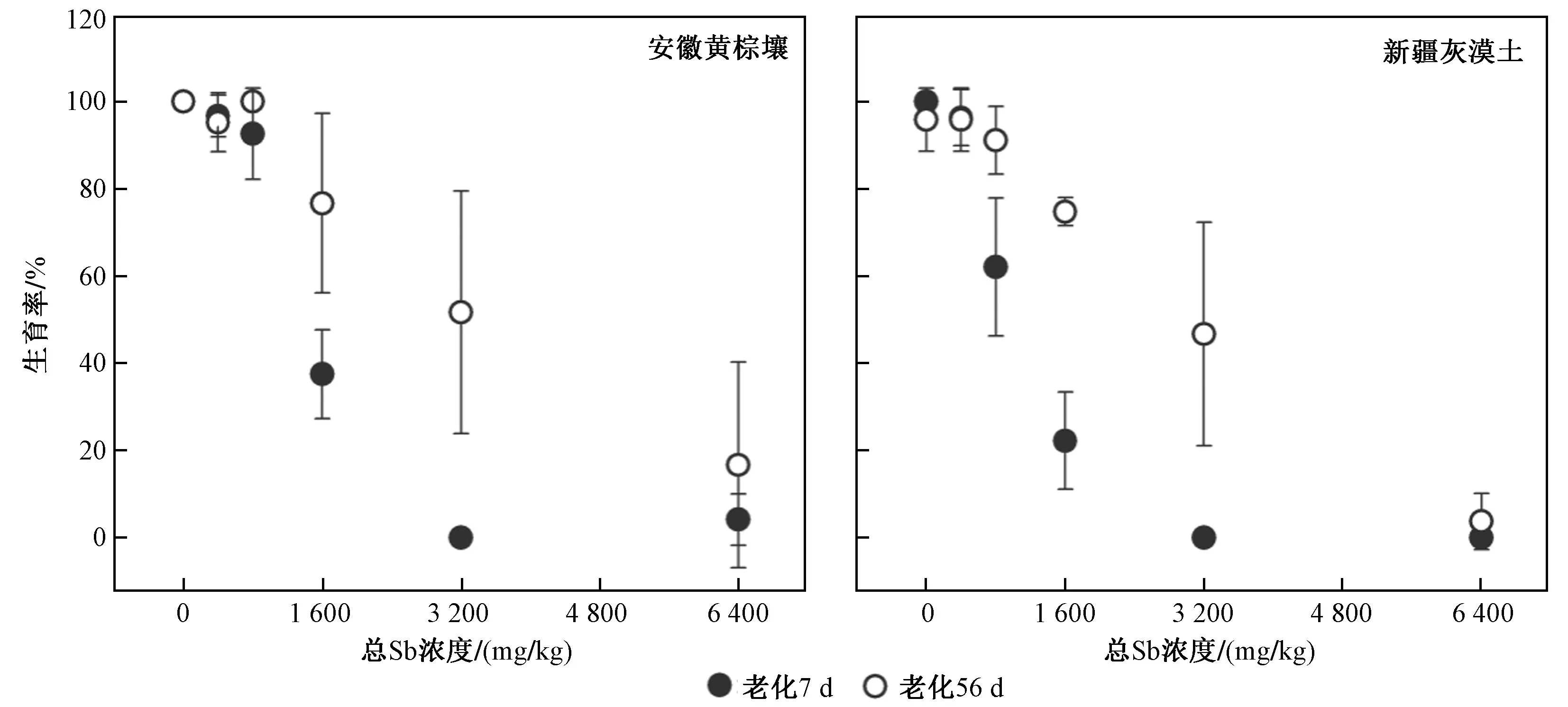
圖4 不同老化時間的安徽黃棕壤和新疆灰漠土中Sb 對線蟲的生育毒性Fig.4 Fertility toxicity of Sb to C. elegans in Anhui yellow-brown soil and Xinjiang grey dessert soil with different aging time
2.3.3 老化土壤中Sb 對線蟲的繁殖毒性
由圖5 可見,經1 600 mg/kg Sb(Ⅲ)處理的安徽黃棕壤和新疆灰漠土老化7 d 后線蟲的繁殖均受到顯著抑制(P<0.05),經3 200 mg/kg Sb(Ⅲ)處理的安徽黃棕壤和新疆灰漠土老化56 d 后線蟲的繁殖均顯著降低(P<0.05). 根據外源Sb(Ⅲ)對線蟲繁殖毒性的閾值(見表3)可知,外源Sb(Ⅲ)對線蟲繁殖毒性的閾值均低于其對生育毒性的閾值. 比較基于不同毒性評價終點計算的外源Sb(Ⅲ)毒性閾值(見表3)可以發現,外源Sb(Ⅲ)對線蟲的繁殖表現出較高的毒性,對線蟲的生育毒性次之,對線蟲的生長毒性最低. 由老化因子(見表3)可知,新疆灰漠土中外源Sb(Ⅲ)的老化效應強于安徽黃棕壤.
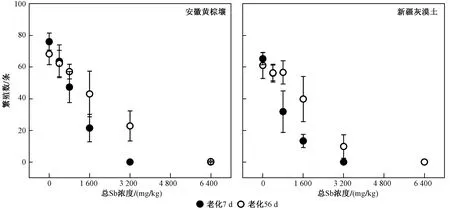
圖5 不同老化時間的安徽黃棕壤和新疆灰漠土中Sb 對線蟲的繁殖毒性Fig.5 Reproduction toxicity of Sb to C. elegans in Anhui yellow-brown soil and Xinjiang grey dessert soil with different aging time
3 討論
土壤中重金屬的生物毒性取決于其生物有效態濃度,研究中多通過化學可提取態對重金屬的生物有效濃度進行表征[30]. 重金屬的生物有效濃度與重金屬進入土壤環境后的物理化學過程緊密相關[12,31]. 馬祥愛等[32]研究發現,高黏粒占比的黑土對Sb 具有較強的吸附能力且對吸附態Sb 的解吸率較低. 林祥龍[33]研究指出,黏粒具有粒徑小、比表面積大、吸附點位多等特點,較砂粒能更好地與土壤中Sb 進行結合. 筆者研究選用的安徽黃棕壤中可提取態Sb 濃度低于新疆灰漠土,可能與其較高的黏粒占比有關. 已有研究[34-35]指出,有機質中的活性官能團能與Sb 結合形成配合物,對土壤中Sb 的遷移能力造成影響. 土壤中天然的鐵錳鋁氧化物同樣能對Sb 進行吸附,從而降低其生物有效濃度[2,36-37]. 筆者研究選用的安徽黃棕壤中有機質和鐵錳鋁氧化物含量均高于新疆灰漠土,降低了外源Sb(Ⅲ)的生物有效性和毒性,一定程度上解釋了經Sb(Ⅲ)處理的安徽黃棕壤中較低的可提取態Sb 濃度以及對線蟲較低的毒性.
外源Sb(Ⅲ)進入土壤環境會發生價態的轉變[38].筆者研究顯示,安徽黃棕壤和新疆灰漠土中Sb(Ⅲ)的氧化效率均隨總Sb 濃度的提升呈下降趨勢. 已有研究同樣指出Sb(Ⅲ)的氧化效率受外源Sb(Ⅲ)濃度的影響, Cai 等[39]研究發現,在較低的初始濃度(0.09 和0.47 mmol/L)下,吸附在土壤表面的Sb(Ⅲ)經過240 h 的反應被完全氧化為Sb(Ⅴ),當Sb(Ⅲ)濃度提至0.94 mmol/L 時,土壤表面所有Sb(Ⅲ)被氧化則需要更多的時間. Lin 等[29]研究同樣指出,外源Sb(Ⅲ)濃度為1 600 mg/kg 時江西土壤經過150 d 的老化,其中Sb(Ⅴ)占總Sb 的比例高達96.9%,而江西土壤中外源Sb(Ⅲ)濃度提至6 400 mg/kg 時,僅有16.6%的Sb(Ⅲ)被轉化為Sb(Ⅴ). 除外源Sb(Ⅲ)濃度的影響外,土壤性質同樣是造成Sb(Ⅲ)氧化效率差異的原因. 已有研究[36,40]指出,較高的土壤pH 有利于Sb(Ⅲ)氧化. 筆者研究顯示,新疆灰漠土中Sb(Ⅲ)的氧化效率高于安徽黃棕壤,這可能是因為新疆灰漠土較高的pH 促進了高毒性的Sb(Ⅲ)向低毒性的Sb(Ⅴ)轉化. 但也有研究[41]指出,pH 較高的條件下,土壤中的OH-與含氧陰離子形式存在的Sb 競爭結合礦物官能團,不利于土壤對Sb 的吸附,這可能是導致新疆灰漠土具有較高的可提取態Sb 濃度以及對線蟲毒性較高的原因.
筆者研究中外源Sb(Ⅲ)對線蟲的毒性隨老化時間的推移呈下降趨勢. 研究[11]指出,重金屬進入土壤環境后,會在短時期內完成固液相的分配和表面的吸附,隨老化時間的推移,通過沉淀、配位、氧化等反應過程達到新的平衡,生物有效性和毒性在老化過程中不斷降低. Lin 等[42]研究同樣發現,Cr(Ⅵ)處理的土壤老化21 d 后對跳蟲的繁殖毒性較老化2 d 的土壤顯著降低. 研究[43]指出,老化作用通過降低重金屬的生物有效態從而削弱其對生物的毒性. 蔡瓊瑤等[44]研究土壤中外源Pb 的老化特征,結果表明EDTA 提取態Pb 濃度隨土壤的老化呈下降趨勢. 筆者研究選用的2 種土壤中,外源Sb(Ⅲ)對線蟲的毒性同樣表現出隨可提取態Sb 濃度降低而減弱的特征,但可提取態Sb 的降幅存在差異. 這是因為安徽黃棕壤pH較低且具有較高的黏粒占比、有機質以及鐵錳鋁氧化物含量,外源Sb(Ⅲ)進入安徽黃棕壤后能在較短的時間內通過物理化學過程被吸附,而上述吸附過程在新疆灰漠土中進行得相對緩慢,經更長時間的老化后,新疆灰漠土中外源Sb(Ⅲ)對線蟲毒性的降幅更高. Lin 等[45]研究同樣表明,與老化7 d 的土壤相比,老化120 d 的土壤中Ni 對跳蟲致死毒性的LC50值和繁殖毒性的EC50值分別增加了1.30~1.94 和1.27~1.82倍,外源Ni 在4 種土壤中的老化效應存在差異. 外源Sb(Ⅲ)在新疆灰漠土中能被更快地氧化為毒性較低的Sb(Ⅴ),導致對線蟲毒性的閾值提升相對較高,表現出更明顯的老化效應.
根據該研究毒性測試結果可知,外源Sb(Ⅲ)對線蟲的繁殖具有更高的毒性,對生育的毒性次之,對生長的毒性最低. Schertzinger 等[46]研究顯示,污染物對線蟲生長的毒害間接抑制了線蟲的生育能力,導致污染物對線蟲生育的毒性高于其對生長的毒性,對線蟲繁殖數的抑制可能是由污染物的直接毒害作用以及對線蟲生育的間接毒害作用共同所致.
4 結論
a) 老化過程降低了Sb(Ⅲ)處理土壤中可提取態Sb 濃度和Sb(Ⅲ)占比,從而減弱了外源Sb(Ⅲ)對線蟲的毒性.
b) 土壤性質(pH、有機質、鐵錳鋁氧化物含量)對Sb(Ⅲ)處理土壤中可提取態Sb 濃度和Sb(Ⅲ)氧化效率的影響,導致不同土壤中外源Sb(Ⅲ)對線蟲毒性的差異.
c) 外源Sb(Ⅲ)在不同土壤中的老化過程存在差異,新疆灰漠土中可提取態Sb 濃度和Sb(Ⅲ)占比的降幅更高,導致外源Sb(Ⅲ)對線蟲毒性的閾值提升更大.

