我國18家三級兒童專科醫院兒童基本藥物可獲得性研究Δ
王志遠,韓泰森,何搖光,范平安,聶小燕,王曉玲,陳敬#,史錄文(1.北京大學藥學院,北京 100191;2.北京大學醫藥管理國際研究中心,北京 100191;.首都醫科大學附屬北京兒童醫院藥學部,北京 100045)
隨著我國生育政策的放開,近年來我國新出生人口大幅提升,兒童醫療服務需求也隨之上升。根據衛生統計年鑒數據,我國兒科門診人次從2010年的1.92億增加至2019年的2.78億[1],兒童用藥需求也隨之增加。保障兒童基本用藥需求,促進兒童用藥可及與合理使用,對于防治兒童疾病、提升兒童健康水平具有重要意義。
兒童用藥的可及性涉及研發、生產、供應和使用等各個環節。既往研究發現,我國兒童用藥研發和兒科臨床試驗水平依然較低[2],兒童醫院藥品短缺情況較成人更為嚴峻,原因更為復雜[3],兒童超年齡、超給藥途徑、超劑量給藥和無指征應用抗生素等現象發生頻率較高[4]。兒童基本藥物是指能滿足兒科最低用藥需求和考慮兒童特殊生理狀況的最安全、有效、經濟的藥物。目前關于我國兒童基本藥物可及性的信息十分有限,僅有少數學者在小范圍區域進行了調查研究,樣本的代表性有限,多聚焦于綜合性醫院或零售藥店,未關注兒童專科醫院中兒童基本藥物的可獲得情況,結果可能會受到非兒童人群的影響,且不同研究結果之間也顯示出較大差異[5-7],故我國兒童基本藥物的可及性到底如何,尚未達成統一認識。因此,有必要以我國兒童專科醫院為樣本,探討我國兒童基本藥物的可及性。
世界衛生組織(WHO)和國際健康行動機構(Health Action International,HAI)的專家學者曾于 2003年提出評估基本藥物可及性的標準調查法,明確了調查藥品和樣本機構的選擇方法,并建議從基本藥物可獲得性、價格和可負擔性3個角度評價醫療機構基本藥物的可及性[8]。本課題組采用WHO/HAI標準調查法,以我國三級兒童專科醫院為樣本醫院,調查了我國兒童基本藥物的可及性及影響因素,以期為我國相關決策者制定和完善兒童用藥相關政策提供實證依據。由于我國暫未出臺兒童基本藥物目錄,故本研究界定的兒童基本藥物是指WHO發布的第7版《WHO兒童基本藥物示范目錄》(WHO Model List of Essential Medicines for Children,WHO EMLc)中收錄的藥品。受限于篇幅所長,本文僅報告了可獲得性研究部分,可負擔性研究部分將另文發表。
1 資料與方法
1.1 樣本醫院
收集中國藥學會全國醫藥經濟信息網(Chinese medicine economic information,CMEI)數據庫中全部18家三級兒童專科醫院(東部地區10家、東北地區3家、中部地區3家、西部地區2家)作為本研究的樣本醫院。查閱《2021中國衛生健康統計年鑒》可知,2020年全國擁有床位數不少于500張(三級兒童專科醫院標準)的兒童專科醫院共36家,本研究樣本醫院占其半數,故可以認為本研究的樣本代表性較好。
1.2 目標藥品
本研究將第7版WHO EMLc收錄的所有藥品作為目標藥品。首先,通過醫藥魔方數據庫查詢目標藥品在國內上市的所有劑型和規格;其次,在CMEI數據庫中提取樣本醫院2016年7月-2019年6月期間的目標藥品采購數據,包括藥品通用名、劑型、規格、季度采購信息等。排除下述藥品:(1)消毒防腐制劑(如酒精手消液、氯基化合物等);(2)劑型不明確的藥品(如疫苗、部分血漿替代物和血液制品等);(3)活性成分不明確的藥品(如腹膜透析液等);(4)麻醉氣體;(5)國內未上市的藥品;(6)樣本醫院未采購的藥品。研究最終納入189個活性成分,對應229種藥品(以通用名計),具體篩選流程見圖1。本研究所指“活性成分”為發揮藥理作用的分子實體,不含酸根或堿基;而“藥品”指活性成分及相應劑型。
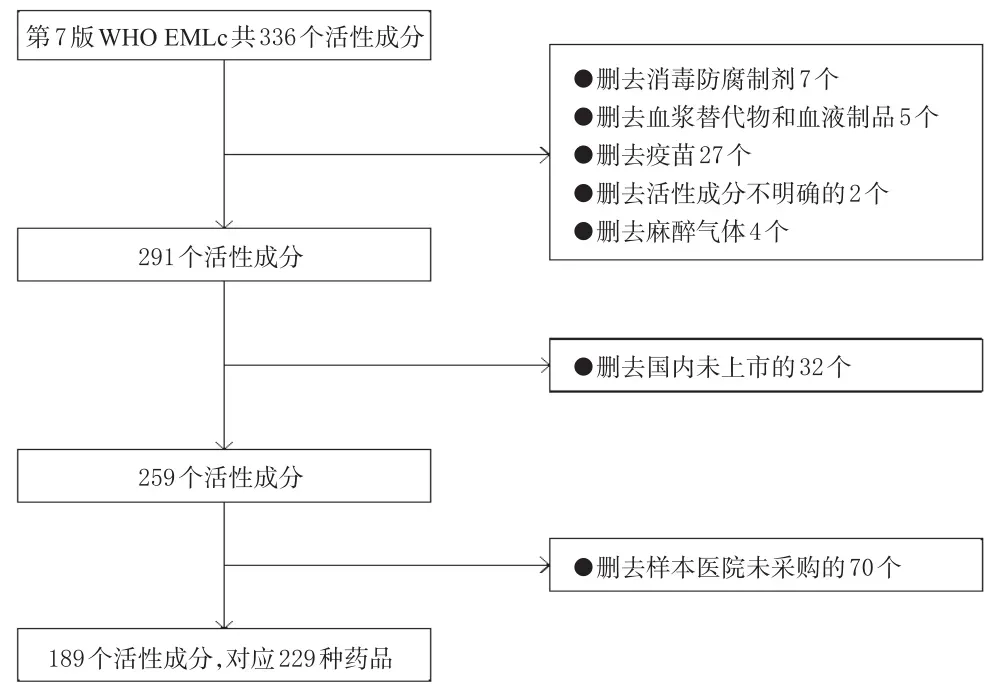
圖1 目標藥品篩選流程圖
1.3 藥品可獲得率
為提高WHO/HAI標準調查法在我國的適應性,有學者基于我國實際情況對該方法進行了改良。在該方法中,藥品可獲得率是藥品可獲得性的重要考核指標。藥品可獲得率即配備該藥品的樣本醫院數量占樣本醫院總數的比值[5,9-10]。本研究采用Excel 2019軟件計算所有目標藥品在樣本醫院的可獲得率并進行排序,分析目標藥品的可獲得率在2016年7月-2019年6月各季度中的變化情況。國際上對藥品可獲得率沒有嚴格統一的標準,一般認為<50%為可獲得率較低,50%~80%為可獲得性較高,>80%為可獲得率很高[11]。本研究參照該標準計算了各季度內樣本醫院中可獲得率較低、較高和很高的目標藥品占比。將目標藥品按照解剖學、治療學及化學分類系統(anatomical therapeutic chemical,ATC)分類后,計算各類別藥品的可獲得率,該數值為該類別下所有藥品可獲得率的算數平均值。
1.4 可獲得率的影響因素
1.4.1 是否在我國獲準可用于兒童 本研究考察了目標藥品是否在我國獲準可用于兒童對其可獲得率的影響。由于我國官方文件并沒有明確的兒童用藥定義,美國FDA和美國兒科學會也未從生理學角度界定什么是兒童藥物[12],故我國部分學者根據藥品名稱、兒童用藥處方集或說明書信息對兒童用藥的概念進行了界定。例如,董大千等[13]將基本藥物處方集中標注兒童用法用量的藥品(包括未標注兒童用法用量,但在注意事項或用法用量中對兒童用藥有相關的語言描述,或者對兒童年齡、給藥劑型的限制等進行了標注的藥品)定義為兒童基本藥物。參考上述方法,本研究界定的在我國獲準可用于兒童的藥品包括以下3種類型:(1)兒童專用藥,指專門針對兒童進行研發、生產,且只有兒童適應證及用法用量的藥品,藥品名稱含“小兒”“嬰兒”“兒童”等字樣或藥品說明書中僅注明兒童適應證[14-16],或在國家醫保藥品目錄的備注欄標明“限兒童”“限新生兒”“限小兒某疾病”的藥品[17];(2)兒童適用藥,指藥品說明書中功能主治包含兒童適應證且具有明確兒童用法用量的藥品(但該類藥品不僅用于兒童),或藥品說明書中標注了適宜兒童的品規,通常帶有“本品適用于兒童”“小兒患者應在醫師指導下服用”等字樣的藥品[14];(3)兒童成人共用藥,指藥品說明書中未注明兒童禁用或慎用,但沒有兒童用法用量的信息,或只標注了成人用法用量,兒童用藥劑量可通過年齡、體質量、體表面積及成人劑量換算而得的藥品[18]。相應地,本研究將藥品說明書無前述信息或注明“未進行兒童臨床試驗且無可靠參考文獻”“兒童用藥安全性、有效性未建立或尚不明確”“兒童禁用”“兒童不宜應用”的藥品界定為在我國未獲準可用于兒童的藥品。本研究由2名研究人員分別查閱并復核目標藥品的中文說明書,以確定藥品是否在我國獲準可用于兒童。
1.4.2 是否納入國家基本藥物目錄 因本研究觀察期內先后有2012年版和2018年版國家基本藥物目錄執行,故本研究同時考察了2012年版和2018年版國家基本藥物的收錄情況對目標藥品可獲得率的影響。
1.5 統計學方法
采用Stata 16.0和Excel 2019軟件進行數據統計和分析。在關聯性分析中,由于初步檢驗顯示藥品可獲得率呈輕微偏態分布,故本研究選用兩獨立樣本Wilcoxon秩和檢驗進行單因素影響分析。雙側P<0.05表示在95%置信區間(CI)上的差異具有統計學意義。
2 結果
2.1 兒童基本藥物的可獲得率
2016年7月-2019年6月,229種目標藥品中吸入用布地奈德混懸液、口服補液鹽、注射用免疫球蛋白、注射用水的可獲得率為100%;另有10種藥品的可獲得率超過95%,從高到低依次為注射用甲潑尼龍(99.5%)、氯化鈉注射液(99.5%)、阿奇霉素顆粒(98.6%)、碳酸氫鈉注射液(98.6%)、布洛芬混懸劑(98.1%)、甘露醇注射液(97.2%)、乳果糖溶液(97.2%)、注射用丙泊酚(96.8%)、葡萄糖注射液(96.8%)、頭孢曲松注射液(95.4%)。可獲得率最低的10種藥品分別為伊曲康唑注射液(3.7%)、灰黃霉素片(3.2%)、洛匹那韋利托那韋片(2.8%)、阿達木單抗注射液(2.3%)、環絲氨酸膠囊(1.9%)、葡萄糖酸銻鈉注射液(1.4%)、齊多拉米雙夫定片(1.4%)、纈更昔洛韋片(1.4%)、利福噴丁膠囊(0.9%)、右旋糖酐70滴眼液(0.9%)。
2016年7月-2019年6月的各季度中,229種目標藥品在樣本醫院的可獲得率情況見圖2。由圖2可見,各季度中,藥品可獲得率基本保持穩定,且均有半數以上的藥品可獲得率超過50%。

圖2 2016年7月-2019年6月各季度中目標藥品的可獲得率情況
將229種藥品依據ATC編碼進行分類,各類藥品的年均可獲得率見圖3。由圖3可見,各類藥品的可獲得率存在明顯差異,其中心血管系統用藥和血液系統用藥的整體可獲得率最高(但其中依那普利片的可獲得率較低,僅為22.2%);抗寄生蟲用藥、皮膚科用藥的整體可獲得率較低(但其中莫匹羅星軟膏的可獲得率較高,為71.8%)。
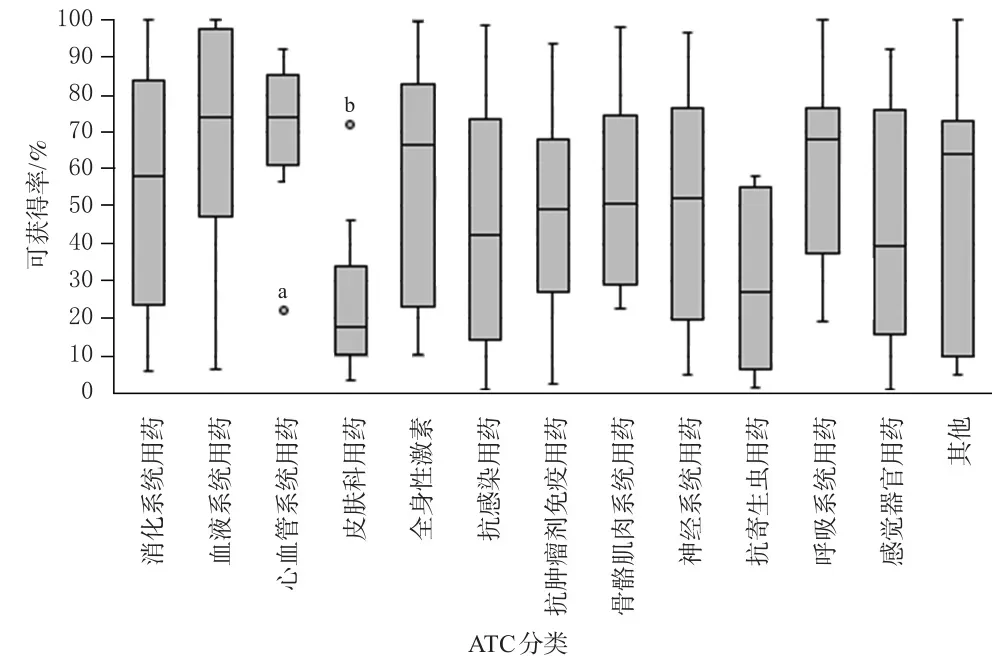
圖3 各類藥品的年均可獲得率
2.2 兒童基本藥物可獲得率的相關影響因素
2.2.1 是否在我國獲準可用于兒童對藥品可獲得率的影響 經研究人員核對藥品說明書之后發現,229種目標藥品中有201種(87.8%)在我國已獲準可用于兒童,這201種藥品在樣本醫院的可獲得率均值為52.4%,顯著高于未獲準的28種藥品(可獲得率為24.4%)(P<0.001)。未獲準的28種藥品(12.2%)在樣本醫院使用尚屬于超說明書用藥,存在一定安全隱患,甚至可能引發醫患間法律糾紛。個別未獲準可用于兒童的藥品在樣本醫院的可獲得率較高,例如多巴胺注射液的可獲得率高達85.2%。
2.2.2 是否納入國家基本藥物目錄對藥品可獲得率的影響 229種目標藥品中,有130種被2012年版國家基本藥物目錄收錄,157種被2018年版國家基本藥物目錄收錄,收錄藥品的可獲得率均顯著高于未收錄的藥品(P=0.002或P<0.001)。結果見表1。
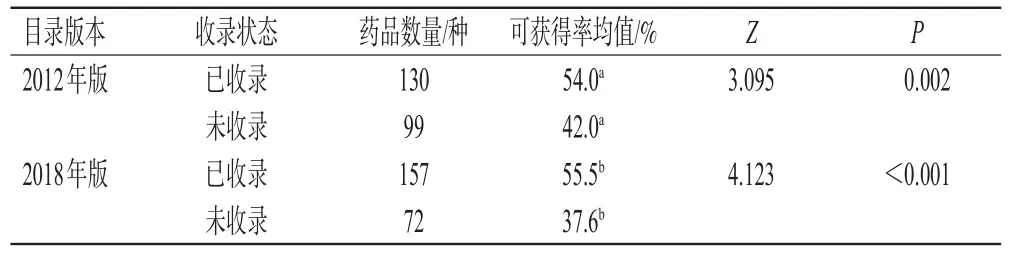
表1 是否納入國家基本藥物目錄對藥品可獲得率的影響
3 討論
3.1 我國三級兒童專科醫院的兒童基本藥物可獲得率總體較好
2016年7月-2019年6月,229種目標藥品中,有半數以上在18家樣本醫院的可獲得率均超過50%,且在調查時間內可獲得率基本保持穩定,表明兒童基本藥物在我國三級兒童專科醫院的可獲得性總體較好。
樣本醫院的兒科常用藥物可獲得率較高,例如吸入用布地奈德混懸液、口服補液鹽、注射用免疫球蛋白的可獲得率一直保持在100%,阿奇霉素顆粒、布洛芬混懸劑、乳果糖溶液的可獲得率均超過95%。此外,急(搶)救類藥物可獲得率也較高,例如碳酸氫鈉注射液、甘露醇注射液的可獲得率均超過95%。注射用丙泊酚作為目前常用的靜脈麻醉藥,其可獲得率也高達96.8%。
從藥品種類來看,抗寄生蟲用藥整體可獲得率較低,這可能與隨著社會經濟發展、生活水平提高,我國人群寄生蟲病的發病率持續降低有關[19-21],也可能與三級兒童專科醫院一般地處經濟發達的城市,收治患兒群體的寄生蟲病發病率較低有關;心血管系統用藥中依那普利片可獲得率低則可能與兒童高血壓發生率較低有關。
3.2 已獲準可用于兒童的藥品可獲得率更高
藥品說明書是藥品使用的法律依據,醫師開具兒童用藥安全性未知的藥品屬于超說明書用藥,這可能也是本研究中未獲準可用于兒童的藥品可獲得率較低的重要原因。但也有少數未獲準可用于兒童的藥品可獲得率極高,例如本研究發現,多巴胺注射液可獲得率為85.2%,這可能與多巴胺注射液屬于醫院常備急(搶)救藥品有關[22]。未來應推動臨床常用藥品在兒童群體中的臨床試驗及相關研究,明確兒童用藥的有效性、安全性和必要性等,并及時更新藥品說明書;同時,應建立完善的法規、規章制度以確保兒童用藥權益,將現行有效措施法律化,鼓勵兒童專用藥品、專屬劑型的研發與生產[23]。
3.3 國家基本藥物目錄對醫院采購兒童用藥具有指導作用
我國于2009年正式建立國家基本藥物制度,并公布了2009年版國家基本藥物目錄,旨在保障人民群眾基本用藥、促進臨床合理用藥、降低藥品價格、減輕患者用藥負擔。國家基本藥物目錄是我國各級醫療衛生機構配備使用藥品的重要依據。本研究結果也證實,國家基本藥物目錄對樣本醫院采購藥品具有一定的指導作用,目標藥品中,納入國家基本藥物目錄的藥品可獲得率顯著高于未納入國家基本藥物目錄的藥品(P=0.002或P<0.001)。2021年底,國家衛生健康委藥政司發布的《國家基本藥物目錄管理辦法(修訂草案)》明確提及,下一版國家基本藥物目錄將單獨設置兒童目錄,并依據兒童專用適用藥分類,以進一步保障我國兒童用藥的可及性。
3.4 規范超說明書用藥行為
本研究納入的229種兒童基本藥物中,有28種(12.2%)屬于兒科超說明書用藥。雖然兒科超說明書用藥的現象在世界范圍內都十分普遍[24-25],但其不僅會帶來臨床用藥安全隱患,甚至會帶來一系列不可避免的道德或法律問題[26]。兒童專科醫院在采購藥品時,應優先選擇已獲國家藥品監管部門明確批準可用于兒童的藥品,減少超說明書用藥現象,從而避免或減少醫療糾紛。近年來,部分三級甲等醫院對于超說明書用藥的管理更加完善,推行了超說明書用藥備案機制[27-29],規定只有在臨床無更優用藥方案,且指南推薦、專家認可、患者知情同意的前提下才可實施超說明書用藥。2022年3月開始實施的《醫師法》,也首次將超說明書用藥寫入法條,規定“在尚無有效或者更好治療手段等特殊情況下,醫師取得患者明確知情同意后,可以采用藥品說明書中未明確但具有循證醫學證據的藥品用法實施治療”,此舉也有助于維護患者及醫療機構雙方利益。
3.5 本研究的局限性
本研究存在以下局限性:(1)本研究僅調查了我國三級兒童專科醫院,缺少其他類型醫療機構和零售藥店的兒科用藥數據,研究結果的外推性可能受到影響;(2)本研究使用的是樣本醫院采購數據,如果調查時醫院未采購某藥品,則認為該藥品在醫院不可獲得,這與藥品實際可獲得情況存在一定差異(例如某些藥品可能通過臨時購藥等渠道在醫院使用,此類數據未納入本文統計);(3)我國民眾目前對兒童用藥的需求可能與WHO EMLc有一定區別,這使得本研究結論的參考價值受到一定的影響。
4 結論
2016年7月-2019年6月,第7版WHO EMLc中收錄的藥品在我國三級兒童專科醫院的可獲得率較高;在我國獲準可用于兒童的藥品及國家基本藥物目錄收錄的藥品的可獲得率更高;同時,臨床上也存在一定程度的超說明書用藥現象。建議我國應盡早出臺兒童基本藥物目錄,推動臨床常用品種在兒童人群中的臨床試驗,并及時更新藥品說明書,以保障兒童基本藥物的可獲得性與安全性。

