單核苷酸多態性微陣列芯片技術在羊水過多孕婦遺傳學病因中的應用效果▲
黃 婧 潘平山 蒙達華 王林琳
(廣西壯族自治區婦幼保健院優生遺傳門診,廣西南寧市 530003)
羊水是胎兒在母體宮內生存所不可缺少的重要成分,主要來源于母體血清經胎膜進入羊膜腔的透析液、胎肺分泌液、臍帶華通氏膠及胎兒皮膚滲出液[1]。正常妊娠時羊水的產生與吸收處于動態平衡,而羊水產生和吸收失衡將導致羊水量異常。羊水過多是一種常見的妊娠期并發癥,發生率為1%~3%[2]。妊娠期間羊水量超過2 000 mL即為羊水過多,超聲表現為最大羊水暗區垂直深度≥8 cm或羊水指數≥25 cm[3]。羊水過多對胎兒危害較大,是妊娠不良結局的重要原因之一。羊水過多的病因十分復雜,有研究表明染色體異常等遺傳病是羊水過多的重要因素之一[3]。染色體微陣列分析技術可以在基因組水平上檢測染色體拷貝數變異(copy number variation,CNV),同時可檢測染色體嵌合體(嵌合比例>20%)、雜合性缺失、單親二倍體等,目前已被廣泛應用于診斷胎兒結構畸形、原發性智力低下、生長發育遲緩、自閉癥、多發畸形及腫瘤等遺傳學領域[4]。本文通過回顧性分析407例羊水過多孕婦的產前診斷檢測結果,探討單核苷酸多態性微陣列芯片(single nucleotide polymorphism microarray,SNP-array)技術在羊水過多孕婦產前診斷中的應用價值。
1 資料與方法
1.1 臨床資料 回顧性分析2016年1月至2019年 12月就診于廣西壯族自治區婦幼保健院的407例妊娠中晚期羊水過多孕婦的臨床資料,孕周均≥17周,年齡20~42(30.16±3.42)歲。納入標準:產前超聲篩查發現羊水過多的孕婦;接受抽取羊水或臍帶血進行染色體核型分析及SNP-array檢測的孕婦;孕婦及家屬對本研究知情同意。排除標準:不能配合行羊膜腔或臍靜脈穿刺者,存在羊膜腔或臍靜脈穿刺術禁忌證者。
1.2 研究方法 所有孕婦均接受檢測前的遺傳咨詢并簽署知情同意書。對于孕17~22周的孕婦,在B超腹部探頭引導下行經腹羊膜腔穿刺并抽取羊水30 mL,對于孕周>22周的孕婦,在B超腹部探頭引導下行經腹臍靜脈穿刺并抽取臍帶血1.5 mL,進行染色體核型分析及SNP-array檢測。30 mL羊水中,20 mL用于染色體核型分析,10 mL用于SNP-array檢測;1.5 mL臍帶血中,0.5 mL用于染色體核型分析,1 mL用于SNP-array檢測。
1.2.1 染色體核型分析:對獲取的樣本進行細胞培養。取20 mL羊水標本接種至培養瓶中進行培養,7 d后用10 μg/mL的秋水仙素干預3.5 h以阻斷細胞有絲分裂,當細胞處于中期分裂相時,使用胰蛋白酶消化貼壁細胞,經離心、低滲處理、固定后,將調整為適合濃度的細胞懸液進行滴片、烤片、制片,第2天進行G顯帶分析。取0.5 mL臍帶血標本接種到淋巴細胞培養液中,培養68~72 h后用40 μg/mL秋水仙素干預15 min以阻斷細胞有絲分裂,獲取中期分裂相細胞,經離心、低滲處理、固定后,將調整為適合濃度的懸液進行滴片、烤片、制片,第2天進行G顯帶分析。每份標本至少計數20個分裂相,分析5個核型。若發現嵌合體核型則增加計數至100個分裂相。參照人類細胞遺傳學國際命名體制(2016)進行染色體核型命名。
1.2.2 SNP-array檢測:采用Lab-Aid 820核酸提取Mini試劑盒(廈門致善生物科技有限公司,批號:200116)提取臍帶血標本中的基因組DNA;采用微量樣品基因組DNA提取試劑盒[天根生化科技(北京)有限公司,批號:DP316]提取羊水標本中的基因組DNA。采用NanoDrop 2000分光光度計測定DNA濃度及純度。采用美國Illumina公司的HumanCytoSNP-12芯片進行SNP-array分析,根據標準操作流程對基因組DNA依次進行全基因組擴增、片段化、雜交和熒光染色,采用美國Illumina公司的iScan芯片掃描儀對制備的基因芯片進行掃描,獲得的數據采用KaryoStudio 1.4.3軟件進行分析。數據分析參照本實驗內部數據庫及正常人基因組變異數據庫DGV(http://dgv.tcag.ca/)、DECIPHER(https://decipher.sanger.ac.uk)、UCSC Genome Browser(https://genome-asia.ucsc.edu/cgi-bin/hgGateway?redirect=manual&source=genome.ucsc.edu)、在線《人類孟德爾遺傳》(Online Mendelian Inheritance in Man,OMIM)(https://omim.org/)等公共在線數據庫。
2 結 果
2.1 染色體核型分析結果 407例羊水過多孕婦中,染色體核型異常24例,檢出率為5.90%(24/407),其中21-三體綜合征14例,18-三體綜合征4例,超雄綜合征1例,染色體缺失/重復5例。
2.2 SNP-array檢測結果 407例羊水過多孕婦中,SNP-array檢測檢出66例芯片異常,檢出率為16.22%(66/407)。66例芯片異常包括33例致病性CNV和33例臨床意義不明CNV。33例致病性CNV中,24例的檢測結果與染色體核型分析結果一致,另9例染色體核型分析未見異常但SNP-array檢測檢出染色體微缺失/微重復綜合征。見表1。
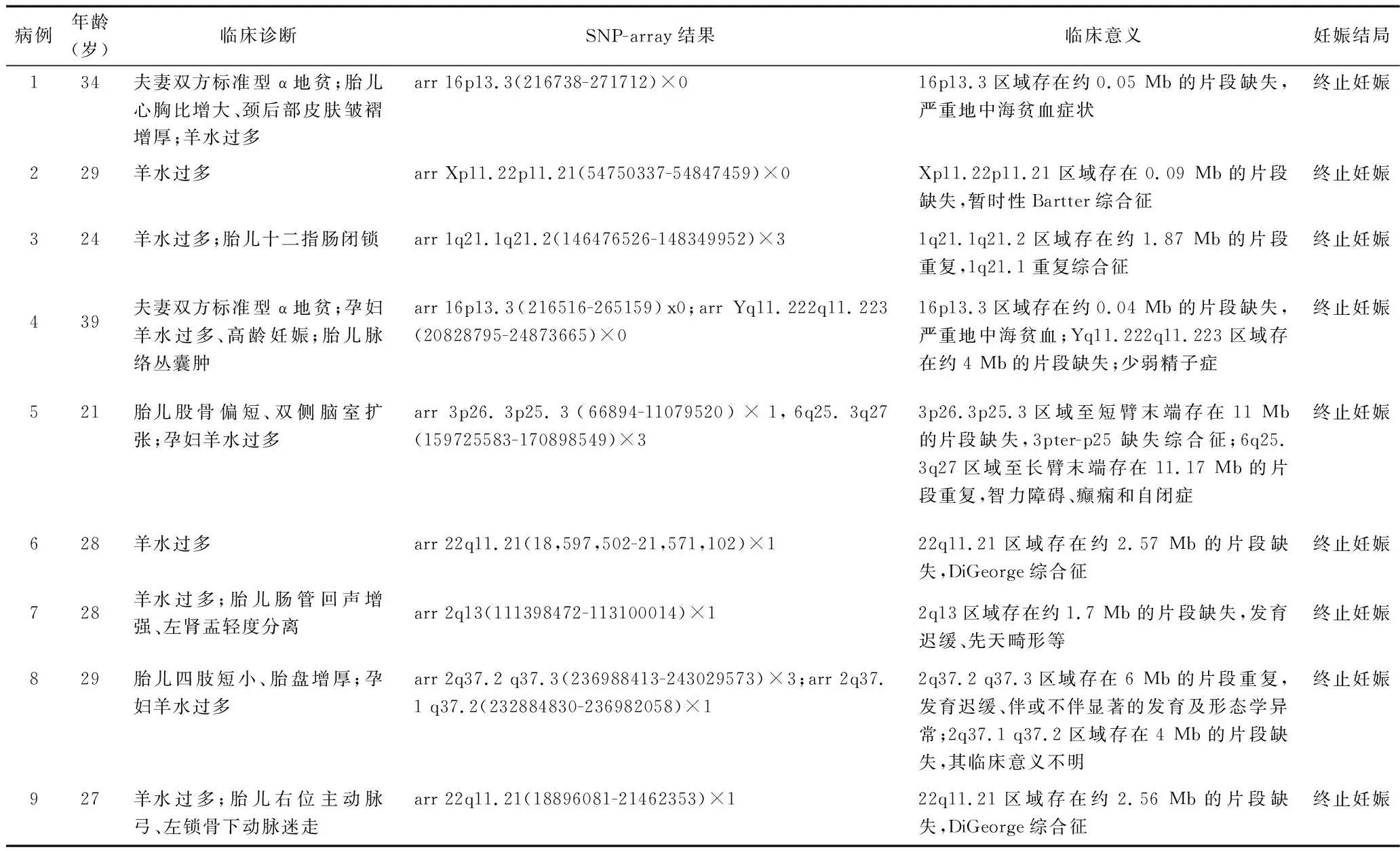
表1 9例微缺失/微重復綜合征孕婦的SNP-array檢測結果
3 討 論
羊水過多時子宮張力增高,影響孕婦休息,使血壓升高、子宮血供不佳,導致子宮、胎盤發生缺血缺氧。羊水過多除了容易導致胎膜早破、早產,還可以引起胎盤早剝,同時,羊水過多引起的子宮肌纖維過度伸展可致子宮收縮乏力,增加產后出血的發生風險[4]。羊水過多會干擾胎兒的生長環境,使得胎兒頻繁活動,進而導致胎位不正及臍帶繞頸,嚴重者可導致胎兒宮內窘迫甚至胎死腹中[5]。2018年美國母胎醫學會發布了相關指南[6],該指南詳細闡述了羊水過多的診斷標準、病因及圍產期管理措施,建議確診羊水過多后應首先進行病因分析,根據病因給予相應臨床處理。Blitz等[7]的研究表明,在羊水過多合并或不合并B超其他異常的胎兒中,染色體非整倍體的發生率分別為10%和1%。另外,部分孕婦由于只存在羊水過多的單一指征,未給予足夠的重視,導致胎兒出生后出現各類代謝性綜合征、神經肌肉病等遺傳性疾病。因此,對羊水過多的孕婦進行產前遺傳學診斷,對指導優生優育、提高出生人口質量、減少出生缺陷具有重要意義。
染色體微陣列分析技術能夠在全基因組水平上檢測染色體CNV,彌補常規核型分析無法檢出亞顯微異常的不足。其中,SNP-array技術是對患者DNA進行熒光標記并雜交到芯片上,與來源于數據庫的標準人類基因組正常序列進行比對,從而發現患者DNA拷貝數變化的一項技術。SNP-array技術除了能夠檢測出CNV,還能夠檢測出雜合性缺失、單親二倍體、三倍體(和其他多倍體)及一定比例的嵌合體[8]。在核型分析結果正常的遺傳咨詢者中,SNP-array技術可以額外檢測出某些致病性基因組不平衡或遺傳突變[9]。近年來研究表明,CNV也與羊水過多密切相關[10-11]。SNP-array技術已被國內與國際細胞遺傳協會推薦為胎兒超聲異常的首選檢查方法[12-13]。本研究407例羊水過多孕婦中,染色體核型分析檢出染色體核型異常24例,檢出率為5.90%(24/407),SNP-array檢出66例芯片異常,檢出率為16.22%(66/407),66例芯片異常包括33例致病性CNV和33例臨床意義不明CNV;33例致病性CNV中,24例與染色體核型分析結果一致,包括14例21-三體綜合征、4例18-三體綜合征、1例超雄綜合征和5例染色體缺失/重復,其余9例為染色體核型分析未見異常但SNP-array檢出染色體微缺失/微重復綜合征。這提示SNP-array技術對非整倍體和不平衡性染色體數量重排的檢出率與傳統核型分析方法相近,并具有更高的分辨率。
本研究SNP-array技術額外檢出的9例致病性染色體微缺失/微重復綜合征病例中,病例1檢測到16號染色體p13.3區域存在約0.05 Mb的純合缺失,為致病性CNV,該缺失片段包含2個致病性OMIM基因:糖化血紅蛋白A1型(glycosylated hemoglobin type A1,HBA1)和糖化血紅蛋白A2型(glycosylated hemoglobin type A2,HBA2)。這兩個基因均與地中海貧血有關,雙基因純合缺失可導致嚴重的地中海貧血癥狀。病例2缺失片段包含黑色素瘤抗原家族D2(melanoma antigen family D2,MAGED2)基因,而MAGED2基因對于胎兒腎臟再吸收鈉鹽、保持羊水平衡并維持妊娠具有重要作用,該基因突變與暫時性Bartter綜合征相關,為X連鎖隱性遺傳。有文獻報告,導致MAGED2基因功能喪失的突變可引起羊水過多及早產,還可引起嚴重但暫時的產前Bartter綜合征[14]。病例3中1q21.1區域片段重復部分與1q21.1重復綜合征有關,包含關鍵基因AMP活化型蛋白激酶β2(非催化亞型)(protein kinase,AMP-activated,beta 2 non-catalytic subunit,PRKAB2)和縫隙連接蛋白α-5(gap junction protein alpha-5,GJA5),1q21.1重復區域外顯率不全,表現度可變,患者具有廣泛的臨床表現,包括發育遲緩、心臟畸形、輕度特殊面容等,但部分患者亦可無明顯臨床表現。研究表明,1q21.1區域的重復與先天性心臟病相關,其中GJA5基因的CNV與心臟發育異常相關[15]。病例4檢出的16p13.3區域缺失片段包含HBA1和HBA2基因,與地中海貧血有關;此外,該病例中Yq11.222q11.223缺失區域涉及Y染色體無精子因子b(azoospermia factor b ,AZFb)區域,AZFb區域整段缺失的患者可存在唯支持細胞綜合征或生精阻滯的典型睪丸組織學特征,其臨床表現主要為少弱精子癥[16]。研究顯示,AZFb區域部分缺失的男性能夠自然生育帶有同樣Y染色體缺失的后代[17],因此筆者建議對此類患者進一步行胎兒產前α地中海貧血基因檢測、Y染色體缺失檢測及父親Y染色體驗證。病例5檢出3號染色體短臂缺失,這可導致3pter-p25缺失綜合征,該病的常見臨床表現為宮內發育遲緩、低出生體重、小頭畸形、三角頭、肌張力低下、精神發育遲緩、上瞼下垂、內眥、小頜畸形等。病例6與病例9均檢測到22q11.21區域存在片段缺失,表現為DiGeorge綜合征,該病缺失的關鍵基因為T-box轉錄因子1(T-box transcription factor 1,TBX1),臨床表現為胸腺發育不全、低血鈣癥、心臟(心血管)畸形、骨骼畸形、特殊面容、身材矮小、學習困難[18]。病例7檢出2q13缺失基因組疾病,該病的主要臨床表現為發育遲緩、小頭畸形、智力障礙及先天畸形相關癥狀等[19-20]。病例8檢出2q37.2 q37.3區域片段重復,其臨床表現包括發育遲緩、伴或不伴顯著的發育及形態學異常、肌張力低下等。
另外,本研究臨床意義不明CNV的病例檢出率為8.11%(33/407),這類病例的結果解讀與遺傳咨詢需結合孕婦及其丈夫的CNV檢測結果,一般而言,若CNV為遺傳性的,則臨床意義較小,若為新發的,則臨床意義較大,但仍需要考慮不完全外顯和臨床表型差異的影響。對于雜合性缺失是否需要報告,應以雜合性缺失區域內是否涉及嚴重的隱性遺傳病基因為參考依據,如果涉及隱性遺傳病相關基因,可在報告中建議行外顯子測序以排除純合致病基因突變的可能。
綜上所述,對于中晚期羊水過多孕婦,在常規染色體核型分析的基礎上進行SNP-array檢測可獲得更多的遺傳學信息,有助于發現染色體核型分析無法檢出的染色體亞顯微結構異常,以及提高對羊水過多胎兒的遺傳學病因診斷率,從而為羊水過多孕婦的胎兒預后評估及遺傳咨詢提供更優的臨床決策。

