血清NDRG4、sB7-H4對上皮性卵巢癌患者腫瘤細胞減滅術后復發的預測價值
裴益明,王 蕾,王 苗△
咸陽市第一人民醫院:1.檢驗科;2.婦產科,陜西咸陽 712000
卵巢癌是全球范圍內女性第七大常見惡性腫瘤,也是導致癌癥死亡的第八大原因[1],多數上皮性卵巢癌(EOC)患者失去根治性手術機會,腫瘤細胞減滅術(PTCR)是治療中晚期EOC的主要方法,但是術后復發率較高,復發促使癌癥進展[2]。分析EOC復發相關因素以及預測復發的生物學標志物對于改善患者預后十分重要。抑癌基因N-myc下游調節因子4(NDRG4)是一種新型廣譜抑癌基因,可抑制腫瘤細胞增殖、侵襲和血管生成,促使腫瘤細胞凋亡,NDRG4低表達與腫瘤復發轉移密切相關[3]。可溶性B7-H4(sB7-H4)是T細胞共抑制分子,可下調抗原特異性免疫反應,抑制T細胞增殖、細胞周期進程和細胞因子產生,在食管鱗狀細胞癌、胰腺癌、胃癌等各種人類腫瘤中過度表達,與腫瘤進展密切相關[4]。本研究通過檢測血清NDRG4、sB7-H4水平,分析其與EOC患者PTCR后復發的關系以及其預測復發的價值。
1 資料與方法
1.1一般資料 選擇2015年6月至2018年6月咸陽市第一人民醫院婦產科收治的85例EOC患者為研究對象,年齡42~65歲,平均(58.12±5.49)歲;組織學類型:漿液性癌68例,黏液性癌12例,內膜樣癌5例;分化程度:中高度分化32例,低度分化53例;國際婦產科學聯合會(FIGO)分期:Ⅲ期48例,Ⅳ期37例。本研究獲得咸陽市第一人民醫院倫理委員會批準,患者及其家屬均簽署同意書。納入標準:(1)經病理學證實為EOC;(2)符合手術指征,且無禁忌證,均接受PTCR;(3)術前未接受任何形式的治療。排除標準:(1)經臨床確診的其他部位惡性腫瘤;(2)嚴重肝腎功能障礙、急慢性感染、骨髓抑制;(3)其他原因無法完成PTCR。
1.2儀器與試劑 FLUO star Omega全自動多功能酶標儀(德國BMG LABTECH公司),羅氏Elecsys2010全自動電化學發光免疫分析儀,sB7-H4試劑盒購自艾美捷科技有限公司,NDRG4試劑盒購自北京科美東雅生物技術有限公司。
1.3方法
1.3.1血清NDRG4、sB7-H4水平檢測 所有患者術前采集靜脈血3 mL注入干燥試管,待血液凝固后取上層液離心(相對離心力699×g)5 min取上清液上機檢測。酶聯免疫吸附試驗檢測血清sB7-H4水平,電化學發光免疫法檢測血清NDRG4水平。
1.3.2治療、隨訪和分組 治療:所有患者均接受PTCR,切除全子宮、雙附件、大網膜、 盆腹腔腫瘤病灶(黏液性卵巢癌切除闌尾),并進行盆腔或腹主動脈旁淋巴結切除術。術后2周左右進行常規靜脈化療6~8個周期,化療方案均為TC(紫杉醇+卡鉑)。隨訪及分組:所有患者自出院起均進行為期3年的隨訪,隨訪方式主要以患者返院復查為主,結合電話隨訪,術后第1年每2個月復查1次,之后每半年復查1次。統計隨訪期間患者腫瘤復發例數,復發定義為糖類抗原(CA)125>35 U/mL,人附睪蛋白4(HE4)>72 pmol/L;影像學檢查發現卵巢出現新發病灶;發生不明原因腸梗阻;出現胸腔積液和腹水[5]。根據復發情況將患者分為復發組和未復發組。
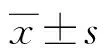
2 結 果
2.1復發情況 隨訪3年,85例患者失訪2例,剩余83例復發32例(復發組),未復發51例(未復發組),復發率為38.55%。
2.2復發組、未復發組術前血清NDRG4、sB7-H4水平比較 復發組術前血清NDRG4水平低于未復發組(P<0.05),sB7-H4水平高于未復發組(P<0.05),見表1。

表1 復發組、未復發組術前血清NDRG4、sB7-H4水平的比較
2.3EOC患者PTCR后復發的單因素分析 單因素分析結果顯示,復發組FIGO分期為Ⅳ期、殘余病灶最大徑≥1 cm、腹水≥1 000 mL、術后2周CA125≥35 U/mL的比例高于未復發組(P<0.05),兩組年齡、分化程度、組織學類型、是否接受新輔助化療比較差異無統計學意義(P>0.05),見表2。
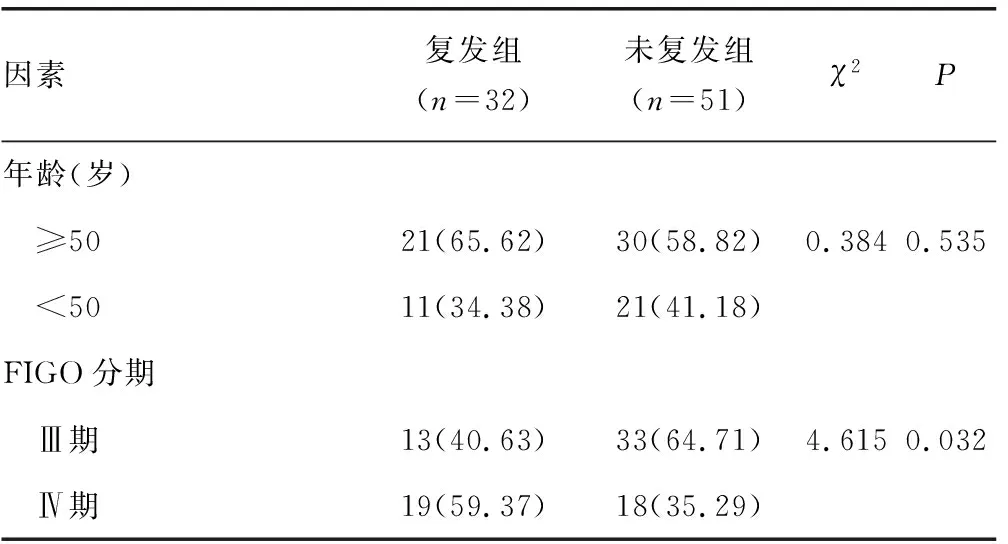
表2 影響EOC患者PTCR后復發的單因素分析結果[n(%)]
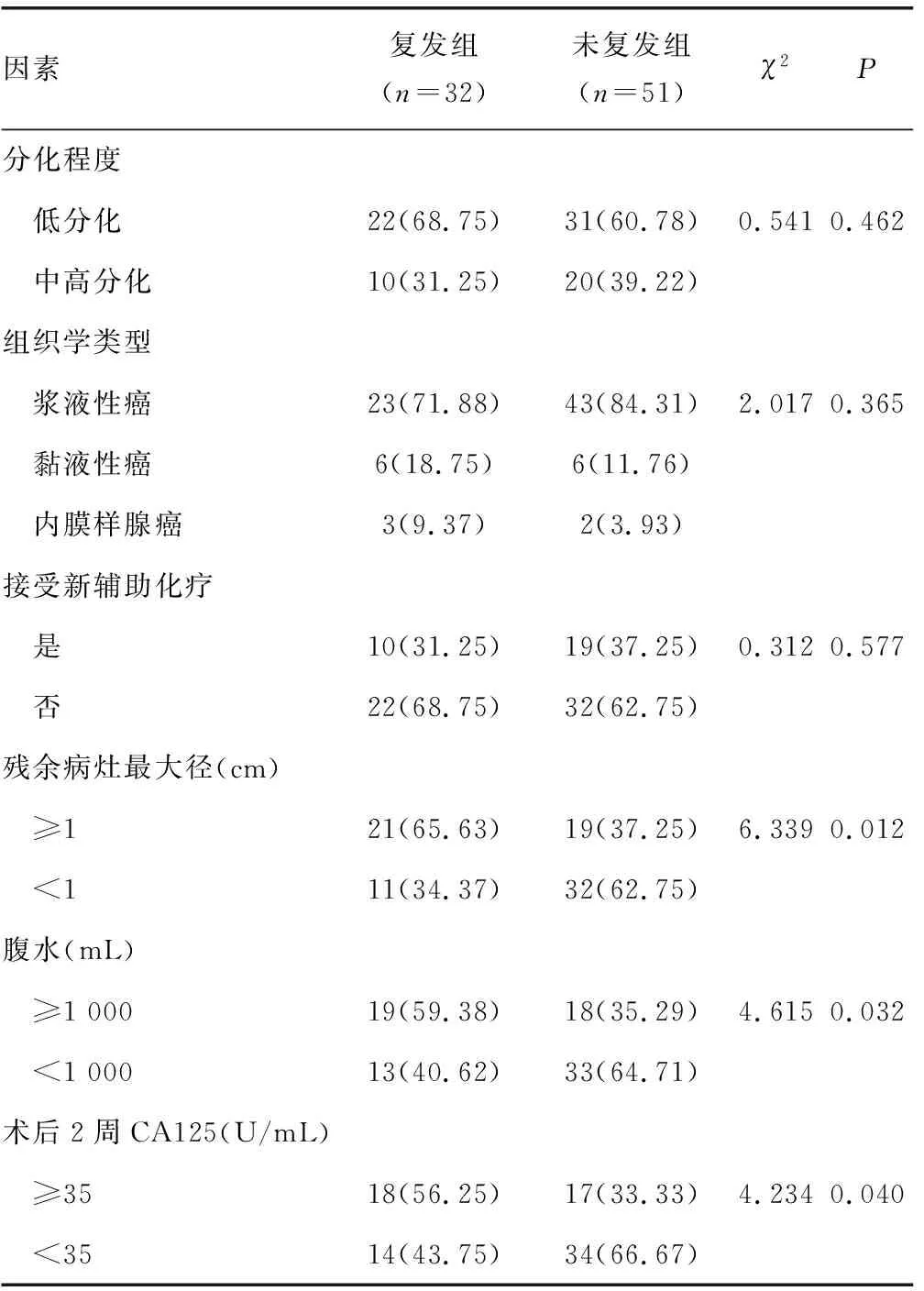
續表2 影響EOC患者PTCR后復發的單因素分析結果[n(%)]
2.4EOC患者PTCR后復發的多因素分析 以術后是否復發為因變量(賦值:0為“否”,1為“是”),以表1、表2中差異有統計學意義的因素/指標為自變量,賦值:FIGO分期(0為“Ⅲ期”,1為“Ⅳ期”)、殘余病灶最大徑(0為“<1 cm”,1為“≥1 cm”)、腹水(0為“<1 000 mL”,1為“≥1 000 mL”)、術后2周CA125(0為“<35 U/mL,”1為“≥35 U/mL”)、NDRG4(原值代入)、sB7-H4(原值代入)為自變量,建立非條件Logistic回歸模型,回歸過程采用逐步后退法(α退出=0.10,α納入=0.05),最終分析結果得出:殘余病灶最大徑≥1 cm、NDRG4水平降低、sB7-H4水平升高是EOC患者PTCR后復發的危險因素(P<0.05),見表3。
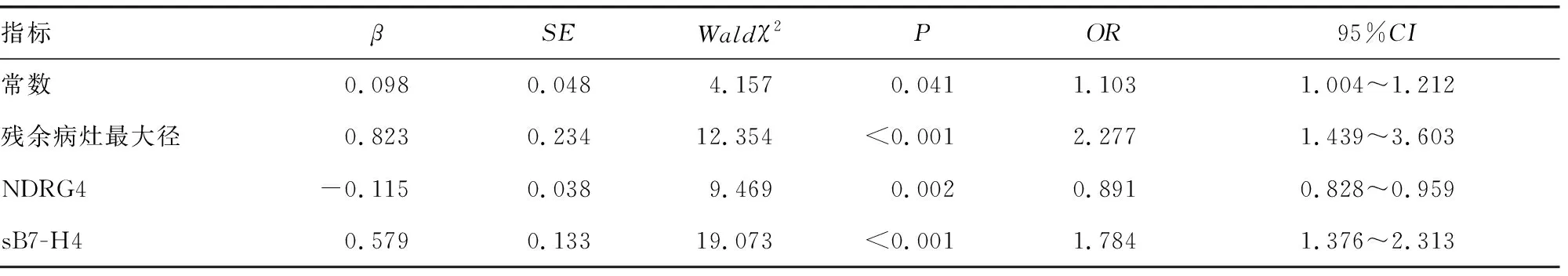
表3 影響EOC患者PTCR后復發的多因素Logistic回歸分析
2.5血清NDRG4、sB7-H4對EOC患者PTCR后復發的預測價值分析 進一步探討血清NDRG4、sB7-H4對EOC患者PTCR后復發的預測價值:以復發組為陽性樣本(n=32),以未復發組為陰性樣本(n=51),建立ROC曲線預測分析模型。兩指標單獨應用:兩指標均參考臨床實踐劃分成若干個組段,再以軟件擬合出ROC曲線讀取約登指數最大值點,對應計算理論閾值和各項參數。并按實測樣本計算靈敏度、特異度、準確度。聯合應用:基于前述回歸結果,建立LogP回歸預測模型,Log[P/(1-P)]=0.098-0.115×NDRG4+0.579×sB7-H4,而后仍參考上述方法(1)進行ROC曲線分析。分析結果顯示,兩指標聯合應用時,診斷效能較高,曲線下面積(AUC)及靈敏度、特異度、準確度均較各單獨應用指標有明顯提升。見表4。
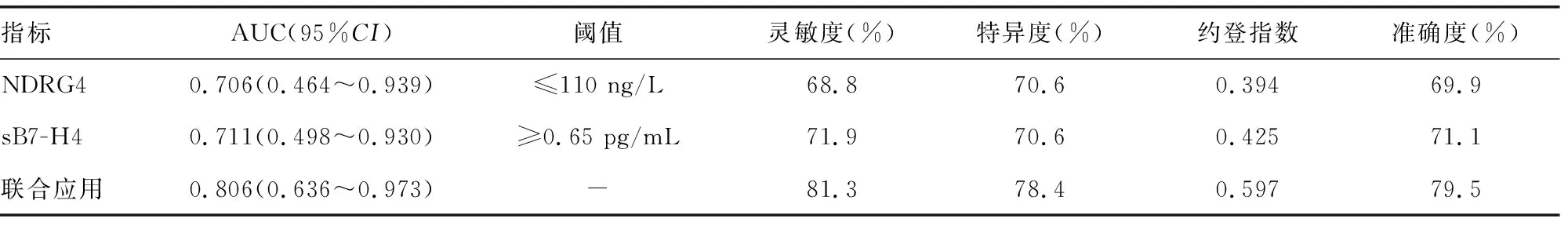
表4 NDRG4、sB7-H4單獨及聯合檢測預測EOC患者PTCR后復發的效能
3 討 論
EOC是最常見的卵巢癌類型,占卵巢癌全部病理類型的85%~90%[6]。EOC通常在中晚期被診斷出來,雖然在初次治療中可獲得較好的反應性,但復發率較高,目前對復發性EOC的治療多采取血管內皮生長因子抑制劑、酪氨酸激酶抑制劑等靶向治療,但療效非常有限,盡管總生存期可能有所延長,但是無進展生存期并沒有增加[7]。CA125既往被用于診斷和監測卵巢癌對治療的反應性[8],但沒有證據表明CA125可預測患者生存獲益。因此急需尋找能夠有效預測EOC治療反應性和復發的生物學標志物。
NDRG4屬于N-myc下游調控基因成員,主要在健康人腦部和心臟中表達,發揮保護神經和心肌細胞的作用[9]。NDRG4與惡性腫瘤的發生密切相關,但是其在惡性腫瘤中的作用尚存有爭議,已有研究證實,NDRG4在食管腺癌[10]、大腸癌[11]中表達下調,通過調控Cyclin D1、CDK4和CDK6表達[10]或通過抑制磷脂酰肌醇-3激酶-蛋白激酶B活性[11]發揮抑癌作用。但在侵襲性腦膜瘤中NDRG4表達上調,并發揮致癌基因作用[12]。本研究發現,復發組術前血清NDRG4水平低于未復發組(P<0.05),回歸分析結果顯示,血清NDRG4水平降低是EOC患者PTCR后復發的危險因素,說明術前血清NDRG4水平降低可能提示術后高復發風險。曹雪嬌等[13]報道顯示,卵巢上皮性腫瘤組織中及卵巢上皮性交界性腫瘤組織中NDRG4表達均低于正常卵巢組織,馬歡等[14]研究結果顯示,血清NDRG4水平降低與腫瘤臨床分期以及T、N分期增加有關。推測NDRG4表達缺失導致其抑制作用下降,促使腫瘤進展和復發,體外試驗也發現NDRG4表達上調可抑制Wnt/β-catenin細胞信號通路,進而阻止上皮間質轉化,降低卵巢癌惡性侵襲行為[15],沉默NDRG4后,卵巢癌細胞增殖能力增加[16]。本研究ROC曲線分析結果顯示,NDRG4單獨預測EOC患者PTCR后復發的AUC為0.706,靈敏度為0.688,特異度為0.706,表明檢測術前血清NDRG4水平一定程度上可預測腫瘤細胞減滅術后復發,分析原因為NDRG4缺失其抑癌作用減弱,導致癌癥進展和復發,但是NDRG4預測效能一般,表明EOC患者PTCR后復發可能受其他因素影響,需結合其他因素進行綜合評估。
sB7-H4是一種新型B7配體,可通過抑制T淋巴細胞活化和增殖,減少T淋巴細胞相關因子分泌,抑制腫瘤免疫應答,促使免疫逃逸及腫瘤發生和進展[17]。現有研究表明,sB7-H4與多種惡性腫瘤有關,肝細胞癌患者血清sB7-H4水平明顯增高,且與TNM分期、淋巴結轉移和分化程度有關[18]。sB7-H4在非小細胞肺癌患者血清中明顯高于良性肺腫瘤患者和健康志愿者,sB7-H4被認為是鑒別非小細胞肺癌的標志物[19]。本研究結果顯示,復發組血清sB7-H4水平明顯高于未復發組(P<0.05),回歸分析結果顯示高水平sB7-H4是EOC患者PTCR后復發的危險因素,提示sB7-H4水平增高與EOC患者PTCR后復發風險增高有關,術前檢測血清sB7-H4水平可為EOC術后復發預測提供參考。于文亮[20]報道結果也顯示,卵巢癌患者血清sB7-H4水平增高,且隨著FIGO分期的增高而增加,說明sB7-H4在卵巢癌發病和發展過程中發揮致癌基因作用。ROC曲線分析結果顯示,術前血清sB7-H4在預測EOC患者PTCR后復發中的AUC為0.711,與NDRG4接近。原因可能為sB7-H4參與腫瘤免疫逃逸,抑制抗腫瘤免疫反應,因此高水平sB7-H4提示腫瘤侵襲、轉移風險較大,術后復發的概率更高。但是單獨檢測sB7-H4預測效能仍一般,當聯合NDRG4和sB7-H4兩項指標后預測效能明顯提高,提示血清NDRG4水平降低同時sB7-H4水平增高預示著更高的復發風險,對臨床更具有價值。
多因素Logistic回歸分析顯示,殘余病灶最大徑與EOC患者PTCR后復發也存在密切關系,殘余病灶最大徑≥1 cm時,術后EOC復發風險較高,分析原因為殘余病灶最大徑越大,體內殘留腫瘤細胞越多,隨著腫瘤細胞增殖、生長、侵襲,可導致疾病復發和進展,臨床在實施PTCR時應最大程度切除腫瘤病灶,以降低復發率和提高存活率。
綜上所述,EOC患者PTCR后復發患者血清NDRG4水平降低,sB7-H4水平增高,低水平NDRG4、高水平sB7-H4是EOC患者PTCR后復發的危險因素,聯合兩項指標檢測可提高EOC患者PTCR后復發的預測價值。術前檢測血清sB7-H4水平增高、NDRG4水平下降的患者應高度警惕術后復發的可能,并采取積極的干預措施,加強術后隨訪,以避免和降低術后復發風險。

