高原藜麥色素提取工藝優化及色素穩定性
曹麗萍,蘇芳,周玉花,黨萬瑪,祁興仁,馬秀梅
青海柴達木職業技術學院 生物工程系(德令哈 817000)
藜麥是一種藜科草本植物,營養價值極其豐富,含有多種氨基酸、蛋白質、維生素、鐵、鈣、磷、鋅、葉酸等營養成分[1-4],此外黃酮類、酚類物質含量也較高[5-7],可為人體均衡補充營養,具有改善體質、調節免疫、增強抗病能力、調節人體酸堿平衡的功效[8-10]。
藜麥適合高原山地氣候,終年低溫地區,且種植海拔越高,品質越好。青海海西州得天獨厚的地理環境成為種植藜麥的主產區,近幾年,海西藜麥更因營養價值極高遠銷國內外,藜麥品質也在貿易中得到保證,一大批藜麥加工業蓬勃發展[11]。青海海西藜麥產業發展有其優勢,也勢必存在其弊端。青海海西生產的藜麥主要有白色、深紅色、棕色三色藜麥,種植面積及產量極其龐大[12-14],但在藜麥加工、成分研究方面,始終處于初級開發階段,市場上的藜麥產品主要是沒有經過加工的袋裝藜麥顆粒及藜麥作為輔助材料的代餐粉,產品單一,附加值低,對于顏色特殊的紅色藜麥未見天然色素提取及藜麥色素加工類產品。食用色素是食品中不可缺少的添加劑,分人工合成色素和天然色素。與人工素色相比,天然色素具有無毒、安全性高、色澤自然鮮艷、營養價值高和藥理功能等優越性,日益受到重視和青睞。天然色素現在主要是從植物、動物和微生物細胞中提取[15-18]。紅、棕藜麥為草本植物,營養價值極高[19-21],是否可以從紅、棕色藜麥中提取藜麥色素,并研究提取后藜麥色素的耐穩定性,進而可開發新天然色素,補充天然色素種類。
已開展天然色素開發的相關研究,其中不乏以紫皮洋蔥和莧菜等富含色素的植物為原料進行的研究,但是有關于紅、棕藜麥色素提取應用的技術并未出現。因此,試驗旨在探究青海海西棕色及深紅色藜麥提取色素最佳工藝的研究,并研究其色素的穩定性,為藜麥生產加工鏈及相關企業開發天然色素類產品提供指導意義,提高該天然色素產業的經濟效益,更是為后續藜麥的深加工提供參考價值,提高天然海西藜麥的潛在使用價值,提高藜麥及其產業的經濟效益。
1 材料與方法
1.1 材料與儀器
1.1.1 試驗材料
紅色藜麥(購于大潤發超市,經粉碎后備用);乙醇(分析純,天津市大茂化學試劑廠);氯化鈉、過氧化氫、氫氧化鈉、抗壞血酸(均為分析純,天津試劑廠)。
1.1.2 試驗儀器
BT224電子天平(北京賽多利斯儀器系統有限公司);T6型紫外可見分光光度儀(上海天美科學儀器有限公司);PHS-3C型酸度計(濟南泰醫生物技術有限公司);SC-5A超聲波清洗器(寧波海曙乙恒儀器有限公司);KH22R離心機(湖南凱達有限公司);PW80高速萬能粉碎機(天津市泰斯特儀器有限公司);HH-S4數顯恒溫水浴鍋(河北中捷儀器制造有限公司)。
1.2 試驗方法
1.2.1 藜麥色素提取劑的選擇
準確稱取10 g藜麥粉,利用水和乙醇作為提取劑,提取藜麥中的色素,通過計算藜麥色素提取含量確定最優提取溶劑。
1.2.2 單因素試驗
準確稱取10 g紅藜麥粉,利用超聲法提取紅藜麥粉中的色素,以藜麥色素得率為考察指標,研究乙醇體積分數(40%,50%,60%,70%和80%)、料液比(1∶50,1∶60,1∶70,1∶80和1∶90 g/mL)、超聲溫度(35,45,55,65,60和75 ℃)、超聲時間(25,30,40,50和60 min)對色素得率的影響。
1.2.3 正交試驗
在單因素試驗基礎上進行正交試驗,確定色素最優提取工藝,正交試驗因素水平見表1。

表1 正交試驗因素水平表
1.2.4 藜麥色素含量的計算
準確稱取10.00 g藜麥粉,分別在上述提取試驗、單因素試驗及正交試驗中進行浸提,離心收集濾液,在538 nm下測量吸光度,根據朗伯比爾定律(Lambert-Beer)A=εbc,藜麥色素含量與其吸光度呈正比,因此可采用式(1)計算藜麥色素含量,確定最佳提取工藝[22-23]。

式中:Bp為藜麥色素含量,mg/g;A為吸光度;DF為稀釋倍數;Mω為藜麥色素的相對摩爾質量,550 g/moL;V為溶液總體積,L;ε為甜菜紅素的摩爾消光系數,61 600 L/(moL·cm);L為光程長,1 cm;m為藜麥質量,g。
1.3 紅藜麥色素穩定性研究
通過正交試驗得出最優提取工藝時,以色素殘存率為指標,研究pH、溫度、光照、氧化劑、還原劑、VC和食鹽對藜麥色素穩定性的研究,并進行平行試驗。色素殘存率按式(2)計算[24-25]。

1.3.1 藜麥紅色素溶液配制
取10 g藜麥粉、在乙醇體積分數70%、料液比1∶60 g/mL、超聲提取溫度30 ℃、超聲提取時間55 min條件下提取色素,制得紅、棕藜麥色素,用蒸餾水定容至250 mL容量瓶中,密封避光保存備用。
1.3.2 光穩定性試驗
取20 mL上述紅藜麥色素溶液,分別置于自然光下與紫外燈下72 h,每隔12 h在538 nm處測定藜麥色素提取液的吸光度,按式(2)計算藜麥色素殘存率。
1.3.3 熱穩定性試驗
取6份20 mL上述藜麥色素溶液,分別置于25,35,45,55,65和75 ℃恒溫水浴55 min,每10 min在538 nm處測定色素提取液的吸光度,按式(2)計算藜麥色素殘存率。
1.3.4 耐氧化性試驗
取20 mL上述色素溶液,分別加入10 mL 0.2%,0.5%,1.0%,1.5%和2.0%的過氧化氫溶液,室溫放置0,6,12,24和48 h后在538 nm處測定色素溶液的吸光度,按式(2)計算色素殘存率。
1.3.5 酸堿穩定性試驗
取6份20 mL上述甜菜紅色素溶液,并做平行試驗。用HCl和NaOH調節色素溶液pH,分別將色素溶液調節成pH 4.0,6.0,7.0,8.0,9.0和11.0并在538nm處測定色素溶液的吸光度,觀察吸光度的變化,按式(2)計算色素殘存率。
1.3.6 護色試驗
取5份20 mL藜麥色素溶液,分別加入2 mL 0,0.5%,0.1%,2.0%和2.5%的抗壞血酸,室溫放置反應48 h,并分別在反應48 h,538 nm處測定藜麥色素的溶液吸光度,按式(2)計算藜麥色素殘存率。
1.4 數據統計與分析
采用SPSS軟件進行數據分析,兩組數據的顯著性差異采用ANOVA檢驗,顯著性水平為P<0.05。正交試驗采用SPSS軟件設計,并進行極差和方差分析。
2 結果與分析
2.1 藜麥色素提取劑的選擇
分別選用水和乙醇提取藜麥色素時,提取時間30 min時,研究顯示藜麥色素微溶于水,多溶于有機溶劑乙醇。提取時間24 h時,藜麥色素均溶于水和乙醇,但通過測定吸光度得出:水作為提取劑時,吸光度為0.054;乙醇作為提取劑時,吸光度為1.854。由此可以判斷藜麥色素在乙醇溶液中溶解率較大,因此試驗選用乙醇作為提取溶劑。
2.2 藜麥色素提取單因素試驗結果與分析
2.2.1 乙醇體積分數對藜麥色素提取的影響
如圖1所示:隨著乙醇體積分數增加,藜麥色素提取率呈現先增后減小趨勢,乙醇體積分數60%時,色素提取率最高,為0.818 g/mg,分析原因可能是適當體積分數的乙醇可破壞藜麥細胞脂質結構,加快了色素的溶出;乙醇體積分數70%時,色素提取率緩慢下降,當乙醇體積分數達到80%,提取含量下降到0.600 g/mg。究其原因可能是隨著乙醇體積分數的升高,藜麥中溶出的物質不只色素,還有很多糖類、酚類等非色素物質,導致雜質增多,使得藜麥色素得率低。經分析,選擇乙醇體積分數為50%,60%和70%用于正交試驗設計。

圖1 乙醇體積分數對藜麥色素提取的影響
2.2.2 料液比對藜麥色素提取率的影響
如圖2所示:隨著料液比中液體比例的增加,藜麥色素提取率呈先增后減趨勢,料液比1∶60 g/mL時,色素提取率最高,為0.892 mg/g。料液比在小于等于1∶70 g/mL時,藜麥色素提取率呈逐漸下降趨勢,分析原因可能是隨著乙醇比例的增加,溶出藜麥中的黃酮類及多酚類物質,雜質增多,影響色素的溶出。經分析,選擇料液比1∶50,1∶60和1∶70 g/mL用于正交試驗設計。
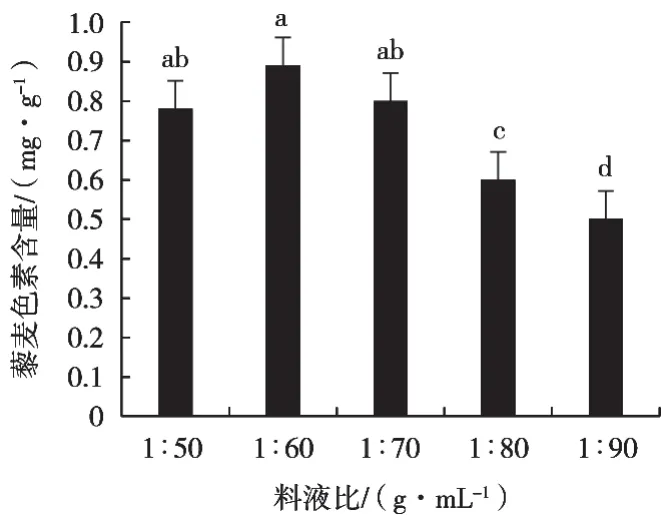
圖2 料液比對藜麥色素提取率的影響
2.2.3 超聲溫度對藜麥色素提取率的影響
如圖3所示:隨著超聲時間的增加,藜麥色素提取率呈先增后減小趨勢,超聲時間40 min時,色素的提取含量最高,為0.789 mg/g。超出40 min時,藜麥色素提取率呈逐漸下降的趨勢,分析原因:其一是藜麥色素耐熱性差,時間過高會破壞藜麥色素結構,導致色素提取率不高;其二是時間過高,導致乙醇揮發過快,溶劑減少,導致色素提取率差。綜上,選擇超聲時間25,30和40 min用于正交試驗設計。
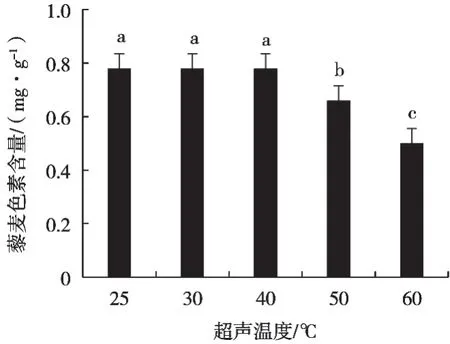
圖3 超聲溫度對藜麥色素提取率的影響
2.2.4 超聲時間對藜麥色素提取率的影響
如圖4所示,藜麥色素提取率隨著超聲溫度的增長呈現先增加后減少的趨勢。超聲溫度55 ℃時,提取含量最高,為0.793 mg/g。超聲溫度35 ℃時,提取含量較低,為0.456 mg/g,原因可能是提取時間太短,乙醇還未滲透藜麥的細胞壁和細胞膜,導致色素部分溶出,提取量較低。提取溫度75℃時,色素提取含量急劇減少,原因可能是:在75 ℃時,色素在之前提取過程中已全部溶出,導致提取率低;也可能是隨著提取溫度的增大,其他雜質析出,因此色素提取含量低。經分析,選擇超聲提取溫度45,55和65 ℃用于正交試驗設計。

圖4 超聲時間對藜麥色素提取率的影響
2.3 正交試驗
由表2可知,影響藜麥色素提取因素大小順序是B>A>D>C。在正交試驗中,藜麥色素提取最佳工藝配方為A2B2C3D1,即乙醇體積分數60%、料液比1∶60 g/mL、超聲時間40 min、超聲溫度45 ℃,此時色素提取率最高,提取含量為0.897 mg/g。
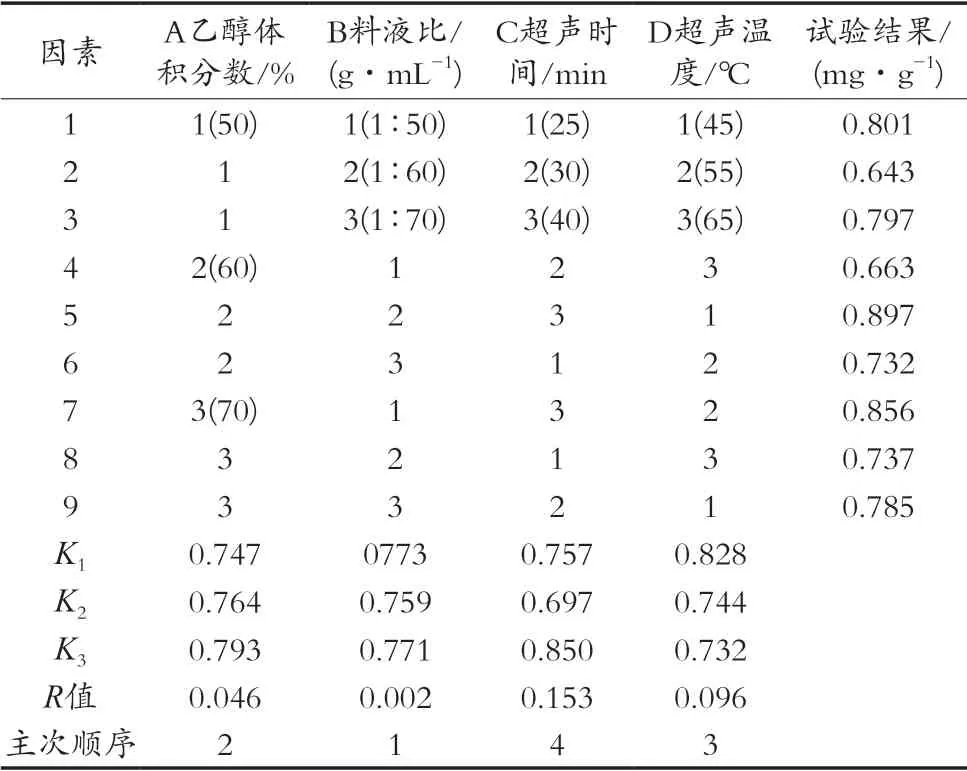
表2 正交試驗結果
由于理論最優水平A3B1C3D1(即乙醇體積分數為70%、料液比為1∶50 g/mL、超聲時間為40 min、超聲溫度為45 ℃)與正交試驗最優水平A2B2C3D1(即乙醇體積分數60%、料液比1∶60 g/mL、超聲時間40 min、超聲溫度45 ℃)結果不一致,因而進行驗證試驗以確定最佳水平組合。由表3分析比較得1組的結果具有顯著性差異,因而選擇最佳水平組合為A2B2C3D1,即乙醇體積分數60%、料液比1∶60 g/mL、超聲時間40 min、超聲溫度45 ℃。

表3 驗證試驗
2.4 藜麥色素穩定性研究
2.4.1 藜麥色素光穩定性試驗
如圖5所示,藜麥色素在自然光和紫外光下隨著照射時間的增大色素均呈現下降趨勢,但色素的降解率很低。藜麥色素在自然光下殘存率達到85.23%,在紫外光下殘存率為89.21%,表明在照射72 h內藜麥色素對光不敏感,尤其對紫外光不敏感,色素的降解率低。但熊勇[18]、任文明等[26]的研究表明,色素不宜長時間暴露在自然光下,隨著時間的延長,色素的降解會越來越快,直至降解完全。綜上,避光保藏有利于藜麥色素的保存,便于加工利用。
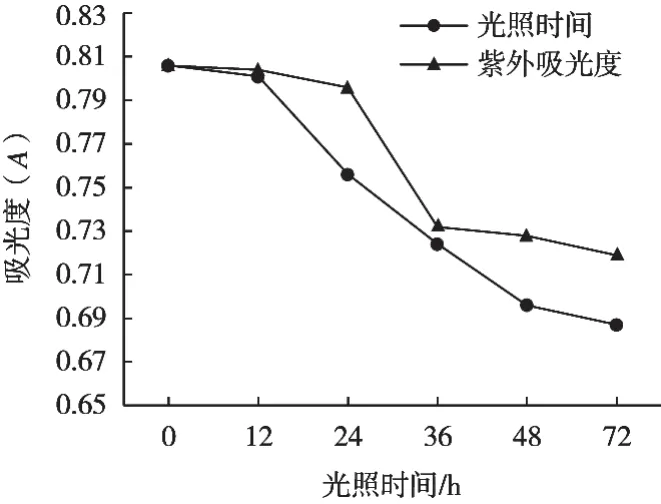
圖5 藜麥色素光穩定性試驗結果
2.4.2 藜麥色素熱穩定性試驗結果
由圖6可知,隨著超聲溫度的升高,藜麥色素的殘存率先緩慢平穩下降,后急劇下降。超聲溫度25 ℃時,色素殘存最高,吸光度為0.804,且藜麥色素顏色呈現黃綠色;超聲溫度75 ℃時,色素急劇降解到最低,測得的吸光度為0.723,藜麥色素顏色呈現出淡黃綠色,且經75 ℃處理后藜麥色素殘存率下降到53.73%。分析原因:藜麥色素對高溫較敏感,在高溫條件下會發生降解現象,破壞色素化學結構,破壞穩定性。因此藜麥色素建議使用溫度應在30 ℃左右,溫度不可過高。
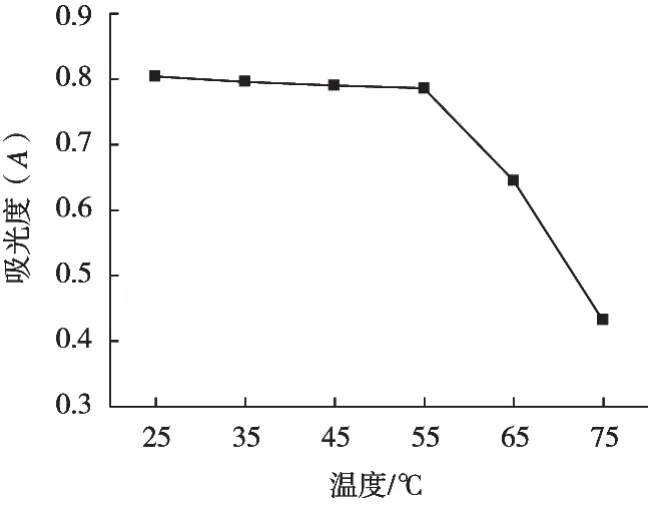
圖6 藜麥色素熱穩定性試驗結果
2.4.3 藜麥色素耐氧化性試驗結果
由圖7可知,隨著H2O2濃度的增大及處理時間的增長,藜麥色素殘存率5個處理組都呈現降低趨勢,但下降趨勢總體不明顯。5個處理組的試驗結果表明,不同濃度的氧化劑隨著氧化時間的增長表現出不同程度的氧化作用,濃度越低氧化作用越小,濃度越大氧化作用越大,用最大濃度(2.0%)H2O2處理藜麥色素48 h后,在5個處理組中色素的降解率最高,但色素殘存率為97.17%,保存率較高。這表明,強氧化劑H2O2對藜麥色素具有一定的保護作用,藜麥色素的耐氧化性較好。

圖7 藜麥色素耐氧化性試驗結果
2.4.4 藜麥色素耐酸堿性試驗結果
由表4可知,酸堿環境對藜麥色素影響較大,藜麥色素溶液pH在4.0~7.0范圍時色素的吸光度隨pH的增大而增加,且溶液中色素的顏色由淡黃色變為深黃色。在pH 7.0時,顏色最深,吸光度最大,為1.092;pH在8.0~11.0時溶液的吸光度隨著pH的增大而逐漸減小,顏色逐漸變淺,但pH為9.0時,出現深黃色,顏色加深,分析原因是可能是當pH 9.0時,藜麥色素中的酚羥基在堿性條件下電離成酚氧負離子,供電性大大增強,同時,藜麥色素中的供吸電子協同作用加強,從而產生深色效應,后pH為11.0時,又恢復淡黃色。綜上,建議藜麥色素最佳使用pH范圍為4.0~8.0。

表4 藜麥色素酸堿穩定性研究試驗結果
2.4.5 藜麥色素護色試驗
如圖8所示,未添加護色劑時,藜麥色素殘存率隨著放置時間的延長呈現緩慢下降的趨勢,殘存率由99.76%下降到99.38%。添加0.5%護色劑時,色素殘存率曲線較未添加護色劑下降緩慢,由99.76%下降到99.50%,表明0.5%的護色劑已發揮護色作用,但效果不明顯;添加1.5%的護色劑時,色素殘存率保持穩定,無下降趨勢,且色素殘存率一直穩定在99.76%;添加2.0%的護色劑時,色素殘存率有小幅上升趨勢,表現出護色劑的增色作用。由此可知,不同濃度的抗壞血酸對藜麥色素殘存率的護色效果差異較大,較低濃度的護色劑,護色效果較差,但較高濃度的護色劑可保護色素,降低色素降解的速率,也可起到增色作用,故建議在藜麥色素的實際應用中應適量加入一定濃度的抗壞血酸,起增色作用。
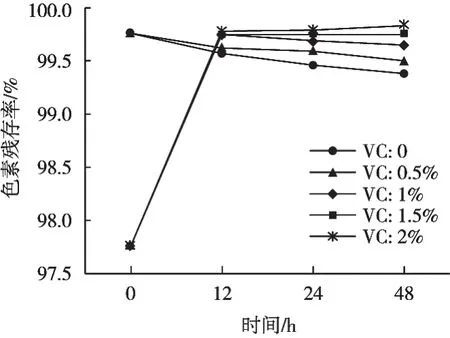
圖8 藜麥色素耐氧化性試驗結果
3 結論
選用青藏高原紅藜麥為主原料,通過單因素試驗和正交試驗得到藜麥色素的最佳提取方法:乙醇體積分數60%、料液比1∶60 g/mL、超聲時間40 min、超聲溫度45 ℃。對色素進行穩定性研究,結果表明藜麥色素在適當酸堿、熱條件及氧化劑作用下都有較好的穩定性,并在pH 4.0~8.0范圍內色素呈現較好的顏色,為黃綠色。但藜麥色素并不耐光,不宜長時間放置在自然光下。綜上,藜麥色素應盡量低溫、避光、低酸性條件下儲存和使用,適當添加抗壞血酸可有效提高藜麥色素顏色強度。

