基于DBS改性的硅基DtBuCH18C6吸附劑的制備及其對Sr(Ⅱ)的吸附性能研究
王乙淇,毛 聰,郭建鋒,桑紅吉,吳 艷,*
(1.上海交通大學 核科學與工程學院,上海 200240;2.中核四〇四有限公司,甘肅 嘉峪關 732850)
對高放廢液中長壽命核素進行分離提取,不僅可提高乏燃料后處理和地質處置過程中的安全性,還可降低放射性核素對環境及公眾安全的危害。90Sr的裂變產額為5.89%,作為高能量β放射源(0.546 MeV),其半衰期較長(T1/2=28.8 a),且釋熱量大(100.51 W/MtU),是高放廢液中前100年放射性及熱量的主要來源[1]。為實現放射性廢物的減容、防止輻射熱在核廢物長期儲存過程中引起基體變形[2]并保護公眾的健康安全[3],在高放廢液的處理處置過程設計中有必要考慮90Sr的去除。此外,純化后的90Sr還可作為醫藥和工業中的輻射源和熱源重復使用[4],從而實現放射性核素的循環利用。
針對高放廢液中分離90Sr的方法,國內外均已進行了廣泛研究,主要有沉淀法、離子交換法、溶劑萃取法、萃取色層法等[5]。由于離子交換法對90Sr的選擇性較差,產品收率及凈化效果有待提高,適宜在高放環境中連續且大量進行分離操作的溶劑萃取法成為分離90Sr的首選方法之一[6]。冠醚具有獨特的冠腔結構,其中心腔帶負電,且對特定半徑的金屬陽離子有較高的選擇性,同時由于冠醚良好的水解穩定性與耐輻照性能,被認為是理想的90Sr選擇性萃取劑[7]。其中,18冠6及其衍生物,如4′,4′(5″)-二(叔丁基環己基)-18-冠-6(DtBuCH18C6)的冠腔尺寸與90Sr離子的半徑匹配良好,可通過絡合作用選擇性地對溶液中的90Sr進行分離提取。
近年來,萃取色層法的研究得到了科研工作者的關注。該方法具有有機試劑與固相載體相結合、核素分離效果好、有機廢液的產生量相對較少和設備及操作流程簡單等特點[8]。由于吸附劑對90Sr的吸附效果很大程度上受負載冠醚的基體材料性能的影響,基于不同載體材料的固體吸附劑得到了廣泛研究。Ma等[9]將雙環己基-18-冠-6浸漬于具有高比表面積和離子交換能力特性的鈦酸鹽納米管中制成復合吸附劑,在酸性條件下可將95%以上的Sr(Ⅱ)從溶液中分離。Mu等[10]通過將4′-氨基苯并-18-冠-6嵌入到α-磷酸鋯的層間結構中制備了AM-ZrP吸附劑,其對Sr(Ⅱ)的吸附速度快且選擇性好。Zhang等[11]制備了硅基冠醚吸附劑,其在2 mol/L硝酸條件下的吸附容量可達317.0 cm3/g。
在前期探索過程中,本課題組研發了高性能的冠醚復合吸附劑[12],將DtBuCH18C6負載于二氧化硅與聚合物的復合粒子(SiO2-P)孔道內,研究發現,與TBP、正辛醇等對比,以正十二烷醇(Dodec)為分子改性劑所合成的吸附劑具有較好的吸附效果、機械強度、耐酸及耐輻照性能,實現了模擬高放廢液中Sr(Ⅱ)的動態選擇性分離。但上述材料在低酸條件下均對Sr(Ⅱ)的吸附效果差,高酸條件下的效果也期待進一步提高,限制了吸附劑的適用范圍。因此,本研究擬在前期研究的基礎上,利用分子改性劑十二烷基苯磺酸對DtBuCH18C6的吸附親和力進行改善,通過將DtBuCH18C6、正十二烷醇和十二烷基苯磺酸在真空負壓條件下負載至SiO2-P載體的孔隙中,合成新型的(DtBuCH18C6+DBS+Dodec)/SiO2-P吸附劑,對吸附劑的表面形態、化學穩定性、吸附機理、吸附動力學及解吸性能進行分析,以評價新型吸附劑對高放廢液中90Sr分離提取的應用前景。
1 方法
1.1 主要試劑
4′,4′(5″)-二(叔丁基環己基)-18-冠-6(≥90%),十二烷基苯磺酸(90%),正十二烷醇(≥99%),硝酸鍶、硝酸銫、硝酸鑭等硝酸鹽試劑及其對應的金屬陽離子標準溶液均為市售分析純試劑。SiO2-P,參照文獻[13]制備,粒徑范圍為30~70 μm。SiO2-P中的P指聚苯乙烯(SDB),固定在多孔SiO2顆粒上,負載量為20%,孔隙直徑約為50 nm。
1.2 (DtBuCH18C6+DBS+Dodec)/SiO2-P吸附劑合成
取適量DtBuCH18C6與正十二烷醇于圓底燒瓶中,攪拌溶解,加入SiO2-P后在室溫下充分攪拌后靜置。調節條件至40 ℃、負壓,利用旋轉蒸發儀(EYELA N-1100)將有機溶劑浸漬到二氧化硅孔隙中,在40 ℃下真空干燥1 d,得到(DtBuCH18C6+DBS+Dodec)/SiO2-P吸附劑。
1.3 材料表征
采用Sirion 200高分辨場發射掃描電子顯微鏡(SEM)研究吸附劑表面形態;使用Shimadzu DTG-60熱重-差熱(TG-DTA)分析法在空氣氛圍下以10 ℃/min的升溫速率對吸附劑熱穩定性情況進行評價;采用Nicolet 6700傅里葉變換紅外光譜(FT-IR)在4 000~450 cm-1的波數范圍內研究吸附劑的官能團組成;采用Kratos AXIS Ultra DLD X射線光電子能譜(XPS)分析吸附前后元素結合能的變化;采用Shimadzu VCPH總有機碳分析儀(TOC)分析浸泡液中有機物的泄漏量,評價吸附劑穩定性能。
1.4 吸附實驗
采用靜態吸附實驗,分別考察硝酸濃度、溫度、共存離子對(DtBuCH18C6+DBS+Dodec)/SiO2-P吸附性能的影響。具體方法為:將5 mmol/L金屬陽離子溶液(5 mL)與50 mg吸附劑在離心管中混合,放置于恒溫水浴搖床(Tokyo RIKAKIKA CO., Ltd.)中反應適當時間,金屬離子由Shimadzu 7510電感耦合等離子體發射光譜儀(ICPS)及SP3880原子吸收光譜(AAS)進行測量。
分配系數(Kd)、平衡吸附容量(qe)和吸附率(R)為吸附性能評價指標,其計算公式如下:
(1)
(2)
(3)
式中:co和ce分別為溶液中金屬離子的初始和平衡濃度(mmol/L);V和m分別為溶液的體積(L)和吸附材料的質量(g)。
1.5 吸附劑的重復利用
在3 mol/L硝酸條件下,使1 g吸附劑與200 mg/L Sr(Ⅱ)溶液(50 mL)進行吸附反應,得到吸附有Sr(Ⅱ)的吸附劑樣品。將其分別與不同種類的洗脫劑接觸不同的時間,并改變吸附劑與洗脫劑的液固比得到吸附劑的最佳洗脫條件。洗脫率(E)的計算公式如下:
(4)
式中,cd為洗脫后溶液中Sr(Ⅱ)的濃度,mmol/L。
2 結果與討論
2.1 吸附劑表征
(DtBuCH18C6+DBS+Dodec)/SiO2-P吸附劑的SEM圖像示于圖1。由圖1可見,吸附劑呈均勻球狀體,粒徑約為50 μm,結構完好,表面僅有少量的絮狀有機物殘留,但基本保持光滑,大部分表面有機試劑成功被負載至SiO2-P孔隙中。
張三爺有和當時大部分武人同樣的經歷,保過鏢、護過院、當過武師,但除此以外,他還有大多數武人沒有的經歷,他曾當過清朝練勇局的把總,宣統年間還護送過去西藏傳詔的欽差。
(DtBuCH18C6+DBS+Dodec)/SiO2-P吸附劑在30~800 ℃范圍內的TG-DTA曲線如圖2所示。分析圖2可知,溫度小于90 ℃時,由于表面水和結晶水的揮發,吸附劑存在少量的質量變化;90 ℃以上的失重主要為負載有機試劑引起的質量變化,其失重過程由95.03~200.74 ℃(階段Ⅰ)、200.74~324.92 ℃(階段Ⅱ)及324.92~682.59 ℃(階段Ⅲ)三個部分組成。階段Ⅰ中損失的質量為21.91%,與DtBuCH18C6和正十二烷醇的理論設計質量(22%)相匹配。前期研究[12]結果表明,冠醚DtBuCH18C6約在170 ℃處發生熱解并吸收熱量,而本文在188.05 ℃處觀察到吸附劑向下的放熱峰,推測是由于改性劑DBS的添加使階段Ⅰ的熱量變化發生了改變。階段Ⅱ的質量損失為18.81%,且伴隨著在305.39 ℃處向上的吸熱峰,推測在此溫度范圍內存在分子改性劑DBS的熱解;階段Ⅲ則是由SiO2-P中的聚合物 (SDB)分解引起,質量損失為15.05%,這與前期研究[12]中SiO2-P載體的熱重分析值一致。由上述結果可知,在溫度由30 ℃升至800 ℃的過程中,吸附劑的總失重量為原始質量的55.45%,其中有40.40%的有機試劑被負載在SiO2-P的孔道中,同時SiO2-P載體的質量占吸附劑質量的59.60%。理論設計中,負載的有機試劑與SiO2-P載體的質量分別占總吸附劑質量的40.00%和60.00%,上述熱重分析所得結果與該理論設計值基本相符。

圖2 (DtBuCH18C6+DBS+Dodec)/SiO2-P的TG-DTA曲線Fig.2 TG-DTA curve for (DtBuCH18C6+DBS+Dodec)/SiO2-P


圖3 (DtBuCH18C6+DBS+Dodec)/SiO2-P與SiO2-P的FT-IR譜Fig.3 FT-IR spectra for (DtBuCH18C6+DBS+Dodec)/SiO2-P and SiO2-P
(DtBuCH18C6+DBS+Dodec)/SiO2-P在3 mol/L硝酸條件下吸附Sr(Ⅱ)前后的XPS譜示于圖4。由圖4a可見,吸附劑的寬譜掃描檢測出了O 1s、C 1s、S 2p和Si 2p的特征峰,其中C與S元素分別占總元素質量濃度的40.33%和4.71%。由圖4b可見,與Sr(Ⅱ)溶液(1 200 mg/L,3 mol/L HNO3)進行相互作用后,在134.8 eV附近檢測到Sr 3p特征峰,證實了吸附劑對Sr(Ⅱ)的吸附效果,且吸附劑中的O通過與Sr(Ⅱ)離子形成Sr—O鍵來實現對其穩定吸附。由于在DtBuCH18C6通過冠腔與Sr(Ⅱ)離子進行配對的過程中,Sr(Ⅱ)離子與冠腔中6個氧電子之間產生強靜電相互作用[16],Sr 3p譜中的Sr—O鍵特征峰可佐證吸附劑對Sr(Ⅱ)的吸附過程存在DtBuCH18C6與Sr(Ⅱ)離子的配對。同時,對吸附劑吸附前、0.5 mol/L硝酸濃度及3 mol/L硝酸濃度條件下吸附Sr(Ⅱ)后的S 2p譜(圖4c)進行分析。在0.5 mol/L硝酸濃度下吸附Sr(Ⅱ)前后磺酸基中S元素的結合能發生了明顯的變化,峰值由167.31 eV增長至168.05 eV;在3 mol/L硝酸濃度下,吸附前后S元素的結合能變化相對0.5 mol/L硝酸濃度下較小,峰值由167.31 eV增長至167.60 eV。可以推測在硝酸濃度較低及較高的條件下,吸附劑對Sr(Ⅱ)的吸附過程中都有DBS的參與,硝酸濃度條件的變化對該作用存在一定的影響。

圖4 (DtBuCH18C6+DBS+Dodec)/SiO2-P的XPS譜Fig.4 XPS spectra of (DtBuCH18C6+DBS+Dodec)/SiO2-P
2.2 吸附劑的化學穩定性
分別在25、50 ℃條件下,將0.1 g(DtBu-CH18C6+DBS+Dodec)/SiO2-P吸附劑與不同濃度的硝酸溶液(5 mL)作用1 d,測定浸泡液中有機成分的總有機碳(TOC),即為負載有機物的泄漏量,結果示于圖5。進一步將有機試劑的泄漏量與2.1節中有機試劑的負載量進行比較得到有機物質的泄漏率,以評價吸附劑化學穩定性。在25 ℃、0.5~7 mol/L硝酸濃度下,泄漏至硝酸溶液中的有機物的TOC量穩定在49 ppm左右;當溫度升高至50 ℃時,TOC量僅上升到50.63 ppm左右,有機物的泄漏量增幅僅為3.3%。考慮到負載的有機成分包括DtBuCH18C6、DBS、正十二烷醇,組成較復雜,將溶液中的有機物假設全部為DtBuCH18C6的泄漏,通過TOC值計算可知,即使在50 ℃、硝酸濃度為7 mol/L條件下,吸附劑中DtBuCH18C6的泄漏量也小于2.03%。分子修飾劑正十二烷醇的添加有效降低了DtBuCH18C6從SiO2-P載體中的泄漏,使吸附劑在不同酸度條件下都具有較好的化學穩定性。
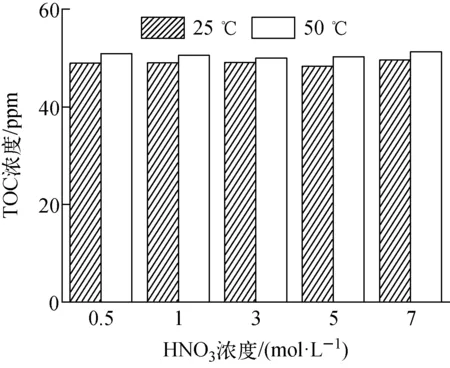
圖5 (DtBuCH18C6+DBS+Dodec)/SiO2-P在硝酸溶液中的TOCFig.5 TOC of (DtBuCH18C6+DBS+Dodec)/SiO2-P in nitric acid solution
2.3 吸附分配系數
Sr(Ⅱ)濃度為5 mmol/L、液固比為0.05 L/g、溫度為25 ℃、硝酸濃度為0.5~5 mol/L時,Sr(Ⅱ)的吸附分配系數示于圖6。為分析分子改性劑DBS的添加對Sr(Ⅱ)吸附的促進效果,在相同條件下使用(DtBuCH18C6+Dodec)/SiO2-P進行了對比實驗。由圖6可見,添加DBS改性劑后,吸附劑對Sr(Ⅱ)的分配系數在0.5~1 mol/L的硝酸濃度范圍內緩慢下降,硝酸濃度為0.5 mol/L時Kd值高達392.19 cm3/g;隨著酸度的進一步升高,Kd在1~3 mol/L范圍內逐漸上升,而硝酸濃度大于3 mol/L后有下降趨勢,在3 mol/L時存在相對較大值355.02 cm3/g。與(DtBuCH18C6+Dodec)/SiO2-P相比,添加DBS改性劑后的吸附劑,在低硝酸濃度(0.5~1 mol/L)下的Kd值明顯提升了2.5~10倍,而在較高硝酸濃度(3~5 mol/L)條件下,Kd值也提高至2倍左右。

圖6 不同硝酸濃度下兩種吸附劑對Sr(Ⅱ)的分配系數Fig.6 Kd of two different adsorbents at varying nitric acid concentration
在前期研究中,僅將正十二烷和DBS負載到SiO2-P中制備成(DBS+Dodec)/SiO2-P的實驗結果表明,(DBS+Dodec)/SiO2-P在0.5~5 mol/L硝酸濃度范圍內對Sr(Ⅱ)基本無吸附[17]。因此推測,添加DBS的(DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)的吸附主要存在3種反應過程:1) DBS中磺酸根基團作為配陰離子參與DtBuCH18C6與Sr(Ⅱ)的絡合反應(式(5));2) 硝酸的鹽析作用(式(6));3) 競爭作用(式(7))。在硝酸濃度低于1 mol/L時,吸附過程主要是DBS中的磺酸根作為配位離子與DtBuCH18C6和Sr(Ⅱ)形成離子絡合性萃取物;當酸度為1~3 mol/L時,溶液中的硝酸根離子含量增加,其作為鹽析劑的作用逐漸顯著,并與DBS呈現出協同作用,較好地提升了冠醚對Sr(Ⅱ)的絡合效果;而當酸度大于3 mol/L后,硝酸分子與DtBuCH18C6的反應會對Sr(Ⅱ)的絡合產生競爭,從而導致分配系數逐漸下降。
Sr(RSO3)2·DtBuCH18C6
(5)
Sr(NO3)2·DtBuCH18C6
(6)

HNO3·DtBuCH18C6
(7)
其中,R代表DBS中的烷基。
2.4 共存離子對于吸附性能的影響

圖7 (DtBuCH18C6+DBS+Dodec)/SiO2-P對各金屬的分配系數Fig.7 Kd value of different metal ions on (DtBuCH18C6+DBS+Dodec)/SiO2-P
由于高放廢液中核素的組分復雜,材料的吸附性能會受到多種共存離子的影響,因此配置了含Sr(Ⅱ)、Zr(Ⅳ)、Cs(Ⅰ)、Ru(Ⅲ)、Re、Pd(Ⅱ)、Mo(Ⅴ)、Gd(Ⅲ)、Sm(Ⅲ)、Nd(Ⅲ)、La(Ⅲ)多種金屬陽離子混合的模擬高放廢液(各金屬陽離子濃度均為5 mmol/L,硝酸濃度為0.5~7 mol/L),研究(DtBuCH18C6+DBS+Dodec)/SiO2-P在多離子共存的模擬高放廢液中對Sr(Ⅱ)的吸附選擇性(25 ℃,液固比為0.05 L/g),結果示于圖7。由圖7可知,吸附劑對Sr(Ⅱ)的分配系數遠大于其他離子,除Zr(Ⅳ)外,0.5~7 mol/L硝酸濃度范圍內吸附劑對其他離子的分配系數均低于10 cm3/g。這是由于在低酸下,Zr(Ⅳ)易與Mo(Ⅴ)離子形成沉淀,導致其在溶液中的含量減小,但Zr(Ⅳ)的分配系數僅為59.45 cm3/g。此外,在共存離子存在下,吸附劑對Sr(Ⅱ)的分配系數與僅對Sr(Ⅱ)進行單一吸附的情況下無明顯變化。冠醚因具有通過冠腔的尺寸與目標離子直徑相匹配形成絡合物從而實現對目標離子的吸附特性[18],使得(DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)有優越的選擇吸附性能。
2.5 吸附動力學
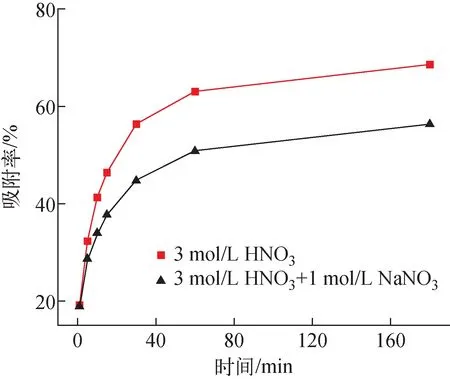
圖8 接觸時間對Sr(Ⅱ)吸附率的影響Fig.8 Effect of contact time on uptake rate of Sr(Ⅱ)
高放廢液一般是由2~3 mol/L的硝酸溶液溶解得到的,且含有一定量的鈉離子[19]。根據2.3節的實驗結果,吸附劑在3 mol/L的硝酸溶液中具有較好的吸附性能,因此進一步對吸附劑在3 mol/L硝酸溶液中的動力學特性進行研究,同時研究3 mol/L硝酸與1 mol/L硝酸鈉混合溶液對吸附劑吸附動力學性能的影響(5 mmol/L Sr(Ⅱ),液固比為0.05 L/g,25 ℃),結果示于圖8。由圖8可見,在3 mol/L硝酸溶液中,反應速度在前60 min內快速上升,吸附率達到63%,在60~180 min內,吸附反應逐漸趨向平衡。該結果表明,在反應初期,吸附劑對Sr(Ⅱ)的吸附為表面吸附,其過程快速且貢獻了平衡吸附容量的主要部分,隨著反應時間的延長,由于表面吸附位點減少,吸附由表面向內部擴散,過程相對緩慢。在添加1 mol/L硝酸鈉的混合溶液中,Sr(Ⅱ)吸附率的變化趨勢基本與3 mol/L硝酸條件下一致,而平衡吸附率下降為原來的77.7%。Na(Ⅰ)與Sr(Ⅱ)的離子半徑分別為0.194 nm與0.226 nm,均可被吸附劑中負載的DtBuCH18C6的冠醚腔所捕集[20],吸附劑在吸附Sr(Ⅱ)的同時對Na(Ⅰ)也有一定的吸附[21],Na(Ⅰ)與Sr(Ⅱ)的競爭性吸附使得達到吸附平衡后吸附劑對Sr(Ⅱ)的吸附率下降。由于Sr(Ⅱ)的離子半徑與冠醚腔的尺寸更吻合[22],在添加1 mol/L硝酸鈉的混合溶液中,吸附劑對Sr(Ⅱ)仍有較高的吸附率。
為進一步研究(DtBuCH18C6+DBS+Dodec)/SiO2-P的吸附動力學機制,使用準一級和準二級吸附動力學模型對反應數據進行擬合。線性準一級及準二級動力學方程如下:
(8)
(9)
其中:qt為t(min)時刻的吸附量(mg/g);k1為準一級動力學方程速率常數;k2為準二級動力學方程速率常數。
采用式(8)、(9)對圖8中實驗數據進行擬合,擬合結果示于圖9,擬合參數列于表1。由表1可見,在3 mol/L硝酸及3 mol/L硝酸混合1 mol/L硝酸鈉的條件下,準一級動力學模型擬合的相關系數均低于0.85,且得到的飽和吸附容量與實驗值相差較大,遠大于實驗值31.73 mg/g與27.48 mg/g;準二級動力學模型擬合后的相關系數均達到0.999,根據擬合數據獲得吸附平衡容量與實驗值基本一致,表明(DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)的吸附符合準二級動力學特性,是一個受化學吸附過程控制的速率控制過程。

圖9 (DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)吸附的動力學擬合結果Fig.9 Kinetic fitting result of Sr(Ⅱ) adsorption on (DtBuCH18C6+DBS+Dodec)/SiO2-P
2.6 吸附等溫線
為研究25 ℃下3 mol/L硝酸溶液中(DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)的吸附機理,采用Langmuir、Freundlich等溫線模型(式(10)、(11))對不同Sr(Ⅱ)濃度的硝酸溶液的平衡吸附容量進行擬合,實驗及擬合結果示于圖10,擬合參數列于表2。

表1 (DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)吸附的動力學擬合參數Table 1 Kinetic parameter evaluated for Sr(Ⅱ) adsorption on (DtBuCH18C6+DBS+Dodec)/SiO2-P
Langmuir等溫線模型:
(10)
Freundlich等溫線模型:
(11)
其中:qm為飽和吸附容量,mg/g;KL為Langmuir參數;KF為Freundlich參數。

圖10 (DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)的吸附等溫線Fig.10 Non-linear isotherm plot of Sr(Ⅱ) adsorption data using (DtBuCH18C6+DBS+Dodec)/SiO2-P
由表2可見,兩個模型的擬合相關系數均在0.94以上,分別為0.997和0.941,說明兩個模型均都具有較好的擬合效果。由于Langmuir等溫線模型的相關系數結果更接近于1,說明吸附劑對Sr(Ⅱ)的吸附過程更接近于表面均一的單層吸附,吸附劑表面的點位數量一定,且各吸附點之間沒有Sr(Ⅱ)的轉移運動[23]。根據Langmuir等溫線模型得到的擬合結果,達到吸附平衡時Sr(Ⅱ)的最大吸附量約為42.13 mg/g,接近實驗得到的最大吸附容量40.69 mg/g,Langmuir等溫線模型對吸附劑的最大吸附容量的估計結果有較好的準確性。

表2 (DtBuCH18C6+DBS+Dodec)/SiO2-P對Sr(Ⅱ)的吸附等溫線擬合參數Table 2 Parameter obtained from isotherm analysis of Sr(Ⅱ) adsorption data using (DtBuCH18C6+DBS+Dodec)/SiO2-P
2.7 吸附劑的重復利用性
對吸附Sr(Ⅱ)后的吸附劑進行洗脫,一方面可實現對放射性90Sr的回收,另一方面可實現吸附劑的重復利用,提升吸附劑的經濟性。在25 ℃下,分別以0.5 mol/L和1 mol/L硝酸(30 mL)作為洗脫劑對吸附Sr(Ⅱ)的吸附劑(0.6 g)進行洗脫,結果示于圖11。由圖11可見,Sr(Ⅱ)的洗脫率均隨接觸時間的增加而上升,3 h左右時基本接近平衡,分別達到20.69%和39.65%。雖然在1 mol/L硝酸條件下的洗脫率更高,但與1 mol/L硝酸接觸5 h后,仍只有42.81%的Sr(Ⅱ)從吸附劑中洗脫下來,遠不能達到吸附劑重復利用的標準。這是由于添加的分子改性劑DBS在0.5 mol/L及1 mol/L硝酸條件下為DtBuCH18C6與Sr(Ⅱ)的絡合提供了配位陰離子,使得這兩種洗脫劑無法在當前條件下對吸附的Sr(Ⅱ)進行高效的洗脫。
進一步考慮改變作為洗脫劑的硝酸溶液的濃度或洗脫劑與吸附劑的液固比(V/m)來改善洗脫效果。由于提高硝酸濃度對材料的耐酸性會產生影響,且對儀器以及操作安全有更高的要求,因此本研究通過調整吸附劑與洗脫劑的液固比來提高Sr(Ⅱ)的回收效果。在25 ℃、1 mol/L硝酸、5 h接觸時間的條件下進一步對洗脫劑與吸附劑的液固比對洗脫率的影響進行探討,結果示于圖12。由圖12可見,將液固比由0.2 L/g提升到0.9 L/g,1 mol/L硝酸對Sr(Ⅱ)的洗脫率隨著吸附劑體積的增加而上升,在液固比為0.9 L/g時,洗脫率達79%。因此,使用1 mol/L硝酸作為洗脫劑對吸附Sr(Ⅱ)后的(DtBuCH18C6+DBS+Dodec)/SiO2-P進行洗脫時,液固比設置為0.9 L/g。

圖11 不同濃度洗脫液下Sr(Ⅱ)的洗脫率隨接觸時間的變化Fig.11 Change of Sr(Ⅱ) elution rate with contact time under different nitric acid concentrations

圖12 液固比對Sr(Ⅱ)洗脫率的影響Fig.12 Effect of liquid solid ratio on elution rate of Sr(Ⅱ)
3 結論
1) 本研究采用DBS作為大環分子化合物冠醚DtBuCH18C6的分子改性劑,以旋轉蒸發真空負壓的方式成功合成了(DtBuCH18C6+DBS+Dodec)/SiO2-P吸附劑。
2) 通過表征手段評價了有機化合物在SiO2-P載體中的負載情況和熱穩定性,并對吸附Sr(Ⅱ)前后的元素結合能變化進行了XPS分析,佐證了DtBuCH18C6及DBS對Sr(Ⅱ)吸附過程中的貢獻。復合吸附劑在硝酸溶液中的泄漏率低且受溫度的影響小,有良好的化學穩定性能。
3) 靜態吸附實驗證明,吸附劑對Sr(Ⅱ)有良好的吸附選擇性,DBS的添加提供了可與DtBuCH18C6進行配位的平衡陰離子,使得在0.5 mol/L硝酸條件下的分配系數提升到392.19 cm3/g,增加了約10倍。吸附劑對Sr(Ⅱ)的吸附過程符合準二級動力學模型和Langmuir模型,表明其吸附速率受化學吸附過程控制且吸附過程更接近表面均一的單層吸附。
4) 以1 mol/L硝酸作為洗脫劑對Sr(Ⅱ)的洗脫率高達約79%,吸附劑具有較好的重復利用性。