基于HPA軸探討二甲雙胍對糖尿病合并抑郁癥大鼠抑郁行為的影響
覃英梅,王 強,尹 瑋,潘紅丹
(廣西國際壯醫醫院健康管理中心,南寧 530001)
二甲雙胍是目前干預糖尿病的一線藥物,不僅可降糖、減重,還能保護神經、抗衰老。二甲雙胍可通過減少循環支鏈氨基酸減輕胰島素抵抗小鼠的抗焦慮和抗抑郁樣反應,提示其抗抑郁作用[1]。本研究通過建立糖尿病合并抑郁癥大鼠模型,觀察二甲雙胍對其抑郁行為的影響,并探討可能機制。
1 實驗材料
1.1 實驗動物
45只SD大鼠,SPF級,雄性,8周齡,體質量(320±20)g,購自北京百奧賽圖基因生物技術有限公司,實驗動物生產許可證號:SCXK(京)2019-0001。
1.2 藥物與試劑
鹽酸二甲雙胍片(國藥準字H20123035,0.5 g,上海信誼藥廠有限公司);鏈脲佐菌素(streptozotocin,STZ),CAS(18883-66-4,成都貝斯特試劑有限公司);皮質醇(cortisol,CORT)、促腎上腺皮質激素(adrenocorticotropic hormone,ACTH)放射免疫分析試劑盒;兔抗大鼠閉鎖小帶蛋白-1(zonula occludens-1,ZO-1)、IV型膠原蛋白(type IV collagen,CoIV)一抗(美國Thermo Fisher Scientific公司)。
1.3 儀器
大小鼠自發活動曠場實驗裝置(上海欣軟信息科技有限公司);Synergy-HD顯微鏡(日本東芝公司);CheniDoc XRS凝膠成像分析系統(美國Biorad公司)。
2 實驗方法
2.1 建立模型[2]
采用一次性腹腔注射STZ的方式建立糖尿病模型。大鼠腹腔注射STZ(采用pH為4.5的枸櫞酸緩沖液配置為濃度80 g·L-1)65 mg·kg-1,給藥后第1、5、10天后隨機血糖>16.70 mmol·L-1,且表現為體質量減輕、多尿為建模成功。糖尿病模型建立成功的大鼠采用慢性刺激法建立抑郁模型:每天隨機從禁食24 h、禁水24 h、夾尾1 min、束縛3 h、4 ℃冰水游泳、45 ℃環境5 min、每分鐘160次水平振蕩30 min 7種刺激方式中隨機選1種刺激大鼠,1周中7種刺激均進行1次,連續3周,以大鼠表現為主動性活動減少、興趣缺失、食欲不振為建模成功。
2.2 分組與干預方式[3]
從45只大鼠中隨機抽取10只僅注射等量枸櫞酸緩沖液,設為對照組,其余35只建立糖尿病合并抑郁癥模型,30只建模成功,隨機分為模型組、實驗A組、實驗B組,各10只。實驗A、B組腹腔注射二甲雙胍生理鹽水溶液1 mL,用藥劑量分別為150 mg·kg-1、300 mg·kg-1,對照組、模型組腹腔注射等體積生理鹽水。每天1次,連續干預4周。
2.3 曠場實驗檢測大鼠自發活動度[4]
末次干預后次日,采用曠場實驗測試大鼠運動能力。在80 cm×120 cm×100 cm實驗黑箱上方放置全方位攝像頭,將大鼠置于中央,攝像頭記錄大鼠5 min內活動影像,計算大鼠總移動距離縮短、移動速度。每只實驗后擦拭、消毒黑箱底面、內壁,避免氣味殘留對后續實驗造成影響。實驗前10 min將大鼠帶入實驗房間適應環境,期間保持房間安靜。
2.4 糖水消耗實驗檢測大鼠糖水偏嗜度[5]
造模前訓練大鼠逐漸適應糖水,末次干預后次日進行糖水消耗實驗。第1天飼喂2瓶1%蔗糖水,第2天將其中1瓶糖水替換為去離子水,第3天禁食、禁水24 h,飼喂去離子水、蔗糖水各1瓶,每瓶100 mL,1 h后檢測去離子水與蔗糖水消耗量(mL),計算糖水偏嗜度(%)=糖水消耗量÷液體總消耗量×100%。
2.5放射免疫分析法檢測下丘腦-垂體-腎上腺軸(hypothalamic pituitary adrenal axis,HPA)軸活性[6]
糖水消耗實驗完成后采集大鼠腹主動脈血2 mL,冰浴試管中靜置30 min,每分鐘3 000轉離心10 min,取血清。采用放射免疫分析法檢測血清CORT、ACTH水平,嚴格按照試劑盒說明書操作。
2.6 免疫印跡法檢測海馬組織ZO-1、CoIV蛋白表達[7]
采血后處死脫頸大鼠,剝離顱骨,迅速取出腦組織,根據《大鼠腦立體定位圖譜》分離海馬組織,分成2份,1份保存于液氮中,1份固定于4%多聚甲醛中,病理切片機切片(厚度5 μm)。取液氮保存海馬組織,充分剪碎,勻漿,加入RIPA裂解液,轉移至離心管,離心后定量蛋白。取50 μg樣本,混合上樣緩沖液混合,100℃金屬浴5 min,離心取上清,電泳,濕轉至硝酸纖維素膜,封閉2 h,加入兔抗大鼠ZO-1、CoIV一抗(1:500),4 ℃搖床孵育2 h,TBST洗膜,加入山羊抗兔IgG二抗(1:2 000),常溫孵育2 h,TBST洗膜,發光液顯色、曝光,凝膠成像系統分析,蛋白表達量以待測蛋白/內參GAPDH的灰度值表示。
2.7 HE染色觀察海馬組織病理變化[8]
取海馬組織切片,二甲苯脫蠟,無水乙醇沖洗,自來水沖洗30 s,蘇木精染液染色5 min,自來水沖洗,鹽酸酒精分化,自來水沖洗,反藍,伊紅染液染色2 min,梯度乙醇脫水、透明,中性樹膠封片,光學顯微鏡下觀察海馬CA1區病理變化。
2.8 統計學方法
統計、分析數據通過SPSS 19.0軟件進行,以均數±標準差(±s)表示計量資料,采用單因素方差分析(One-Way ANOVA)比較多樣本計量資料,以LSD-t檢驗進行兩兩比較。以P<0.05為差異有統計學意義。
3 結果
3.1 各組曠場實驗結果比較
見表1。
表1 各組曠場實驗結果比較(±s,n= 10)

表1 各組曠場實驗結果比較(±s,n= 10)
注:與對照組比較,# P<0.05;與模型組比較,△P<0.05;與實驗A組比較,▲P<0.05
組別 劑量/(mg·kg-1)總移動距離 /cm 移動速度/(cm·s-1)對照組 0 1623.54±175.73 6.35±0.74模型組 0 832.14±95.43# 2.24±0.32#實驗A組 150 1119.98±130.54△ 3.98±0.48△實驗B組 300 1365.52±158.27▲ 5.06±0.65▲
3.2 各組糖水偏嗜度比較
見表2。
表2 各組糖水偏嗜度比較(±s,n= 10)

表2 各組糖水偏嗜度比較(±s,n= 10)
注:與對照組比較,# P<0.05;與模型組比較,△P<0.05;與實驗A組比較,▲P<0.05
組別 劑量/(mg·kg-1) 糖水偏嗜度/%對照組 0 82.51±8.96模型組 0 51.33±6.52#實驗A組 150 62.32±7.49△實驗B組 300 75.67±8.71▲
3.3 各組HPA軸活性比較
見表3。
表3 各組HPA軸活性比較(±s,n= 10)
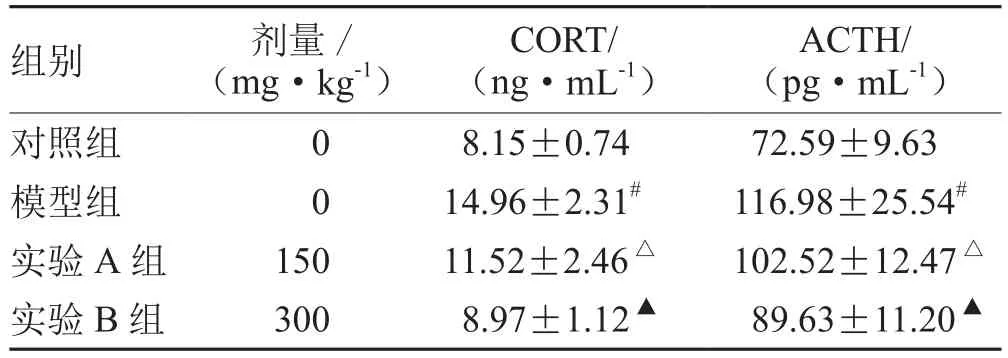
表3 各組HPA軸活性比較(±s,n= 10)
注:與對照組比較,# P<0.05;與模型組比較,△P<0.05;與實驗A組比較,▲P<0.05
ACTH/(pg·mL-1)對照組 0 8.15±0.74 72.59±9.63模型組 0 14.96±2.31# 116.98±25.54#實驗A組 150 11.52±2.46△ 102.52±12.47△實驗B組 300 8.97±1.12▲ 89.63±11.20▲組別 劑量/(mg·kg-1)CORT/(ng·mL-1)
3.4 各組海馬組織ZO-1、CoIV蛋白表達量比較
見表4、圖1。
表4 各組海馬組織ZO-1、CoIV蛋白表達量比較(±s,n= 10)
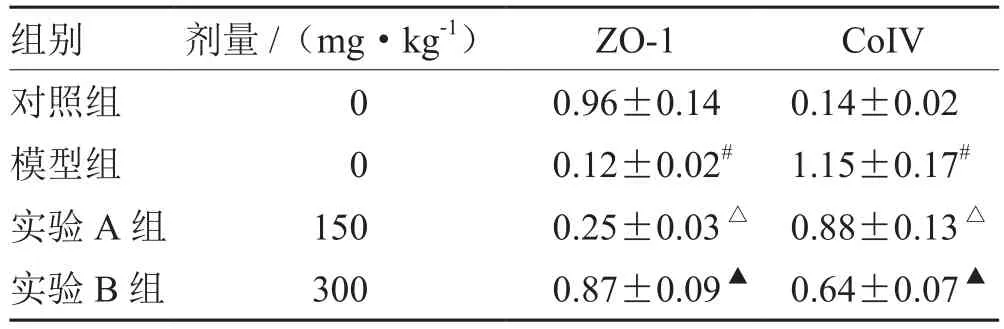
表4 各組海馬組織ZO-1、CoIV蛋白表達量比較(±s,n= 10)
注:與對照組比較,# P<0.05;與模型組比較,△P<0.05;與實驗A組比較,▲P<0.05
組別 劑量/(mg·kg-1) ZO-1 CoIV對照組 0 0.96±0.14 0.14±0.02模型組 0 0.12±0.02# 1.15±0.17#實驗A組 150 0.25±0.03△ 0.88±0.13△實驗B組 300 0.87±0.09▲ 0.64±0.07▲
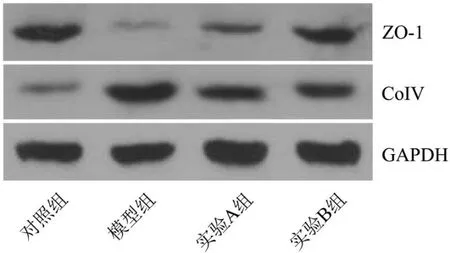
圖 1 免疫印跡法檢測各組海馬組織ZO-1、CoIV蛋白表達
3.5 各組海馬組織病理變化
HE染色結果顯示,對照組海馬CA1區神經元排列整齊、結構完整、形態規則、核仁清晰,具有明顯的極性;模型組神經元腫脹或萎縮,溶解或碎裂,細胞層數減少,較多發生壞死,排列疏松;實驗A、B組神經元數量有所增加,細胞排列較為緊密、層數增加,腫脹、萎縮、溶解、碎裂減少,其中實驗B組改善效果優于實驗A組。見圖2。
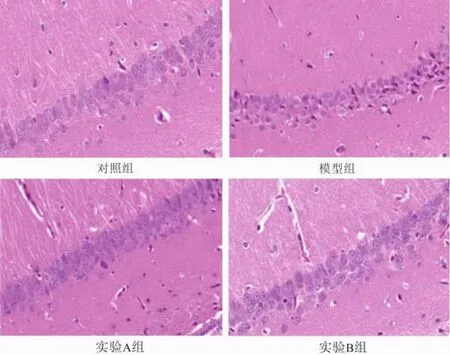
圖 2 各組蘇木精—伊紅染色后光學顯微鏡下海馬CA1區病理學改變(×400)
4 討論
ZO-1是一種高分子量磷蛋白,分布在上皮與血管內皮細胞,主要功能是緊密連接內皮細胞,其表達量高低與血腦屏障的關閉與開放密切相關[9]。CoIV主要分布在血腦屏障基底膜的透明層,可結合層黏連蛋白構成基底膜骨架。研究發現,高血糖可誘導層黏連蛋白、CoIV合成,導致毛細血管基底膜厚度增加。二甲雙胍屬于雙胍類口服降血糖藥,可延緩胃腸道攝取葡萄糖,并增強機體對胰島素的敏感性從而提高外周葡萄糖利用效率,降低血糖。此次,二甲雙胍被食品藥品監督管理局認為是神經再生、優化的藥物,可促進神經干細胞的增殖與分化,從而保護神經功能。二甲雙胍可改善脂多糖誘導的抑郁小鼠抑郁樣行為并糾正異常的谷氨酸能傳遞[10]。本研究結果顯示,與模型組比較,實驗A組總移動距離延長,移動速度加快,糖水偏嗜度、ZO-1蛋白表達量升高,CoIV蛋白表達量降低,且實驗B組效果優于實驗A組,提示二甲雙胍可改善糖尿病并發抑郁癥大鼠抑郁樣行為,減輕血腦屏障損傷。
HPA軸是由下丘腦、垂體及腎上腺構成的反饋調節系統,三者互相協調,形成神經內分泌免疫網絡樞紐,通過對外界刺激做出心理與生理反應維持機體內環境穩定[11]。HPA軸功能亢進是抑郁癥的主要發病機制之一,機體長期處于應激狀態,下丘腦釋放大量促腎上腺皮質激素釋放激素,誘導垂體合成并釋放大量ACTH,作用于腎上腺皮質,刺激腎上腺皮質與外周血中CORT水平升高。HPA軸功能的改變是抑郁癥發生及認知惡化的一種可能機制,抑郁癥與較高的CORT、ACTH水平有關[12]。本研究結果顯示,與模型組比較,實驗A組血清CORT、ACTH水平降低,且實驗B組效果優于實驗A組,提示二甲雙胍對糖尿病并發抑郁癥大鼠的治療作用可能通過抑制HPA軸活性來實現。

