基于UHPLC-Q-Exactive-Orbitrap-MS的苦黃注射液化學成分分析
王允吉,王海丹,劉璐,張引蘭,童寧,曹輝*(.南京中醫藥大學附屬南京醫院/南京市第二醫院藥學部,南京 0003;.南京中醫藥大學附屬江蘇省中醫院藥理實驗室,南京 009)
苦黃注射液源于張仲景《傷寒論》的茵陳蒿湯(茵陳、大黃、山梔),鄒良才老中醫改良茵陳蒿湯而得到由大黃、苦參、茵陳、柴胡和大青葉組成的苦黃注射液。該藥具有清熱利濕、疏肝退黃的功效,主治濕熱型黃疸,即因濕熱內蘊引起的黃疸型病毒性肝炎患者的退黃[1-2]。目前,有關苦黃注射液的研究多集中于臨床療效觀察,研究表明苦黃注射液對黃疸型病毒性肝炎[3]、膽汁淤積性肝病[4]、原發性膽汁性肝硬化[5]等疾病均有較好的療效。
關于苦黃注射液中的化學成分研究僅有針對某類或某幾個特征性成分進行定量分析的報道[6-7],尚未見對苦黃注射液中化學成分進行全面分析的研究。超高效液相色譜-四極桿-靜電軌道場離子阱質譜(UHPLC-Q-Exactive-Orbitrap-MS)技術具有高分離性能、高靈敏度及高檢測能力,可以進行高精度的定量和定性分析,已廣泛用于中藥成分分析、藥物動力學、體內藥物分析等領域[8]。本研究首次采用UHPLC-Q-Exactive-Orbitrap-MS 對苦黃注射液中化學成分進行全面分析,并對其進行藥材歸屬,為明確苦黃注射液藥效物質基礎,闡明其藥理學作用機制提供實驗依據。
1 材料
1.1 儀器
Thermo Q-Extractive 液相色譜-四極桿-靜電場軌道阱高分辨質譜聯用儀(含高壓二元泵、自動進樣器、柱溫箱、四極桿-靜電場軌道阱質量分析器)、Xcalibur 3.1 數據分析系統(美國Thermo公司);Heraeus Multifuge X1R 冷凍離心機(美國Thermo 公司);ACQUITY UPLC HSS T3 色譜柱(2.1 mm×100 mm,1.8 μm,美國Waters 公司);Milli-Q Direct 超純水儀(德國默克Millipore 公司)。
1.2 試藥
苦黃注射液(常熟雷允上制藥有限公司,批號:2106281,規格:10 mL);乙腈、乙醇(HPLC 級,德國Merck 公司);甲酸(HPLC 級,美國Sigma-Aldrich 公司);純水取自超純水儀。
2 方法
2.1 供試品溶液制備
吸取苦黃注射液1 mL,加入純乙醇溶液3 mL 沉淀后,于2~8℃冰箱中放置24 h 后,離心5 min(4 ℃、12 000 r·min-1),吸取上清液后經0.22 μm 微孔濾膜過濾后得到供試品溶液。
2.2 色譜條件
色譜柱:Waters ACQUITY UPLC HSS T3(2.1 mm×100 mm,1.8 μm);流速:0.35 mL·min-1;柱溫:35℃;0.1%甲酸水為流動相A,乙腈為流動相B,梯度洗脫(0~8 min,0%~25%A;8~23 min,25%~55%A;23~25 min,55%~80%A;25~26 min,80%~100%A;26~27 min,100%A;27~28 min,100%~0%A;28~30 min,0%A);進樣量:5 μL。
2.3 質譜條件
離子源為HESI 源,正、負離子檢測模式,毛細管電壓為3500 V,毛細管溫度為350 ℃,離子源溫度為350℃,鞘氣流速為9 L·min-1,輔助氣流速為3 L·min-1,階梯碰撞能量:25、35、45 eV,檢測方式為Full MS/dd-MS2,一級質譜分辨率Full MS 70 000 FWHM(Full Width at Half Maximum),二級質譜分辨率dd-MS217 500 FWHM,掃描范圍m/z100~1000 Da。
2.4 數據處理
通過查閱Scifinder、Chemspider 數據庫和相關文獻,收集整理了苦黃注射液中各類化學成分的結構式以及化合物的裂解規律。運用Xcalibur 3.0 軟件進行質譜數據處理,通過高分辨質譜計算出分子式(誤差范圍±1×10-5),結合目前已有文獻信息推測可能的化合物的裂解規律,并根據相同類型的化合物的裂解規律對化合物進行質譜鑒定。
3 結果
3.1 苦黃注射液中化學成分分析
采用UHPLC-Q-Exactive Orbitrap-MS 正負離子模式分析苦黃注射液乙醇沉淀后的(+)HESIMS、(-)HESI-MS 的質譜總離子流圖(TIC)(見圖1),通過UHPLC-Q-Exactive Orbitrap-MS 技術檢測得到離子流峰的保留時間和質譜數據信息,進行數據處理,共鑒定出苦黃注射液中化學成分123 個[9-25],其中包括黃酮類36 個、酚酸類20 個、生物堿類19 個、蒽醌類15 個、氨基酸11 個、核苷類8 個、萜類6 個、脂肪酸類3 個,糖類1 個等,化合物結果見表1。
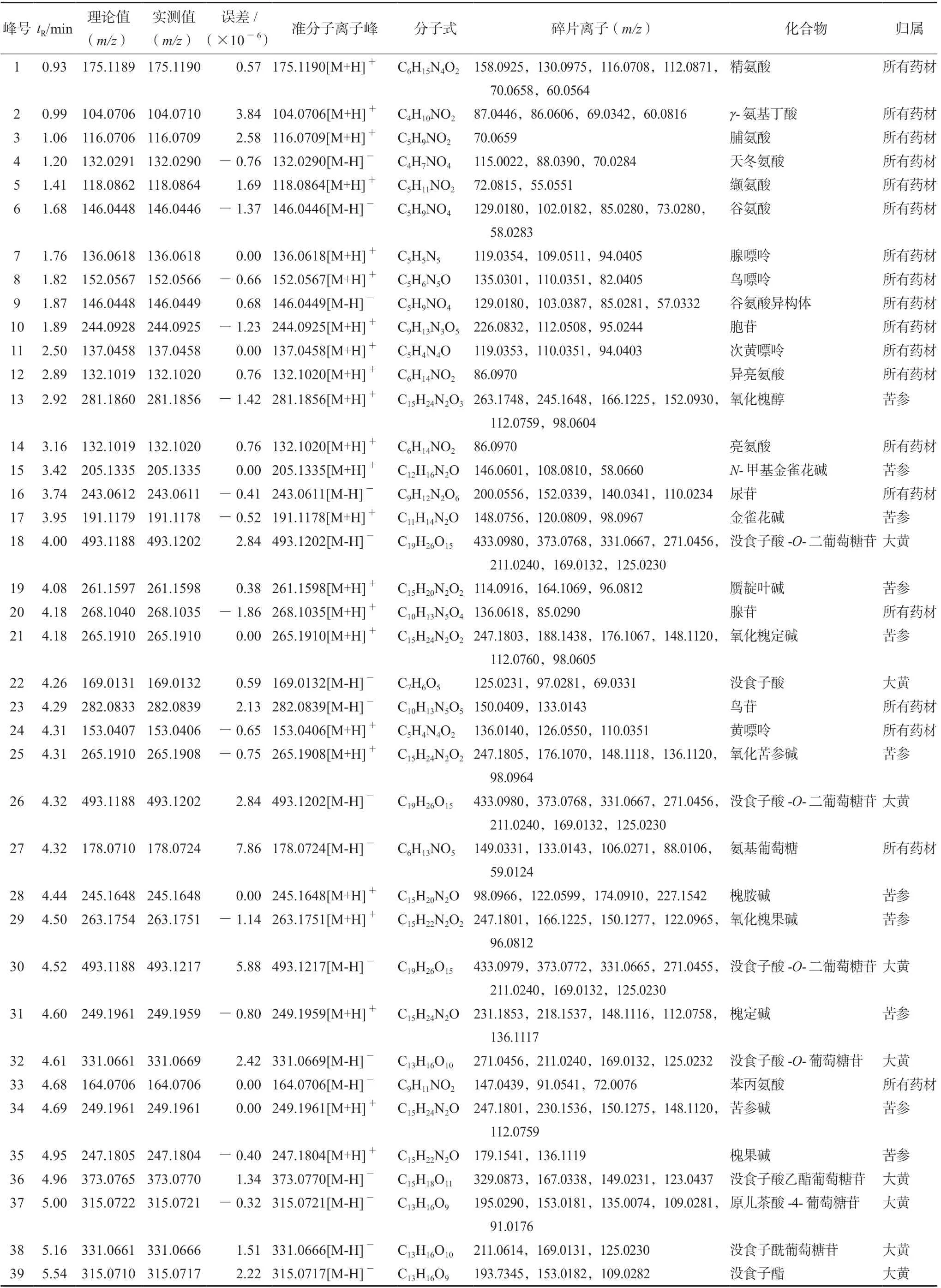
表1 苦黃注射液中化學成分的UHPLC-Q-Exactive-Orbitrap-MS 鑒定結果Tab 1 Identified chemical constituents in Kuhuang injection by UHPLC-Q-Exactive-Orbitrap-MS

續表1
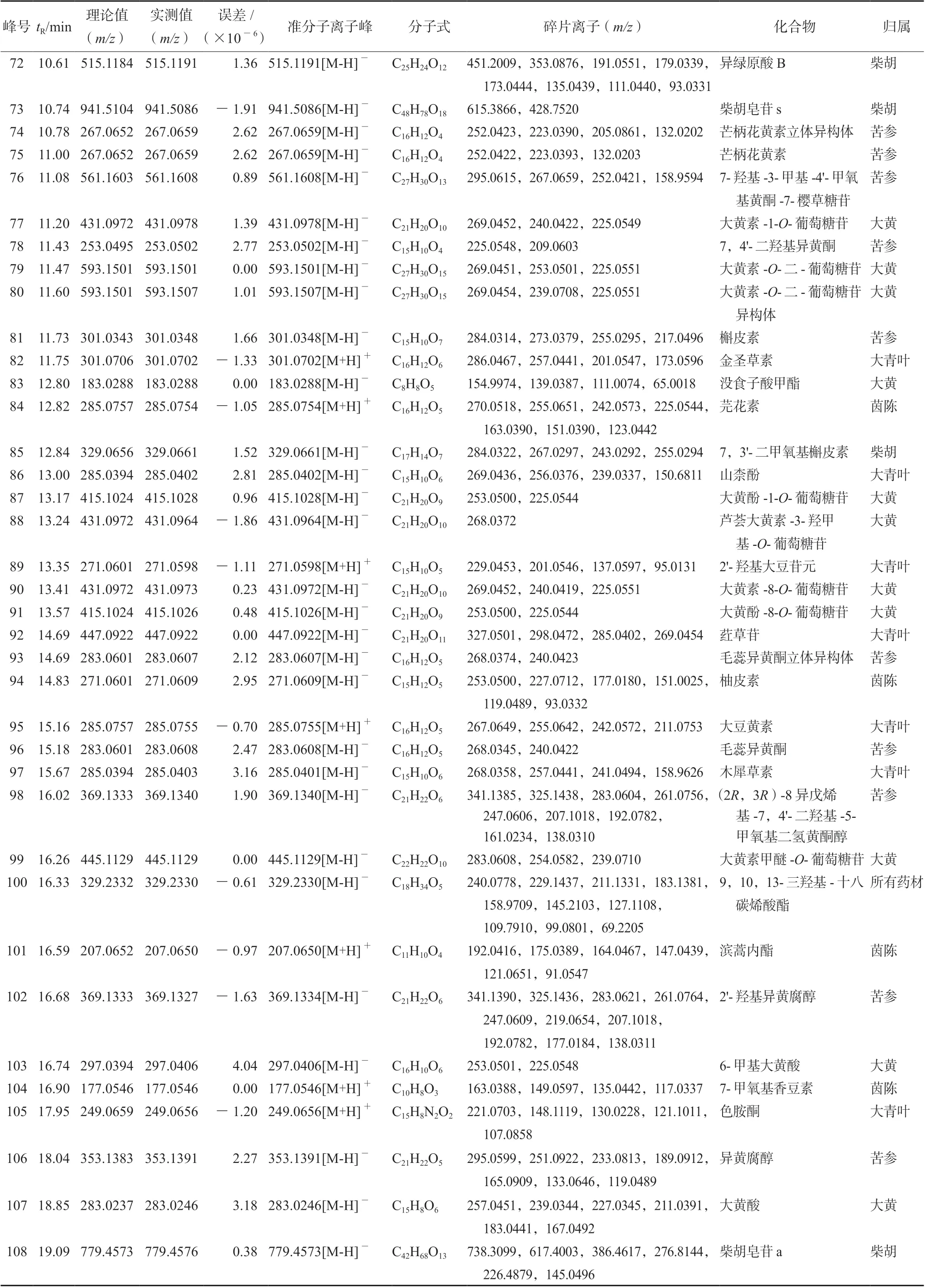
續表1

續表1
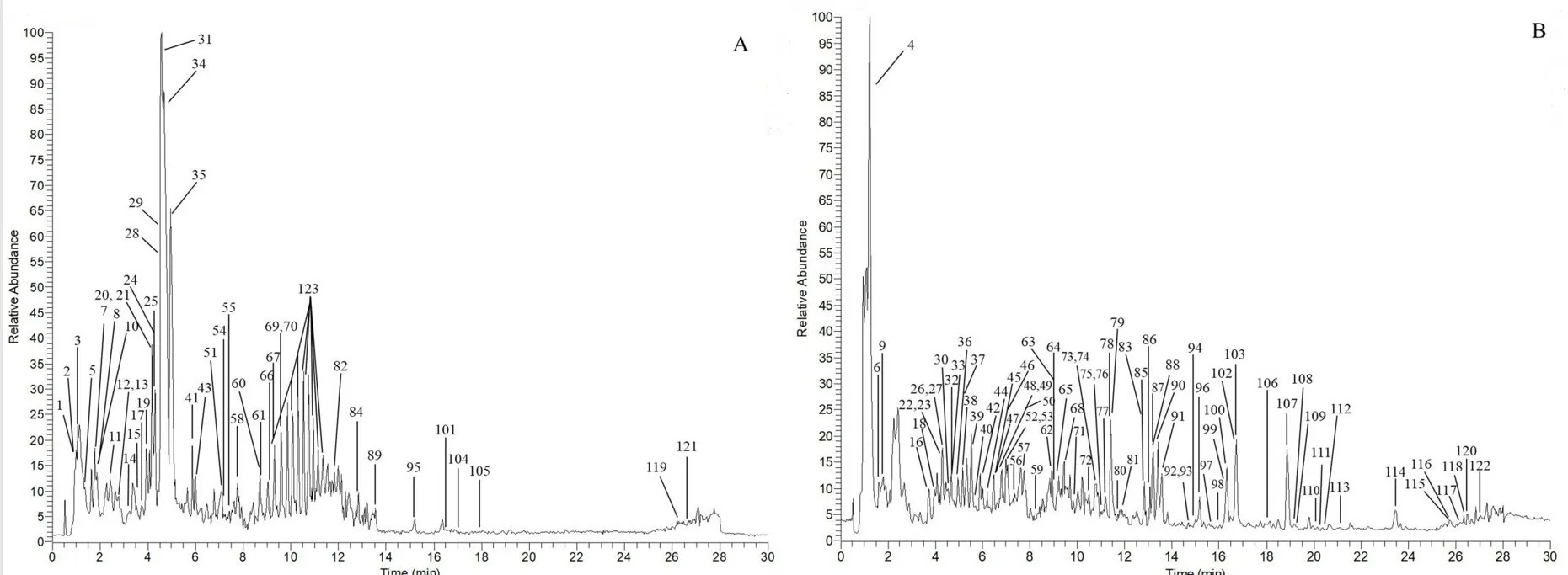
圖1 ESI+模式(A)和ESI-模式(B)下苦黃注射液的總離子流圖Fig 1 Total ion chromatogram of Kuhuang injection under the positive ion(A)and the negative ion(B)modes
3.2 苦黃注射液中主要化合成分的質譜裂解規律
3.2.1 黃酮類化合物的分析鑒定 苦黃注射液中共鑒定出黃酮類化合物36 種,該類成分主要來自于大黃、茵陳和大青葉。現以芫花素、柚皮素為例,依據多級碎片信息,解析苦黃注射液中黃酮類成分的質譜裂解規律。
峰84 保留時間為12.82 min,可觀察到準分子離子峰m/z285.0754 [M+H]+,同時可觀察到主要的碎片離子分別為m/z270.0518、255.0651、242.0573、225.0544、163.0390、151.0390、123.0442,分別對應的分子式為[M+HCH3]+、[M+H-CH2O]+、[M+H-C2H2O]+、[M+H-CO3]+、[M+H-C7H6O2]+、[M+H-C8H6O2]+、[M+HC9H6O3]+,根據正離子模式下的精確分子質量及特征碎片的質量,結合相關文獻[9-11]可判斷該化合物為芫花素,其裂解規律見圖2。
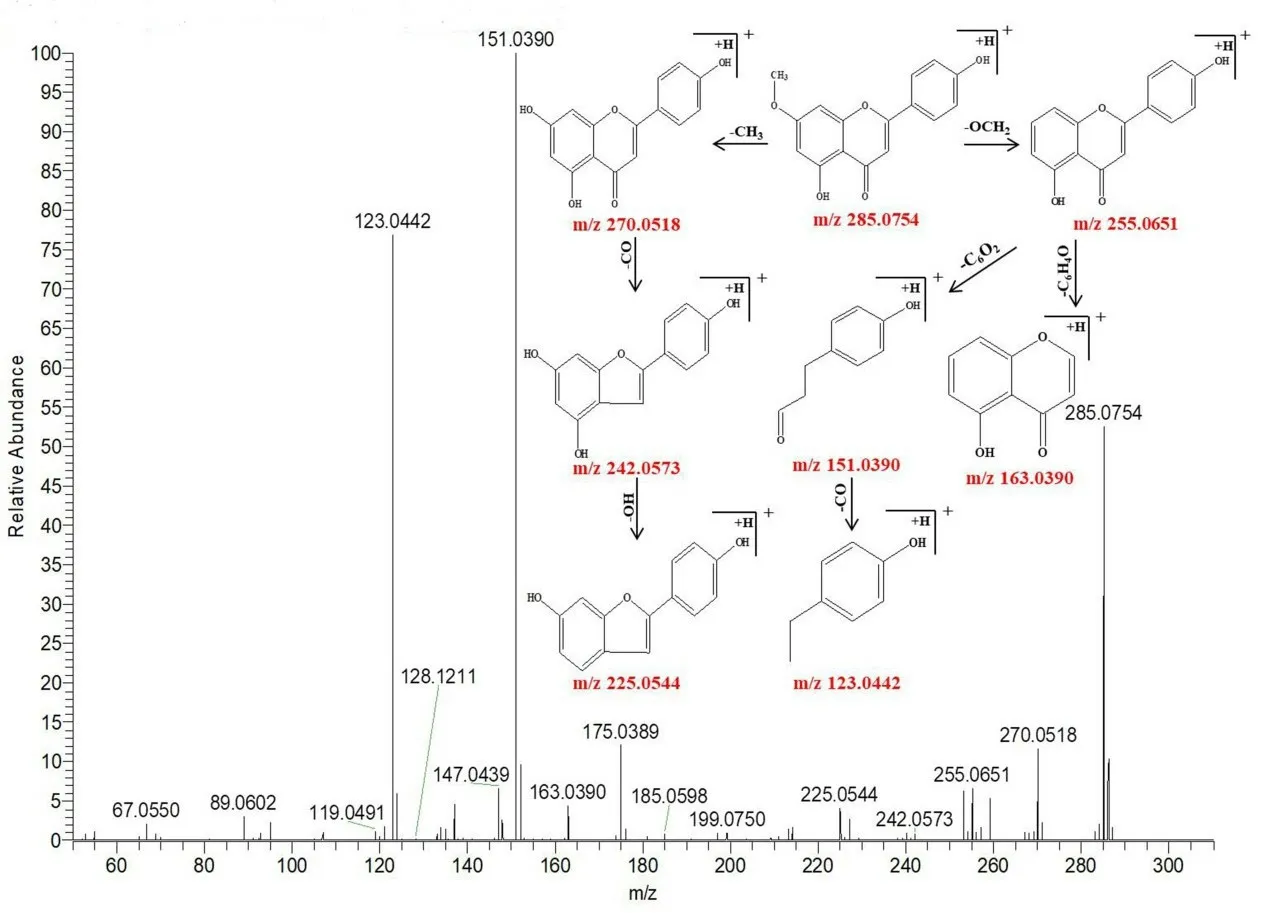
圖2 芫花素可能的裂解途徑Fig 2 Possible fragmentation pathways of genkwanin
峰94 保留時間為14.83 min,可觀察到準分子離子峰m/z271.0609 [M-H]-,同時可觀察到主要的碎片離子分別為m/z253.0500、227.0712、177.0180、151.0025、119.0489、93.0332,分別對應的分子式為[M-H-OH]-、[M-H-CO2]-、[MH-C6H6O]-、[M-H-C8H8O]-、[M-H-C7H4O4]-、[M-HC9H6O4]-,根據負離子模式下的精確分子質量及特征碎片的質量,結合相關文獻[9-11]可判斷該化合物為柚皮素,其裂解規律見圖3。
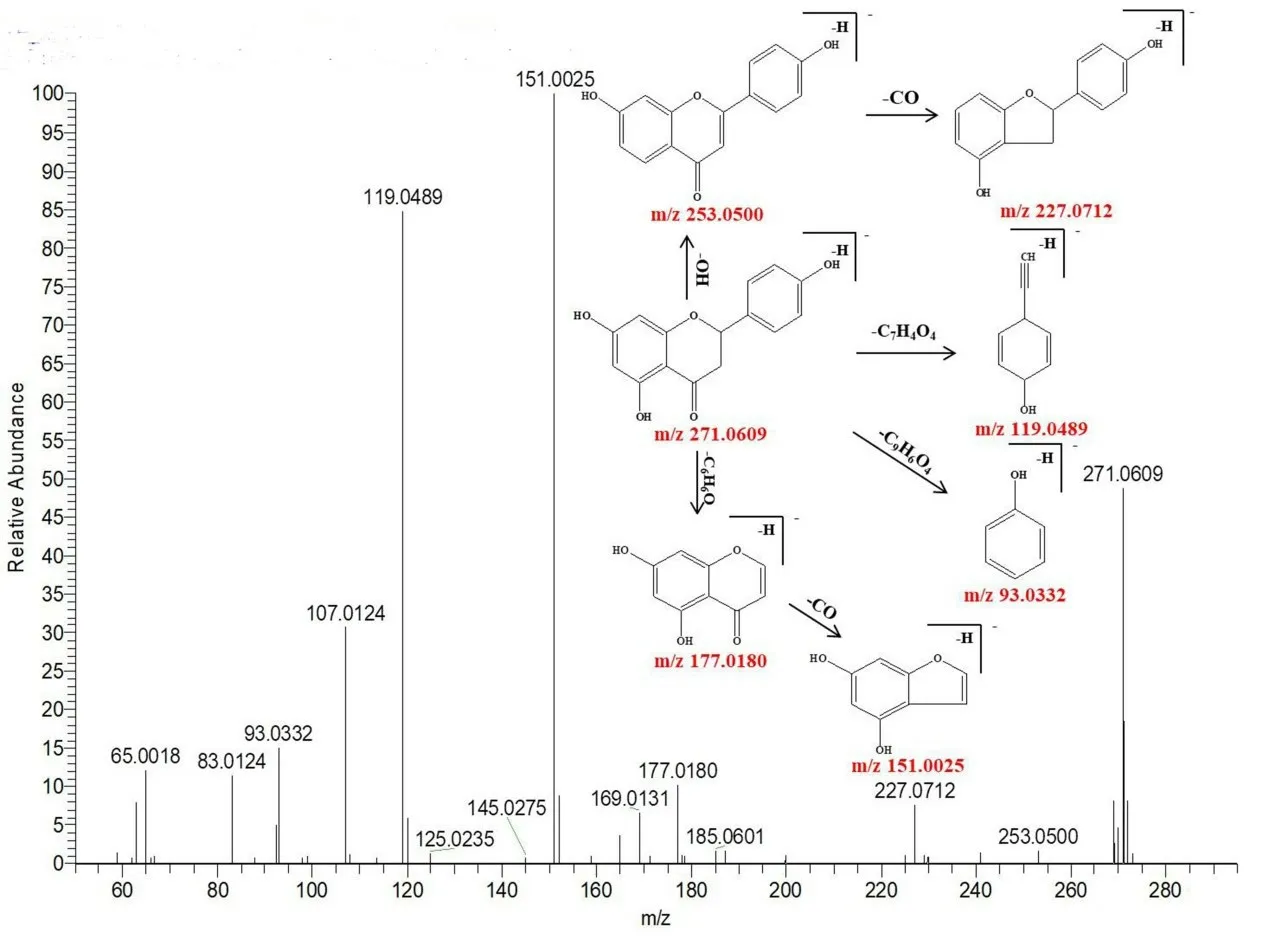
圖3 柚皮素可能的裂解途徑Fig 3 Proposed fragmentation pathways of naringenin
3.2.2 酚酸類及其化合物的分析鑒定 苦黃注射液中共鑒定出酚酸類成分20 種,該類成分主要存在于該組方中的大黃、柴胡和茵陳。
峰42 保留時間為5.90 min,可觀察到該化合物的準分子離子峰為m/z353.0872 [M-H]-,與其分子式C16H18O9相符,其主要的碎片離子分別為m/z191.0551、179.0339、173.0441、161.0231、135.0438,歸屬各碎片離子分別為[M-H-C9H6O3]-、[M-HC7H10O5]-、[M-H-C9H8O4]-、[M-H-C7H12O6]-、[M-HC8H10O7]-,根據負離子模式下精確相對分子質量和二級質譜碎片信息,結合相關文獻[10,12-13]可判斷該化合物為綠原酸,其裂解規律見圖4。
峰22 保留時間為4.26 min,可觀察到該化合物的準分子離子峰為m/z169.0132 [M-H]-,與其分子式C7H6O5相符,其主要的碎片離子分別為m/z125.0231、97.0281、69.0331,歸屬各碎片離子分別為[M-H-CHO]-、[M-H-C3H4O3]-、[M-HC3O4]-,根據負離子模式下精確相對分子質量和二級質譜碎片信息,結合相關文獻[15-17,21-22]可判斷該化合物為沒食子酸,其裂解規律見圖5。

圖5 沒食子酸可能的裂解途徑Fig 5 Proposed fragmentation pathways of gallic acid
3.2.3 生物堿類化合物的分析鑒定 苦黃注射液中共鑒定出種生物堿類化合物19 種,該類成分主要來自于苦參和大青葉。峰17 保留時間為3.95 min,可觀察到該化合物的準分子離子峰為m/z191.1178 [M+H]+,與其C11H14N2O 分子式相符,其主要的碎片離子分別為m/z148.0756、120.0809,歸屬各碎片離子分別為[M+H-C2H5N]+、[M+HC3H5NO]+,結合相關文獻[18-19]可判斷該化合物為金雀花堿,其裂解規律見圖6。
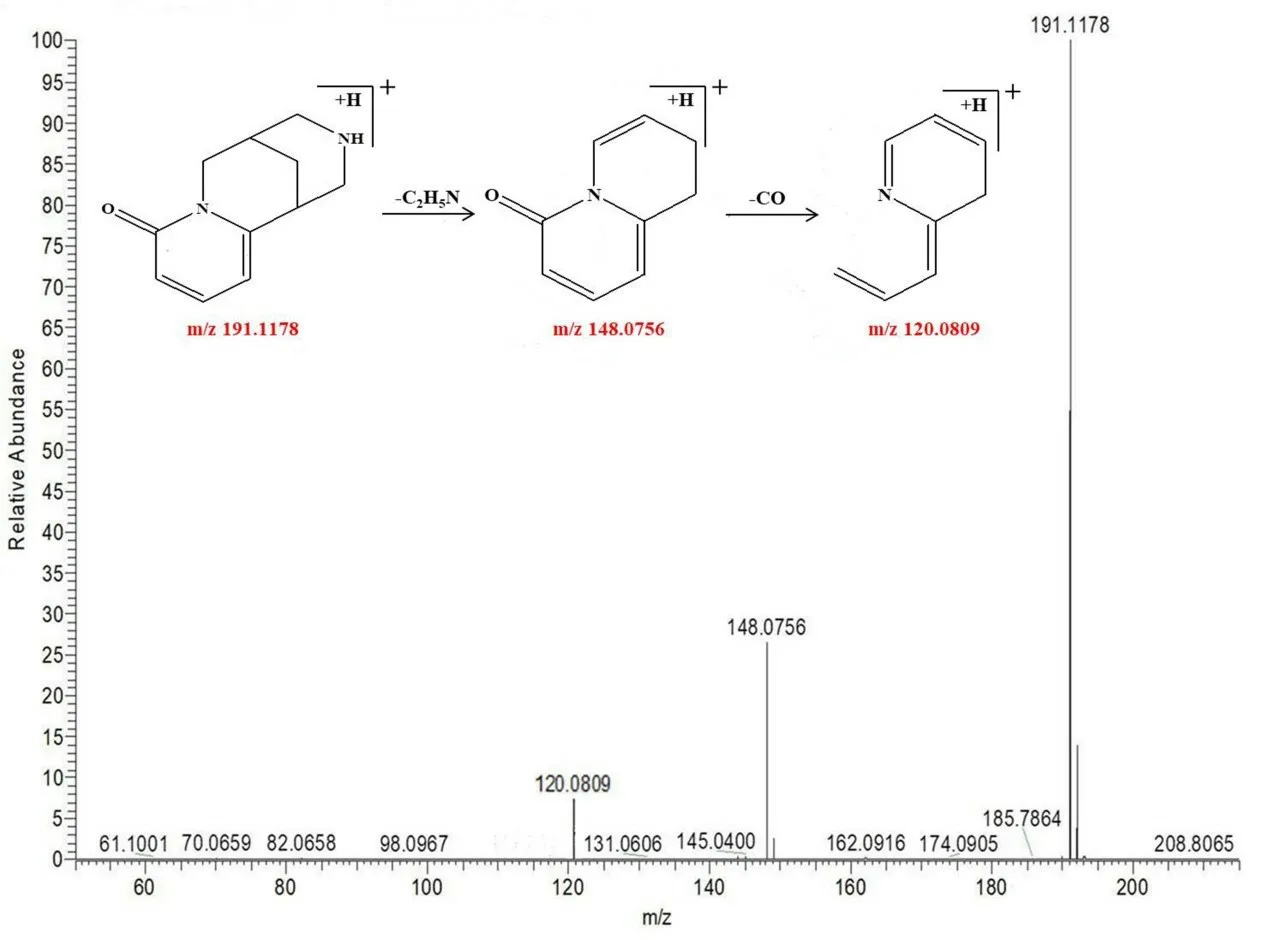
圖6 金雀花堿可能的裂解途徑Fig 6 Proposed fragmentation pathways of cytisine
峰34 保留時間為4.69 min,可觀察到該化合物的準分子離子峰為m/z249.1961 [M+H]+,與其C15H24N2O 分子式相符,其主要的碎片離子分別為m/z247.1801、230.1536、150.1275、148.1120、112.0759,歸屬各碎片離子分別為[M+H-H2]+、[M+H-OH]+、[M+H-C5H8NO]+、[M+HC5H10NO]+、[M+H-C8H10NO]+,結合相關文獻[18-20]可判斷該化合物為苦參堿,其裂解規律見圖7。

圖7 苦參堿可能的裂解途徑Fig 7 Proposed fragmentation pathways of matrine
3.2.4 蒽醌類化合物的分析鑒定 苦黃注射液中共鑒定出種蒽醌類化合物15 種,該類成分主要來自于大黃。現以大黃酸、大黃素、大黃酚為例,依據多級碎片信息,解析苦黃注射液中蒽醌類成分的質譜裂解規律。
其中峰107 保留時間為18.85 min,可觀察到準分子離子峰m/z283.0246 [M-H]-,同時可觀察到主要的碎片離子分別為m/z239.0344、211.0391、183.0441,分別對應的分子式為[M-H-CO2]-、[M-HC2O3]-、[M-H-C3O4]-,根據負離子模式下的精確分子質量及特征碎片的質量,結合相關文獻[15-17,21-22]可判斷該化合物為大黃酸,其裂解規律見圖8。

圖8 大黃酸可能的裂解途徑Fig 8 Proposed fragmentation pathways of rhein
峰114 保留時間為23.44 min,可觀察到準分子離子峰m/z269.0452 [M-H]-,可觀察到主要的碎片離子分別為m/z241.0504、225.0553、210.0307、197.0596、181.0647,分別對應的分子式為[M-H-CO]-、[M-H-CO2]-、[M-H-C2H3O2]-、[MH-C2O3]-、[M-H-C3H3O3]-,根據負離子模式下的精確分子質量及特征碎片的質量,結合相關文獻[15-17,21-22]可判斷該化合物為大黃素,其裂解規律見圖9。

圖9 大黃素可能的裂解途徑Fig 9 Proposed fragmentation pathways of emodin
峰118 保留時間為26.33 min,可觀察到準分子離子峰m/z253.0501 [M-H]-,可觀察到主要的碎片離子分別為m/z225.0503、183.0665,分別對應的分子式為[M-H-CO]-和[M-H-C3H3O3]-,根據負離子模式下的精確分子質量及特征碎片的質量,結合相關文獻[15-17,21-22]可判斷該化合物為大黃酚,其裂解規律見圖10。
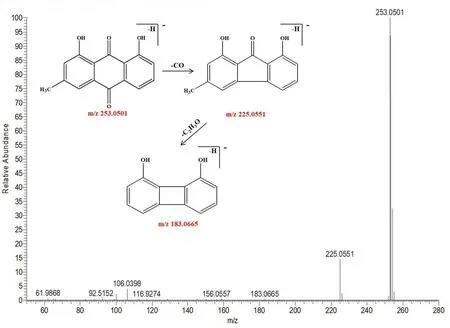
圖10 大黃酚可能的裂解途徑Fig 10 Proposed fragmentation pathways of chrysophanol
3.2.5 氨基酸與核苷類化合物分析鑒定 苦黃注射液中共鑒定出氨基酸與核苷類成分分別為11種和8 種,該類成分主要存在于本組方中的各味中藥材。
峰1 保留時間為0.93 min,可觀察到該化合物的準分子離子峰為m/z175.1190 [M+H]+,與其分子式C6H15N4O2相符,其主要的碎片離子分別為m/z158.0925、130.0957、116.0708、112.0871、70.0658、60.0564,歸屬各碎片離子分別為[M+HOH]+、[M+H-COOH]+、[M+H-CH6N3]+、[M+HCH6NO2]+、[M+H-C2H8N3O2]+、[M+H-C5H10NO2]+,根據正離子模式下精確相對分子質量和二級質譜碎片信息,結合數據庫HMDB 和文獻[23]中化合物信息,可判斷該化合物為精氨酸,其裂解規律見圖11。

圖11 精氨酸可能的裂解途徑Fig 11 Proposed fragmentation pathways of arginine
峰7 保留時間為1.76 min,可觀察到該化合物的準分子離子峰為m/z136.0618 [M+H]+,與其分子式C5H5N5相符,其主要的碎片離子分別為m/z119.0354、109.0511,94.0405,歸屬各碎片離子分別為[M+H-NH3]+、[M+H-CHN]+、[M+HCH3N2]+,結合數據庫HMDB 和文獻[23]中化合物信息,可判斷該化合物為腺嘌呤,其裂解規律見圖12。

圖12 腺嘌呤可能的裂解途徑Fig 12 Proposed fragmentation pathways of adenine
4 討論
本研究利用UHPLC-Q-Exactive Orbitrap-MS技術對苦黃注射液的化學成分進行了系統分析,通過分析正負離子模式下質譜提供的準分子離子[M+H]+和[M-H]-數據,并結合質譜的高分辨率可得到化合物的可靠相對分子質量,從而快速分析苦黃注射液中的組分結構,并對其中12 種主要成分可能的裂解規律進行了描述,以期為苦黃注射液的質量控制以及后續闡明苦黃注射液的藥效物質基礎提供了詳實的數據支撐。
本次研究中鑒定出的化合物中,黃酮類、酚酸類、生物堿類和蒽醌類成分中有保肝退黃的相關報道[26-33]。如苦參的生物堿類化學成分苦參堿和氧化苦參堿可通過抑制Notch 信號通路促進肝卵圓細胞向肝細胞分化,減輕肝損傷[26];也可通過與表皮生長因子受體(EGFR)結合在細胞表面,抑制其功能,阻斷與EGFR 相關的下游信號通路,可減緩肝纖維化的發生和發展,保護肝實質細胞,從而改善肝功能[27];還具有抗乙肝病毒活性作用[28]。柴胡的主要成分柴胡皂苷對膽堿酯酶有抑制作用,能發揮擬膽堿樣作用,調節消化系統和神經系統的功能[29],也可抑制機體脂質過氧化作用的發生,對生物細胞膜產生保護作用,減少自由基與生物細胞膜的接觸,避免自由基對細胞膜的破壞從而降低肝損傷[30-31]。茵陳中主要活性物質綠原酸能減輕肝組織的慢性炎性反應及匯管區膽管增生反應,減緩肝纖維化進程[32]。大黃中的大黃素、大黃酸、蘆薈大黃素和鞣質等成分能促進膽汁、膽汁酸和膽紅素分泌,引起膽囊收縮,增強十二指腸和膽管舒張,疏通膽道和微細膽小管內瘀積的膽汁,而起利膽、退黃作用[33]。上述化合物的藥理作用與苦黃注射液清熱利濕、疏肝退黃的功效一致,且在譜圖中有明顯的峰形,可能是苦黃注射液主要的藥效物質基礎。

