神經(jīng)外科開顱術(shù)后顱內(nèi)感染的危險因素
李深譽,韋開亮,吳修富,張眾一,黃春琴
(桂林醫(yī)學(xué)院第二附屬醫(yī)院,廣西 桂林 541011)
神經(jīng)外科疾病通常需行外科手術(shù)來解除患者顱內(nèi)壓升高、神經(jīng)系統(tǒng)功能受損、腦疝、循環(huán)呼吸衰竭等病理反應(yīng),以控制住其病情來降低患者死亡風(fēng)險。但外科手術(shù)的有創(chuàng)性明顯高于其他治療手段,且患者圍術(shù)期存在較高的顱內(nèi)感染發(fā)生風(fēng)險,導(dǎo)致其術(shù)后誘發(fā)其他病癥,影響預(yù)后的同時還可能加劇患者基礎(chǔ)病情,延緩其康復(fù)進度,嚴重者還會因為感染并發(fā)癥造成死亡[1]。與此同時,有報道指出,大部分顱內(nèi)感染患者后續(xù)經(jīng)抗生素治療后即可消除其體內(nèi)炎性反應(yīng)因子,但一旦控制不當(dāng),從細菌性腦膜炎發(fā)展至顱骨骨髓炎、硬膜下積膿及腦膿腫,藥物保守治療一般難以達到預(yù)期治療效果,需行二次手術(shù),增加患者機體負擔(dān)的同時提高治愈難度。由此可見,神經(jīng)外科強調(diào)針對患者術(shù)后并發(fā)顱內(nèi)感染需落實相關(guān)防控手段,對提高其生存質(zhì)量和促進轉(zhuǎn)歸有重要意義[2]。本研究旨在探究神經(jīng)外科開顱術(shù)和顱內(nèi)感染的相關(guān)危險因素。
1 資料與方法
1.1一般資料:選取2019年1月~2020年1月本院行神經(jīng)外科開顱術(shù)治療的患者100例作為觀察對象,后根據(jù)其術(shù)后顱內(nèi)感染情況進行分組,合并顱內(nèi)感染患者作為觀察組(n=36),未感染者作為對照組(n=64)。納入標準:①病癥類型包括神經(jīng)系統(tǒng)腫瘤、開放性及閉合性顱腦損傷、腦出血及腦血管病、顱骨修補、蛛網(wǎng)膜囊腫、三叉神經(jīng)痛等;②腦脊液細菌培養(yǎng)結(jié)果呈現(xiàn)陽性反應(yīng);③年齡18~60歲。排除標準:①患者僅進行腦室外引流、腦室腹腔分流;②患者術(shù)前已經(jīng)并發(fā)顱內(nèi)感染;③患者術(shù)后1周死亡或未遵循醫(yī)囑執(zhí)行離院;④合并糖尿病、嚴重貧血及需二次手術(shù)者。本研究經(jīng)本院醫(yī)學(xué)倫理委員會同意。
1.2顱內(nèi)感染評估標準:患者臨床上出現(xiàn)與病程不相符的發(fā)熱、頭痛、頸強直等癥狀,經(jīng)實驗室檢查后,患者滿足以下其中三項指標,即可確診顱內(nèi)感染:①腦脊液常規(guī)實驗室結(jié)果顯示,白細胞超過10×106/L,白細胞分類中可見多核細胞所占比例超過55%,潘氏試驗呈現(xiàn)陽性反應(yīng),外周白細胞超過10×109/L;②CSF中糖定量檢測低于450 mg/L,蛋白定量超過0.45 g/L;③經(jīng)抗菌藥物治療后,患者癥狀或體征有明顯改善或完全消失;④腦脊液中培養(yǎng)出病原菌或是腦脊液涂片上可見病原菌[3]。
1.3ASA評分:根據(jù)患者體質(zhì)情況和手術(shù)風(fēng)險,采取美國麻醉師協(xié)會(ASA)相關(guān)標準進行分離,在患者麻醉前進行等級劃分,其中,患者只有局部病變,未見其他系統(tǒng)性疾病,機體健康視為Ⅰ級;患者存在輕/中度系統(tǒng)性疾病,視為Ⅱ級;患者系統(tǒng)性疾病嚴重,限制其日常活動,但還保留有工作能力,視為Ⅲ級;患者系統(tǒng)性疾病嚴重,工作能力完全喪失,并對其生命安全有一定威脅,視為Ⅳ級;患者病情危重,難以維持生命,處于瀕死狀態(tài),視為Ⅴ級[4]。
1.4方法:收集100例患者年齡、性別、ASA評分、外傷、腫瘤、血管或其他等疾病類型、急診手術(shù)、幕上、幕下或兩者等手術(shù)部位、手術(shù)時間、腦室外引流管、顱內(nèi)植入異物、術(shù)后腦脊液漏、激素應(yīng)用、術(shù)前合并其他部位感染(如血液系統(tǒng)、泌尿系統(tǒng)感染、肺炎等)相關(guān)指標,并根據(jù)術(shù)后顱腦感染情況進行觀察、對照分組,分析兩組各項臨床指標差異性,總結(jié)出誘發(fā)其術(shù)后顱內(nèi)感染的相關(guān)危險因素。
1.5統(tǒng)計學(xué)分析:采用SPSS20.0統(tǒng)計學(xué)軟件進行t檢驗與χ2檢驗;相關(guān)性分析采用單因素及多因素Logistic回歸分析。
2 結(jié)果
2.1患者術(shù)后顱內(nèi)感染的單因素分析:觀察組手術(shù)時間、ASA評分、激素應(yīng)用、術(shù)后腦脊液漏、腦室外引流、術(shù)前合并其他部位感染、顱內(nèi)植入異物等指標與對照組比較,差異有統(tǒng)計學(xué)意義(P<0.05)。見表1。
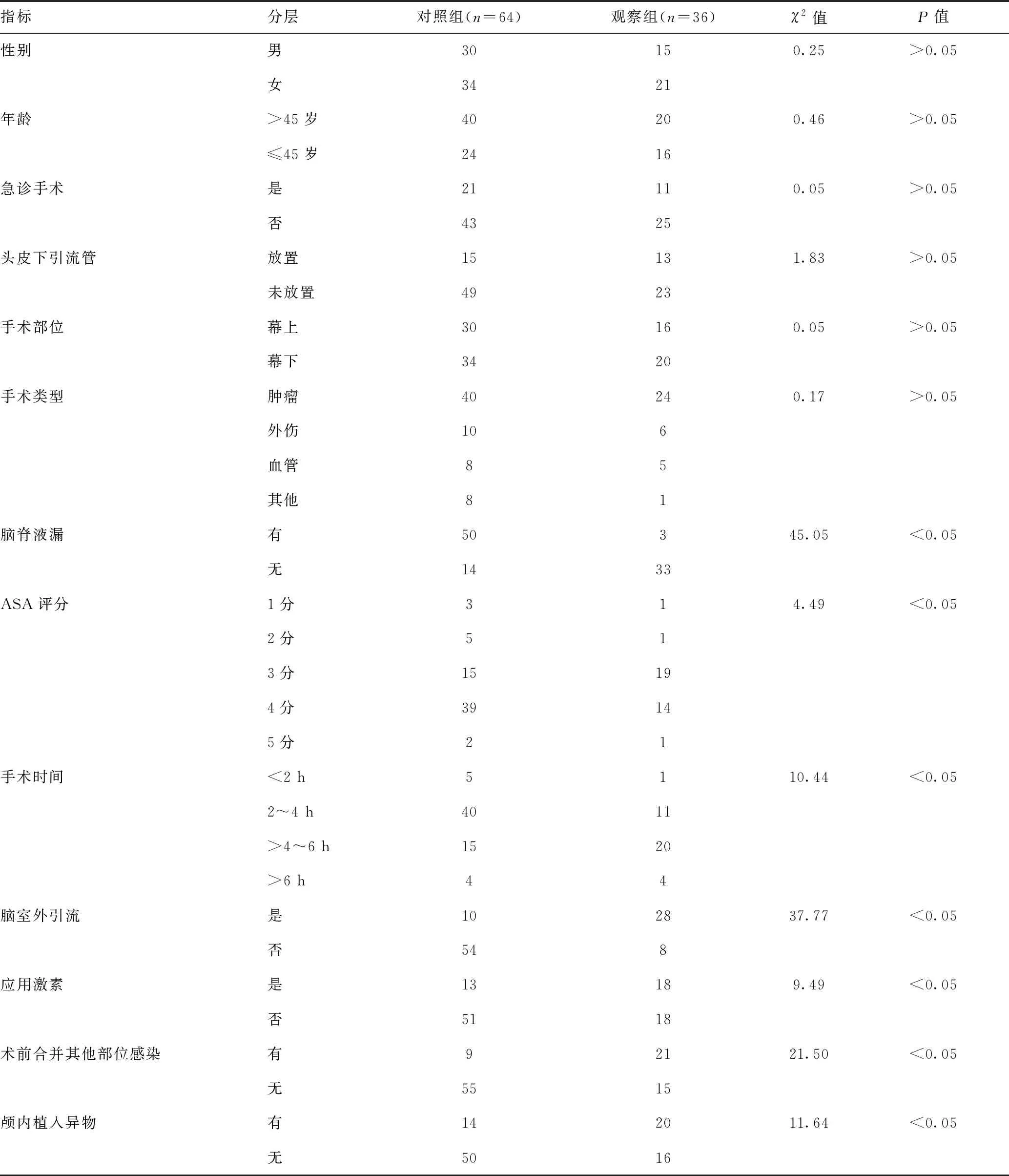
表1 患者術(shù)后顱內(nèi)感染的單因素分析(n)
2.2影響患者術(shù)后顱內(nèi)感染的獨立危險因素分析:多因素Logistic回歸分析中,手術(shù)時間、術(shù)后腦脊液漏、腦室外引流、術(shù)前合并其他部位感染,是致使患者術(shù)后誘發(fā)顱內(nèi)感染的獨立危險因素,差異有統(tǒng)計學(xué)意義(P<0.05)。見表2。

表2 影響患者術(shù)后顱內(nèi)感染的獨立危險因素分析
3 討論
行顱腦手術(shù)治療患者術(shù)后常合并有多種并發(fā)癥,如顱內(nèi)高壓、顱內(nèi)感染、腦積水、腦膨出等,其中又以顱內(nèi)感染在術(shù)后發(fā)病率最高,達3.97%~8.99%。術(shù)后顱內(nèi)感染不僅會對患者預(yù)后造成負面影響,還會延長其治療時間,增加患者經(jīng)濟負擔(dān)的同時嚴重者還可能會危及生命,降低患者生存質(zhì)量[5]。因此,臨床強調(diào)需明確患者顱腦術(shù)后關(guān)于顱內(nèi)感染的危險因素,早期采取有預(yù)見性的防控手段進行干預(yù),為降低患者顱內(nèi)感染風(fēng)險提供科學(xué)依據(jù),對其預(yù)后改善同樣有重要現(xiàn)實意義。
與此同時有報道指出,顱內(nèi)感染發(fā)病機制復(fù)雜,而在神經(jīng)外科開顱手術(shù)患者中,特別是重度顱腦損傷患者,其圍術(shù)期間因為血腦屏障破壞、開顱術(shù)式所建立的開放性通道也為各種致病菌提供了進入路徑,造成顱內(nèi)感染。手術(shù)模式、手術(shù)時間長、術(shù)后引流管留置、腦脊液漏和其他合并癥狀等主客觀因素,都會極大影響患者體內(nèi)環(huán)境平衡,降低機體免疫力,為細菌感染機體建立條件和提高感染控制難度[6]。本研究顯示,腦脊液漏是患者行開顱術(shù)后常見病癥,因腦脊液腔直接通向顱外,當(dāng)顱外漏出腦脊液時即可稱為腦脊液漏,促使細菌經(jīng)腦脊液做媒介進入到患者顱內(nèi)造成感染。究其主要病發(fā)機制,具體可包括以下幾點:①患者硬腦膜縫合不密實或是未縫合,多見于開放性顱腦損傷患者所致硬腦膜缺損,術(shù)中未行修補,手術(shù)術(shù)式復(fù)雜,尤其是患者硬腦膜行減壓手術(shù)剪開后,其硬腦膜外各層組織未能縫合嚴密。②引流不當(dāng):患者術(shù)后引流有堵塞跡象,拔除管道后引流口后局部出現(xiàn)漏液,與此同時,引流口周圍組織愈合效果或直接壞死也是造成引流不暢的危險因素。③切口愈合不佳:患者手術(shù)局部所承受壓力受術(shù)后過高顱內(nèi)壓影響而持續(xù)提升,直至切口裂開。臨床中可通過采取以下幾點措施預(yù)防患者術(shù)后腦脊液漏:①將患者硬腦膜和頭進行嚴密縫合,并固定好顱骨;②必要情況下可酌情考慮應(yīng)用脫水劑來降低患者顱內(nèi)壓;③確診腦脊液漏者第一時間需保持絕對臥床休息,禁止劇烈活動,必要時可建議采取腰大池腦脊液引流術(shù)來降低顱內(nèi)壓,加快漏口愈合進度[7]。
手術(shù)時間過長也會增加患者顱內(nèi)感染風(fēng)險,術(shù)野長時間處于暴露狀態(tài),加上空氣和術(shù)者的手及其他物品頻繁接觸,細菌會通過附著在手術(shù)器械或主刀醫(yī)生的手部為路徑進入到患者顱內(nèi),提高術(shù)后感染率。此外,神經(jīng)外科手術(shù)所用顯微鏡技術(shù)雖然具有微創(chuàng)優(yōu)勢,但操作的精密性也間接性延長了手術(shù)時間,加上室內(nèi)空氣污染問題會隨手術(shù)時間延長而加劇,難以保持完全無菌環(huán)境。因此,臨床在患者病情允許下,盡量先做好完善的術(shù)前準備,開放性顱腦損傷者可有預(yù)防性地使用抗生素,要求醫(yī)生具備熟練手術(shù)操作和豐富臨床經(jīng)驗,嚴格無菌操作流程,盡可能縮減手術(shù)時長,降低感染發(fā)生風(fēng)險。
持續(xù)性腦室外引流促使患者誘發(fā)顱內(nèi)感染的高危因素,有報道指出,患者腦室外引流管放置時間超過7 d,腦內(nèi)感染概率就會有明顯提升,嚴重者還可能出現(xiàn)致命性腦室炎,威脅患者生命安全。此類感染多見于患者術(shù)后3~7 d,及時使用抗生素也難以預(yù)防感染問題,究其原因可能為患者放置引流管后其腦組織與外界建立了相通路徑,導(dǎo)致細菌經(jīng)引流管反流進腦組織,其腦脊液中補體和IgM含量極低,且缺乏吞噬細胞,為細菌的生長繁殖建立了良好環(huán)境。當(dāng)細菌侵入患者腦室,將難以控制其感染癥狀。因此,臨床主治醫(yī)生需嚴格掌握引流管留置的適應(yīng)證和原則,患者行開顱術(shù)后即使需留置引流管,通常在術(shù)后24 h~48 h內(nèi)盡早拔除,留置時間不可超過5 d。若患者因手術(shù)需求導(dǎo)管留置時間要超過10 d,建議采取內(nèi)引流術(shù),定期做好引流袋更換及無菌拔管,并縫合引流口[8]。
術(shù)前合并其他感染會增加患者術(shù)后顱內(nèi)感染風(fēng)險,如術(shù)前合并上呼吸道、肺部、血液或泌尿系統(tǒng)感染者,都會間接影響其機體正常生理反射功能,加上麻醉誘導(dǎo)所行氣管插管會對患者呼吸道黏膜造成損傷,術(shù)后需長期臥床且后組顱神經(jīng)麻痹,都會導(dǎo)致其術(shù)前感染癥狀加劇。與此同時,開顱手術(shù)會破壞患者血-腦脊液屏障,細菌從多個途徑(血液、感染局部處)侵襲顱內(nèi)組織,造成感染。因此,臨床表示術(shù)前需積極治療患者基礎(chǔ)病癥,解除病理反應(yīng)后再制定后續(xù)手術(shù)方案,保障手術(shù)安全。
綜上所述,針對行神經(jīng)外科開顱術(shù)治療的患者,其術(shù)后顱內(nèi)感染的主要危險因素包括手術(shù)時間過長、術(shù)后腦脊液漏、腦室外引流及其他部位感染等,臨床可根據(jù)其誘發(fā)因素來實施對應(yīng)防控手段,進而降低患者開顱術(shù)后顱內(nèi)感染風(fēng)險。
- 吉林醫(yī)學(xué)的其它文章
- 客觀結(jié)構(gòu)化臨床考核模式在藥學(xué)本科生實習(xí)前臨床技能考核中的應(yīng)用與研究
- 腦卒中患者吞咽障礙的飲食護理干預(yù)效果
- 基于德爾菲法與層次分析法構(gòu)建腹膜透析護理質(zhì)量體系在腹膜透析患者護理中的應(yīng)用
- 術(shù)前系統(tǒng)免疫炎性指數(shù)及預(yù)后營養(yǎng)指數(shù)對Ⅲ期結(jié)腸癌患者預(yù)后預(yù)測價值及護理指導(dǎo)意義
- 加強階段性康復(fù)護理對髖關(guān)節(jié)置換術(shù)后患者VAS及Harris髖關(guān)節(jié)評分的影響
- 老年菌陽肺結(jié)核病患者規(guī)律抗結(jié)核治療的療效及其危險因素

