MOFs 的合成及其在食品包裝中的應用研究進展
全鑫瑤,隋思瑤,黃桂麗,孫靈湘,馬佳佳,王毓寧
(蘇州市農業科學院,江蘇 蘇州 215105)
食品包裝是現代食品工業的最后一道工序,不僅利于食品的宣傳和銷售,更便于食品的貯藏和運輸。食品包裝材料作為食品的“貼身衣物”,能夠有效地解決由化學殘留、物理損傷和微生物侵染等導致的食品腐爛或病變問題。隨著經濟的發展,現代社會對食品包裝材料的保鮮、保質性能提出了更高的要求[1]。納米復合材料作為納米高新技術的產物之一,正逐漸進入人們的日常生活中,也為食品包裝材料的進一步發展注入了新活力[2-3]。
納米復合材料一般由傳統包裝材料與新型納米材料(金屬或氧化物納米顆粒、石墨烯、碳納米管和黏土等)復合而來,用以增強食品包裝材料的功能屬性[4-5]。由于納米效應的存在,納米材料可作為酶載體、抗氧化劑、抗褐變劑、香料和抗菌劑等[3],因此與傳統包裝材料相比,納米復合材料通常具有更高的強度、韌性、阻隔性、抗菌性[6]。例如,將ZnO[7]、TiO2[8]、Ag[9]和殼聚糖[10]納米顆粒添加至聚合物薄膜中,不僅可以大幅提高薄膜對氧氣和水氣的阻隔性能,還可以顯著提高薄膜的機械強度、阻光性能和抗菌活性等。納米復合材料另一個突出的優勢在于具備比傳統塑料更好的食品保鮮能力,同時兼具良好的可降解性,對環境十分友好[11]。例如,納米黏土(無菌皂石)/細菌纖維素復合薄膜與傳統PET 薄膜相比,具有更加優異的特性(超強、超韌、透明、低熱膨脹系數),并且在2 個月內就可完全降解。該納米復合材料有望作為塑料薄膜的替代品,以減少“白色污染”[12]。隨著納米復合材料在食品包裝中的應用和推廣,實現對食品的抗氧化性、抗菌性、水分遷移規律、呼吸強度等特性的精準調控將成為可能[13]。此外,納米復合材料可以提高綠色包裝材料的減量化、資源及回收處理等方面的性能,在使用時不會與食品相互作用,而且對人類、動物和環境的危害性較低。基于上述優勢,納米復合材料在食品包裝領域中具有廣闊的應用前景[11]。
納米復合材料的核心是包含納米材料,不同的納米材料往往會賦予復合材料不同的特性。金屬有機框架(Metal Organic Frames,MOFs)是一類納米多孔材料,它由有機配體與金屬節點(離子或簇)依靠配位鍵結合組裝而成,具有規則的孔道和巨大的比表面積(1 000~10 000 m2/g)。金屬元素和有機配體的多樣性使得MOFs 材料具有種類繁多、形貌尺寸多樣、孔結構多變及功能豐富多彩等特點[14]。自1990 年MOF 材料首次被報道以來,在過去短短30 多年時間就已經有超過20 000 種不同的 MOFs 材料被合成出來[15]。源于獨特的金屬-有機晶體結構,MOFs 不僅具有金屬活性,還兼具有機配體的柔性和其他物理化學性能,同時還有特殊的孔道結構。在這些有利因素的協同作用下,MOFs 被賦予了卓越的氣體吸附或分離能力、優異的催化活性、良好的抗菌性、低細胞毒性和靈敏的傳感性等[15],使得MOFs 成為構建新型納米復合食品包裝材料的重要角色之一[16-17]。目前,已有大量的研究證實MOFs 作為食品包裝材料的可行性和獨特優勢[18]。例如,在聚合物薄膜中添加MOFs晶體可以增強薄膜的氣體分離能力、機械強度和熱穩定性等[19-20],各種聚合物-MOFs 復合材料可通過釋放金屬離子或表面相互作用進行抗菌和殺菌[21-23]。
這篇關于MOFs 材料在食品包裝材料中的應用研究進展的綜述首先總結了MOFs 的合成方法,接著按照功能進行分類,對MOFs 及其復合材料的研究進展進行了介紹。此外,還討論了MOFs 面臨的問題和發展趨勢。
1 MOFs 的合成機理
1.1 MOFs 的形核與生長
理解MOFs 材料的液相成核機制和早期生長的過程,對于MOFs 的設計和制備至關重要,如圖1 所示[14]。過去的10 多年里,隨著各種無創原位散射技術(XRD、SAXS、DLS、EXAFS 等)、顯微技術(AFM、SEM、STM、HRTEM 等)、光譜分析技術(NMR、MS、ICP、SPR 等)、模擬技術(First Principle、Molecular Dynamic、Monte Carlo 等)的發展和完善,在不同時間尺度、空間尺度和相態內的MOFs 的形核與生長機制研究取得了大量成果[24]。結果表明,MOFs的成核方式與傳統晶體材料一樣,也可以分為經典和非經典成核兩大類。

圖1 MOFs 的組成結構[14]Fig.1 Formation of MOFs[14]
MOFs 經典成核的晶核是形核單元(Nucleation Building Units, NBUs),該單元是原子、離子或分子通過基團凝聚成的最小集合體。NBUs 作為MOFs 的次級結構單元(Secondary Building Units, SBUs)的亞單元,其尺寸介于金屬離子與SBUs 之間,是一種可溶性金屬配合物或絡合物。NBUs 在等電點與金屬離子、有機配體或者其他NBUs 發生縮合形成SBUs,SBUs 再與有機配體周期性重復橋聯組裝形成最終的MOFs。此外,非經典成核也是MOFs 材料的常見形核方式之一,其過程大致可以分為3 個步驟:第1 步為相分離,反應溶液中液-液相分離,形成溶質豐富區域;第2 步為濃縮,已經形成的溶質豐富區域進一步濃縮, 形成了無定型的聚集體(Amorphous Aggregation);第3 步為晶化,無定型聚集體進一步晶化,形成了MOFs 晶核[25]。
MOFs 晶體的生長過程較為多樣化,會受到熱力學和動力學條件的協同控制。在過飽和狀態下,熱力學條件占主導地位,此時生長單元的擴散和表面整合共同控制著晶體的生長過程[26]。具體來講,在過飽和度較低時,生長單元更傾向于不斷附著在螺型位錯產生的局部臺階處,而整個晶面則呈螺旋狀上升,且逐層向上延展成長。在過飽和度稍高時,生長單元除了可以附著在臺階處外,還可以附著在紐結部位,實現晶體的層生長。隨著過飽和度的進一步增加,生長驅動力大大升高,生長單元可以整合至任何缺陷,而不受吸附能的影響,從而導致晶體連續生長,并最終生成球狀、樹杈狀晶體。簡單來說,在熱力學條件控制下MOFs 晶體的生長過程始終遵循2 個條件:一是晶核(晶體內部)在整個生長過程中保持與最終產物相同的晶相;另一個是晶體的生長始終通過生長單元逐漸聚集而成。
在動力學條件控制下,MOFs 晶體的生長機制多種多樣,包括無定形粒子的聚集機制[24]、奧斯特瓦爾德熟化(Ostwald's Rule of Stages)機制、非晶到晶態轉變機制[27]、晶面溶解和再生機制、定向連接生長機制[28](Orientated Attachment)等。例如,趙學波團隊[29]研究發現,HKUST-1 的生長過程是一種非經典的結晶模型“定向附著晶化”過程(Crystallization by Particle Attachment, CPA)。如圖2 所示,該MOF 晶體的生長經歷了3 個過程,分別為納米晶體、超結構顆粒和單晶的形成。在形核階段,溶液中的金屬離子與有機配體進行隨機組裝配位,產生了超細納米初晶;隨后,納米顆粒再有序地組裝成超結構大顆粒,該大顆粒具有規則的形貌;反應時間進一步延長,超結構大顆粒發生Ostwald 熟化,褶皺的外表逐漸被修補完善,最后生長成為完美的單晶。該CPA 過程與建房子類似,先建造出房屋框架,再“添磚加瓦”。不同類型房屋的主體框架不同,不同MOFs 材料也有各自不同的特殊超結構,并且這種超結構具有與其本征MOFs 材料不同的特殊性質。
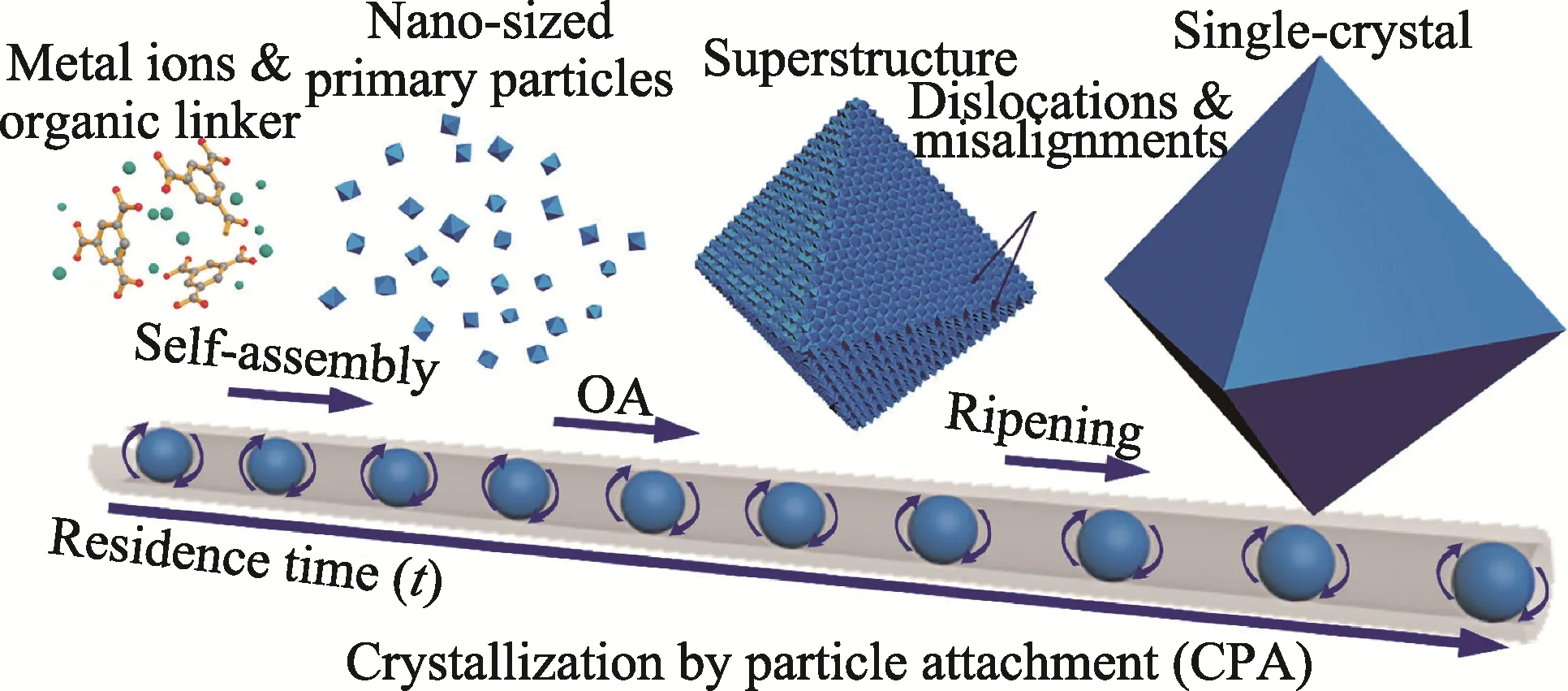
圖2 HKUST-1 晶體形核與生長示意圖[29]Fig.2 Schematic diagram on the pathway of CPA process for HKUST-1[29]
需要特別注意的是,MOFs 的形核和生長過程并不是一成不變的。反應試劑、調節劑和溶劑的選擇,以及加熱方法、反應時間甚至升溫速率的調節均會改變合成反應的熱力學和動力學條件,從而對MOFs的形核和生長過程進行調控。例如,采用微波或超聲波方法改變了結晶機制,并普遍提高了成核/生長速率[30-31]。強酸弱堿型金屬鹽比弱酸弱堿型金屬鹽的電離能力更強,也能提高成核/生長速率[32]。由此可見,MOFs 合成中的一個關鍵挑戰是目前仍無法準確預測某給定試劑組合產生晶粒的尺寸和形貌。不斷發展的時間分辨和原位表征手段將會加深人們對MOFs 成核和生長過程的了解,從而為MOFs 晶體合成反應參數的選擇提供理論指導。
1.2 MOFs 晶體的尺寸效應
除了化學組成外,晶體尺寸是控制納米材料物化性質的另一個重要因素。例如,沸石晶體的尺寸和形貌與其工業催化效果密切相關[33]。晶體尺寸效應同樣存在于MOFs 材料中,對吸附、催化和光電性能有著重要影響,尤其在柔性MOFs 材料中的作用更加顯著。柔性MOFs 指在外界刺激下能發生可逆的框架結構轉變的一些MOFs[34]。框架結構的靈活性使得柔性MOFs 在氣體儲存與分離、藥物控制釋放和減震等領域具有廣闊的應用前景。MOFs 框架靈活性主要體現在3 種模式上[35]。
1)開孔-閉孔轉變,即在外界刺激下有機配體的距離發生明顯變化,使得內部孔結構消失或者出現。例如,Zr 基MOF-NU-910[36]在N, N-二乙基甲酰胺(DEF)中呈開孔狀態,相鄰咪唑配體π-π 堆積距離為0.832 nm,而在丙酮中浸泡一段時間后則呈閉孔狀態,此時相鄰咪唑配體π-π 堆積距離僅為0.320 nm,將閉孔的NU-910 浸泡在DEF 中又可恢復為開孔狀態。
2)呼吸作用,指由客體吸附-脫附驅動的結構轉變,涉及MOF 的晶胞體積和相應孔徑的顯著變化。例如,在Cd-MOF[36]的初始框架結構中,晶格間隙間存在一定量的結晶水,晶胞結構松弛。在加熱或真空條件下,MOF 框架會發生動態呼吸,將晶格間隙間的水分子分步呼出,晶胞結構收縮。當回到室溫和空氣條件時,晶胞結構又回復到初始的含水松弛狀態。
3)負氣體吸附,指當外界客體分子的壓力達到一定程度后,MOFs 結構突然變形后孔隙收縮,并吐出之前已經吸附的客體物質。例如,這種與負熱膨脹、負折射率等反直覺現象類似的負氣體吸附在DUT-49中被觀測到[37]。
MOFs 晶體尺寸效應最先在柱撐層類MOFs 中被發現[38-39],大塊晶體(粒徑>300 nm)在吸附和去除甲醇中表現出由開孔相到閉孔相的結構轉變,而粒徑小于臨界尺寸的晶體無論孔道內是否含有甲醇都始終保持開孔結構。隨后,ZIF-8 在N2氛圍中存在開閉孔的靈活性也得到驗證,且其開-閉孔轉換的開啟壓力會隨著晶體尺寸的減小而增加[40]。此外,DUT-8中也觀察到晶體尺寸對開閉孔的影響,DUT-8(Ni)和DUT-8(Zn)的臨界粒徑分別約為500、200 nm。當晶粒直徑小于臨界值時,MOFs 無法實現開閉孔的轉變。對于呼吸型MOFs 和負氣體吸附型MOFs 而言,晶體尺寸也存在臨界值。例如,MIL-53(Al)-NH2尺寸低于臨界值,則無法對二甲基甲酰胺(DMF)進行吸脫附[41],DUT-49 的晶粒直徑低于1 000 nm 時,對N2的負吸附作用會消失[42]。
以上研究均表明,晶體的縮小會抑制柔性MOFs框架結構的轉變,但是有些MOFs 晶體并非如此。大塊Fe(py)2[Pt(CN)4]晶體在吸附方面沒有表現出靈活性,當其厚度在16 nm 以下時具有開-閉孔轉換行為[43]。這是因為大塊晶體中吡啶配體的強層間π-π 相互作用,阻止了客體分子在框架中的深入擴散,但縮小尺寸后,每個框架層之間的π-π 相互作用減弱,客體分子得以自由進出。2D-ELM-11 的納米片在對N2和CO2吸附中,開閉孔轉變也表現出了相似的尺寸效應[44]。
由此可見,晶體尺寸效應對框架靈活性的影響應具體情況具體分析,要獲得柔性MOFs,一定要確保其晶體尺寸在合理范圍之內,這也為柔性MOFs 的合成提供了指導[45]。
2 MOFs 的合成方法
理論上,通過設計有機配體和金屬離子或簇構筑的次級構建單元,可以實現對 MOFs 最終框架結構的預測,可以合成具有預期結構和功能的MOFs。該設計思路在熱力學上是簡單合理的,但是受到反應動力學因素的影響,所得MOFs 結構往往難以符合預期[32]。MOFs 合成過程的反應動力學因素主要為溫度、壓力、時間、溶劑、pH 值、反應物濃度等工藝參數,它們都會影響MOFs 的物相結構、微觀形貌、粒徑分布等性質[46]。目前,絕大部分MOFs 材料的發現和優化通常是在反復試驗、化學直覺或大規模篩選的基礎上完成的[38]。其中,大多數MOFs 是在高溫高壓下通過溶劑(水)熱法合成的,這是制備MOFs 的經典方法。此外,如圖3 所示,MOFs 的合成方法還有擴散合成法、溶劑熱合成法、離子熱合成法、微波合成法、聲化學合成法、電化學合成法等。
2.1 共沉淀法
共沉淀法的主要過程(圖3)是將有機配體、金屬元素與其他原材料在某溶劑中混合后,再在常溫常壓下連續攪拌一定時間,然后將沉淀物過濾,從而分離反應產物,并進一步干燥后獲得MOFs 晶體。通過此方法合成的納米晶體包括 ZIF-8、Ag-MOF、MIL-53-Fe 等,ZIF-8 是粒徑為85 nm的正六面體[47],Ag-MOF 是粒徑為40 nm 左右的棒狀晶體[48],MIL-53-Fe 是粒徑為50 nm 左右的正八面體[49]。

圖3 MOFs 的不同合成方式Fig.3 Different synthesis methods of MOFs
共沉淀法的優勢在于過程較簡單、條件溫和,且制備出的MOFs 通常具有較高的化學穩定性和熱穩定性。由于反應條件為常溫常壓,故該方法合成出的MOFs 晶體一般較小且結晶度不高。尤其是對于惰性金屬離子,需要升高反應溫度來提高其結晶性[32]。
2.2 擴散合成法
擴散合成法包括液相擴散法、凝膠擴散法和氣相擴散法等。液相擴散法:將2 種分別溶有金屬鹽和有機配體但互不相溶的溶劑混合后,金屬離子和有機配體同時向溶劑界面處擴散,二者接觸后生成相應的MOFs[50]。凝膠擴散法:首先將有機配體分散在凝膠基質中,然后將凝膠與金屬離子溶液浸泡一段時間,金屬離子逐漸向凝膠中擴散,并與分散其中的配體反應后,即可得到分布在凝膠中的MOFs 晶體[51]。氣相擴散法(圖3):將易揮發的有機配體溶液作為反應物,當配體隨著溶劑揮發后與金屬離子溶液接觸,并充分反應后生成了MOFs[52]。
擴散合成法可用于溫和反應條件下合成結構敏感型MOFs,但是其反應時間較長。Shearer 等[53]通過擴散合成法在100 ℃下反應14 d 制備了UiO-661。
2.3 溶劑熱合成法
溶劑熱合成法(圖3)概括來講就是將有機配體、金屬離子、水或有機溶劑與調節劑按比例均勻混合后,轉移至反應釜中高溫反應一段時間,然后將獲得的產物用去離子水和無水乙醇連續洗滌數次,以除去雜質,最后經真空干燥后得到純MOFs[54]。
溶劑熱法合成出的MOFs 的結晶性一般較高,且容易獲得單晶。此外,溶劑熱合成法還可通過改變反應條件來控制晶體的形核速率和生長速率,故該方法的適用性非常高,應用最為廣泛。例如,MOF-5、MOF-74、MOF-177、ZIP-8 等均可通過該方法制備[18]。不過,溶劑熱合成法往往需要高溫高壓,危險系數較高,且廢物產生率較高。
2.4 離子熱合成法
離子熱合成法(圖3)是將離子液體作為常規有機介質或水的替代物來合成 MOFs。與傳統溶劑相比,離子液體具有可回收性、零蒸汽壓、優異的溶解性和高穩定性等特點[55]。此外,離子液體還可提供陰離子或陽離子作為中和離子,同時充當合成MOFs 的硬模板。這些優勢使得離子熱合成法已經成為MOFs 的主要制備方法之一。例如,HUSK-1是以氯化膽堿/二甲基膽堿為溶劑,通過離子熱合成法制備得到[18]。
離子熱合成法是一種綠色合成方法,可以在沒有回流冷凝器的情況下進行中高溫合成,且MOFs 的物理化學性質可通過改變離子液體的組成來控制。如果離子液體中存在少量雜質或殘留物,則合成出的MOFs 的熱穩定性會降低[56]。
2.5 微波合成法
微波合成法(圖3)的原理是利用電磁能轉化為熱能,以促進反應的發生。在外加交變電磁場的作用下,反應物中的極性分子會發生極化,并隨外加交變電磁場極性的變更而交變取向,如此眾多的極性分子因頻繁相互摩擦損耗,使得電磁能轉化為熱能,使反應體系的溫度迅速提高,從而使金屬離子與有機配體鍵合。
微波合成法具有反應裝置小、能耗低、反應速度快、產生的化學廢棄物少等特點,且合成出的MOFs純度高、晶體尺寸可控,被認為是MOFs 的主要制備方法之一。Fe-MIL-53[57]、ZIF-8[58]和Fe-MIL-101-NH2[59]等均被證實可由微波合成法制得。微波合成法的缺點在于很難通過調節輻照功率來改變反應條件,不同的儀器無法提供相同的條件,最終會影響實驗的可重復性。
2.6 聲化學合成法
聲化學合成法(圖3)利用超聲波的“空化作用”來合成MOFs。當高能超聲波(20 kHz~10 MHz)輻射反應溶液時,其內部的氣泡快速破裂,瞬間會產生高溫高壓(約為5 000 K、100 MPa),從而促進化學反應,生成所需的MOFs[32]。
超聲空化十分有利于均勻形核,可大大縮短反應時間、減小晶粒尺寸。例如,Son 等[31]首次使用聲化學方法在顯著縮短合成時間(約30 min)的情況下合成了尺寸為5 ~ 25 μm 的MOF-5 晶體,與溶劑熱合成法(24 h)相比,所得晶體的質量更高。此外,高質量IRMOF-9[60]、HUSK-1 和Mg-MOF-74[61]等也可通過聲化學合成法快速制備。聲化學合成法具有節能環保的優勢,在室溫下即可進行,但有時無法控制其合成溫度。
2.7 電化學合成法
如圖3 所示,電化學合成法需要在電解槽中進行,將陽極(純金屬)和陰極(碳棒或鉑片)浸入溶有有機配體的酸性電解液中。在發生電化學反應時,金屬陽極被氧化溶解,從而持續產生金屬離子,并進入電解液中,隨后與有機配體反應,會在陰極產生氫氣。HKUST-13、Al-MIL-53-NH2、ZIF-8 和Al-MIL-100 是使用電化學法合成的MOFs[62]。
電解質、溫度、電壓電流密度、合成產率和織構性質是MOFs 電化學合成過程中的重要參數。與上述6 種間歇反應合成法相比,電化學合成是一個連續的過程,產量、產率較高,可以作為一種工業方法來合成MOFs。
一般而言,使用相同的反應前軀體(金屬源、有機配體和溶劑),但采用不同的合成方法和條件,能夠得到不同粒徑、孔隙率和形貌的MOFs,從而進一步影響MOFs 的功能。如上所述,已有多種方法可以制備出結構新穎、性能優異的MOFs 材料,比如溶劑熱合成法、聲化學合成法、微波合成法、電化學合成法等。如表1 所示,各類方法均有優缺點,在一定程度上拓寬了MOFs 的發展與應用。

表1 各種MOFs 合成方法的優缺點對比Tab.1 Advantages and disadvantages of MOFs synthesis methods
3 MOFs 在食品包裝材料中的應用
隨著生活水平的不斷提高,食品安全和品質越來越受到人們的重視,傳統包裝材料的被動惰性屏障效應已無法滿足當代消費者的需求。針對食品的不同特點,設計相應的功能化包裝體系實現食品的貯藏保鮮是目前食品包裝行業領域亟待解決的問題。受益于結構和功能的多樣性,各種各樣的MOFs 材料越來越多地應用于食品包裝領域。
3.1 MOFs 作為食品包裝材料中的抗菌劑
如圖4 所示,MOFs 是一種良好的金屬離子儲存庫,可緩慢釋放出金屬離子。一方面,MOFs 緩釋出的金屬離子可通過接觸反應直接造成微生物固有成分的破壞,或產生功能性障礙,例如細胞膜破裂、細胞質流失和物質傳輸受阻等。金屬離子緩釋的難易程度決定了 MOFs 的抗菌效果。例如,若MOFs 的結構穩定性較差,則更容易釋放出金屬陽離子,抗菌效果更好。此外,MOFs 中的某些有機配體,如咪唑類、噻唑類和酚類等也具有抗菌性,可與MOFs 釋放的金屬離子協同作用來提高其抗菌能力[23]。另一方面,MOFs 本身具有催化作用,在光的作用下會激活水和空氣中的氧,產生活性氧自由基(Reactive Oxygen Species,ROS),ROS 的氧化能力極強,能在短時間內導致細菌的死亡,從而達到抗菌的目的[21]。

圖4 MOFs 的抗菌機理示意圖[21]Fig.4 Antibacterial mechanisms of MOFs[21]
近年來,MOFs 的優異抗菌性能受到越來越多的關注,這方面的研究也日益增多。例如,Liu 等[21]研究發現,由于Ag+具有優越的抗菌能力,Ag-MOFs 在菌群中也可展現出較好的抗菌活性。同時,Colinas 等[22]研究評估了2 種Zn-MOF 對大腸桿菌和表皮葡萄球菌的殺菌活性,由于Zn-MOF 可與細胞膜表面的親脂酸或羥基相互作用,并穿透細菌,引起細胞的損傷,因此這2 種Zn-MOFs 在液體和固體介質中均表現出比Zn單質更高的抗菌活性。Zhuang 等[63]報道了一種新的Co-MOF,它可以有效破壞大腸桿菌的外膜。Guo 等[23]合成了核殼型 Ag@ZIF-8 納米線,隨后評估了Ag@ZIF-8 納米線對枯草芽孢桿菌和大腸桿菌的抗菌效果,當Ag@ZIF-8 的質量濃度為200 μg/mL 時,可以完全抑制枯草芽孢桿菌細菌的生長。
MOFs 除了自身為抗菌劑外,還可充當其他抗菌物質的載體。Zhao 等[64]研究發現,紅辣椒提取物——辣椒素是一種有效的抗菌物質,于是將Fe-MOF 作為載體負載辣椒素,并且添加于明膠/殼聚糖的薄膜基質中,制成抗菌包裝薄膜。此法不僅極大地提高了薄膜的水蒸氣滲透性、紫外線阻隔性能和拉伸強度,還對大腸桿菌也表現出良好的抗菌性。
總之,由于MOFs 能夠控制/刺激分解具有殺菌活性的成分,可以與細菌膜產生強相互作用,在光催化下會形成ROS,且還具有高負載和持續釋放能力等優異特性,使得MOF 材料具有優異的抗菌特性。MOFs 已成為抗菌的理想材料,為食品用抗菌包裝材料提供了一種有效的改性方法[65]。
3.2 MOFs 作為果蔬的催熟控制器
控制果蔬,尤其是躍變型水果在儲運過程中的成熟度,對于確保產品在到達市場時處于最佳狀態非常重要,果蔬成熟度的關鍵影響因素為乙烯的濃度。目前,行業內主要依靠提前采摘、低溫貯藏和O2/CO2氣氛調節來延緩乙烯的產生,或根據需要利用乙烯利促使乙烯的釋放。實際上,直接對果蔬所處環境中的乙烯進行調控是最有效的方法,但是基于安全問題,乙烯不能直接用于果蔬的貯藏。
MOFs 具有可調組成、結構、孔徑、體積、官能化、柔性結構等特點,使得MOFs 可以作為乙烯分子的吸附和釋放調控器。Zhang 和Banerjee 等[66]利用溶劑熱法合成了一種孔隙率為0.39 cm3/g 的Cu-TPA MOFs,先將乙烯在其孔道內充滿,再讓其釋放出乙烯,并對水果進行催熟。50 mg 的Cu-TPA 可以吸收/釋放654 μL的乙烯,構成了一個富含足夠乙烯的環境,以控制水果的成熟度,且滿足乙烯的安全使用標準(< 27 000 μL/L)。在使用MOFs 對乙烯進行控制后,水果的組織硬度降低,與成熟相關的顏色變化加速。
MOFs 還可以實現在特定條件下對乙烯的釋放。Chopra 等[67]通過電化學合成法制備了MOF-199,它是一種以偏苯三甲酸為有機配體的銅基MOF。作者還評估了其在調節乙烯水平以控制易腐農產品的成熟度的實用性。研究發現,充滿乙烯的MOF-199 暴露在干燥的空氣中時,它們基本不會釋放出乙烯,在相對濕度超過50%時,MOF-199 脫附了大部分乙烯。這一選擇性解吸現象為MOFs 按需調控水果的成熟度提供了可能。MOFs 不僅可用于水果的催熟,還可以用于抑制水果的成熟。例如鈣-4,4′-磺酰二苯甲酸、銅-2,4,6-三(3,5-二羧基苯氨基)-1,3,5-三嗪、鋅-四(4-溴代苯基)乙烯等MOFs 均可以高效吸附和解吸乙烯抑制劑(1-甲基環丙烷),從而減緩水果過早成熟的進程。
以上研究表明,隨著MOFs 材料研究和應用的不斷深入,MOFs 封裝乙烯或1-甲基環丙烷在果蔬活性包裝領域具有較好的應用潛質。
3.3 MOFs 作為水分和氧氣清除劑
氧化反應會導致食品在短時間內變質,這是食品生產商面臨的主要挑戰之一。由于食物捕獲水和氧分子的能力較強,即使充入惰性氣體仍然無法徹底避免氧化問題。MOFs 材料在具有超高比表面積的同時,也具有較好的水穩定性,使得它能夠清除食品包裝袋/盒內的殘余水和氧分子,可成為干燥劑的有效替代品[68]。
例如,一些MOFs 在5 次吸脫附循環后,水的吸附容量無衰減,且自身結構未發生改變[69-70]。有學者合成了一種MIL-101(Cr)包覆二茂鐵(Fe(η-C5H5)2)的復合材料,其較高的比表面積可用于吸附水分子;同時二茂鐵中的Fe2+具有還原活性,在接觸氧氣的同時可以原位轉化為Fe3+,從而消耗氧氣[69]。Burtch 等[71]通過溶劑熱法合成了MIL-101,發現MIL-101 具有良好的熱力學穩定性、動力學穩定性和水穩定性等,在室溫下能有效去除氧氣。馬益平等[72]對MIL-101(Cr)進行氨基功能化處理,該功能化材料具有優異的水蒸氣吸附能力,在常溫、常壓下可以將相對濕度從71%降至38%,在氣調包裝領域具有潛在的應用價值。
3.4 MOFs 作為生物活性物質的載體
MOFs 中的大孔可以封裝一些活性物質,在不改變物質活性的同時還能提高其穩定性。Moussa 等[73]研究發現,與堿性條件下的游離姜黃素相比,通過CD-MOFs 封裝的姜黃素的穩定性提高了至少3 倍。Wang 等[74]使用微孔Zn-MOF 封裝 AITC(異硫氰酸烯丙酯),用來有效保護AITC 免受相對濕度的影響,封裝后的Zn-MOF 依然可以維持結構穩定性。隨后,Lashkari 等[75]研究發現,HKUST-1、MOF-74 和RPM6-Zn 均能在寬濕度范圍內有效捕獲和釋放AITC 分子。Al-Ghamdi 等[76]通過合成高表面積、多孔結構的γ-CD-MOF 成功地包裹封裝了乙醛。以上研究均證明,MOFs 具有把揮發性有機物封裝在其孔道,并保持其化學活性的良好能力。
3.5 MOFs 作為毒害物質檢測劑
由于農藥污染、環境污染等因素,一些有毒、有害物質會殘留在果蔬產品中。其中,多氯二苯并二噁英(PCDDs)及其代表物是持久性有機污染物中毒性較大的化合物[77]。盡管這些化合物的總攝入量非常低,但它們會通過飲食在人體內進行生物積累,所以食品中的二噁英風險不容忽視[78]。然而,對于PCDDs及其代表物的識別和檢測非常具有挑戰性。
Wang 等[79]合成了一種高度穩定的鋯基金屬有機骨架(BUT-17),其具有一維六方孔道和富苯基孔表面,基于結構的熒光淬滅性質,可以識別和檢測2 種具有代表性的PCDDs:2,3-二氯二苯并二噁英(BCDD)和2,3,7,8-四氯二苯并二噁英(TCDD)。BUT-17 對BCDD和TCDD 的檢測限分別為27、57 ng/mL,靈敏度非常高,并且具有很強的選擇性,不受類似化合物的干擾。
MOFs 對PCDDs 識別和檢測具有潛在的應用價值,為將功能MOFs 應用于食品包裝領域開辟了新的方向。MOFs 作為一種有機化-無極雜化納米材料,針對其毒性的評估是必不可少的,有機配體和金屬離子的存在、晶體納米尺寸、合成過程均是MOFs 具有毒性的主要原因[31,80-81],食品包裝材料中對于材料安全性的要求極高,因此大力開發無毒MOFs 材料,并用于食品包裝材料成為目前的研究目標。例如,Smaldone 等[82]研發獲得的 CD-MOF-1、環糊精MOF-1 材料是采用食品級γ 環糊精與苯甲酸鉀通過蒸汽擴散法制備而成,具有無毒安全等特性。此外,Yang 等[83]也開發了2 種無毒的MOF——MOF-1203、MOF-1201,是由鈣鹽和L-乳酸通過水熱法制備得到的棒狀晶體。
4 結語
MOFs 呈現出優異的功能可調性、生物相容性及與其他材料的復合性,在抗菌保鮮、果蔬催熟、除水除氧、活性化合物的控釋、毒害物質的檢測等方面具有巨大的應用潛力和優勢。將所需原子或有機官能團接枝到金屬離子/簇或有機配體上進行功能化修飾,與將特定客體分子(特殊氣體、生物大分子、納米顆粒等)封裝/限制在孔道內是目前開發功能化和智能化MOFs 材料的有效方法。盡管MOFs 材料在食品包裝中的應用取得了巨大進展,但是仍然存在一些挑戰。首先,需要考慮MOFs 的潛在毒性,必須對食品接觸中MOFs 的釋放及其對人類健康的安全性做出評估,這意味著開發可食用、可再生和可生物降解的MOFs 十分重要;其次,需要加強對MOFs 合成和改性方法的研究,期望設計并開發出更多具有可調節尺寸、形態和功能的MOFs 材料;今后的研究應側重于制備納米MOFs 改性的宏觀復合材料,如膜、紙和涂層等。因為目前多數研究都基于MOFs 粉末的開展,粉末的使用和回收問題限制了其大規模應用。希望MOFs 基食品包裝材料的研究能夠吸引更多跨學科團隊的關注,從而加大食品包裝材料的研究力度,以推進其實際應用。