注重基礎知識 助力“雙減”落地
——淺析2022年全國甲卷命題特點
安徽 尉言勛 楊 旭
2022年高考全國甲卷化學試題,認真貫徹“一點四面”命題思想,全面落實“一核四層四翼”高考評價體系的要求。試題契合教育教學基本規律、化學學科內容邏輯、高中學生認知特點,注重傳遞化學的應用價值,讓學生體會到化學的實用性。試題情境素材取材廣、立意新、情景真,突出考查化學學科主干內容,積極銜接高中育人方式改革,助力“雙減”工作,體現了高考積極的育人導向,有利于推進新一輪課程改革。
一、試卷結構分析

表1
【整體分析】選擇題考點基本保持穩定,與2021年的高考化學甲卷試卷相比,更加注重對離子方程式、化學實驗的考查,增加了陌生有機物結構簡式的分析,沒有出現難溶電解質溶解平衡的圖像題。離子方程式的考查注重引導學生了解反應的本質,有三個選項涉及量的問題,B項即使氨水過量,Al(OH)3也不與氨水繼續反應;C項通入二氧化碳氣體要分過量和少量兩種情況分析,產物有所差異;D項Ba(OH)2為二元堿,當兩者等濃度,體積比為1∶2混合時,溶液中電離出的氫離子和氫氧根恰好完全反應。元素推斷題的創新之處是Q、Z兩種元素的不確定性,拓展了學生的思維空間。學生備考時,要熟練掌握前20號元素之間的位置關系以及特征,能夠熟練運用元素周期律的相關知識分析問題和解決問題。
非選擇題類型和題目順序與2021年保持一致。第四周期過渡元素在近年高考中基本上均有考查,是工藝流程題的熱點載體。第Ⅷ族鐵元素的考查頻率非常高,每年均有涉及,2022年試題鐵元素依然以雜質形式呈現。27題為無機實驗和有機實驗的綜合考查,今年的實驗題更加注重考查考生的綜合能力,要用所學的知識結合題目中所給的信息,對整個實驗過程進行分析,考查學生理解提煉信息的水平。有四個設問考查了原因分析,要求學生具有運用學科知識進行說理和表達的能力,引導教師重視訓練學生的文字表達和邏輯思維能力。要讓學生遇到類似開放性的問題,有話可說,明白應該說什么,知道應該怎么說。化學反應原理題考查了金屬鈦(Ti)在航空航天、醫療器械等工業領域的重要用途。題目與生產實際結合得更加緊密,給出不同條件對“鈦氯化”反應平衡轉化率的影響,考查變化觀念與平衡思想核心素養,引導學生深刻理解化學平衡的本質。題目考查了壓強平衡常數的計算,側重考查學生提取圖像信息解決問題、分析問題的能力。
選考題的難度和呈現形式與2021年保持一致。第35題考查2022年北京冬奧會場館使用的高分子材料的結構與性質的關系,展現我國化學新材料的研發應用。側重考查碳、氮、氧、氟元素電離能的變化規律,讓學生理解原子結構與元素性質之間的關系。題目對氫鍵的考查方式十分新穎,要求畫出(HF)3的鏈狀結構,別出心裁。有機化學基礎題無傳統的有機合成路線圖的設計,①③步中的反應條件均源于教材,②步中的反應條件在2020年全國卷Ⅲ中第36題作為新信息給予,在魯科版新教材選擇性必修三第121頁作為香豆素合成路線的步驟呈現,可見命題者不是要求學生記住信息,而是希望學生能夠了解其知識本質,進而能夠遷移應用。第7問手性碳的考查,對學生知識面的廣度提出了較高要求。
二、試卷特點分析
1.注重情境選擇,突出價值引領
近兩年高考全國甲卷試題素材情境的選擇符合《普通高中化學課程標準(2017年版2020年修訂)》(以下簡稱《課程標準》)的要求,準確把握“素養”“情境”“問題”和“知識”四個要素在命題中的定位和相互關系。以陌生的情境考查學生熟悉的知識內容,既滿足高等學校的人才選拔要求,又有利于學生發揮出真實水平,題目密切聯系日常生活,圍繞材料、生命、環境、能源與信息等領域,體現了化學知識在社會生產實踐中的廣泛應用,凸顯化學學科的社會價值。例如全國甲卷第8題輔酶Q10具有預防動脈硬化的功效,26題硫酸鋅在防腐、電鍍、醫學上應用廣泛,27題硫化鈉廣泛用于染料、醫藥行業,28題金屬鈦(Ti)應用于航空航天、醫療器械等工業領域,35題美麗的透光氣囊材料,展現化學在生活中的重要性以及我國化學新材料領域的研發成果。
【例1】(2022·全國甲卷·8)輔酶Q10具有預防動脈硬化的功效,其結構簡式如圖1所示。下列有關輔酶Q10的說法正確的是

圖1
( )
A.分子式為C60H90O4
B.分子中含有14個甲基
C.分子中的四個氧原子不在同一平面
D.可發生加成反應,不能發生取代反應
【參考答案】B
【試題分析】試題素材情境取材廣泛,如第8題輔酶Q10的性質,表現化學研究成果在人類健康中的作用。本題與2021年全國甲卷第10題均考查有機物的結構與性質,不同之處是增加了試題情境的創設,比如考查反應類型,2021年試題直接呈現甲醇可發生的反應,本題需要學生先判斷該結構式中有哪幾種官能團,哪種官能團能夠發生加成反應,要求學生熟練掌握各官能團的性質以及官能團之間的轉化。本題的創新點是甲基數目的判斷,鍵線式的端點代表的是甲基,中括號右側端點的碳原子為甲基,所以分子中含有3+10+1=14個甲基,題目側重考查學生分析能力、運用知識的能力。
2.注重考查基礎性知識,通過經典題型,助力落實“雙減”
全國甲卷試題引導中學教學遵循教育規律,嚴格按照《課程標準》進行教學。以基礎知識為載體,引導教學回歸教材、夯實基礎,提質增效,助力“雙減”落地生根。比如阿伏加德羅常數,在2020年全國卷Ⅲ、2021年全國甲卷均進行了考查,需要學生具備推理能力;離子方程式,在2020年全國卷Ⅲ、2021年全國乙卷均進行了考查,要求學生掌握在溶液中化學反應的實質是離子之間的結合。實驗表格題在全國甲卷中也連續考查,2021年此類型試題側重氣體制備,2022年考查角度更加廣泛,考查化學學科素養中的科學探究與創新意識。
【例2】(2022·全國甲卷·11)NA為阿伏加德羅常數的值,下列說法正確的是
( )
A.25℃,101 kPa下,28 L氫氣中質子的數目為2.5NA
B.2.0 L 1.0 mol·L-1AlCl3溶液中,Al3+的數目為2.0NA
C.0.20 mol苯甲酸完全燃燒,生成CO2的數目為1.4NA
D.電解熔融CuCl2,陰極增重6.4 g,外電路中通過電子的數目為0.10NA
【參考答案】C
【試題分析】近兩年試題均有考查阿伏加德羅常數,題目增大了考查的覆蓋面,四個選項從四個不同角度分別考查質子數、離子數、分子數以及電子轉移數。前兩項陷阱的設置在歷年高考中多次出現,與往年的突破之處是C項考查了有機物的燃燒,D項考查了電解熔融鹽。1 mol的苯甲酸含有7 mol碳原子,所以0.2 mol苯甲酸完全燃燒生成二氧化碳數目是1.4NA,C項正確;D項可根據關系式Cu2+~Cl2~2 mol e-進行計算,陰極增重6.4 g Cu時,外電路中通過電子的數目為0.2NA,D項錯誤。
3.轉變設問角度、變換考查方法,考查實驗基礎原理
全國甲卷化學試題轉變設問角度及考查方法,培養學生基于圖像、數據和實驗現象等,分析影響物質性質的原因、推測實驗現象或反應得到的產物等,引導高中教師重視實驗教學,帶領學生多角度、多層次、多維度地認識化學基本規律。
【例3】(2022·全國甲卷·13)根據實驗目的,表2中實驗及現象、結論都正確的是
( )
【參考答案】C


4.注重學科內容理解,把握知識本質,養成獨立思考習慣
全國甲卷化學試題與《課程標準》相契合,注重培養學生的推理能力、分析問題、解析問題的能力。引導學生思考知識本源,養成自主學習、獨立思考的習慣。例如第36題,淡化了學生對比合成路線的能力以及模仿能力,考查學生提取合成路線中的有效信息的能力。再例如全國甲卷第10題,圍繞一種水性電解液鋅—二氧化錳離子選擇雙隔膜電池設置情境,要求學生利用電化學原理分析離子遷移方向、判斷正負極以及推測電極反應等。
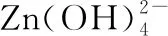

圖2
( )
A.Ⅱ區的K+通過隔膜向Ⅲ區遷移
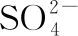

【參考答案】A

5.聚焦核心素養,考查學科關鍵能力
全國甲卷化學試題重視對學生化學學科核心素養的培養,通過試題提升學生對有關物質結構的基本認識,引導學生進一步認識化學變化所遵循的基本原理。例如第12題元素在周期表中的位置關系,以及電子之間的定量關系,考查學生的分析推理能力,第35題考查元素第一電離能的變化規律,從化學鍵的角度分析解釋物質的穩定性,讓學生理解原子結構與元素性質之間的關系,培養學生證據推理與模型認知、宏觀辨識與微觀探析的化學學科核心素養,第28題給出不同條件對“鈦氯化”反應平衡轉化率的影響,引導學生深刻理解化學平衡的本質,考查變化觀念與平衡思想的化學學科核心素養。
【例5】(2022·全國甲卷·28)金屬鈦(Ti)在航空航天、醫療器械等工業領域有著重要用途,目前生產鈦的方法之一是將金紅石(TiO2)轉化為TiCl4,再進一步還原得到鈦。回答下列問題:
(1)TiO2轉化為TiCl4有直接氯化法和碳氯化法。在1 000℃ 時反應的熱化學方程式及其平衡常數如下:



②碳氯化的反應趨勢遠大于直接氯化,其原因是________________________________________________________________________________________。
③對于碳氯化反應:增大壓強,平衡________(填“向左”“向右”或“不”)移動;溫度升高,平衡轉化率________(填“變大”“變小”或“不變”)。
(2)在1.0×105Pa,將TiO2、C、Cl2以物質的量比1∶2.2∶2 進行反應。體系中氣體平衡組成比例(物質的量分數)隨溫度變化的理論計算結果如圖3所示。

圖3

②圖中顯示,在200℃平衡時TiO2幾乎完全轉化為TiCl4,但實際生產中反應溫度卻遠高于此溫度,其原因是____________________________________________。
(3)TiO2碳氯化是一個“氣—固—固”反應,有利于TiO2-C“固—固”接觸的措施是____________________________________________。
【參考答案】(1)①-223 1.2×1014②碳氯化反應氣體分子數增加,ΔH小于0,是熵增、放熱過程,熵判據與焓判據均是自發過程,而直接氯化的體系氣體分子數不變、且是吸熱過程 ③向左 變小
(2)①7.2×105②為了提高反應速率,在相同時間內得到更多的TiCl4產品,提高效益
(3)將兩固體粉碎后混合,同時鼓入Cl2,使固體粉末“沸騰”


②為了效益最佳,實際生產中需要綜合考慮速率、產率等因素,所以為了提高反應速率,在相同時間內得到更多的TiCl4產品,實際反應溫度遠高于200℃。
(3)固體顆粒越小,比表面積越大,反應接觸面積越大,所以可將兩固體粉碎后混合,同時鼓入Cl2,使固體粉末“沸騰”,增大接觸面積。
總之,2022高考全國甲卷化學試題立足基礎知識,深入貫徹落實立德樹人的根本任務,注重情境的選擇和化學核心素養的落實,有效考查學生的基礎知識與基本能力,培養學生分析問題、解決問題的能力。促進考生化學觀念、科學思維和正確價值觀念的形成與發展,對引導考生綜合素質的提升具有較好的導向作用,同時也助力基礎教育改革和高考綜合改革穩步推進。

