培養(yǎng)命題創(chuàng)新意識(shí) 體現(xiàn)創(chuàng)新變式思維
——2022年創(chuàng)新性高考試題及創(chuàng)新變式
湖南 戴儒儉 吳振興 浙江 蔡 冰
【真題展示】(2022·全國乙卷·13)常溫下,一元酸HA的Ka(HA)=1.0×10-3。在某體系中,H+與A-離子不能穿過隔膜,未電離的HA可自由穿過該膜(如圖1所示)。
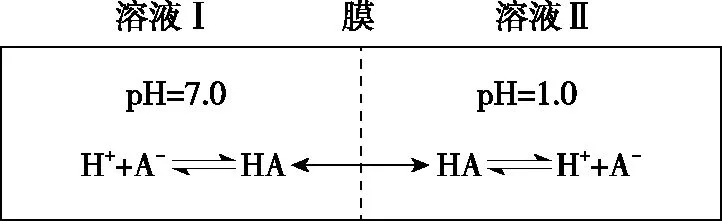
圖1
設(shè)溶液中c總(HA)=c(HA)+c(A-),當(dāng)達(dá)到平衡時(shí),下列敘述正確的是
( )
A.溶液Ⅰ中c(H+)=c(OH-)+c(A-)
C.溶液Ⅰ和Ⅱ中的c(HA)不相等
D.溶液Ⅰ和Ⅱ中的c總(HA)之比為10-4
【參考答案】B
【創(chuàng)新點(diǎn)說明】其一是考查電解質(zhì)溶液時(shí)改變了屢見不鮮的坐標(biāo)式圖像的試題呈現(xiàn)形式,改以相對(duì)靜態(tài)的圖表式來呈現(xiàn)信息;其二是將常在電化學(xué)中用到的交換膜引入圖表中;其三是將只允許分子自由穿過選擇性交換膜引入圖表中,而非傳統(tǒng)的、常見的離子交換膜。均為試題創(chuàng)新求異點(diǎn)。
【變式】常溫下,一元酸HA的Ka(HA)=10-4。在某體系中,陰、陽離子不能穿過分子選擇性透過膜,未電離的HA及水分子均可自由穿過該膜(如圖2所示)。

圖2
設(shè)溶液中c總(HA)=c(HA)+c(A-),且溶液Ⅱ中只存在一種溶質(zhì),當(dāng)達(dá)到平衡時(shí),下列敘述錯(cuò)誤的是
( )
A.溶液Ⅱ的c(HA)約為1.0 mol·L-1
B.若溶液Ⅰ中含有Na+,則存在2c(Na+)=c(A-)+c(HA)
C.若溶液Ⅰ與溶液Ⅱ體積相同,則溶液Ⅰ與溶液Ⅱ含相同數(shù)目的水分子
D.溶液Ⅰ中的c總(HA)約為溶液Ⅱ的2倍
【參考答案】B
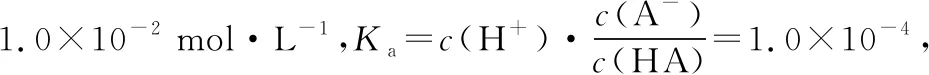
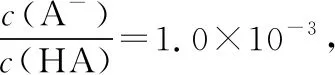
筆者優(yōu)化變式創(chuàng)設(shè)本題時(shí)參考了2022年高考全國乙卷第13題,通過修改電離常數(shù)、選取pH=2與pH=4的2個(gè)相對(duì)接近點(diǎn)作為參照情境,數(shù)據(jù)簡化、科學(xué)合理,設(shè)問時(shí)依然注重考查考生的理解能力、思維能力、分析能力和計(jì)算能力,如對(duì)分子選擇性透過膜在溶液Ⅰ與溶液Ⅱ中間作用的理解,通過電離常數(shù)表達(dá)式建立計(jì)算模型的思維,通過電解質(zhì)溶液里守恒關(guān)系建立變化觀念與平衡思想的核心素養(yǎng)。
【真題展示】(2022·全國乙卷·11)化合物(YW4X5Z8·4W2Z)可用于電訊器材、高級(jí)玻璃的制造。W、X、Y、Z為短周期元素,原子序數(shù)依次增加,且加和為21。YZ2分子的總電子數(shù)為奇數(shù),常溫下為氣體。該化合物的熱重曲線如圖3所示,在200℃以下熱分解時(shí)無刺激性氣體逸出。下列敘述正確的是
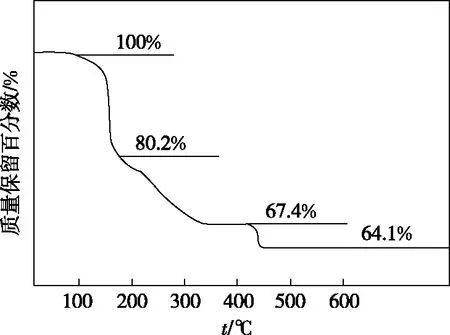
圖3
( )
A.W、X、Y、Z的單質(zhì)常溫下均為氣體
B.最高價(jià)氧化物的水化物酸性:Y C.100~200℃階段熱分解失去4個(gè)W2Z D.500℃熱分解后生成固體化合物X2Z3 【參考答案】D 【創(chuàng)新點(diǎn)說明】本題考查的是物質(zhì)結(jié)構(gòu)與元素周期律相關(guān)考點(diǎn),該題穩(wěn)中有變,變中創(chuàng)新,創(chuàng)新試題呈現(xiàn)形式,把熱重曲線與元素推斷有機(jī)地結(jié)合在一起,深入考查學(xué)生的信息整理能力、計(jì)算能力、分析問題與解決問題的能力,考查學(xué)生關(guān)鍵能力,加強(qiáng)思維考查,突出選拔功能。 【變式】化合物[RY(ZX4)2·12W2X]可用作滅火劑、緩沖劑,同時(shí)具有藥用功能和食用功能。W、X、Y、Z、R為前20號(hào)主族元素,原子序數(shù)依次增加,最外層電子數(shù)之和為17。X和Z同主族且ZX2分子的總電子數(shù)為偶數(shù),常溫下為氣體。4.74 g該化合物的熱重曲線如圖4所示,在熱分解時(shí)無刺激性氣體逸出。下列敘述正確的是 圖4 ( ) A.氫化物的沸點(diǎn):X B.最高價(jià)氧化物的水化物堿性:Y C.64.5~100℃階段熱分解失去12個(gè)W2X D.770℃熱分解后生成固體化合物Y2X3和R2X 【參考答案】B 【解題思路】化合物[RY(ZX4)2·12W2X]可用作滅火劑、緩沖劑同時(shí)具有藥用功能和食用功能。W、X、Y、Z、R為前20號(hào)主族元素,原子序數(shù)依次增加,最外層電子數(shù)之和為17。4.74 g該化合物的熱重曲線如圖4所示,在熱分解時(shí)無刺激性氣體逸出,則說明失去的是水,即W為H,X為O,Z和X同主族且ZX2分子的總電子數(shù)為偶數(shù),常溫下為氣體,則Z為S,原子序數(shù)依次增加,且最外層電子數(shù)之和為17,則Y為Al,R為K。H2O分子間可以形成氫鍵,氫化物沸點(diǎn)X(H2O)>Z(H2S),故A項(xiàng)錯(cuò)誤;根據(jù)金屬性越強(qiáng),其最高價(jià)氧化物的水化物堿性越強(qiáng),則最高價(jià)氧化物的水化物堿性Y[Al(OH)3] 【變式說明】本題命制時(shí)參考了2022年全國乙卷第11題,同時(shí)關(guān)聯(lián)教材涉及的物質(zhì)明礬,拓展明礬其他的用途,發(fā)揮出化學(xué)學(xué)科的社會(huì)價(jià)值。本題創(chuàng)新試題呈現(xiàn)形式,將元素推斷和熱重曲線圖相融合,試題命題角度和呈現(xiàn)方式均較新穎,考查內(nèi)容和考查要求均符合新高考命題方向,試題信息量較大,注重考查學(xué)生的思維,突出選拔功能。本題還落實(shí)了宏觀辨識(shí)與微觀探析、變化觀念與平衡思想、證據(jù)推理與模型認(rèn)知等化學(xué)學(xué)科核心素養(yǎng)。 【真題展示】(2022·湖南卷·10)室溫時(shí),用0.100 mol·L-1的標(biāo)準(zhǔn)AgNO3溶液滴定15.00 mL濃度相等的Cl-、Br-和I-混合溶液,通過電位滴定法獲得lgc(Ag+)與V(AgNO3)的關(guān)系曲線如圖5所示(忽略沉淀對(duì)離子的吸附作用。若溶液中離子濃度小于1.0×10-5mol·L-1時(shí),認(rèn)為該離子沉淀完全。Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=5.4×10-13,Ksp(AgI)=8.5×10-17)。下列說法正確的是 圖5 ( ) A.a點(diǎn):有白色沉淀生成 B.原溶液中I-的濃度為0.100 mol·L-1 C.當(dāng)Br-沉淀完全時(shí),已經(jīng)有部分Cl-沉淀 D.b點(diǎn):c(Cl-)>c(Br-)>c(I-)>c(Ag+) 【參考答案】C 【創(chuàng)新點(diǎn)說明】2022年高考湖南卷第10題以真實(shí)實(shí)驗(yàn)情境中采用的數(shù)字化實(shí)驗(yàn)技術(shù)(電位滴定法)為載體,所考查的必備知識(shí)涉及“難溶物的沉淀溶解平衡”“Ksp的計(jì)算”和“離子反應(yīng)及其現(xiàn)象”,考查的關(guān)鍵能力是“化學(xué)計(jì)算能力”“化學(xué)信息(圖像)處理能力”和“證據(jù)推理與模型論證能力”,同時(shí)發(fā)展學(xué)生證據(jù)推理與模型認(rèn)知、宏觀辨識(shí)與微觀探析的化學(xué)學(xué)科核心素養(yǎng)。本題屬于情境素材上的創(chuàng)新(即內(nèi)容創(chuàng)新),使用基于現(xiàn)代信息技術(shù)的電位滴定法探究AgNO3溶液滴定相等濃度的Cl-、Br-和I-混合溶液的微觀反應(yīng)過程,將微觀粒子的變化轉(zhuǎn)化為直觀、形象的曲線變化,有利于考查學(xué)生對(duì)難溶物沉淀溶解平衡模型的理解和應(yīng)用能力。同時(shí),命題設(shè)問指向信息處理(曲線解讀)能力和模型認(rèn)知能力的考查。而能力要求的考查與學(xué)科知識(shí)內(nèi)容的基礎(chǔ)性呈現(xiàn)相互關(guān)聯(lián)的關(guān)系,可劃分為SOLO能力結(jié)構(gòu)水平層次中的關(guān)聯(lián)結(jié)構(gòu)水平。 【試題分析】向含相等濃度的Cl-、Br-和I-混合溶液中滴加硝酸銀溶液,根據(jù)三種沉淀的溶度積常數(shù),三種離子沉淀的先后順序?yàn)镮-、Br-、Cl-,根據(jù)滴定圖示,當(dāng)?shù)稳?.50 mL 硝酸銀溶液時(shí),Cl-恰好沉淀完全,此時(shí)共消耗硝酸銀的物質(zhì)的量為4.50 mL×10-3L/mL×0.1 000 mol·L-1=4.5×10-4mol,所以Cl-、Br-和I-均為1.5×10-4mol。 【變式1】數(shù)字化實(shí)驗(yàn)是利用傳感器和信息處理終端進(jìn)行數(shù)據(jù)采集與分析的一種實(shí)驗(yàn)手段。某化學(xué)研究小組利用電位滴定法研究鹽酸滴加到亞磷酸鈉(Na2HPO3)溶液過程中的化學(xué)變化,得到電極電位和溶液pH隨鹽酸滴加的體積變化曲線如圖6所示。下列說法錯(cuò)誤的是 圖6 ( ) [已知:①電位滴定法的原理:在化學(xué)計(jì)量點(diǎn)附近,被測離子濃度發(fā)生突躍,指示電極電位也發(fā)生了突躍,進(jìn)而確定滴定終點(diǎn)。②亞磷酸(H3PO3)是二元弱酸,其電離常數(shù)分別是Ka1=1×10-1.4,Ka2=1×10-6.7] A.a點(diǎn)對(duì)應(yīng)溶液的溶質(zhì)為NaH2PO3和NaCl,pH<7 C.水的電離程度:a>b 【參考答案】D 【變式說明】《普通高中化學(xué)課程標(biāo)準(zhǔn)(2017年版2020年修訂)》(以下簡稱《課程標(biāo)準(zhǔn)》)中提出:要精心設(shè)計(jì)實(shí)驗(yàn)探究活動(dòng),積極探索現(xiàn)代信息技術(shù)與化學(xué)實(shí)驗(yàn)的深度融合;應(yīng)當(dāng)精心設(shè)計(jì)學(xué)生必做實(shí)驗(yàn),適當(dāng)增加數(shù)字化實(shí)驗(yàn),讓學(xué)生體會(huì)、認(rèn)識(shí)到技術(shù)手段的創(chuàng)新對(duì)化學(xué)科學(xué)的重要價(jià)值。因此,筆者在參考2022年湖南卷第10題的基礎(chǔ)上,繼續(xù)以數(shù)字化實(shí)驗(yàn)常用的電位滴定法作為試題的情境素材,以鹽酸和次磷酸鈉溶液的化學(xué)反應(yīng)為試題載體,命制試題考查電解質(zhì)溶液中三大平衡與三大守恒式、影響水電離程度的因素等基礎(chǔ)化學(xué)知識(shí),考查學(xué)生的化學(xué)信息(圖像)處理能力、化學(xué)計(jì)算能力和模型認(rèn)知能力,落實(shí)了變化觀念與平衡思想、證據(jù)推理與模型認(rèn)知等化學(xué)學(xué)科核心素養(yǎng)。試題命題角度和呈現(xiàn)方式均較新穎,符合新高考命題趨勢和《課程標(biāo)準(zhǔn)》中關(guān)于數(shù)字化實(shí)驗(yàn)的要求,試題信息量較大,具有一定的區(qū)分度。 【變式2】數(shù)字化實(shí)驗(yàn)是利用傳感器和信息處理終端進(jìn)行數(shù)據(jù)采集與分析的一種實(shí)驗(yàn)手段,其中pH計(jì)是常用的數(shù)據(jù)采集器。某研究性學(xué)習(xí)小組用pH計(jì)測量0.1 000 mol·L-1的鹽酸分別滴定20.00 mL濃度均為0.1 000 mol·L-1的三種一元弱酸的鈉鹽(NaX、NaY、NaZ)溶液過程中的pH變化,得到的滴定曲線如圖7所示。下列判斷正確的是 圖7 ( ) A.在NaZ溶液中,粒子濃度大小c(Na+)>c(OH-)>c(Z-)>c(H+) B.濃度分別為0.1 000 mol·L-1的NaX、NaY、NaZ三種溶液中,水的電離程度由大到小為NaZ>NaY>NaX C.當(dāng)pH=7時(shí),三種溶液中:c(X-) D.分別滴加20.00 mL鹽酸后,再將三種溶液混合可以得到等式c(Na+)+3c(H+)=c(X-)+c(Y-)+c(Z-)+c(OH-) 【參考答案】B 【解題思路】由圖7可知,沒有加入鹽酸時(shí),NaX、NaY、NaZ溶液的pH依次增大,根據(jù)鹽類水解規(guī)律越弱越水解,則HX、HY、HZ三種一元弱酸的酸性依次減弱。 NaZ為強(qiáng)堿弱酸鹽,雖然水解反應(yīng)會(huì)使溶液呈堿性,但水解較為微弱,產(chǎn)生的氫氧根離子濃度小于c(Z-),則溶液中離子濃度的大小順序?yàn)閏(Na+)>c(Z-)>c(OH-)>c(H+),故A錯(cuò)誤;鹽類的水解反應(yīng)促進(jìn)了水的電離,而HX、HY、HZ三種一元弱酸的酸性依次減弱,三種等濃度鈉鹽的水解程度大小為NaZ>NaY>NaX,因此水的電離程度大小為NaZ>NaY>NaX,故B正確;當(dāng)溶液pH為7時(shí),n(H+)=n(OH-),根據(jù)電荷守恒式可得三個(gè)溶液中分別存在:n0(Na+)=n1(Cl-)+n(X-),n0(Na+)=n2(Cl-)+n(Y-),n0(Na+)=n3(Cl-)+n(Z-)。酸越弱,向鹽溶液中加入鹽酸的體積越大,n1(Cl-) 【變式說明】筆者在參考2022年高考湖南卷第10題和2021年高考湖南卷第9題的基礎(chǔ)上,強(qiáng)化數(shù)字化實(shí)驗(yàn)的應(yīng)用場景,落實(shí)《課程標(biāo)準(zhǔn)》中關(guān)于促進(jìn)現(xiàn)代信息技術(shù)與高中化學(xué)實(shí)驗(yàn)深度融合的新要求。試題變式的亮點(diǎn)在于,由硝酸銀溶液分步滴定混合溶液中三種陰離子的縱向?qū)Ρ雀臑辂}酸分別滴定三種強(qiáng)堿弱酸鹽溶液的橫向?qū)Ρ龋卣沽藢W(xué)生的認(rèn)知范圍,促進(jìn)了學(xué)生的深層次思考;圖像中的曲線由一元變?yōu)槿龃罅嘶瘜W(xué)信息分析和處理的難度;B選項(xiàng)比較相同濃度的不同種類鹽溶液的水解程度大小,考查了鹽類水解規(guī)律和影響水電離程度的因素等知識(shí),增大了知識(shí)考查的范圍。 【變式3】pH計(jì)和壓力傳感器是數(shù)字化實(shí)驗(yàn)中常用的數(shù)據(jù)采集器。某研究性學(xué)習(xí)小組在兩個(gè)相同的特制容器中分別加入20 mL 0.4 mol·L-1的Na2CO3溶液和40 mL 0.2 mol·L-1的NaHCO3溶液,再分別用0.4 mol·L-1的鹽酸滴定,利用pH計(jì)和壓力傳感器檢測,得到如圖8所示的曲線: 圖8 下列說法錯(cuò)誤的是 ( ) A.圖中甲、丁線表示向Na2CO3溶液中滴加鹽酸,乙、丙線表示向NaHCO3溶液中滴加鹽酸 B.在曲線甲所代表的溶液中,a、b、c三點(diǎn)水的電離程度大小順序?yàn)閏>a>d C.根據(jù)pH-V(HCl)圖,滴定分析時(shí),c點(diǎn)可用酚酞、d點(diǎn)可用甲基橙作指示劑指示滴定終點(diǎn) 【參考答案】D 【變式說明】筆者在參考2022年湖南卷第10題和2022年1月浙江省普通高校招生選考科目考試化學(xué)第23題的基礎(chǔ)上,強(qiáng)化數(shù)字化實(shí)驗(yàn)的應(yīng)用場景,落實(shí)《課程標(biāo)準(zhǔn)》中關(guān)于促進(jìn)現(xiàn)代信息技術(shù)與高中化學(xué)實(shí)驗(yàn)深度融合的新要求。本次變式的亮點(diǎn)在于,由硝酸銀溶液分步滴定混合溶液中三種陰離子的縱向?qū)Ρ龋臑辂}酸分別滴定碳酸鈉溶液和碳酸氫鈉溶液的橫向?qū)Ρ龋龃罅藢W(xué)生思維的難度和深度;圖像中的曲線由單一因變量[lgc(Ag+)]變?yōu)閮山M四變量(兩個(gè)pH變量、兩個(gè)氣體壓力變量),增大了化學(xué)信息分析和處理的難度。另外試題命題角度和呈現(xiàn)方式均較新穎,符合新高考命題趨勢,試題信息量較大,具有一定的區(qū)分度。