康柏西普治療病理性近視脈絡膜新生血管與濕性年齡相關性黃斑變性效果比較
魏向陽 段凝 李瑛 李清華 杜兆東
(青島大學附屬醫院眼科,山東 青島 266003)
脈絡膜新生血管(choroidal neovascularization,CNV)是因玻璃膜變性損害后誘發的來自于脈絡膜毛細血管的增殖血管,通常由于引發視網膜內或視網膜下液體滲出、出血和黃斑纖維化而導致患者視力下降。引起CNV的最常見原因是年齡相關性黃斑變性(age-related macular degeneration,AMD)和病理性近視(pathological myopia, PM)[1]。其中濕性AMD(wAMD)和pmCNV分別是導致老年人和中青年人視力下降的主要原因[2-3],均會引起CNV的形成。CNV在玻璃膜破裂后于視網膜下再生,這些新生血管容易破裂,引起血液或液體滲漏,損害中央視力。目前,抗血管內皮生長因子(VEGF)藥物屬于CNV的一線治療藥物[4-6]。康柏西普是一種與VEGF受體相關的重組融合蛋白,通過競爭性結合VEGF來抑制VEGF與其受體之間的結合并阻止VEGF家族受體的激活,抑制內皮細胞增殖和新生血管形成[7-8]。另有研究表明雷珠單抗治療多灶性脈絡膜炎CNV的療效優于AMD患者[9]。目前已有康柏西普治療pmCNV和wAMD的相關研究報道,但是關于兩者的療效對比卻鮮較少有報道。本研究通過回顧性分析玻璃體腔注射康柏西普治療pmCNV與wAMD的效果及差異,旨在為繼發于不同原因的CNV患者治療方案的選擇和預后評估提供數據參考和理論指導。
1 資料與方法
1.1 資料來源
回顧性分析2020年1月—2021年1月我院眼科經玻璃體腔注射康柏西普治療的14例pmCNV患者(pmCNV組)及25例wAMD患者(wAMD組)的臨床相關資料。其中pmCNV組患者的納入標準為:①經眼科常規檢查、眼底熒光血管造影(FFA)、吲哚菁綠血管造影(ICGA)和光學相干斷層掃描(OCT)等檢查診斷為CNV的高度近視患者,屈光度數>-6.00 D;②眼軸長度>26.00 mm者;③OCT檢查示黃斑中心凹處或旁中心凹處出現視網膜色素上皮(RPE)或脈絡膜毛細血管復合層斷裂,處于活動期者;④FFA檢查呈強熒光或出現熒光素滲漏者;⑤對康柏西普等治療藥物無禁忌證者。wAMD組患者的納入標準為:①年齡>50歲者;②FFA、ICGA、OCT等眼科檢查確診者,且CNV處于活動期。兩組患者排除標準:①患有其他嚴重影響視力的眼部疾病者,如明顯的老年性白內障、青光眼,糖尿病視網膜病變、視網膜分支靜脈阻塞等視網膜疾病,其他原因引起的CNV以及已經進行過玻璃體切除手術者;②合并有嚴重全身基礎疾病者;③在接受康柏西普治療前接受過其他眼部治療者。
收集兩組患者治療前和首次玻璃體腔注射治療后6個月時的最佳矯正視力(BCVA)和OCT檢查結果。BCVA結果轉換為最小分辨角對數(LogMAR)視力進行統計分析,記錄OCT圖像中黃斑中心凹視網膜厚度(CMT)及近中心凹處視網膜外界膜(ELM)、橢圓體帶(EZ)的完整性,分別以ELM(+)和EZ(+)代表ELM完整和EZ完整,計算兩組ELM(+)和EZ(+)的構成比。
1.2 統計學分析
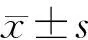
2 結 果
2.1 兩組患者的一般資料比較
pmCNV組患者14例(14眼),其中男9例,女5例;wAMD組患者25例(25眼),其中男16例,女9例,兩組患者性別比較差異無顯著性(P>0.05)。
2.2 治療前后兩組患者BCVA比較
pmCNV組患者治療前BCVA(LogMAR)為0.50(0.30,0.90),治療后為0.20(0.10,0.50),治療前后差值為-0.50(-0.70,-0.28),wAMD組患者治療前BCVA(LogMAR)為0.70(0.46,1.00),治療后為0.40(0.21,0.70),治療前后差值則為-0.30(-0.38,-0.15)。與治療前相比,兩組患者治療后BCVA均得到明顯改善(Z=-2.720、-3.513,P<0.05),兩組患者BCVA(LogMAR)治療前后差值比較,差異具有顯著性(Z=-2.187,P<0.05)。
2.3 治療前后兩組OCT結果分析
pmCNV組患者治療前CMT為286.00(228.25,330.25)μm,治療后為229.50(209.75,275.25)μm,治療前后差值為-33.50(-81.25,-11.75)μm,wAMD組的患者治療前CMT為406.00(338.50,607.50)μm,治療后為298.00(234.50,357.50)μm,治療前后差值為-127.00(-244.50,-30.00)μm。與治療前比較,兩組患者經康柏西普治療后CMT顯著降低(Z=-2.291、-3.511,P<0.05),兩組患者CMT治療前后差值比較差異具有顯著性(Z=-2.137,P<0.05)。pmCNV組患者治療前ELM(+)、EZ(+)構成比分別為21.43%、28.57%,治療后均為78.66%;wAMD組患者治療前ELM(+)、EZ(+)構成比分別為28.00%、24.00%,治療后分別為64.00%、56.0%。與治療前比較,兩組患者治療后ELM(+)、EZ(+)構成比比較差異均有顯著性(χ2=4.083~7.000,P<0.05)。兩組治療前和治療后ELM(+)、EZ(+)構成比比較,差異均無顯著性(P>0.05)。
2.4 兩組患者治療前后ELM(+)、EZ(+)構成比及CMT與BCVA(LogMAR)相關性分析
相關性分析結果顯示,治療前后兩組患者ELM(+)、EZ(+)構成比與BCVA(LogMAR)均呈負相關(r=-0.754~-0.559,P<0.05)。但是治療前后兩組CMT與BCVA(LogMAR)無明顯相關性(P>0.05)。
3 討 論
據報道,大約有5%~11%的PM患者會出現pmCNV[10]。以前,pmCNV的首選治療方式是光動力治療(PDT),但是接受PDT治療患者的長期視力預后卻不佳[11]。近年來,已經證明抗VEGF藥物治療pmCNV及wAMD效果較好,并作為治療該病的一線用藥。較早應用于臨床的抗VEGF藥物有雷珠單抗和阿柏西普,兩種藥物均可提高患者的BCVA和恢復受損視網膜的正常形態[12-15]。康柏西普亦可以有效改善pmCNV和wAMD患者的CMT和BCVA[16-17],且在抑制CNV產生的同時,還可改善視網膜血流灌注情況,有助于患者相關并發癥恢復,從而改善預后[18]。但康柏西普對這兩種原因所引起的CNV治療效果的對比卻鮮有報道。
本研究結果顯示,與治療前相比,pmCNV組與wAMD組患者治療后CMT均降低。但通過對比兩組治療前后CMT的差值,發現wAMD組患者治療后CMT降低更加顯著。這種差異是因為治療前wAMD組患者黃斑部水腫更為嚴重,而與wAMD組患者不同,pmCNV組患者眼底黃斑視網膜水腫并不顯著[19]。pmCNV與wAMD的發病機制不同。在PM患者,因為眼軸的延長牽引眼球組織,引起脈絡膜缺血,最終導致視網膜色素上皮(RPE)萎縮和隨后的VEGF釋放,形成CNV[20-21];但是炎癥和補體系統的失調在wAMD患者的發病機制中起著關鍵作用,而炎癥反應使wAMD的黃斑水腫更加嚴重[22]。相對于其他原因引起的視網膜損害,水腫引起的視網膜結構的破壞對視力的影響更加難以恢復。所以即使wAMD組患者CMT降低更多,但視力的改善不如pmCNV組患者。因此pmCNV組患者在康柏西普治療后可以比wAMD組患者獲得更好的術后視力,可能是由于兩組患者發病機制的不同引起的,并且有研究表明由于發病機制的不同,不同原因形成的CNV對抗VEGF藥物的反應存在著差異[23]。所以,pmCNV與wAMD在康柏西普治療后CMT以及BCVA的改善情況的差異性,與它們不同的發病機制有關。
ELM是OCT上靠近外顆粒層的超反射帶,被認為由Müller細胞末端突起和微絨毛組成[24],而Müller細胞則可以將黃斑中心凹的感光細胞結合在一起[25]。EZ則與ELM相鄰且靠近RPE層,是OCT上的第二個外部超反射帶。以前認為它是感光器的內段和外段(IS/OS)之間的連接[26]。但最近的研究表明,它與解剖學上與感光器內段的橢圓體部分相關,這是一個包含有大量線粒體的細胞聚集區[27]。所以視網膜上這兩個區域的受損會使視網膜內的感光細胞被破壞從而影響視力。本研究結果顯示,pmCNV與wAMD引起的黃斑病變均會使ELM和EZ不完整,并且治療后兩組都有明顯改善。通過對OCT檢查結果與BCVA進行相關性分析,可以明顯看到治療前和治療后患者ELM(+)、EZ(+)的構成比均與BCVA相關。因此可通過判斷ELM與EZ完整性來評估CNV患者視力預后。有文獻報道,在pmCNV和wAMD患者中,ELM和EZ的完整性可作為BCVA可能預后評估因素[28]。
另外,本研究具有一定局限性,主要為樣本量太小,尤其是pmCNV組,并且在其治療過程中,有一部分患者只完成注射1~2次,根據DING等[29]研究確定的評估pmCNV活動性的方法,CNV處于穩定期,且BCVA也較前明顯改善,暫停治療無法隨訪,未納入分組。而因為樣本量小,研究的結果會有一定的偏倚。有必要進行多中心、隨機、長期的對照研究來驗證這些結果。
綜上所述,玻璃體腔注射康柏西普治療pmCNV和wAMD患者均有較好的效果,可有效提高BCVA,改善ELM及EZ的完整性,降低CMT。但對于pmCNV患者來說,可以獲得更好的視力預后。
利益沖突聲明:所有作者聲明不存在利益沖突。
ConflictsofInterest: All authors disclose no relevant conflicts of interest.
倫理批準和知情同意:本研究涉及的所有試驗均已通過青島大學附屬醫院醫學倫理委員會的審核批準(文件號QYFYWZLL26882)。所有試驗過程均遵照《赫爾辛基宣言》的條例進行。受試對象或其親屬已經簽署知情同意書。
EthicsApprovalandPatientConsent: All experimental protocols in this study were reviewed and approved by The Medical Ethics Committee of The Affiliated Hospital of Qingdao University (Approval Letter No. QYFYWZLL26882), and all experimental protocols were carried out by following the guidelines of The Helsinki Declaration. Consent letters have been signed by the research participants or their relatives.
作者貢獻:魏向陽、段凝、李瑛、李清華參與了研究設計;魏向陽、段凝、杜兆東參與了論文的寫作和修改。所有作者均閱讀并同意發表該論文。
Contributions: The study was designed byWEIXiangyang,DUANNing,LIYing, andLIQinghua. The manuscript was drafted and revised byWEIXiangyang,DUANNing, andDUZhaodong. All the authors have read the last version of the paper and consented submission.

