低分子肝素鈉聯合孕激素治療妊娠早期先兆流產的臨床效果分析
張慧鵬,董 彤,張 麗,崔秀紅
(1.北京中西醫結合醫院婦產科,北京 100039;2.解放軍總醫院第六醫學中心婦產科,北京 100142;3.北京市門頭溝區婦幼保健院婦產科,北京 102300)
先兆流產是婦產科臨床工作中常見的生殖疾病,妊娠早期出現少量陰道出血,并伴有小腹墜脹、腰腹酸痛等癥狀,如不及時處理可進展為難免流產。早期給予治療可使多數患者獲得良好的妊娠結局[1]。目前,臨床對于先兆流產的治療以補充孕酮(progesterone,P)和人絨毛膜促性腺激素(β-human chorionic gonadotropin,β-HCG)為主。地屈孕酮是一種口服孕激素類藥物,在內源性孕激素不足引起的疾病治療中應用廣泛,尤其適用于孕激素缺乏所致的先兆流產,但仍有部分患者療效欠佳[2]。
先兆流產一般采用補充孕激素治療,但該方法無法改善患者血液高凝狀態。有研究發現,抗磷脂抗體是引起先兆流產的重要致病因素之一,可引起血栓前狀態而造成胎盤缺血,抗凝治療可有效改善子宮微環境而有利于胚胎發育,從而改善妊娠結局[3]。低分子肝素鈉是臨床常用的抗凝藥物,在先兆流產的治療中應用較多[4],但其對妊娠相關因子水平影響的相關研究較少。本研究觀察了低分子肝素鈉聯合孕激素治療妊娠早期先兆流產的臨床療效,分析其對患者生殖激素、血栓前狀態標志物及妊娠相關因子水平的影響,以期為臨床提供參考。
1 資料與方法
1.1 研究對象
選取2018年6月至2020年1月間我院收治的妊娠早期先兆流產患者120例為研究對象,根據治療方案將其隨機分為觀察組和對照組,各60例。研究對象納入標準:①符合《婦產科學》第8版中先兆流產的診斷標準[5],且妊娠<12周;②18歲≤年齡≤35歲;③單胎妊娠;④妊娠期間未服用其他保胎藥物者;⑤男方精液檢查正常。排除標準:①具有習慣性流產史;②合并TORCH綜合征、生殖道病毒或其他病原體感染者;③合并造血功能和凝血功能異常者;④合并心腦血管、肝、腎等嚴重疾病者;⑤具有出血傾向疾病者;⑥合并精神疾病或惡性腫瘤者;⑦藥物過敏者。所有研究對象及其家屬對本研究知情,并簽署知情同意書。
1.2 治療方案
所有患者均臥床休息,減少活動,禁止性生活,口服葉酸(常州制藥廠有限公司,規格:0.4mg,國藥準字H20003143),0.4mg/d,頓服。對照組口服地屈孕酮片(荷蘭Abbott Healthcare Products B.V.,規格:10mg,注冊證號H20130110),首劑量40mg,頓服,1d后每8 h口服10mg。觀察組在口服地屈孕酮的基礎上給予低分子肝素鈉注射液(吉林華康藥業股份有限公司,規格為0.5mL:5 000U,國藥準字H20010233)5 000U腹壁皮下注射,1次/d。兩組皆地屈孕酮用藥至陰道流血停止、孕酮檢查結果正常。觀察組低分子肝素鈉注射液用藥1周。如用藥后出現出血性不良反應立即停藥。
1.3 評估標準
1.3.1 療效評估
參考《婦產科疾病診斷標準》[6]評價療效:①顯效:經12h治療,臨床癥狀消失,宮縮停止,療程結束后B超與婦科檢查均證實為正常妊娠;②有效:經24h治療,臨床癥狀消失,宮縮停止或明顯減輕,療程結束后B超與婦科檢查均證實為正常妊娠;③無效:未達到上述標準。總有效率=(顯效例數+有效例數)/總例數×100%。
1.3.2 相關指標監測
所有患者均在治療前、治療后抽取靜脈血標本8mL,采血前至少禁食8h。取血后上離心機處理,轉速4 000r/min,離心時長10min。①生殖激素水平:取血清采用電化學發光法試劑盒(羅氏公司)檢測β-HCG、P水平,檢測儀器為化學發光免疫分析儀(羅氏公司,型號E601)。②血栓前狀態標志物水平:取血清采用酶聯免疫吸附法試劑盒(南京建成生物工程研究所)檢測蛋白C(protein C,PC);采用URIT-600全自動血凝分析儀檢測D-二聚體(D-dimer,D-D);采用發色底物法檢測纖溶酶原(plasminogen,PLG),檢測儀器為美國伯騰公司ELX酶標儀;③健康及妊娠相關指標:采用放射免疫法檢測白細胞介素-4(interleukin-4,IL-4)、干擾素-γ(interferon-γ,INF-γ)、妊娠相關血漿蛋白A(pregnancy associated plasma protein-A,PAPP-A)水平;采用免疫組化法檢測血紅素氧合酶-1(heme oxygenase-1,HO-1)水平,以磷酸鹽緩沖液為陰性對照,已知陽性片為陽性對照,試劑盒為武漢博士德生物工程有限公司產品,細胞漿內有棕黃色顆粒為陽性,采用MIAS-12000 全自動圖像分析系統測量陽性區域的積分光密度。以上操作均嚴格按照檢測儀器及說明進行。
1.4 觀察指標
記錄兩組治療前后生殖激素、血栓前狀態標志物、IL-4、INF-γ、PAPP-A和HO-1水平變化。隨訪至子代出生,統計并比較兩組治療總有效率、便秘發生率、分娩期并發癥發生率、妊娠結局及新生兒情況。
1.5 統計學方法
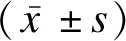
2 結果
2.1 兩組患者基本情況的比較
兩組患者年齡、孕次、孕周、體重及流產史間的差異均無統計學意義(P>0.05),具有可比性,見表1。
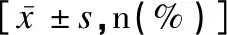
表1 兩組患者基本情況比較Table 1 Comparison of general data between the two
2.2 兩組患者療效的比較
觀察組的治療總有效率為91.67%,高于對照組的78.33%,差異具有統計學意義(χ2=4.183,P<0.05),見表2。

表2 兩組患者療效比較[n(%)]Table 2 Comparison of curative effect between the two groups[n(%)]
2.3 兩組患者生殖激素水平的比較
治療前,兩組各指標水平差異不顯著(P>0.05)。治療后,兩組的P、β-HCG水平均有所增加(P<0.05),觀察組的P、β-HCG水平均高于對照組,差異具有統計學意義(t值分別為-9.428和-2.095,P<0.05),見表3。
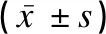
表3 兩組患者生殖激素水平比較Table 3 Comparison of reproductive hormone levels between the two
2.4 兩組患者血栓前狀態標志物水平比較
治療前,兩組各指標水平差異不顯著(P>0.05)。治療后,兩組的PLG水平增加(P<0.05),PC和D-D水平均下降(P<0.05)。進一步組間比較發現,觀察組PLG水平高于對照組(t=-2.090,P<0.05),而PC、D-D水平低于對照組(t值分別為4.485和3.397,P<0.05)。詳見表4。
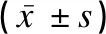
表4 兩組患者血栓前狀態標志物水平比較Table 4 Comparison of prethrombotic state marker levels between the two
2.5 兩組患者IL-4、INF-γ、PAPP-A、HO-1水平比較
治療前,各指標水平差異不顯著(P>0.05)。治療后,兩組的IL-4、PAPP-A、HO-1水平均上升(P<0.05),INF-γ水平下降(P<0.05)。進一步組間比較發現,觀察組的IL-4、PAPP-A、HO-1水平均高于對照組(t值分別為-5.731、-19.169和-5.491,P<0.05),INF-γ低于對照組(t=14.320,P<0.05),詳見表5。
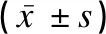
表5 兩組患者IL-4、INF-γ、PAPP-A、HO-1水平比較Table 5 Comparison of the levels of IL-4,INF-γ,PAPP-A,HO-1 between the two
2.6 兩組患者便秘發生率比較
觀察組便秘發生率為8.33%(5/60),低于對照組的23.33%(14/60),差異具有統計學意義(χ2=5.065,P=0.024)。
2.7 兩組患者分娩期并發癥比較
兩組前置胎盤率、胎盤粘連率、胎膜早破率、產后出血率差異均無統計學意義(P>0.05),見表6。

表6 兩組患者分娩期并發癥比較[n(%)]Table 6 Comparison of complications during childbirth between the two groups[n(%)]
2.8 兩組妊娠結局及新生兒情況比較
觀察組的流產率、早產率及低體重兒率分別均低于對照組,差異有統計學意義(χ2值分別為5.551、4.615和6.536,P<0.05)。兩組的Apgar評分<7分、新生兒死亡率差異無統計學意義(P>0.05),見表7。

表7 兩組妊娠結局及新生兒情況比較[n(%)]Table 7 Comparison of pregnancy outcomes and neonatal conditions between the two groups[n(%)]
3 討論
3.1 先兆流產的因素及臨床治療
先兆流產是指宮內妊娠的孕婦在孕12周內發生的陰道血性白帶或出血、無孕囊排出,常伴有陣發性小腹墜脹或腰酸。其發病因素尚未完全明確,既往研究認為與胚胎、母體、父體、環境等多種因素有關。其中,以母體因素比較常見,黃體功能不全、子宮解剖結構異常、不良生活習慣、不良情緒、血栓前狀態等均可導致先兆流產[7-8]。近年來,先兆流產的發病率逐漸升高,嚴重影響人類生殖健康,也給廣大患者造成巨大的身心痛苦[9]。地屈孕酮與天然孕激素結構相似,在孕酮不足引起的痛經、子宮內膜異位癥、月經紊亂、功能失調性子宮出血、經前期綜合征以及孕激素缺乏所致的先兆流產、習慣性流產、不孕等疾病的治療中均有所應用[10]。有研究調查2014—2020年中國先兆流產患者用藥的信息,結果表明地屈孕酮是最為普遍的處方藥。然而,值得注意的是,使用孕激素治療先兆流產仍然存在爭議,單一用藥未能有效改善血液的高凝狀態,且多種聯合用藥的安全性和合理性仍然需要高質量的研究[11]。
此外,抗磷脂抗體異常、抗凝蛋白缺陷等引起的血栓前狀態是引起先兆流產的重要原因之一。抗磷脂抗體可作用于血管內皮細胞、血小板的靶點,引起血液高凝、高黏,使胎盤、蛻膜血管栓塞而致血流灌注減少。抗凝蛋白缺陷可導致凝血功能異常,微血栓形成,子宮及胎盤絨毛微血管血流灌注不足,還可干擾花生四烯酸合成,減少前列環素釋放,造成胎盤血管痙攣、缺血,使胎兒缺血、缺氧而發生流產[12-13]。積極的抗凝治療有助于改善妊娠結局,低分子肝素鈉是比較常用的抗凝藥物,在先兆流產的治療中應用效果較好[14]。李慧等[15]研究發現,在常規治療的基礎上采用低分子肝素鈉聯合地屈孕酮治療先兆流產的療效和安全性均較好。
3.2 低分子肝素鈉聯合孕激素治療先兆流產的臨床療效及妊娠結局
本研究發現,采用低分子肝素鈉聯合孕激素治療先兆流產的總有效率高于單用孕激素治療,流產率、早產率及低體重兒率均低于單用孕激素治療者,便秘發生率低于單用孕激素治療者。兩組前置胎盤率、胎盤粘連率、胎膜早破率、產后出血率、新生兒Apgar評分<7分率、新生兒死亡率比較,差異不顯著。這一結果提示,低分子肝素鈉聯合孕激素治療妊娠早期先兆流產可提高療效,降低便秘、流產、早產及新生兒低體重的發生風險。這是由于地屈孕酮對孕酮受體的親和力較好,可減少妊娠期子宮興奮性,抑制異常宮縮,維持子宮內環境穩定,減少炎性介質釋放,促進胚胎生長發育。低分子肝素鈉可增加抗凝血酶Ⅲ活性,降低胎盤血管阻力和血黏度,阻斷纖維蛋白原向纖維蛋白轉化,減少纖維蛋白胎盤血管基底膜的沉積,有利于增加胎盤血流灌注,改善子宮內環境而促進胚胎生長發育。兩種藥物通過不同的作用機制發揮協同保胎作用,改善患者的妊娠結局。
3.3 低分子肝素鈉聯合孕激素治療對健康及生育指標的影響
P、β-HCG是促進子宮內膜增生、抑制異常宮縮、保障胚胎發育的重要物質。先兆流產患者體內P、β-HCG處于較低水平,隔日翻倍情況較差[16]。PLG、PC、D-D均是血栓前狀態標志物,PLG缺乏會引起凝血亢進時機體反應力下降[17]。本研究發現,采用低分子肝素鈉聯合孕激素治療先兆流產患者,治療后的P、β-HCG、PLG水平均高于單用孕激素治療者,PC、D-D水平均低于單用孕激素治療者。這一結果提示低分子肝素鈉聯合孕激素治療妊娠早期先兆流產可減輕血栓前狀態,升高P、β-HCG激素水平。低分子肝素鈉可有效緩解機體高凝狀態,改善子宮、胎盤血流,有助于地屈孕酮在子宮發揮作用。
INF-γ屬于Th1型細胞因子,與免疫炎癥反應、組織炎性損傷有關,不利于胚胎發育[18]。IL-4屬于Th2型細胞因子,是重要的抑炎因子,可抑制母體對胚胎的免疫應答,有利于促進胚胎發育、維持妊娠[19]。PAPP-A在妊娠早期來源于妊娠黃體,之后來源于胎盤,可促進促腎上腺皮質激素釋放和紅細胞生成,促進早期胚胎形成和性腺發育,參與子宮內膜蛻膜化、胚胎植入、滋養細胞分化等過程[20]。HO-1具有抗氧化、抗炎、抗細胞凋亡、免疫調節等生理作用,可保護子宮、胎盤[21]。本研究發現,采用低分子肝素鈉聯合孕激素治療先兆流產后的IL-4、PAPP-A、HO-1水平均高于單用孕激素治療者,INF-γ低于單用孕激素治療者。調節Th1/Th2平衡、增加妊娠保護性因子的表達,可能是其治療先兆流產的重要機制。
綜上所述,低分子肝素鈉聯合孕激素治療妊娠早期先兆流產可減輕血栓前狀態,調節相關因子的表達,降低便秘、流產、低出生體重及早產的發生。

