早產兒維生素D 營養狀況及活性維生素D 補充對骨代謝的影響
何云霞, 黃久浪
(四川省遂寧市中心醫院新生兒科, 四川遂寧 629000)
早產兒是指胎齡<37 w 的新生兒。 近年來, 隨著圍生期醫學的發展、 新生兒診療技術的提高, 早產兒存活率越來越高, 而同時伴隨的營養不良和發育問題也得到越來越突出, 其中, 維生素D 缺乏對于早產兒來說極為普遍[1]。 維生素D 缺乏與早產兒代謝性骨病密切相關, 嚴重影響著早產兒的體格發育, 臨床應對代謝性骨病主要依靠維生素D 和鈣磷制劑的補充。 本研究收集在本院分娩的早產兒為研究對象, 旨在探索早產兒維生素D 營養狀況, 以及活性維生素D 補充治療對早產兒骨代謝指標的影響。
1 材料與方法
1.1 一般資料
研究對象選自我院2020年7月—2021年12月出生的80例28~37 w 早產兒和80例同期出生的足月兒。 納入標準為產婦孕前和孕期無疾病, 新生兒無先天性畸形; 產婦孕前無吸煙、 飲酒和藥物濫用; 產婦孕期無干擾維生素D 吸收及代謝藥物使用史。 排除標準為早產兒患有新生兒窒息、 遺傳代謝性疾病、 嚴重感染性疾病、糖尿病母親嬰兒、 新生兒呼吸窘迫綜合征等嚴重疾病。經納入和排除后, 共納入80例早產兒為研究組, 同期出生的80例足月兒為對照組。 本研究已經過本院倫理委員審核批準, 所有研究對象家屬均已簽署知情同意書。
1.2 方法
取得所有參與者同意, 留取臍帶血4 ~5 mL, 放入4℃冰箱保存, 24 h 內離心取血清, -20℃保存。 采用ELISA 測定技術測定血清骨鈣素(OC) 、 25-羥維生素D3[25 (OH) D3]及堿性磷酸酶(ALP) 水平; 采用全自動生化分析儀測定血清鈣、 磷水平。 根據維生素D 缺乏標準, 將血清25 (OH) D3水平<20 μg/L 定義為維生素D 缺乏組, 血清25 (OH) D3水平≥20 μg/L 定義為非維生素D 缺乏組。 80例早產兒于能經口喂養時, 添加維生素D 800 U/d (維生素D 滴劑), 平均添加時間為(10.03±1.23) d, 于出生28 d 后復查血清25 (OH) D3、OC、 ALP、 鈣和磷水平。 營養管理按照新生兒營養支持應用指南[2], 出院后隨訪喂養情況, 并予以適當營養指導。分析早產兒維生素D 營養狀況, 比較28 d 后早產兒血清維生素D 水平變化和骨代謝指標變化情況。
1.3 統計分析
應用SPSS 20.0 軟件對數據進行統計學處理。 計量資料采用均數±標準差表示, 采用研究組與對照組數據比較采用兩樣本獨立t檢驗進行分析, 維生素D 干預28 d后與干預前數據比較采用配對t檢驗; 計數資料用率表示, 采用χ2檢驗進行統計分析,P<0.05 為差異有統計學意義。
2 結果與分析
2.1 兩組新生兒一般情況描述
如表1 所示, 早產兒胎齡更短, 剖宮產比例更高,且嬰兒體重、 身高、 頭圍更小, 差異均有統計學意義(P<0.05)。
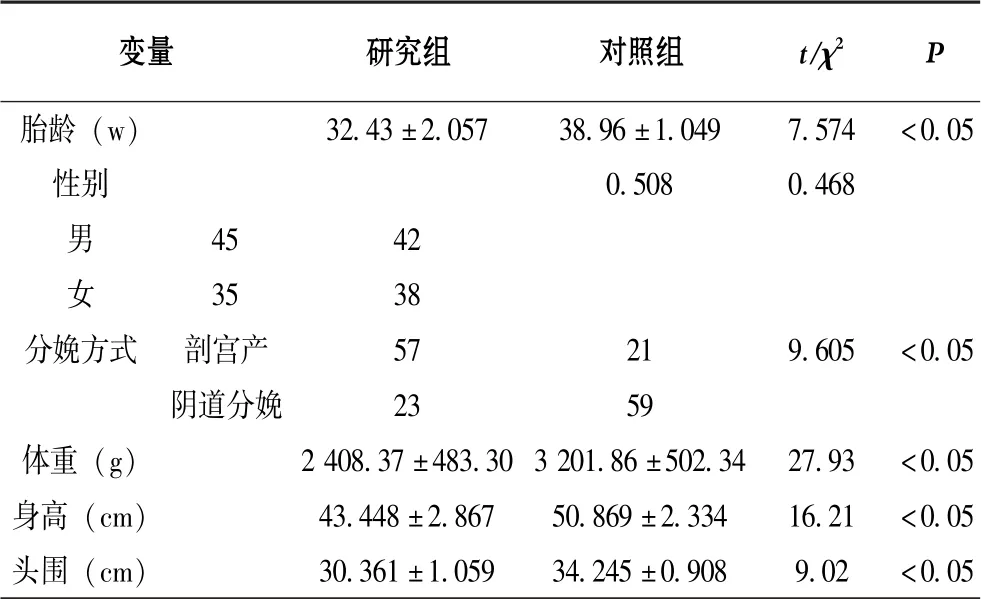
表1 2 組新生兒一般情況比較
2.2 早產兒維生素D 營養狀況
由表2 可知, 早產兒血清25 (OH) D3平均水平為(22.03±2.48) μg/L, 顯著低于對照組的(26.43 ±2.59) μg /L, 差異有統計學意義(P<0.05)。 且早產兒維生素D 缺乏率也顯著高于正常新生兒(32/80 vs 12/80,P<0.05)。

表2 2 組新生兒血清維生素D 水平比較
2.3 活性維生素D 補充對早產兒骨代謝的影響
早產兒經28 d 的活性維生素D 補充, 結果發現,血清25 (OH) D3[ (24.32±3.01) vs (22.03±2.48)]μg /L、 OC [ (78.32±28.92) vs (70.25±32.02)]μg/L 及ALP [ (526.38 ±32.29) vs (483.92 ±38.83)]IU/L 均顯著增高(P<0.05), 而血清鈣及磷水平無差異(P>0.05) (表3)。
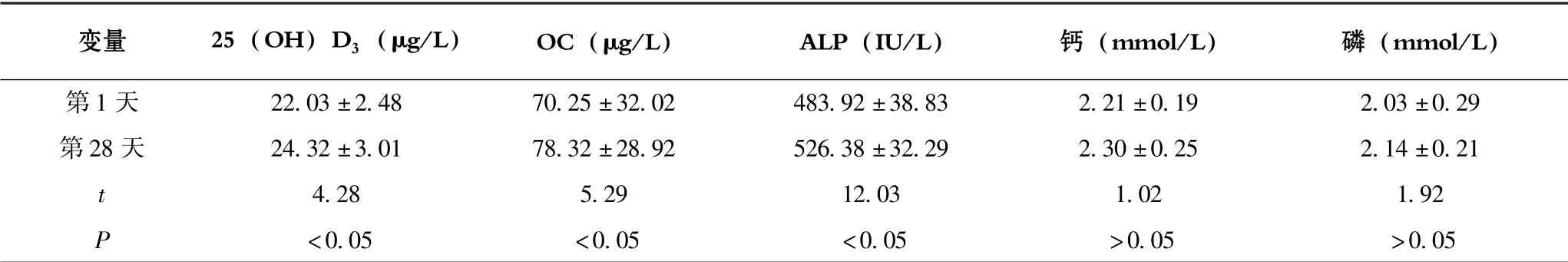
表3 活性維生素D 補充對早產兒骨代謝的影響
3 討論
嬰幼兒時期 維生素D 缺乏廣泛存在, 研究顯示,即使是健康的兒童也普遍存在維生素D 缺乏[3], 而早產兒維生素D 缺乏率則顯著高于健康新生兒[4], 原因可能是早產兒胃腸道結構和功能不成熟, 腎臟發育不成熟,鈣磷經尿液排出增加相關, 另外, 早產兒出生后一般會長時間進行腸內外營養支持, 限制全面營養的攝入, 如鈣磷、 維生素等骨礦物質, 而出生后追趕性增長對鈣磷需求量較高, 但身體不能及時自行合成維生素D, 進而導致早產兒維生素D 缺乏率顯著增高[5]。 維生素D 的缺乏會導致早產兒代謝性骨病發病率增高, 即生后骨礦化落后于適于胎齡的宮內骨密度, 此種疾病在出生胎齡越小的早產兒中更為常見[6], 研究顯示, 胎齡<28w 的早產兒, 代謝性骨病發病率可高達30%, 嚴重影響了早產兒的骨骼健康發育, 也與成年期骨病密切相關[7]。 因此維生素D 補充對早產兒骨發育至關重要。
維生素D 在體內的活性形式為1, 25-二羥維生素D3[1, 25 (OH)2D3], 在體內發揮者促進小腸黏膜對鈣、 磷的吸收及腎小管對鈣、 磷的重吸收, 是影響鈣在體內代謝的重要因素。 維生素D 對骨的作用表現為, 既可促進骨骼生長與鈣化, 又可促進骨吸收, 以維持血清鈣、 磷的正常水平。 25 (OH) D3是維生素D 代謝的中間產物, 也是合成活性1, 25 (OH)2D3的前體, 是反映體內維生素D 營養狀況的最佳指標[8]。 劉穎等[9]研究結果表明, 早產兒血清25 (OH) D3平均水平為(17.0 ±7.0) μg/L, 處于缺乏水平, 本研究納入的80例早產兒血清25 (OH) D3平均水平為(22.03 ±2.48) μg/L,顯著低于對照組的(26.43 ±2.59) μg/L, 且缺乏率也顯著高于正常新生兒[ (32/80) vs (12/80)]。 早產兒維生素D 狀況除了受自身發育影響, 研究還表明與母親孕期維生素D 營養狀況相關, 孕期維生素D 補充不足是早產兒發生維生素D 缺乏的危險因素[9], 故應關注女性孕期維生素D 營養狀況, 以及維生素D 的充足補充。
骨代謝標志物是檢測骨質形成及成骨破骨狀態的重要指標, 能有效評估骨骼生長發育狀態, 為臨床疾病診治提供有效依據。 OC 是調節鈣磷代謝的重要激素之一,由成熟的成骨細胞分泌的骨非膠原蛋白, 其生理功能尚不明確, 但普遍認為與骨形成及轉化有關, 被認為是一種特異且敏感的骨形成標志物。 近年來研究顯示, 維生素D 對OC 的分泌及功能發揮起著重要作用, 可能是維生素D 活性形式1, 25 (OH)2D3在原始的人類成骨細胞的分化過程中具有刺激OC 分泌和mRNA 表達的作用相關[10]。 本研究結果顯示, 對早產兒進行28 天的活性維生素D 補充, 即可使血清OC 水平顯著增高, 表明維生素D 可是成骨細胞活躍, 進而促進骨骼發育。 ALP 是成骨細胞活性的標志, 是臨床診斷佝僂病的重要指標。ALP 活力隨著年齡呈現波動變化, 從年齡分組來看,ALP 在嬰兒期和青春期前顯著高于其他年齡段, 這與嬰兒期和青春期體格快速發育相關[11]。 而對于早產兒,本研究發現, 補充活性維生素D 可顯著提高血清OC 水平, 進而促進早產兒骨骼發育, 滿足追趕性生長的物質需求。 另外, 血清磷水平是早期診斷代謝性骨病的重要指標[12], 且磷對礦物質代謝及佝僂病的診斷具有特異性, 當早產兒血清磷水平<2 mmol/L 時, 表明礦物質不足, 當<1.8 mmol/L 時, 常存在明顯的佝僂病影響學改變[13]。 但血鈣水平對骨代謝無特異性, 當血鈣水平發生異常時, 身體會犧牲一部分骨鈣以維持血鈣水平的正常, 且即使身體處于低磷狀態, 仍可表現為正常血鈣水平。 本研究結果表明, 雖然活性維生素D 補充未使血清磷水平顯著增高(P>0.05), 但處于上升趨勢, 表明骨代謝處于活躍狀態。
綜上所述, 早產兒維生素D 營養狀況不佳, 缺乏率高達40%。 活性維生素D 補充可顯著改善骨代謝指標,包括血清OC、 ALP 水平的增高, 改善鈣磷代謝, 以促進早產兒骨骼發育。 故對于存在早產風險的新生兒, 一方面在產婦孕期即要關注維生素D 營養狀況, 充足補充維生素D 及鈣磷制劑, 另一方面, 要密切關注早產兒維生素D 營養狀況, 及時補充, 糾正不足, 以滿足骨骼發育的物質需求, 實現追趕性生長。

