單孔胸腔鏡精準肺段切除術治療早期非小細胞肺癌
王晨,姜靜遠,張樂寧,許哲男,張 哲,馮崇,張川,林風武*
(1.吉林大學中日聯誼醫院,長春 130033;2.吉林大學第一醫院,長春 130021)
肺癌是目前發病率及病死率最高的惡性腫瘤,是威脅人們健康的主要疾病。2020年,我國新確診的肺部惡性腫瘤患者數量超過了80萬例,且該疾病直接導致超過70萬例患者死亡[1]。肺部惡性腫瘤常見的為非小細胞型肺癌(non-smallcelllungcancer,NSCLC),發病比例超過肺部惡性腫瘤總數的4/5[2-3]。肺葉切除術合并系統性淋巴結清掃術是指南中推薦的手術方式。隨著醫療技術的進步以及人們對生活質量的更高要求,大量早期磨玻璃結節通過體檢被篩查出來;隨著我國人口平均壽命的延長,老年肺部惡性腫瘤患者的發病率也逐漸上升,由于老年患者年齡較大,心肺功能較差且可能合并有其他疾病,臨床學者開始重視起肺段切除術手術方式[4-5]。目前缺乏針對肺葉切除術、肺段切除術及楔形切除術等不同術式對肺部惡性腫瘤患者術后生存期的大樣本及前瞻性的統計學研究數據,肺段切除術的安全性仍未得到充分證實。本研究分析行肺葉、肺段、楔形切除術的早期非小細胞肺癌患者的臨床數據結果,探究不同術式應用于早期肺部惡性腫瘤的效果,報道如下。
1 資料與方法
1.1 一般資料
選擇2019年6月—2020年8月于吉林大學中日聯誼醫院胸外科病房住院手術患者180例,納入病例術中及術后病理均證實為非小細胞型肺癌,且患者病理及臨床分期均為I期。根據患者手術方式的不同分為A組(單孔胸腔鏡肺葉切除術組)、B組(單孔胸腔鏡精準肺段切除術組)、C組(單孔胸腔鏡肺楔形切除術組),各60例。A組,男36例,女24例,平均年齡(57.5±8.66)歲;B組,男33例,女27例,平均年齡(59.0±10.11)歲;C組,男39例,女21例,平均年齡(60.2±8.19)歲。3組性別、年齡等一般資料比較,差異無統計學意義(P>0.05),具有可比性。
1.2 納入與排除標準
1)根據國際癌癥控制聯盟第八版病理標準診斷[6],入選患者均為I期非小細胞肺癌,并且在接受手術治療前未接受抗腫瘤相關治療;2)入選個案均行快速冰凍檢查,且所有病理學相關檢查結果均提示為NSCLC;3)入院個案不包括既往有嚴重心腦血管等疾病者;4)入院個案均為單一病變的個體,不包含肺部含有多處結節、需進行多部位肺部手術案例。本研究經吉林大學中日聯誼醫院倫理委員會批準。
1.3 治療方法
手術患者均采用靜脈吸入復合麻醉的方法麻醉后取健側臥位,手術切口位置根據患者術前胸部CT提示結節部位及患者身高、體質量等綜合因素決定,一般為第4肋或第5肋間,切口長度一般為3~4 cm。
1.3.1 A組首先探查患者肺部病灶位置,確定病灶所在肺葉,核對與患者術前影像學檢查是否相符,確定無誤后首先行肺楔形切除術切除腫物,送術中快速冰凍病理,術中病理確定為惡性腫瘤后則進一步將葉間裂打開并游離出肺葉支氣管和肺動、靜脈,分別采用直線切割閉合器進行切割閉合,并進行系統性淋巴結清掃術,最后留置引流管。
1.3.2 B組首先探查患者肺部病灶位置,確定病灶所在肺段,與術前影像學檢查核對無誤后游離相應的肺段動、靜脈和相對應的肺段支氣管,采用直線切割閉合器進行切割閉合。采取肺膨脹-萎陷法確定目標靶肺段的邊界,然后采用直線切割閉合器進行切割,切除標本送快速冰凍。如果術中病理為惡性,則需進一步確定腫瘤距手術切除邊緣是否超過2 cm或大于腫瘤直徑,如果符合則進一步行淋巴結清掃術后留置引流管。
1.3.3 C組探查患者肺部病灶位置,核對與患者術前影像學檢查是否相符,確定無誤后行肺楔形切除術切除腫物,送術中快速冰凍病理,術中病理結果如果提示為惡性腫瘤,則需確定手術切除邊緣距腫瘤距離超過2 cm或大于腫瘤直徑,并進行淋巴結清掃,確定無誤后留置引流管。
1.4 觀察指標
入選個體均需記錄患者手術實際時間、手術過程中出血量、術后住院時間,統計患者手術治療前后肺通氣功能變化情況;記錄各組統計個體手術過程中摘除的淋巴結個數及站數;記錄入選個體手術治療后并發癥發生情況,如手術治療后出現漏氣、肺部感染、皮下氣腫、術后心臟功能異常等。
1.5 統計學方法
統計數據結果均由SPSS 26.0軟件完成,計量資料通過均數±標準差(±s )方式表示,通過t檢驗進行,計數資料通過例(%)方式表示,通過χ2檢驗進行,以P<0.05表示差異有統計學意義。
2 結果
2.1 3組臨床相關指標比較
見表1。
表1 3組臨床相關指標比較(±s,n= 60)
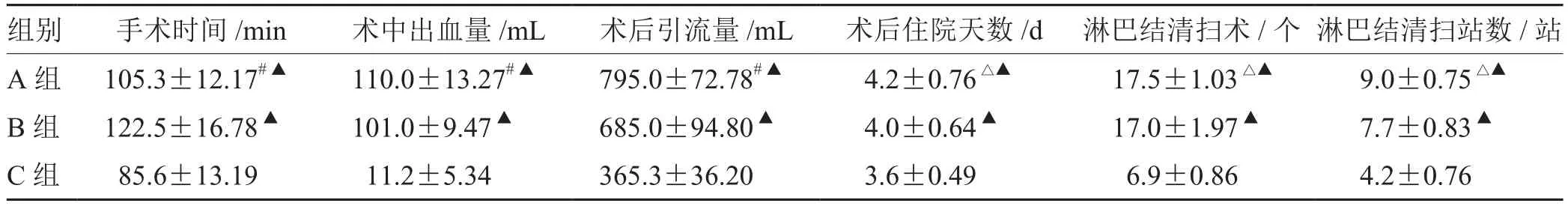
表1 3組臨床相關指標比較(±s,n= 60)
注:與B組比較,# P<0.05,△P>0.05;與C組比較,▲P<0.05
組別 手術時間/min 術中出血量/mL術后引流量/mL術后住院天數/d 淋巴結清掃術/個 淋巴結清掃站數/站A組105.3±12.17#▲110.0±13.27#▲795.0±72.78#▲4.2±0.76△▲17.5±1.03△▲9.0±0.75△▲B組122.5±16.78▲101.0±9.47▲685.0±94.80▲4.0±0.64▲17.0±1.97▲7.7±0.83▲C 組 85.6±13.19 11.2±5.34365.3±36.203.6±0.49 6.9±0.864.2±0.76
2.2 3組治療前后肺功能變化比較
見表2。
表2 3組治療前后肺功能變化比較(±s,n= 60)

表2 3組治療前后肺功能變化比較(±s,n= 60)
注:與治療前比較,# P<0.05;與A組比較,△P<0.05;與B組比較,▲P<0.05
-1組別 時間 F E V 1/L M V V/(L·m i n)A組 治療前2.8±0.0 8 9 5.2±0.8 6治療后1.9±0.1 1# 7 1.3±0.6 8#B組 治療前2.7±0.0 7 9 4.3±1.1 0治療后2.1±0.0 8△8 3.3±1.1 1△C組 治療前2.8±0.1 0 9 4.2±1.1 5治療后2.5±0.1 2△▲8 7.3±1.1 3△▲
2.3 3組術后并發癥發生情況比較
見表3。

表3 3組術后并發癥發生情況比較( n = 60) 例
3 討論
隨著肺部惡性腫瘤的高發病率與科學技術的進步,針對肺癌的手術治療方式在過去十幾年的時間里也發生較大變化。經過十多年的發展,四孔、三孔及單操作孔等微創手術方法逐漸得到普及。隨著人們對微創及快速康復理念的極致追求,單孔胸腔鏡技術逐漸走入了人們的視野[7]。研究[8]首次報道應用單孔胸腔鏡技術手術治療1例自發性氣胸患者,術后恢復良好。隨著科研人員對單孔胸腔鏡手術的反復研究觀察,更多的證據表明該手術方式是安全可行的。并且研究發現與傳統多孔胸腔鏡肺切除手術比較,單孔胸腔鏡手術患者切口僅有位于腋中線第4肋、第5肋間1處,由于該位置肋間隙寬并且肌肉組織更少,因此該切口容易止血且對機體正常組織損傷更輕微,并且患者術后疼痛反應減輕,對于術后康復鍛煉更有益處[9-10]。由于單孔胸腔鏡手術過程中所有的器械及操作僅能通過1個切口進入,因此各種器械之間會出現相互影響,結合既往報道及本中心研究經驗,手術過程建議由3個醫生共同完成,術者和第一助手位于同側,第二助手位于對側將胸腔鏡提起緊貼切口上端,盡可能給術者留有足夠的操作空間;手術應遵循循序漸進的過程,術者需要一定的學習曲線,從簡單手術開始逐漸過渡到復雜手術,并且手術過程中注意吸引器的靈活運用,在保持視野清晰、清掃淋巴結等方面具有十分重要的作用[11-12]。
目前,針對肺部早期惡性腫瘤手術治療的方式主要包括三大類:肺葉切除術、肺段切除術(解剖性肺段切除術及肺段聯合切除術)、肺楔形切除術。既往1項針對早期非小細胞肺癌不同手術方式對患者預后影響的研究表明,對于I期NSCLC患者,行亞肺葉切除術患者的預后復發率較肺葉切除術后的患者更高,引起人們對于早期肺部惡性腫瘤肺段切除術安全性的擔憂[13]。對于早期肺部惡性腫瘤,肺段切除術對于患者的復發及預后生存期與肺葉切除術并無差異,且肺段切除術患者術后恢復時間更短,肺楔形切除術患者術后預后生存期較其他兩種術式差[14-15]。研究[16]發現對于直徑小于2 cm的腫物,肺段切除術患者術后5年生存率要優于肺葉切除組。由于肺葉切除會導致機體肺臟器組織表面臟層胸膜面積減小,臟層胸膜在調節肺臟水、電解質平衡方面具有重要作用,因此肺葉切除后的患者除去對肺功能損失更多之外,術后引流積液量也較肺段切除患者更多[17-19]。肺葉切除的患者由于同側剩余肺葉在術后會代償性膨大,使得剩余肺組織盡可能充填整個胸腔,因此容易出現肺葉支氣管扭曲變形,使得通氣不順暢,導致肺通氣功能受限。肺段切除后的患者由于未損傷到較大氣道,且剩余肺組織所需充盈體積較小,發生該事件的概率較低;肺段切除后所形成的胸腔殘腔較小,術后不易發生感染[20-21]。因此,對于早期肺部惡性腫瘤,肺段切除術成為更受推崇的手術治療方式。
上述研究結果表明,肺葉切除組患者在手術時間上要優于肺段切除組,然而其術后胸腔引流積液量更多,且對患者術后肺功能損傷(FEV1,MVV)更大,在術中出血量、術后住院時間、淋巴結清掃數目及淋巴結清掃站數上兩者并無明顯統計學差異;肺葉切除組術后更容易發生不良反應,根據統計數據表明,其術后漏氣、感染、皮下氣腫等不良反應發生比例高于其他2組;對于肺楔形切除術,其手術較為容易,對肺臟損傷較小,因此其手術時間、術中出血量、術后住院時間、引流量、肺功能等指標優于其他2組,然而其淋巴結清掃數目及站數明顯低于其他2組。因此,對于肺段切除術治療早期非小細胞肺癌是安全的,并且與肺葉切除比較,由于其對肺功能損傷更小,術后不良反應更少,因此更有利于患者術后盡早康復。研究[14-15]表明,早期肺惡性腫瘤楔形切除患者術后生存期較肺葉及肺段組差,并且楔形切除術受病灶位置的影響較大。并且研究中發現,C組出現因腫瘤距切緣距離過少而繼續擴大切除范圍的情況,而在其他2組中并未出現該情況。因此,針對早期肺惡性腫瘤,肺段切除術式安全、可靠,是值得推薦的治療方式。
研究過程中發現,肺部手術過程中切口部位的選擇尤為重要,主要是因為切口與改善手術視野以及避免手術過程中器械相互干擾,提高手術流暢度具有密切關系。合理的切口位置常使得手術能夠事半功倍,縮短手術時間,避免術中出現因視野原因造成的損傷。術前切口的選擇需要綜合患者術前影像學檢查結果及患者體型等因素,對于中等身材及瘦長體型的患者,手術切口的位置一般選擇為腋中線第5肋間;針對超力型的手術病例,由于其膈肌可能會比正力型高,因此切口位置一般會適當上移1個肋間;針對上葉結節的手術患者,一般也會選擇將手術切口上移1個肋間。另外在肺段切除術的患者,可以根據其目標靶肺段的位置適當確定切口偏向胸側還是背側,達到切口的個體化,避免選擇策略導致病人因體型等因素引起切口過高或過低影響操作的情況。手術清掃淋巴結的過程中,需盡可能避免損傷迷走神經肺支,通過術后觀察發現,保留迷走神經肺支后的術后患者不自主咳嗽明顯減輕。行肺段切除時需要盡可能精準識別斷間平面,目前主流的方法為肺膨脹-萎陷法。即手術過程中待目標切除肺段的動、靜脈及支氣管切斷后,雙肺用純氧正壓通氣,至萎陷的肺葉完全膨脹后改為健側通氣,由于目標切除肺段缺乏肺段動脈,因此該部分肺組織內氣體無法迅速排出,正常肺組織內氧氣被循環血流迅速帶走,兩者之間形成一條界限,即斷間平面,隨后沿該界限進行裁剪即可[22]。由于目前低劑量CT的普及,體檢中發現越來越多的磨玻璃結節,磨玻璃結節體積較小,不容易觸及,因此會對手術帶來一定的難度。對于此類手術患者,可以術前進行結節定位,包括Hook-wire法、亞甲藍穿刺定位法、三維重建法、電磁導航技術等多種定位方法[23-24]。
綜上所述,隨著低劑量CT被廣泛應用于臨床以及人們對自身健康狀況的重視,肺部惡性腫瘤早期被發現的概率逐漸增加。本研究證實,肺段切除術治療早期NSCLC患者術后疼痛更輕,不良反應更少,恢復時間更短,有利于術后患者早期進行康復鍛煉,有助于患者術后盡快康復,提高患者生活質量,也為老年患者、基礎情況較差難以耐受肺葉切除術的患者以及結節位置欠佳、無法進行楔形切除的患者提供了更好的選擇。本研究是單中心的回顧性實驗,樣本量較小,統計數據分析結果可能存在一定偏倚,希望后續有更大樣本量的實驗研究進一步探討單孔胸腔鏡精準肺段切除術治療早期非小細胞肺癌的臨床療效。

