基于SEER數據庫構建早發性直腸癌患者死亡風險預測模型的研究
仲建平, 王正兵, 張強, 黃曉
(1.揚州大學附屬醫院胃腸外科, 江蘇 揚州 225012;2. 揚州大學醫學院, 江蘇 揚州 225009)
0 引言
結直腸癌是世界上第三大常見惡性腫瘤, 其死亡率居于世界第二, 其中直腸癌約占所有結直腸惡性腫瘤的40%。近年直腸癌總發病率正在下降[1], 但與此同時年輕人群的直腸癌發病率卻不成比例地增加了[2,3], 目前直腸癌已經成為年輕患者中最常見的結直腸惡性腫瘤[4]。研究顯示直腸癌患者總體生存正在改善, 但對年輕患者而言并非如此;自1970以來, 年輕患者的直腸癌死亡率隨著時間的推移而持續增加[5,6]。由于這個患者群體呈現出病理分化等級差, 淋巴結轉移率高及總體分期相對比較晚等特點, 因此這一人群的生存特點也與其他人群存在較大的不同, 有必要對這一人群單獨分析其生存特點。并且相較于老年人群, 年輕人群一旦確診, 往往面臨著更長的壽命損失, 對社會及經濟方面造成更嚴重的影響[7,8]。因此, 為了進一步探求這一人群的生存特征, 及早對高危人群進行干預, 我們使用SEER數據庫回顧性分析早發性直腸癌患者生存特征并構建死亡風險預測模型。
1 資料與方法
1.1 一般資料
選取SEER數據庫2010-2017年確診為直腸癌的患者共計24954例。提取變量包括年齡、性別、種族、確診年份、腫瘤原發部位、分化程度、病理類型、TNM分期、腫瘤大小、檢出淋巴結數(examined lymph node, ELN)、陽性淋巴結數(positive lymph node, PLN)、腫瘤沉積、周圍神經侵犯( peripheral nerve invasion, PNI)、婚姻狀況生存時間及生存狀態。
1.2 病例篩選
納入標準:①診斷時間是2010-2017年;②病理確診為直腸腺癌, 并且為第一原發癌;③臨床資料完整;④確診時年齡在20~50歲。排除標準:①患者預后資料不完整;②臨床資料不完整;③患者在一個月內死亡;④排除多原發癌;⑤非腫瘤因素死亡。
在種族中, 美洲印第安人/阿拉斯加土著或亞洲/太平洋島民歸為其他人種。TNM分期使用AJCC第七版TNM分期;根據X-tile軟件選取LNR及腫瘤大小的最佳截斷值轉化為分類變量。本研究是在簽署SEER數據使用協議的基礎上開展。因SEER數據庫的數據均為匿名且消除過識別信息, 本研究不需要倫理委員會的批準。
1.3 統計學分析
使用R語言工具提取人群基線數據, 對變量進行Cox單因素分析, 將單因素分析中有統計學意義的因素納入多因素Cox回歸分析, 確定早發性直腸癌預后的獨立影響因素。對變量進行lasso回歸, 壓縮變量個數構建出精簡的直腸癌列線圖預測模型。計算列線圖對應的C指數;計算每個病例的死亡風險評分, 繪制列線圖預測模型ROC曲線及校準曲線評價其區分度、準確度。所有統計分析采用R軟件4.1.3版本。P<0.05為差異有統計學意義。
2 結果
(1)通過逐步篩選后納入(2010~2017年)4754例早發性直腸癌病人, 根據X-tile軟件選取腫瘤大小最佳截斷值為≤5.5cm、>5.5cm;LNR最佳截斷值為≤0.07、0.07~0.36、>0.36。患者的基本特征見表1。
(2)使用Cox單因素回歸進行分析, 年齡、性別、種族、分化程度、病理類型、TNM分期、腫瘤沉積、PNI、CEA、腫瘤大小、淋巴結采集數、LNR、化療、婚姻狀態是早發性直腸癌患者死亡相關因素(表1);將單因素分析中有統計學意義的變量納入多因素分析, 多因素Cox逐步回歸分析顯示, 性別、分化程度、病理類型、TNM分期、腫瘤沉積、PNI、C E A、化療、腫瘤大小、淋巴結采集數、LNR、婚姻狀態是早發性直腸癌患者獨立危險因素(表2)。

表2 COX多因素分析
(3)構建早發性直腸癌患者腫瘤相關死亡風險列線圖:整合多因素分析結果中早發性直腸癌死亡風險因素, 由于變量數量較多, 使用lasso回歸壓縮變量數目, 經壓縮后剩余變量為:分化程度、病理類型、T分期、M分期、LNR、腫瘤沉積、PNI。將壓縮后的變量整合, 構建早發性直腸癌患者1, 3, 5年腫瘤相關死亡風險預測列線圖(圖1)。列線圖顯示, T分期對早發性直腸癌病人死亡風險影響最大, 其次是M分期、病理分化程度、LNR、病理類型、PNI, 影響最小的是腫瘤沉積。
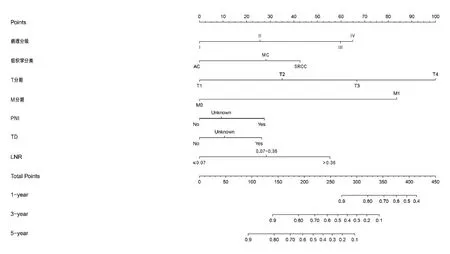
圖1
3 評價列線圖預測模型
計算模型的C指數, 該列線圖的C指數為0.7 97(95%CI:0.7 83~0.811)。使用患者一年生存率R O C曲線下面積的0.83(95%CI:0.87-0.78), 三年生存ROC曲線下面積:0.84(95%CI:0.85-0.82), 五年生存:0.83(95%CI:0.84-0.81)。(圖2)表明良好的區分能力。校正曲線顯示預測模型具有良好的準確性(圖3)。
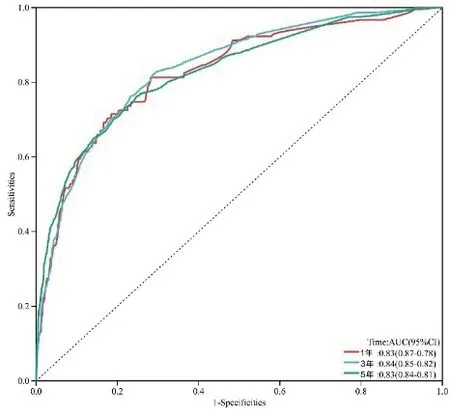
圖2
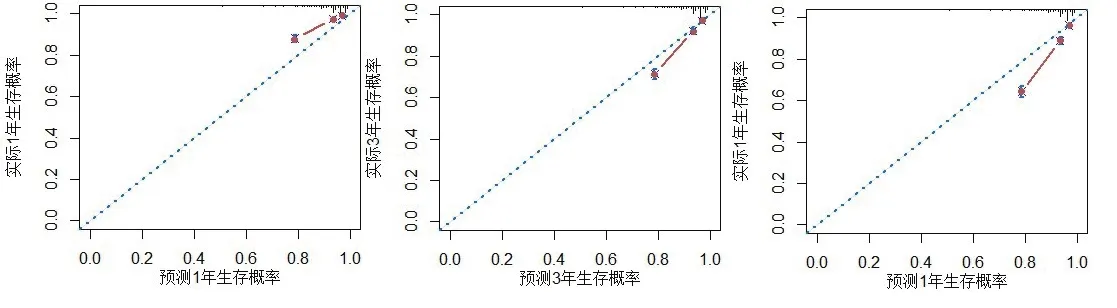
圖3
4 討論
結直腸癌是20-49歲人群的第二大發病癌癥和癌癥死亡原因, 近年來年輕人結直腸癌的發病率和死亡率在增加[9]。其中主要表現為直腸癌的增加[10], 相比之下結腸癌升高的比例卻并不明顯。近年來相關研究揭示了早發性直腸癌的多種危險因素:全球飲食西化、紅肉消費增加、應激、抗生素、合成食用色素、久坐行為和腸道微生物群。然而, EORC發病率呈上升趨勢的根本原因仍然未知。這表明早發性直腸癌在發生發展上有其特殊之處。結腸和直腸除了在胚胎、解剖和生理上的差異外, 結腸癌和直腸癌在致癌方面似乎也不同。已有研究發現結腸癌和直腸癌之間存在不同的基因表達差異[11]。正因為結腸癌與直腸癌諸多的不同之處, 因此我們并未像之前的研究將結直腸癌合并分析, 而是單獨分析早發性直腸癌這一特殊患者群體。EORC的癥狀出現晚, 容易出現診斷延誤, 腫瘤惡性程度高、分期晚、可切除性差及術后遠處復發風險高, 病理類型中, 黏液腺癌和印戒細胞腺癌等惡性程度類型占比明顯增加, 印戒細胞癌占比可達 3%-13%[12]。
近年來直腸癌患者的治療在包括病理檢查、影像技術、新輔助治療和外科手術的進步和標準化, 以及多學科決策的常規實施方法, 患者的生活質量和長期生存有了較大的提升。以往的關于早發性直腸癌預后的相關回顧性研究中已經不太適用于如今患者生存預測。并且隨著腫瘤沉積與神經脈管浸潤等對患者生存影響的揭示, seer數據庫中也著手收錄了更多的臨床項目, 我們能夠獲得更多方面的資料內容用于研究。在我們的研究中除了納入臨床病理等基本特征外, 還納入腫瘤沉積、PNI等變量, 并明確了它們在EORC患者長期生存中的獨立預測價值, 與以往的研究相比內容更加豐富。在逐步多因素Cox回歸分析中, 性別、分化程度、病理類型、TNM分期、腫瘤沉積、PNI、CEA、化療、腫瘤大小、淋巴結采集數、LNR、婚姻狀態是早發性直腸癌患者獨立預后因素。在目前的國際指南中, 建議在結直腸癌切除術中淋巴結采集數為12枚或更高。較低的淋巴結采集數(小于12)與直腸癌預后意義存在爭議[13], 我們的研究顯示淋巴結采集數獨立地影響患者的預后, 這需要更多的臨床研究來闡明。
列線圖在一定程度上可以反映出患者的長期生存情況, 為了使得列線圖更加簡潔, 利于使用, 我們使用lasso回歸對變量進行壓縮, 摒棄了一些對患者生存影響較小的變量, 剩余的變量為:分化程度、病理類型、T分期、M分期、LNR、腫瘤沉積、PNI, 將壓縮后的變量整合后構建列線圖。使用ROC評估模型, 顯示構建的列線圖模型具有良好的預測性能。列線圖顯示T分期對早發性直腸癌病人死亡風險影響最大, 其次是M分期、分化程度、LNR、病理類型、PNI, 影響最小的是腫瘤沉積。列線圖肯定了TNM分期在患者生存分析中的“基石”作用, 也反映出遠處轉移是直腸癌治療失敗、患者長期生存威脅的主要原因。輔助化療通常用于遠處轉移的控制, 尤其是應用于局部晚期直腸癌的治療。然而, 并非所有患者都能從輔助化療中受益, 特別是有些患者在治療后甚至可能會出現更差的結果, 但是關于輔助化療在直腸癌尤其是局部晚期直腸癌中的“不作為”行為的原因仍然存在爭論[14]。LNR自出現以來就受到臨床研究者的追捧, 是一項強有力的預測因素。在一項多中心回顧性研究中, LNR表現出比陽性淋巴結總數更可靠的預后價值[15]。PNI是結直腸癌患者預后的獨立危險因素, PNI與腫瘤分化程度,淋巴結轉移顯著相關, 在預測患者預后方面發揮著重要作用[16]。我們的分析所涉及變量極易獲取, 并且模型表現出不俗的區分度, 貼近臨床實際工作需要。
與現有的預測模型相比, 我們的列線圖整合了更多的預測變量, 如腫瘤沉積和周圍神經侵犯, 為EORC患者提供了全面的預測。此外, 我們通過X-tile軟件建立了一個具有最優截斷值的風險分級系統, 該系統更加精確和可靠。構建的列線圖預測模型的準確性由ROC曲線和C指數進行驗證, ROC曲線、C指數及校準曲線顯示出模型預測早發性直腸癌年死亡風險較為精準。
由于本研究是基于大數據庫的回顧性分析研究, 存在一些局限性, 比如在數據庫中未能提供詳細的化療方案和患者的生化指標等信息, 不能將患者個體的特殊性納入考慮。但由于病例數的巨大, 個體差異造成的影響較小, 因此我們構建的預測模型仍能夠在一定程度上預測早發性直腸癌死亡風險, 后續的研究依舊需要大樣本臨床隊列研究或隨機對照試驗驗證。
我們構建的列線圖模型顯示出很高的敏感性和準確性, 能有效預測年輕直腸癌病人1, 3, 5年內死亡風險, 對早發性直腸癌的預后干預具有臨床指導意義, 是治療決策的潛在工具。
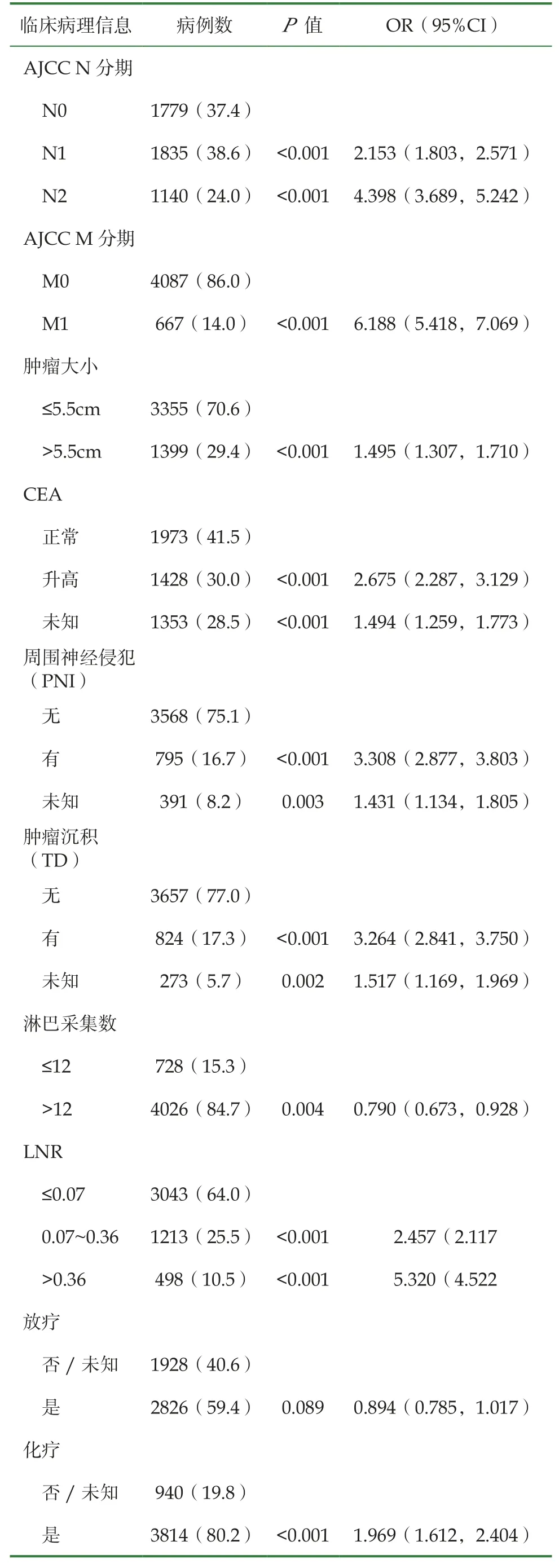
續表1
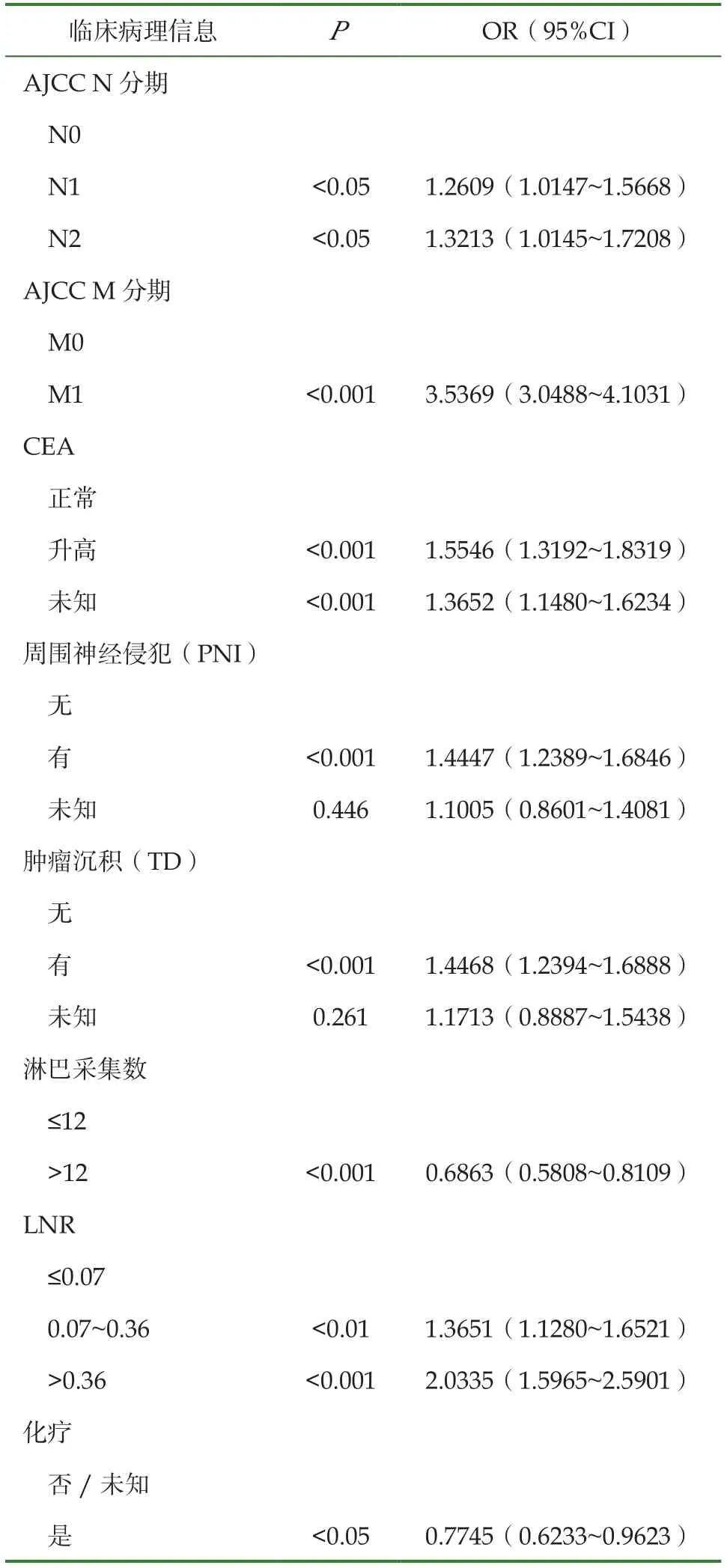
續表2

